苏教版高中化学选修五有机化学基础
- 格式:docx
- 大小:474.04 KB
- 文档页数:23

专题5 生命活动的物质基础第二单元氨基酸蛋白质核酸课前预习情景导入1.蛋白质的水解产物是氨基酸,天然蛋白质的水解产物都是α-氨基酸。
鸡蛋白溶液、大豆蛋白溶液中,加入浓的Na2SO4溶液时会有沉淀析出,再继续加入蒸馏水后,沉淀又溶解,又构成蛋白质溶液。
但加入甲醛或加热时,也能析出沉淀,再继续加入蒸馏水后,沉淀不能继续溶解。
这些都是蛋白质的特性。
酶是一类具有催化作用的蛋白质,在人类的生命中起着举足轻重的作用,是天然的最有效的生物催化剂。
在生命活动中,新陈代谢以及与遗传信息传递和表达有关的所有化学变化都是在酶的催化作用下进行的。
2.核酸有两种类型即脱氧核糖核酸(DNA)和核糖核酸(RNA),基因全部由核酸组成,基因控制着生物从诞生到死亡的全部代谢过程,基因指导着蛋白质、酶、激素及一切生理活性物质的合成、分解,控制着生物体的生长、发育、繁殖、复制,同时自身也处于不断地代谢中。
基因的代谢实际上就是核酸的代谢,核酸的代谢决定了整个生命过程的兴衰。
人类基因组拥有大约32亿对碱基,不同人的基因组中碱基对序列的99.9%都是一样的,只有不到千分之一的序列有所不同。
知识预览一、氨基酸1.蛋白质是构成生命的基础物质,它是由多种不同的________构成的,而核酸对蛋白质的生物合成又起着决定的作用。
因此,研究这些基本的生命物质的结构和性质,有助于揭示生命现象的本质。
2.蛋白质是由氨基酸构成的,迄今人类在自然界已发现数百种________,但是从蛋白质水解得到的氨基酸,最常见的大约有________,并且绝大多数是________,除甘氨酸外,α-氨基酸都是________,构成天然蛋白质的α-氨基酸都是________。
3.由于氨基酸的系统命名通常比较烦琐,实际使用较多的是其俗名。
在表示多肽和蛋白质结构时,普便使用的是氨基酸的缩写,通常情况下,氨基酸的英文缩写取其英文名称前三个字母,中文缩写则将其俗名中的“氨酸”省略。

高中化学学习材料《有机化学基础》知识点整理一、重要的物理性质1. 有机物的溶解性(1) 难溶于水:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的醇、醛、羧酸等。
(2) 易溶于水:低级[n(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(都能与水形成氢键)。
(3) 具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2. 有机物的密度(1) 小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2) 大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3. 有机物的状态[常温常压(1个大气压、20℃左右)](1) 气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2=CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2=CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2) 液态:一般N(C)在5~16的烃及绝大多数低级衍生物。


专题2有机物的结构与分类(A)——本章准备一、背景知识本专题由两个单元组成,第一单元“有机化合物体的结构突出了碳原子的成键特点,即有机化合物中碳原子的成键的三空间取向——四面体、平面三角形和直线形,并用杂化轨道理论对期作出了简单的解释;有机化合物结构的三种表示方法(结构式、结构简式和键线式);最后介绍有机化合物的同分异构体。
在第二单元“有机化合物的分类和命名”中,关于有机化合物的分类,重点介绍的是以官能团为依据的分类方法,简单介绍了其他两种分类方法;关于有机化合物的系统命名法。
同时简单的介绍了习惯命名法的基本原则。
有机化合物的结构是本专题的重要内容,也是贯穿于有机化学基础的主线,学习有机化合物结构的目的,是为了让学生能够进一步探究结构与性质之间的关系,更好地将所学到的有机化学知识加以应用,并以帮助学生将庞杂的有机化学知识系统地梳理起来,由于在化学2中已经对有机化合物中碳原子的成键方式作了一些简单要求,所以本模块的标准内容对有机化合物的结构需要从更高的层次上的加以阐述。
对有机化合物的结构表示也提出了明确的要求,要能准确,简单表示出有机化合物分子中原子之间价键连接情况,要能表示出简单有机化合物分子内原子之间的空间位置关系。
对于有机化合物分类的知识,要明确其教育意义在于对分类知识建构:通过学习,让学生了解有机化合物的一般分类方法,建立有机化合物的分类框架,了解有机化合物的主要类别并能通过所学方法对简单的有机化合物进行分类。
学习中要结合“有机化合物中常见的官能团”并通过运用“问题解决”的栏目,建立有机化合物分类的基本思路。
有机化合物的命名是本专题教学的又一重点。
由于课时有限,教材主要介绍烷烃的系统命名法,对于有机物中基的电子式书写不作要求。
烷烃系统命名法是其他有机化合物进行系统命名的基础,在“观察与思考”、“整理与归纳”栏目中烷烃命名的相关内容都采用不同颜色进行呈现,目的是能动态地呈现烷烃的命名规则。
教师在进行烷烃系统命名规则时也要动态地反映命名法的具体过程,让学生能更好地体会命名规则。

第五章进入合成有机高分子化合物的时代第一节合成高分子化合物的基本方法一、教学目标1、了解有机高分子化合物的链节、聚合度、单体的概念。
2、了解加聚反应和缩聚反应的一般特点。
3、由简单的单体写出聚合反应方程式(重点是缩合聚合反应方程式),聚合物结构式。
4、由简单的聚合物结构式分析出它的单体。
二、教学重点加聚反应和缩聚反应的特点;能用常见的单体写出简单的聚合反应方程式和聚合物的结构简式三、教学难点用常见的单体写出简单的聚合反应方程式和聚合物的结构简式;用简单的聚合物结构式分析出单体四、课时安排1课时五、教学过程【引入】从这一节课开始,我们要对高分子化合物做一个比较系统的了解。
那么,究竟什么是高分子化合物呢?它们与低分子有机物有什么不同?【板书】第五章进入合成有机高分子化合物的时代(学生思考、讨论)【回答】1、它们最大的不同是相对分子质量的大小。
有机高分子的相对分子质量一般高达104~106,而低分子有机物的相对分子质量在1000以下。
2、合成有机高分子的基本结构与低分子有机物的单一结构不同,它是由若干个重复结构单元组成的高分子。
师:很好!接下来我们先学习第一节。
【板书】第一节合成高分子化合物的基本方法一、加聚反应师:大家对加聚反应并不陌生,它是加成聚合反应的简称,我们从高一到现在,已经学过好几个加聚反应了。
比如用乙烯为原料制取高分子化合物——聚乙烯,大家还记得其化学方程式吗?(学生回答,教师根据回答的情况给予评价)【板书】nCH2=CH2 →乙烯(单体)聚乙烯(聚合物)师:像乙烯这类能够进行聚合反应形成高分子化合物的低分子化合物被称为单体;高分子化合物中化学组成相同、可重复的最小单位称为链节,也称重复结构单元,聚乙烯的链节为—CH2CH2—;高分子链中含有链节的数目称为聚合度,通常用n表示。
【板书】聚合物的平均相对分子质量 = 链节的相对质量×n【思考与交流】思考、讨论、交流,完成下表。
单体名称单体结构简式聚合物乙烯CH2=CH2丙烯CH2=CHCH3氯乙烯CH2=CH丙烯晴CH2=CHCN丙烯酸CH2=CHCOOH醋酸乙烯酯CH3COOCH=CH2丁二烯CH2=CH—CH=CH2乙炔CH≡CH师:通过聚合物的链节,可以看出聚合物的单体,你知道下面两个聚合物是由何种单体聚合而成的吗?【回答】和(顺便介绍一种找聚合物的单体的方法——弯箭头法)师:聚合反应中除了加聚反应之外,还有另外一种——缩合聚合反应,简称缩聚反应。

江苏省江阴市成化高级中学高中化学有机知识点苏教版选修5 一、重要的反应1.能使溴水(Br2/H2O)褪色的有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③ 通过氧化反应使之褪色:含有—CHO(醛基)的有机物(有水参加反应)注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯2.能使酸性高锰酸钾溶液KMnO4/H+褪色的有机物:含有、—C≡C—、—OH(较慢)、—CHO的物质;与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应)3.与Na反应的有机物:含有—OH、—COOH的有机物与NaOH反应的有机物:常温下,易与含有酚羟基、—COOH的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na2CO3反应的有机物:含有酚羟基的有机物反应生成酚钠和NaHCO3;含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;含有—SO3H的有机物反应生成磺酸钠并放出CO2气体。
与NaHCO3反应的有机物:含有—COOH、—SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
4.银镜反应的有机物(1)发生银镜反应的有机物:含有—CHO的物质:醛、甲酸、甲酸盐、甲酸酯、还原性糖(葡萄糖、麦芽糖等)(2)银氨溶液[Ag(NH3)2OH](多伦试剂)的配制:向一定量2%的AgNO3溶液中逐滴加入2%的稀氨水至刚刚产生的沉淀恰好完全溶解消失。
(3)反应条件:碱性、水浴加热若在酸性条件下,则有Ag(NH3)2+ + OH - + 3H+ == Ag+ + 2NH4+ + H2O而被破坏。
(4)实验现象:①反应液由澄清变成灰黑色浑浊;②试管内壁有银白色金属析出(5)有关反应方程式:AgNO3 + NH3·H2O == AgOH↓ + NH4NO3AgOH + 2NH3·H2O == Ag(NH3)2OH + 2H2O银镜反应的一般通式:RCHO + 2Ag(NH3)2OH 2 Ag↓+ RCOONH4 + 3NH3 + H2O 【记忆诀窍】:1—水(盐)、2—银、3—氨(6)定量关系:—CHO~2Ag(NH3)2OH~2 Ag HCHO~4Ag(NH3)2OH~4 Ag5.与新制Cu(OH)2悬浊液(斐林试剂)的反应(1)有机物:羧酸(中和)、甲酸(先中和,但NaOH仍过量,后氧化)、醛、还原性糖(葡萄糖、麦芽糖)、甘油等多羟基化合物。
专题3 常见的烃领先一步,领跑一生:每一个成功者都有一个开始。
勇于开始,才能找到成功的路。
第一单元 脂肪烃细品书中知识 关键词:烷烃和烯烃、取代反应、加成反应1.烃的分类 ①烃的分类 脂肪烃和芳香烃属于脂肪族化合物的烃是脂肪烃,属于芳香族化合物的烃是芳香烃。
脂肪烃中一定没有苯环,芳香烃中一定有苯环。
②脂肪烃的分类 饱和烃和不饱和烃把含有双键或者叁键等不饱和键的脂肪烃叫做不饱和脂肪烃,简称不饱和烃;把不含有双键或者叁键等不饱和键的脂肪烃叫做饱和脂肪烃,简称饱和烃。
例1 下列物质属于芳香烃,但不是苯的同系物的是解析:含有苯环的化合物就属于芳香族化合物,含有苯环的烃属于芳香烃,而苯的同系物的定义是含有一个苯环且侧链为饱和烃基的芳香烃。
A 、B 属于苯的同系物,C 不属于芳香烃,D 属于芳香烃但侧链不饱和,不属于苯的同系物。
答案:D点拨: 注意烃在不同角度分类时结果是不一样的,还要理解分类的范围,如饱和烃和不饱和烃都是脂肪烃。
2.脂肪烃的物性(1)甲烷的物理性质甲烷为无色无味的气体,密度比空气小,所以收集甲烷可以用向下排空气法,又因为甲烷不溶于水,所以甲烷也可用排水法收集,甲烷是有机物分子中相对分子质量最小的烃。
(2)乙烯的物理性质通常情况下,乙烯是一种无色稍有气味的气体,密度与空气相近,难溶于水。
(3)物理性质的递变规律①烷烃随着碳原子数的增加,相对分子质量增大,分子间作用力增大,熔沸点逐渐升高。
②分子式相同的不同烷烃,支链越多,熔沸点越低。
例如:CH3(CH2)3CH3> (CH3)2CHCH2CH3>C(CH3)4。
③烷烃都不溶于水,且比水的密度小。
例2 含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:* 燃烧热:1 mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量。
根据表中数据,下列判断错误的是( )A.正庚烷在常温常压下肯定不是气体B.烷烃燃烧热和其所含碳原子数成线性关系C.随碳原子数增加,烷烃沸点逐渐升高D.随碳原子数增加,烷烃沸点和燃烧热都成比例增加解析:从表中数据可知,烷烃随碳原子数目递增沸点依次升高,燃烧热依次升高,但这种增长只是一种趋势,不是成比例增长。


江苏省选修5《有机化学基础》教案第一章认识有机化合物【课时安排】共13课时第一节:1课时第二节:3课时第三节:2课时第四节:4课时复习:1课时测验:1课时讲评:1课时第一节有机化合物的分类【教学重点】了解有机化合物的分类方法,认识一些重要的官能团。
【教学难点】分类思想在科学研究中的重要意义。
【教学过程设计】【思考与交流】1.什么叫有机化合物?2.怎样区分的机物和无机物?有机物的定义:含碳化合物。
CO、CO2、H2CO3及其盐、氢氰酸(HCN)及其盐、硫氰酸(HSCN)、氰酸(HCNO)及其盐、金属碳化物等除外。
有机物的特性:容易燃烧;容易碳化;受热易分解;化学反应慢、复杂;一般难溶于水。
从化学的角度来看又怎样区分的机物和无机物呢?组成元素:C 、H、O N、P、S、卤素等有机物种类繁多。
(2000多万种)一、按碳的骨架分类:有机化合物链状化合物脂肪环状化合物脂环化合物化合物芳香化合物1.链状化合物这类化合物分子中的碳原子相互连接成链状。
(因其最初是在脂肪中发现的,所以又叫脂肪族化合物。
)如:CH3CH2CH2CH3CH3CH2CH2CH2OH正丁烷正丁醇2.环状化合物 这类化合物分子中含有由碳原子组成的环状结构。
它又可分为两类: (1)脂环化合物:是一类性质和脂肪族化合物相似的碳环化合物。
如:环戊烷环己醇(2)芳香化合物:是分子中含有苯环的化合物。
如:苯 萘二、按官能团分类:什么叫官能团?什么叫烃的衍生物?官能团:是指决定化合物化学特性的原子或原子团. 常见的官能团有:P.5表1-1烃的衍生物:是指烃分子里的氢原子被其他原子或原子团取代所生成的一系列新的有机化合物。
可以分为以下12种类型: 练习:1.下列有机物中属于芳香化合物的是( )2.〖归纳〗芳香族化合物、芳香烃、苯的同系物三者之间的关系:〖变形练习〗下列有机物中(1)属于芳香化合物的是_______________,(2)属于芳香烃的是________,(3)属于苯的同系物的是______________。

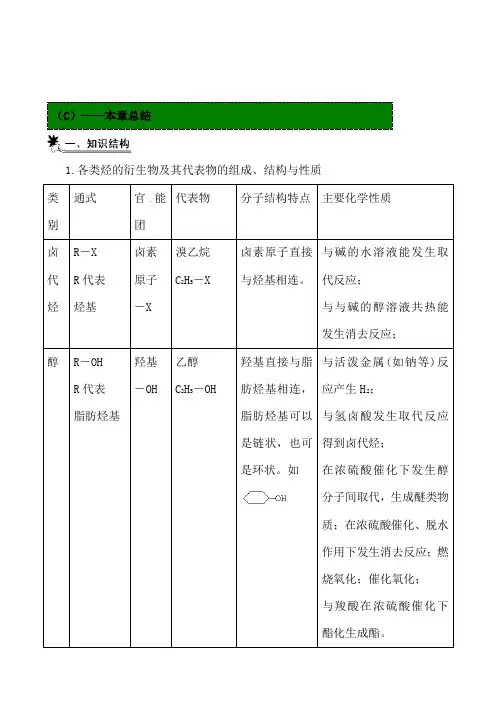
(C)——本章总结1.各类烃的衍生物及其代表物的组成、结构与性质H在浓硫酸催化下发生醇与甲醛发生缩聚有极性,有极性,2.有机物之间的相互转化关系(卤代烃、醇、醛、羧酸、酯的相互转化关系)3.醇、醛、酸、酯转化关系的延伸4.烃的羟基衍生物比较5.烃的羰基衍生物比较6.有机反应主要类型归纳、加氢反应、专题一 有机物的类别与通式有机化合物种类多,要以一些典型的烃类衍生物(乙醇、溴乙烷、苯酚、乙醛、乙酸、乙酸乙酯、脂肪酸、甘油酯、多羟基醛酮、氨基酸等)为例,了解官能团在化合物中的作用。
掌握各主要官能团的性质和主要化学反应,并能结合同系物原理加以应用。
例 1 二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。
二甘醇的结构简式是HO —CH 2CH 2—O —CH 2CH 2—OH 。
下列有关二甘醇的叙述正确的是A.不能发生消去反应B.能发生取代反应C.能溶于水,不溶于乙醇D.符合通式C n H 2n O 3解析:与-OH 相连的碳的邻位碳原子上有氢,所以能发生消去反应,能与羧酸发生酯化反应,是取代反应,所以B 正确。
根据相似相溶原理二甘醇含羟基(-OH ),所以它既能溶于H 2O ,也能溶于乙醇。
它的分子式为C 4H 10O 3。
二甘醇的通式应是C n H 2n+2O 3,不符合D 项中的通式。
答案:B 。
点拨:有机反应的复杂性和有机物种类的多样性,导致了有机反应类型的多样性,各类反应皆有自己的特征,这也与官能团的特征是分不开的。
例2 A 、B 、C 、D 、E 五种芳香化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。
它们的结构简式如下所示:3 3 CH 2CH=CH 2 CH 2CH=CH 2 CH 2CH=CH 2 CH 2CH=CH 2A B C D E请回答下列问题:⑴这五种化合物中,互为同分异构体的是_______________。
⑵W 氧化反应①−→−−反应②−→−−X反应①采取了适当措施,使分子中烯键不起反应。
专题2 有机物的结构与分类细品书中知识关键词:结构式饱和键不饱和键同分异构体碳原子最外层有4个电子,不易失去或获得电子而形成阳离子或阴离子。
碳原子通过共价键与氢、氧、氮、硫、磷等多种非金属形成共价化合物。
1、碳原子的成键方式与分子的空间构型当1个碳原子与其他4个原子连接时,这个碳原子将采取四面体取向与之成键。
在所有碳四价原子形成的共价化合物中,四个共价键均以四面体形分布,如果与碳原子连接的原子无相同,则分子的构型为正四面体。
科学实验证明,甲烷分子里,1个碳原子与4个氢原子形成4个共价键,构成以碳原子位中心,4个氢原子位于四个顶点的正四面体立体结构。
键角均为109º28’。
由于碳原子的成键特点,每个碳原子不仅能与氢原子或其他原子形成4个共价键,而且碳原子之间也能与共价键相结合。
碳原子间可以形成单键、双键和三键;多个碳原子可以结合成长短不一的碳链,碳链也可以带有支链,还可以结合成碳环,碳链和碳环也可以互相结合。
当碳原子之间或碳原子与其它原子之间形成双键时,形成该双键的原子以及与之直接相连的原子处于同一平面上;当碳原子之间或碳原子与其他原子之间形成叁键时,形成该叁键的原子以及与之直接相连的原子处于同一直线上。
在烃分子中,仅以单键方式成键的碳原子称为饱和碳原子,以双键或叁键成键的碳原子称为不饱和碳原子。
例1 甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( ) A.CH3Cl不存在同分异构体B.CH2Cl2不存在同分异构体C.CHCl3不存在同分异构体D.CCl4是非极性分子解析:如果甲烷是正方形的平面结构,则CH2Cl2分子里的五个原子必在同一平面上,应有两种同分异构体:,CH2Cl2实际上没有同分异构体(反证法),说明甲烷为正四面体结构,所以应选B。
点拨:在碳的化合物或单质中,如果是正四面体型结构,则碳在中心位置,与碳相连的四个原子必为相同原子,若不是连有四个相同原子,则一定不为正四面体构型。
江苏省选修5《有机化学基础》教案第一章认识有机化合物【课时安排】共13课时第一节:1课时第二节:3课时第三节:2课时第四节:4课时复习:1课时测验:1课时讲评:1课时第一节有机化合物的分类【教学重点】了解有机化合物的分类方法,认识一些重要的官能团。
【教学难点】分类思想在科学研究中的重要意义。
【教学过程设计】【思考与交流】1.什么叫有机化合物?2.怎样区分的机物和无机物?有机物的定义:含碳化合物。
CO、CO2、H2CO3及其盐、氢氰酸(HCN)及其盐、硫氰酸(HSCN)、氰酸(HCNO)及其盐、金属碳化物等除外。
有机物的特性:容易燃烧;容易碳化;受热易分解;化学反应慢、复杂;一般难溶于水。
从化学的角度来看又怎样区分的机物和无机物呢?组成元素:C 、H、O N、P、S、卤素等有机物种类繁多。
(2000多万种)一、按碳的骨架分类:有机化合物链状化合物脂肪环状化合物脂环化合物化合物芳香化合物1.链状化合物这类化合物分子中的碳原子相互连接成链状。
(因其最初是在脂肪中发现的,所以又叫脂肪族化合物。
)如:CH3CH2CH2CH3CH3CH2CH2CH2OH正丁烷正丁醇2.环状化合物 这类化合物分子中含有由碳原子组成的环状结构。
它又可分为两类: (1)脂环化合物:是一类性质和脂肪族化合物相似的碳环化合物。
如:环戊烷环己醇(2)芳香化合物:是分子中含有苯环的化合物。
如:苯 萘二、按官能团分类:什么叫官能团?什么叫烃的衍生物?官能团:是指决定化合物化学特性的原子或原子团. 常见的官能团有:P.5表1-1烃的衍生物:是指烃分子里的氢原子被其他原子或原子团取代所生成的一系列新的有机化合物。
可以分为以下12种类型: 练习:1.下列有机物中属于芳香化合物的是( )2.〖归纳〗芳香族化合物、芳香烃、苯的同系物三者之间的关系:〖变形练习〗下列有机物中(1)属于芳香化合物的是_______________,(2)属于芳香烃的是________,(3)属于苯的同系物的是______________。
高二化学新课程培训苏教版选修B5《有机化学基础》解读“高中化学选修课程是在必修课程基础上为满足学生的不同需要而设置的。
设置了六个具有不同特点的选修课程模块,目的是为更好地体现高中化学课程的选择性,满足学生个性发展的多样化需要”。
选修模块共有6个模块,这些模块可以分为两大类:社会类和学科类,如下表。
按选修课开设指导意见,选化学的学生要学习3-4个选修模块。
其中理科学生:《化学反应原理》《有机化学基础》《实验化学》属于选修IA,即选修中的必修,《化学与生活》《化学与技术》为选修IB,《物质结构与性质》为选修IC;文科学生对《化学与生活》《化学与技术》两个模块中任选一个模块,属于选修IA。
《有机化学基础》是普通高中化学课程的6个选修模块之一,供对有机化学感兴趣的高中学生选择学习。
作为选修课程,《有机化学基础》学习的基础是义务教育阶段化学课程和普通高中必修化学课程中的有机化学知识。
根据《普通高中化学课程标准(实验)》编写的《有机化学基础》模块教材按专题组织教学内容,共分5个专题:专题1“认识有机化合物”、专题2“有机物的结构与分类”、专题3“常见的烃”、专题4“烃的衍生物”、专题5“生命活动的物质基础”。
在《普通高中化学课程标准(实验)》中,《有机化学基础》的内容主题分为4个,分别是:主题1“有机化合物的组成与结构”、主题2“烃及其衍生物的性质与应用”、主题3“糖类、氨基酸和蛋白质”和主题4“合成高分子化合物”。
可见,教材的专题1和专题2涵盖了内容标准中主题1的内容,专题3和专题4涵盖了内容标准中主题2的内容,专题5的内容即内容标准中主题3的内容,而内容标准中主题4的内容主要被安排在教材的专题3和专题4中。
一、教材的地位和作用1.高中化学课程标准的要求“有机化学基础”是为高中学生提供的选修课程模块。
通过本课程模块的学习,学生应主要在以下几个方面得到发展:1. 初步掌握有机化合物的组成、结构、性能等方面的基础知识。
高中化学学习材料(精心收集**整理制作)2015年苏教版高中化学选修5有机化学基础专题同步练习训练专题1 第1单元1.下列叙述:①我国科学家在世界上第一次人工合成结晶牛胰岛素;②最早发现电子的是英国科学家道尔顿;③创造联合制碱法的是我国著名科学家侯德榜;④首先制得氧气的是法国科学家拉瓦锡;⑤首先在实验室合成尿素的是维勒,其中正确的是A.只有①B.①和③C.①③⑤D.①②③④2.人类第一次用无机化合物人工合成的有机物是()A.乙醇B.食醋C.甲烷D.尿素3.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如下所示,它属于()A.无机物B.烃C.高分子化合物D.有机物4.环境毒品“二英”是目前人类制造的可怕的化学物质,其结构简式如图所示(),它属于A.高分子化合物B.芳香烃C.烃D.有机物5.萤火虫会在夏日的夜空发出点点光亮,这是一种最高效的发光机制。
萤火虫发光的原理是荧光素在荧光酶和ATP催化下发生氧化还原反应时伴随着化学能转变为光能:荧光素属于()A.无机物B.烃C.烃的衍生物D.高分子化合物6.(热点题)北京国家游泳馆“水立方”是在国内首次采用膜结构的建筑,以钢材为支架,覆盖ETFE薄膜。
ETFE是乙烯和四氟乙烯的共聚物,是一种轻质透明的新材料。
(1)该材料属于________。
A.新型无机非金属材料B.金属材料C.有机高分子材料D.复合材料(2)下列说法错误的是________。
A.ETFE极易分解,符合环保要求B.ETFE韧性好,拉伸强度高C.ETFE比玻璃轻、安全D.ETFE是纯净物,有固定的熔点E.CFCF2和CH2CH2均是平面分子(3)写出由乙烯和四氟乙烯共聚生成ETFE的反应方程式________________________________________________________________________。
专题1 第2单元1.下列有机物在H-NMR上只给出一组峰的是()A.HCHO B.CH3OHC.HCOOH D.CH3COOCH32.实验测得某碳氢化合物A中,含碳80%,含氢20%,又测得该化合物的相对分子质量是30,该化合物的分子式是()A.CH4B.C2H6 C.C2H4D.C3H63.下列具有手性碳原子的分子是()4.某有机物C3H6O2的核磁共振氢谱中有两个共振峰,面积比为1∶1,该有机物的结构简式是()5.某含C 、H 、O 三种元素的有机物,其C 、H 、O 的质量比为6∶1∶8,它的实验式为________,该有机物蒸气的密度是相同条件下氢气密度的30倍,则该有机物的分子式为________。
6.(实验题)为测定一种气态烃的化学式,取一定量的A 置于密闭容器中燃烧,定性实验表明产物是CO 2、CO 和水蒸气。
学生甲、乙设计了如下两个方案,均认为根据自己的方案能求出A 的最简式。
他们测得的有关数据如下(图中的箭头表示气体的流向,实验前系统内的空气已排除):甲方案:燃烧产物――→浓硫酸增重――→碱石灰增重――→点燃生成CO 2 2.52 g 1.32 g 1.76 g 乙方案:燃烧产物――→碱石灰增重――――→灼热CuO减轻――→石灰水增重 5.6 g 0.64 g 4 g 试回答:(1)根据两方案,你认为能否求出A 的最简式(填“能”或“不能”)? 甲方案:________;乙方案:________。
(2)根据你选出的方案,求出A 的最简式(实验式)为________________________________________________________________________ ________________________________________________________________________。
(3)若要确定A 的化学式,是否还需要测定其他数据?如果需要,应该测定哪些数据? ________________________________________________________________________ ________________________________________________________________________。
专题2 第1单元1.下列分子中,所有原子不可能共处在同一平面上的是( ) A .C 2H 2 B .CS 2 C .NH 3D .C 6H 62.下列属于碳链异构的是( ) A .CH 3CH 2CH 2CH 3和CH 3CH(CH 3)2 B .CH 2===C(CH 3)2和CH 3CH===CHCH 3 C .CH 3CH 2OH 和CH 3OCH 3D .CH 3CH 2CH 2COOH 和CH 3COOCH 2CH 33.某化合物的分子式是C 5H 11Cl ,实验结果表明:分子中有2个—CH 3、2个—CH 2—、1个和1个—Cl,它的结构有几种(不考虑对映异构现象)()A.2 B.3 C.4 D.54.下列各组物质与CH3CH2C(CH3)2CH2CH3互为同分异构体的是()A.CH3(CH2)4CH(CH3)2B.(CH3CH2)3CHC.(CH3)2C(CH2CH3)2D.CH3CHBrC(CH3)2CH2CH35.(热点题)有效地利用现有能源和开发新能源已受到各国的普遍重视。
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。
例如,加入CH3OC(CH3)3来生产“无铅汽油”。
CH3OC(CH3)3分子中必存在的原子间连接形式有________(填写编号,下同)。
(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要成分是________。
能说明它是正四面体而非平面正方形结构的理由是________(填字母代号)。
a.其一氯取代物不存在同分异构体b.其二氯取代物不存在同分异构体c.它是非极性分子d.它的键长和键角都相等(3)1980年我国首次制成一辆燃氢汽车,乘员12人,以50公里/小时行驶了40公里。
为了有效发展民用氢能源,首先必须制得廉价的氢气。
下列可供开发又较经济的制氢方法是________。
A.电解水B.锌和稀硫酸反应C.光解海水其次,制得纯氢气后还需要解决的问题是________(写出其中一个)。
专题2 第2单元1.下列各组物质中互为同系物并且有关其原因的叙述也正确的是()A.乙烯和环丙烷:分子组成相差1个CH2原子团B.甲醛(CH2O)和丙烷(C3H8):相对分子质量相差14,正好是CH2的式量C.乙醇(C2H6O)与水(H2O):相对分子质量相差28,正好是两个CH2的式量D.甲烷和十七烷(C17H36):它们都是烷烃,结构相似,组成相差16个CH2原子团2.下列各物质中,互为同系物的一组是()①C2H5COOH②C6H5COOH③C15H31COOH④C17H31COOH⑤CH2===CH—COOH⑥CH3CH2CHO A.①③B.③④ C.④⑤D.⑤⑥3.下列烷烃命名的名称中,正确的是()A.4-甲基-4,5-二乙基己烷B.3-甲基-2,3-二乙基己烷C.4,5-二甲基-4-乙基庚烷D.3,4-二甲基-4-乙基庚烷4.下列有机物命名正确的是()A.2-乙基丙烷:B.CH3CH2CH2CH2OH:1-丁醇C.:间二甲苯D.:2-甲基-2-丙烯5.下列四种烃的名称所表示的物质,命名正确的是________。
不可能存在的是________。
A.2-甲基-2-丁炔B.2-乙基丙烷C.3-甲基-2-丁烯D.2-甲基-2-丁烯6.(1)按系统命名法给下列有机物命名:①________。
②________。
(2)写出下列有机化合物的结构简式。
①2,2,3-三甲基-3-乙基己烷:_________________________________________________。
②2-甲基-3-乙基庚烷:______________________________________________________。
7.(探究题)如图所示是由4个碳原子结合成的6种有机物(氢原子没有画出)。
(1)写出有机物a的系统命名法的名称:____________。
(2)有机物a有一种同分异构体,试写出其结构简式:________________________________________。
(3)上述有机物中与c 互为同分异构体的是________(填代号)。
(4)任写一种与e 互为同系物的有机物的结构简式:___________________________________。
(5)上述有机物中不能与溴水反应使其褪色的有__________(填代号)。
(6)a 、b 、c 、e 四种物质中,4个碳原子一定处于同一平面的有__________(填代号)。
专题3 第1单元1.下列有机反应中,不.属于取代反应的是( ) A .+Cl 2――→光照+HClB .2CH 3CH 2OH +O 2――→Cu△2CH 3CHO +2H 2O C .ClCH 2CH===CH 2+NaOH ――→H 2O△HOCH 2CH===CH 2+NaCl D .+HO —NO 2――→浓硫酸△+H 2O2.下列有关烃的说法正确的是( )A .乙烯和乙炔中都存在碳碳双键B .甲烷和乙烯都可与氯气反应C .高锰酸钾可以氧化甲烷和乙炔D .乙烯可以与氢气发生加成反应,但不能与H 2O 加成 3.下列反应的生成物为纯净物的是( )A .CH 4和Cl 2光照发生取代反应B .1,3-丁二烯与等物质的量的溴发生反应C .乙炔在空气中的燃烧反应D .乙烯和氯化氢加成 4.对下列有机反应类型的认识中,错误的是( ) A .+HNO 3――→浓硫酸△+H 2O ;取代反应B .CH 2===CH 2+Br 2―→CH 2Br —CH 2Br ;加成反应C .2CH 3CH 2OH +O 2――→Cu△2CH 3CHO +2H 2O ;取代反应 D .CH 3COOH +CH 3CH 2OH ―――→浓H 2SO 4△CH 3COOCH 2CH 3+H 2O ;酯化反应 5.石油裂解的目的是( )A .提高轻质液体燃料的产量B .主要是提高汽油的产量C .获得短链不饱和气态烃D .主要是提高汽油的质量6.(实验题)把1体积CH 4和4体积Cl 2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是:(1)__________________ ______;(2)________________________;(3)________________________;(4)________________________。