苏教版高中化学选修五《有机化学基础》知识点整理.doc
- 格式:doc
- 大小:909.38 KB
- 文档页数:11

高二化学选修5《有机化学基础》知识点整理2010-2-26一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

高二化学选修5《有机化学基础》知识点整理2010-2-26一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

高二化学选修5 有机化学基础知识点整理----74b58128-7166-11ec-88da-7cb59b590d7d高二化学选修5有机化学基础知识点整理高二化学选修课5[有机化学基础]知识点的安排高二化学选修5《有机化学基础》知识点整理2022-2-26一、重要的物理性质1.有机物的溶解性(1)不溶于水:各种碳氢化合物、卤代烃、硝基化合物、酯类、大多数聚合物、高级(指分子中含有大量碳原子的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指n(c)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐,单糖,双糖。
(它们都能与水形成氢键)。
(3)具有特殊的溶解性:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇也常用作反应溶剂,使参与反应的有机物和无机物溶解,增加接触面积,提高反应速率。
例如,在油的皂化反应中,加入乙醇可以溶解NaOH和油,使它们在均相(同一溶剂的溶液)中充分接触,从而加快反应速度,提高反应极限。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高在65℃时可与水混溶。
冷却后,它是分层的。
上层为苯酚水溶液,下层为苯酚水溶液。
摇动后形成乳状液。
由于可溶钠盐的形成,苯酚很容易溶于碱溶液和苏打溶液。
③ 乙酸乙酯更不溶于饱和碳酸钠溶液,饱和碳酸钠溶液也能通过反应被吸收和挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④ 一些淀粉和蛋白质可以溶解在水中形成胶体。
蛋白质溶于浓缩的轻金属盐(包括铵盐)度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤ 线性和部分支化聚合物可溶于某些有机溶剂,而主体类型难以溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色解决方案2.有机质密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)超过水的密度并与水(溶液)分层:多氯烃、溴化烃(溴苯等)、碘化烃和硝酸盐3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 碳氢化合物:一般为n(c)≤ 4.② 衍生产品:一氯甲烷(ch3cl,沸点为-24.2℃)氟里昂(ccl2f2,沸点为-29.8℃)氯乙烯(ch2==chcl,沸点为-13.9℃)甲醛(hcho,沸点为-21℃)氯乙烷(ch3ch2cl,沸点为12.3℃)一溴甲烷(ch3br,沸点为3.6℃)注:新戊烷[C(CH3)4]也是气态的四氟乙烯(cf2==cf2,沸点为-76.3℃)甲醚(ch3och3,沸点为-23℃)*甲乙醚(ch3oc2h5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液体:通常指n(c)在5到16之间的碳氢化合物和大多数低级衍生物。

有机化学知识点归纳(一)一、有机物的结构与性质1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无;通式:CnH2n+2;代表物:CH4B) 结构特点:键角为109°28′,空间正四面体分子。
烷烃分子中的每个C原子的四个价键也都如此。
C) 化学性质:(2)烯烃:A) 官能团:;通式:CnH2n(n≥2);代表物:H2C=CH2B) 结构特点:键角为120°。
双键碳原子与其所连接的四个原子共平面。
C) 化学性质:(3)炔烃:A) 官能团:—C≡C—;通式:CnH2n—2(n≥2);代表物:HC≡CHB) 结构特点:碳碳叁键与单键间的键角为180°。
两个叁键碳原子与其所连接的两个原子在同一条直线上。
(4)苯及苯的同系物:A) 通式:CnH2n—6(n≥6);代表物:B)结构特点:苯分子中键角为120°,平面正六边形结构,6个C原子和6个H原子共平面。
C)化学性质:①取代反应(与液溴、HNO3、H2SO4等)(5)醇类:A) 官能团:—OH(醇羟基);代表物:CH3CH2OH、HOCH2CH2OHB) 结构特点:羟基取代链烃分子(或脂环烃分子、苯环侧链上)的氢原子而得到的产物。
结构与相应的烃类似。
C) 化学性质:(与官能团直接相连的碳原子称为α碳原子,与α碳原子相邻的碳原子称为β碳原子,依次类推。
与α碳原子、β碳原子、……相连的氢原子分别称为α氢原子、β氢原子、……)④酯化反应(跟羧酸或含氧无机酸)(6)醛酮B) 结构特点:醛基或羰基碳原子伸出的各键所成键角为120°,该碳原子跟其相连接的各原子在同一平面上。
C) 化学性质:(7)羧酸3、常见糖类、蛋白质和油脂的结构和性质(1)单糖A) 代表物:葡萄糖、果糖(C6H12O6)B) 结构特点:葡萄糖为多羟基醛、果糖为多羟基酮C) 化学性质:①葡萄糖类似醛类,能发生银镜反应、费林反应等;②具有多元醇的化学性质。

选修5有机化学基础知识点整理有机化学基础知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物.②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(.....CH..3.Cl..,.沸点为...-.24.2℃.....).氟.里昂(...CCl...2.F.2.,沸点为....-.29.8℃.....).氯乙烯(....CH..2.==CHCl......,沸点为....-.13.9℃.....).甲.醛(..HCHO....,沸点为....-.21℃...).氯乙烷(....CH..3.CH..2.C.l.,沸点为....12.3....℃.).一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

高二化学选修5《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解④有的淀粉、蛋白质可溶于水形成胶体..度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
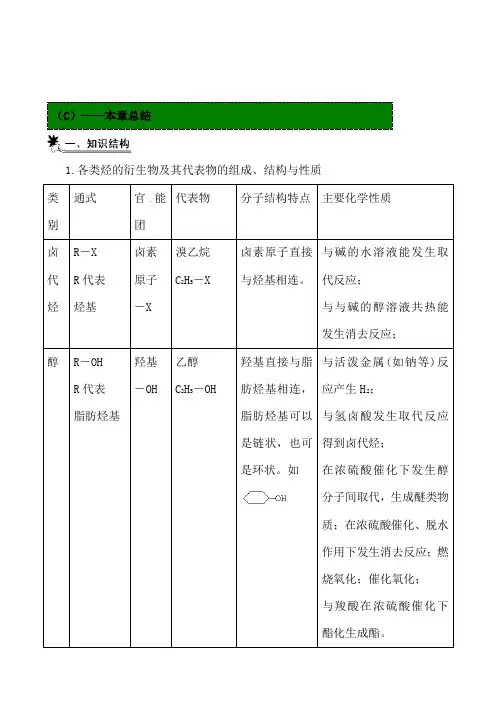
(C)——本章总结1.各类烃的衍生物及其代表物的组成、结构与性质H在浓硫酸催化下发生醇与甲醛发生缩聚有极性,有极性,2.有机物之间的相互转化关系(卤代烃、醇、醛、羧酸、酯的相互转化关系)3.醇、醛、酸、酯转化关系的延伸4.烃的羟基衍生物比较5.烃的羰基衍生物比较6.有机反应主要类型归纳、加氢反应、专题一 有机物的类别与通式有机化合物种类多,要以一些典型的烃类衍生物(乙醇、溴乙烷、苯酚、乙醛、乙酸、乙酸乙酯、脂肪酸、甘油酯、多羟基醛酮、氨基酸等)为例,了解官能团在化合物中的作用。
掌握各主要官能团的性质和主要化学反应,并能结合同系物原理加以应用。
例 1 二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。
二甘醇的结构简式是HO —CH 2CH 2—O —CH 2CH 2—OH 。
下列有关二甘醇的叙述正确的是A.不能发生消去反应B.能发生取代反应C.能溶于水,不溶于乙醇D.符合通式C n H 2n O 3解析:与-OH 相连的碳的邻位碳原子上有氢,所以能发生消去反应,能与羧酸发生酯化反应,是取代反应,所以B 正确。
根据相似相溶原理二甘醇含羟基(-OH ),所以它既能溶于H 2O ,也能溶于乙醇。
它的分子式为C 4H 10O 3。
二甘醇的通式应是C n H 2n+2O 3,不符合D 项中的通式。
答案:B 。
点拨:有机反应的复杂性和有机物种类的多样性,导致了有机反应类型的多样性,各类反应皆有自己的特征,这也与官能团的特征是分不开的。
例2 A 、B 、C 、D 、E 五种芳香化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。
它们的结构简式如下所示:3 3 CH 2CH=CH 2 CH 2CH=CH 2 CH 2CH=CH 2 CH 2CH=CH 2A B C D E请回答下列问题:⑴这五种化合物中,互为同分异构体的是_______________。
⑵W 氧化反应①−→−−反应②−→−−X反应①采取了适当措施,使分子中烯键不起反应。
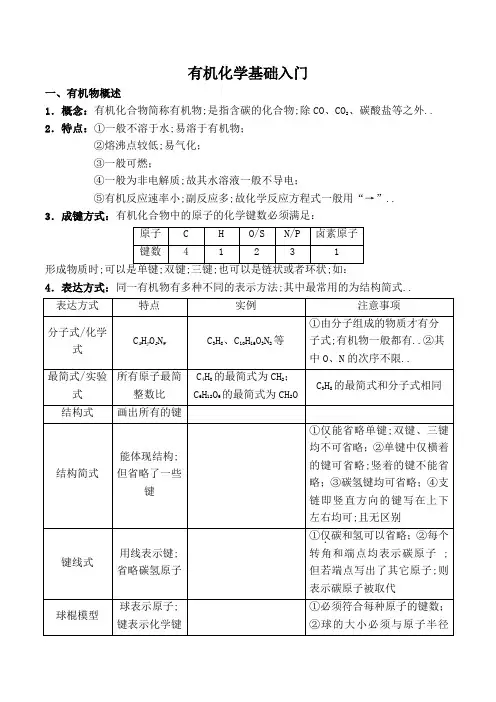
有机化学基础入门一、有机物概述、碳酸盐等之外.. 1.概念:有机化合物简称有机物;是指含碳的化合物;除CO、CO22.特点:①一般不溶于水;易溶于有机物;②熔沸点较低;易气化;③一般可燃;④一般为非电解质;故其水溶液一般不导电;⑤有机反应速率小;副反应多;故化学反应方程式一般用“→”..3.成键方式:有机化合物中的原子的化学键数必须满足:形成物质时;4.表达方式:同一有机物有多种不同的表示方法;其中最常用的为结构简式..简式..5.同分异构现象:即相同分子式;不同结构的现象..相互间互称为同分异构体..如:6.取代基与官能团1取代基:指有机物去氢后剩余的原子或原子团;它们均是一个有机片段;可以相互连接成有机物..如:2官能团:指能体现有机物特殊性质的原子或原子团;由此可划物质类别..如:二、烷烃1.定义:烃分子中的碳原子之间只以单键结合成链状;碳原子剩余的价键全部跟氢原子相结合;使每个碳原子的化合价都已充分利用;都达到“饱和”..这样的烃叫做饱和烃;又叫烷烃..1关键词:①烃:指只含C和H的有机物;②饱和烃:指只含单键;不含碳碳双键、碳碳三键的烃..类似有饱和醇、饱和醛等;③链状:链状的饱和烃叫烷烃;环状的饱和烃叫环烷烃..2烷烃的通式:C n H2n+2..任何有机物的氢原子数都不能大于烷烃;比如C10H24O3N不存在..2.同系物:即同一系列的物质..比如烷烃这一系列互称为同系物;环烷烃之间也互为同系物;但烷烃和环烷烃之间不是同系物..它的概念是指结构相似;分子组成相差若干个不小于1个CH2的有机物之间..1关键词:①结构相似:指含有相同的官能团;②分子组成:指分子式上相差CH2;而不是结构式上相差..2“四同”比较:3.烷烃的命名1普通命名法:又称为习惯命名法;用于简单有机物的命名..①碳原子数在10个以内;依次用“天干”甲、乙、丙、丁、戊、已、庚、辛、壬、癸代表碳原子数;其后加上“烷”字;碳原子数在10个以上;用汉字数字表示如十二烷..②同一烷烃;出现同分异构体时;支链由少到多依次加上前缀;正异新..如:2系统命名法:适用于任何有机物的系统的命名方法..步骤:①选主链.. 原则:a、碳链最长;b、一样长时;支链最多..如:②对主链碳编号.. 原则:a、从支链近端开始编号;b、一样时;甲基优先..如:③命名.. 原则:a、先简单基团再复杂基团;b、阿拉伯数字之间用“;”相隔;阿拉伯数字和汉字之间用“-”相连;如:4.等效氢与卤代物种类数1等效氢:即相同效果的氢..因为有机物是空间结构;故其在纸平面上只是投影;凡是在空间中一样的H原子即称为等效氢;它们被卤素取代后的产物相同..等效氢有两种:①对称;②旋转重合..如:2一卤代物:即用一个卤素原子取代一个氢原子剩下的有机物..有几种等效氢就有几种一卤代物..如:3二卤代物:即一卤代物的一卤代物..方法是先用等效氢找出一卤代物;再找它的一卤代物..如:4多卤代物:若烷烃有n个氢;则其m卤代物m<n种类数与n-m卤代物种类数相同..如:C 3H8的二氯代物和六氯代物种类数都是4种;因为前者是找两个氯的相对位置;后者是找两个氢的相对位置..5.同分异构体的书写:方法是先写碳骨架;再补充氢原子利用碳四个键;具体规则为:①主链碳由长到短;②支链碳由中间到两边;注意避免重复;不能改变主链碳数;③两个支链时;先定一个;再定另一个..如:6.有机物的物理性质1溶解性:有机物除了醇、醛、酸外基本均不溶于水;有机物和有机物是互溶的..2密度:有机物密度一般比水小;比水大的常见物质是:CCl4、溴苯、硝基苯等..3熔沸点:同系物随相对分子质量增大;熔沸点升高..如烷烃随碳数增加;熔沸点增大;烷烃的同分异构体之间;支链越多;熔沸点越低;如正戊烷>异戊烷>新戊烷..常温下碳数小于等于4的烃为气态;烃的含氧衍生物仅HCHO甲醛为气体..4颜 色:高中阶段的有机物一般为无色.. 7.烷烃的化学性质1燃烧:有机物完全燃烧产物均为CO 2、H 2O 等;不完全燃烧会产生黑烟碳单质、CO 等..①烃的完全燃烧通式:222C H ()O CO H O 42点燃++−−−→+x y yy x x②规律:a 、求算nCO 2:nH 2O;只能求最简式;要求分子式得算n 有机物:nCO 2:nH 2O;即1mol 有机物燃烧得x mol 碳和y mol 氢;b 、等物质的量....的烃耗氧量大小;比较4+yx 即可..如:C 3H 84+y x =5比C 4H 64+y x =5.5耗氧量小;c 、等质量..的烃耗氧量大小;比较y x 即可..如:C 3H 8yx=2.67比C 4H 64+y x =1.5耗氧量大..2取代反应:即取而代之的意思..烷烃有几个氢原子;就可以被卤素原子取代几次..如: 产物为它们的混合物..产物中CH 3Cl 为气体;其它三种有机产物为液体..同理;每mol 乙烷C 2H 6最多可以与6mol Cl 6反应;共有1+2+2+2+1+1=9种有机产物.. 3烷烃的高温裂解:烷烃受热均可分解;产物为C 、烯烃、炔烃等..如:81841048C H C H C H 高温−−−→+ 或 818383624C H C H C H +C H 高温−−−→+等。

选修5有机化学基础知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(....-.29.8℃.....).....CCl...2.F.2.,沸点为.....CH..3.Cl..,.沸点为...-.24.2℃.....).氟里昂(氯乙烯(...HCHO....,沸点为....-.21℃...)......).甲醛(....-.13.9℃..2.==CHCl....CH......,沸点为氯乙烷(....12.3....℃.).一溴甲烷(CH3Br,沸点为3.6℃)..2.C.l.,沸点为..3.CH....CH四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。

高二化学选修5《有机化学基础》知识点整理2010-2-26一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为℃)氟里昂(CCl2F2,沸点为℃)氯乙烯(CH2==CHCl,沸点为℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为℃)一溴甲烷(CH3Br,沸点为℃)四氟乙烯(CF2==CF2,沸点为℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为℃)*环氧乙烷(,沸点为℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
高二化学选修5《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
高中化学学习材料《有机化学基础》知识点整理一、重要的物理性质1. 有机物的溶解性(1) 难溶于水:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的醇、醛、羧酸等。
(2) 易溶于水:低级[n(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(都能与水形成氢键)。
(3) 具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2. 有机物的密度(1) 小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2) 大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3. 有机物的状态[常温常压(1个大气压、20℃左右)](1) 气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2=CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2=CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2) 液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
如,己烷CH3(CH2)4CH3环己烷甲醇CH3OH 甲酸HCOOH溴乙烷C2H5Br 乙醛CH3CHO溴苯C6H5Br 硝基苯C6H5NO2★特殊:不饱和程度高的高级脂肪酸甘油酯,如植物油脂等在常温下也为液态(3) 固态:一般N(C)在17或17以上的链烃及高级衍生物,如,石蜡。
12C以上的烃饱和程度高的高级脂肪酸甘油酯,如动物油脂在常温下为固态。
★特殊:苯酚(C6H5OH)、苯甲酸(C6H5COOH)、氨基酸等在常温下亦为固态4.有机物的颜色☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色,常见的如下所示:三硝基甲苯(俗称TNT)为淡黄色晶体;部分被空气中氧气所氧化变质的苯酚为粉红色;2, 4, 6−三溴苯酚为白色、难溶于水的固体(但易溶于苯等有机溶剂);苯酚溶液与Fe3+溶液作用形成紫色[H3Fe(OC6H5)6]溶液;多羟基有机物如甘油、葡萄糖等能使新制的氢氧化铜悬浊液溶解生成绛蓝色溶液;淀粉溶液(胶体)遇碘(I2)变蓝色溶液;含苯环的蛋白质溶胶遇浓硝酸会有白色沉淀产生,加热或较长时间后,沉淀变黄色。
5. 有机物的气味许多有机物具有特殊的气味,但在中学阶段只需要了解下列有机物的气味:物质名称气味物质名称气味甲烷无味乙烯稍有甜味(植物生长的调节剂) 液态烯烃汽油的气味乙炔无味苯及其同系物芳香气味,有一定的毒性一卤代烷不愉快气味,有毒,避免吸入二氟二氯甲烷(氟里无味气体,不燃烧4C以下的一元醇有酒味的流动液体昂)5C~11C的一元醇不愉快气味的油状液体12C以上的一元醇无嗅无味的蜡状固体乙醇特殊香味乙二醇甜味(无色黏稠液体)丙三醇(甘油)甜味(无色黏稠液体)苯酚特殊气味乙醛刺激性气味乙酸强烈刺激性气味(酸味)低级酯果香气味丙酮令人愉快的气味二、重要的反应1. 能使溴水(Br2/H2O)褪色的物质(1) 有机物①通过加成反应使之褪色:含有、−C≡C−的不饱和化合物②通过取代反应使之褪色:酚类(注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
)③通过氧化反应使之褪色:含有−CHO(醛基)的有机物(有水参加反应)(注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色)④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯(2) 无机物①通过与碱发生歧化反应:3Br2 + 6OH- ══ 5Br- + BrO3- + 3H2O或Br2 + 2OH-══ Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2. 能使酸性高锰酸钾溶液KMnO4/H+褪色的物质(1) 有机物:含有、−C≡C−、−OH(较慢)、−CHO的物质与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应)(2) 无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+3. 与Na反应的有机物:含有−OH、−COOH的有机物与NaOH反应的有机物:常温下易与含有酚羟基、−COOH的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na2CO3反应的有机物:含有酚羟基的有机物反应生成酚钠和NaHCO3;含有−COOH的有机物反应生成羧酸钠,并放出CO2气体;含有−SO3H的有机物反应生成磺酸钠并放出CO2气体。
与NaHCO3反应的有机物:含有−COOH、−SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
4.既能与强酸,又能与强碱反应的物质(1) 2Al + 6H+══2 Al3+ + 3H2↑2Al + + 2H2O ══+ 3H2↑(2) Al2O3 + 6H+ ══ 2 Al3+ + 3H2O Al2O3 + ══+ H2O(3) Al(OH)3 + 3H+══ Al3+ + 3H2O Al(OH)3 + ══+ 2H2O(4) 弱酸的酸式盐,如NaHCO3、NaHS等等NaHCO3 + HCl ══ NaCl + CO2↑ + H2O NaHCO3 + NaOH ══ Na2CO3 + H2ONaHS + HCl ══ NaCl + H2S↑NaHS + NaOH ══ Na2S + H2O(5) 弱酸弱碱盐,如CH3COONH4、(NH4)2S等等2CH3COONH4 + H2SO4══ (NH4)2SO4 + 2CH3COOHCH3COONH4 + NaOH ══ CH3COONa + NH3↑+ H2O(NH4)2S + H2SO4══ (NH4)2SO4 + H2S↑(NH4)2S +2NaOH ══ Na2S + 2NH3↑+ 2H2O(6) 氨基酸,如甘氨酸等H2NCH2COOH + HCl → HOOCCH2NH3Cl H2NCH2COOH + NaOH → H2NCH2COONa + H2O(7) 蛋白质分子中的肽链的链端或支链上仍有呈酸性的−COOH和呈碱性的−NH2,故蛋白质仍能与碱和酸反应。
5. 银镜反应的有机物(1) 发生银镜反应的有机物:含有−CHO的物质:醛、甲酸、甲酸盐、甲酸酯、还原性糖(葡萄糖、麦芽糖等)(2) 银氨溶液[Ag(NH3)2OH](多伦试剂)的配制:向一定量2%的AgNO3溶液中逐滴加入2%的稀氨水至刚刚产生的沉淀恰好完全溶解消失。
(3) 反应条件:碱性、水浴加热若在酸性条件下,则有Ag(NH3)2+ ++ 3H+══ Ag+ + 2NH4+ + H2O而被破坏。
(4) 实验现象:①反应液由澄清变成灰黑色浑浊;②试管内壁有银白色金属析出(5) 有关反应方程式:AgNO3 + NH3·H2O ══ AgOH↓ + NH4NO3 AgOH + 2NH3·H2O ══ Ag(NH3)2OH + 2H2O银镜反应的一般通式: RCHO + 2Ag(NH3)2OH 2 Ag↓+ RCOONH4 + 3NH3 + H2O甲醛(相当于两个醛基):HCHO + 4Ag(NH3)2OH4Ag↓+ (NH4)2CO3 + 6NH3 + 2H2O乙二醛:OHC−CHO + 4Ag(NH3)2OH4Ag↓+ (NH4)2C2O4 + 6NH3 + 2H2O甲酸:HCOOH + 2Ag(NH3)2OH2Ag↓+ (NH4)2CO3 + 2NH3 + H2O葡萄糖:CH2OH(CHOH)4CHO +2Ag(NH3)2OH2Ag↓+CH2OH(CHOH)4COONH4+3NH3 + H2O(6) 定量关系:−CHO + 2Ag(NH3)2OH→2Ag HCHO + 4Ag(NH3)2OH→4Ag6. 与新制Cu(OH)2悬浊液(斐林试剂)的反应(1) 有机物:羧酸(中和)、甲酸(先中和,但NaOH仍过量,后氧化)、醛、还原性糖(葡萄糖、麦芽糖)、甘油等多羟基化合物。
(2) 斐林试剂的配制:向一定量10%的NaOH溶液中,滴几滴2%的CuSO4溶液,得到蓝色絮状悬浊液。
(3) 反应条件:碱过量、加热煮沸(4) 实验现象:①若有机物只有官能团醛基,则滴入新制的氢氧化铜悬浊液中,常温时无变化,加热煮沸后有(砖)红色沉淀生成;②若有机物为多羟基醛(如葡萄糖),则滴入新制的氢氧化铜悬浊液中,常温时溶解变成绛蓝色溶液,加热煮沸后有(砖)红色沉淀生成;(5) 有关反应方程式:2NaOH + CuSO4══ Cu(OH)2↓+ Na2SO4 RCHO + 2Cu(OH)2RCOOH + Cu2O↓+ 2H2OHCHO+4Cu(OH)2CO2+2Cu2O↓+5H2O OHC−CHO + 4Cu(OH)2HOOC−COOH + 2Cu2O↓+ 4H2OHCOOH+2Cu(OH)2CO2+Cu2O↓+3H2O CH2OH(CHOH)4CHO+2Cu(OH)2CH2OH(CHOH)4COOH+Cu2O↓+2H2O(6) 定量关系:−COOH + ½ Cu(OH)2~½→Cu2+(酸使不溶性的碱溶解)−CHO + 2Cu(OH)2→Cu2O HCHO + 4Cu(OH)2→2Cu2O7. 能发生水解反应的有机物是:卤代烃、酯、糖类(单糖除外)、肽类(包括蛋白质)。