第三讲 酶学基础
- 格式:ppt
- 大小:1.14 MB
- 文档页数:66

第三章酶Enzyme一、授课章节及主要内容:第四章酶二、授课对象:临床医学、预防、法医(五年制)、临床医学(七年制)三、授课学时本章共6学时4节课时(每个课时为45分钟)。
讲授安排如下:第一学时:概述;第一节酶的分子结构与功能第二学时:第二节酶促反应的特点与机制第三、四、五学时:酶促反应机制;第三节酶动力学第六学时:第四节酶的调节四、教学目的与要求在掌握蛋白质结构与功能的基础上进一步掌握酶活性中心的结构与功能;酶促反应的特点与机制;酶动力学的概念及影响酶促反应的因素以及机体如何调节酶活性,为临床学习与应用打下基础。
五、重点与难点重点:掌握酶活性中心的概念;酶促反应的特点与机制;酶动力学的概念及影响酶促反应的因素。
难点:抑制剂对酶活性的影响六、教学方法及授课大致安排以面授为主,适当结合临床提问启发。
每次课预留5分钟小结本次课掌握内容及预留复习题,全章结束后小结本章内容。
七、主要外文专业词汇八、思考题1. 试述酶能加速化学反应的机制。
2. 试述在酶促反应中酶蛋白与辅酶(辅基)的相互关系。
3. 比较三种可逆性抑制作用的特点。
4. 试述竞争性抑制的特点及磺胺类药物抑菌的机制。
5. 别构调节有何生理意义?九、教材与教具:人民卫生出版社《生物化学》第六版十、授课提纲(或基本内容)概述Introduction一.酶的生物学重要性一切生物都须不断地进行新陈代谢过程,以维持它们的生命活动,而酶是生物用以进行代谢过程的工具。
因为物质代谢过程都需要酶的催化作用,在体内只有极少数不需酶参加而自发进行的化学反应。
有些在体外能自发进行的化学反应例:H2O+CO2 = H2CO3。
在体内也要依赖特殊的酶---碳酸酐酶的催化。
在酶的作用下,生物体内复杂的化学反应,能在温和的条件下迅速,准确,平稳而且有规律的进行。
我们来看看食物蛋白质在体内外的分解情况:在体内温和的条件(近中性pH。
37℃)下食物蛋白质就能迅速彻底水解成AA,而且AA不会遭破坏。

第3讲酶和ATP★ [最新考纲]1.酶在代谢中的作用(Ⅱ);2.ATP在能量代谢中的作用(Ⅱ)。
精读教材——记一记1.Fe3+和过氧化氢酶促使H2O2分解,但它们并未供给H2O2能量,而是降低了H2O2分解反应的活化能。
(P80正文上部)2.酸既能催化蛋白质水解,又能催化脂肪和淀粉水解。
(P83右边学科交叉)3.建议用淀粉酶探究温度对酶活性的影响,用过氧化氢酶探究pH对酶活性的影响。
原因:温度(高温)本身会影响过氧化氢自然分解的速度;酸本身也可以作为无机催化剂催化淀粉的水解。
(P84实验)4.图5—3,5—4中,只有低温时曲线和横轴不相交,即酶的结构未改变,活性降低而已。
(P85图)5.酶为生活添姿彩(1)溶菌酶能溶解细菌的细胞壁而抗菌消炎,常与抗生素复合使用。
(2)加酶洗衣粉中的酶不是直接来自生物体,而是经过酶工程改造过的,稳定性更强。
(P87科学·技术·社会)6.(1)ATP的组成元素有C、H、O、N、P。
(P88相关信息)(2)细胞中绝大多数需要能量的生命活动都是由ATP直接提供能量的(只是绝大多数,不是所有)。
(P89正文)7.吸能反应一般与ATP水解的反应相联系,由ATP水解提供能量。
(P89正文下部)8.1分子葡萄糖彻底氧化分解所释放的能量是1分子ATP水解所释放能量的94倍。
(P90思考与讨论)自我诊断——判一判1.有关酶的正误判断(1)酶的基本组成单位是氨基酸和脱氧核糖核苷酸。
(×)(2)水稻细胞内合成的某物质,能够在常温下高效分解淀粉,该物质含有羧基。
(√)(3)滴加FeCl3溶液提高过氧化氢的分解速率不涉及“降低化学反应活化能”的原理。
(×)(4)过酸、过碱或温度过高,会使酶的空间结构遭到破坏,使酶永久失活。
(√)(5)(2018·全国Ⅱ卷,T3B)饥饿时,胰高血糖素水平升高,促进糖原分解,说明激素具有酶的催化活性。
(×)解析:激素不具有酶的催化特性。

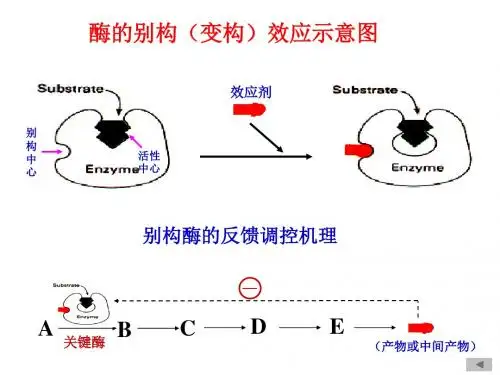

酶考纲考点酶学概论酶的概念酶的催化特点酶的组成酶底物的专一性酶的命名与分类影响酶促反应的因素酶促反应速度的测定多种因素对酶促反应的影响酶的作用机理酶的活性中心酶与底物分子的结合影响酶催化效率的因素别构酶同工酶诱导酶基本知识点酶通论新陈代谢是生命活动的基础,是生命活动最重要的特征,而构成新城代谢的许多复杂而有规律的物质变化和能量变化,都是在酶催化下进行的。
生物的生长发育、繁殖、遗传、运动、神经传导等生命活动都与酶的催化过程紧密相关,可以说没有酶的参与,生命活动一刻也不能进行。
Payen和Persoz 首先发现了酶Fisher提出了酶和底物的“锁与钥匙”学说,可以解释酶作用的专一性Henri提出了酶与底物的中间复合物学说Northrop和Kunitz得到了胃蛋白酶、胰蛋白酶和胰凝乳蛋白酶结晶,并用相应方法证明酶是一种蛋白质后,酶是蛋白质的属性才逐渐被人所接受。
Cech和Altman分别发现了具有催化功能的RNA-核酶,这一发现打破了人们对酶的传统观念。
酶与一般催化剂的比较酶作为生物催化剂和一般催化剂相比有其共同性,首先酶和其他催化剂一样,都能显著改善化学反应速率,使之加快达到平衡,但不能改变反应的反应常数,酶本身在反应前后也不发生变化。
在一个化学反应体系中个,因为各分子所含能量高低不同,每一瞬间并非全部反应物分子都能进行反应,只有那些具有高能量,处于活化态的分子即活化分子,反应中活化分子越多,则反映速率越快。
活化分子要比一般分子高出一定的能量称为活化能。
活化能定义:在一定温度下1摩尔底物全部进入活化态所需要的自由能反应所需活化能越高,相对的活化分子就越少,反应速率越慢。
在有催化剂存在时,由于催化剂能瞬时的与反应物结合成过渡态,因而降低了反应所需的活化能。
酶作为催化剂比一般催化剂更能显著得降低活化能,催化效率更高酶作为生物催化剂的特点1.酶易失活:酶是细胞产生的生物大分子,凡能使生物大分子变性的因素都能够使酶失去催化活性2.酶具有很高的催化效率:通常用酶的转换数(TN)来表示酶的催化效率,是指在一定条件下每个酶分子转换底物的分子数,3.酶具有高度专一性:所谓高度专一性是指酶对催化的反应和反应物有严格的选择性。




