中考化学一轮复习重点题型突破专题一化学思想方法精练
- 格式:pptx
- 大小:2.82 MB
- 文档页数:30

一、中考初中化学流程图1.硅是一种重要的半导体材料,应用范围广。
三氯硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图所示:(1)硅属于__________(选填“金属”或“非金属”)元素;(2)写出上述流程中一种氧化物的化学式:______________________;(3)上述流程中最后一步反应的化学方程式为______________________________,该反应属于________(填基本反应类型)反应;(4)如果还原SiHCl3过程中混入O2,可能引起的后果是________________________;(5)该流程中可以循环利用的物质的化学式是____________________。
【答案】非金属 SiO2(其他答案合理均可) SiHCl3+H2Si+3HCl 置换爆炸 HCl 【解析】(1)根据元素的名称分析解答;(2)根据物质的组成分析属于氧化物的物质,写出化学式;(3)分析流程中最后一步发生反应的化学方程式,根据反应特点分析类型;(4)根据氢气和氧气的混合气体点燃时会发生爆炸解答;(5)根据流程分析可循环利用的物质。
解:(1) (1)硅的名称中带有“石”字旁,属于非金属元素;(2)二氧化硅是由硅元素和氧元素组成的,属于氧合物,化学式为:SiO2;(3)上述流程中最后一步反应的化学方程式为:SiHCl3+H2高温Si+3HCl,该反应是由一种单质与一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;(4)如果还原SiHCl3过程中混入O2,会形成氢气和氧气的混合体,点燃时易引起爆炸;(5)该流程中可以循环利用的物质的化学式是HCl。
2.某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染。
于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属。
实验过程如下:请回答:(1)操作①的名称是_______,其中玻璃棒的作用是______。


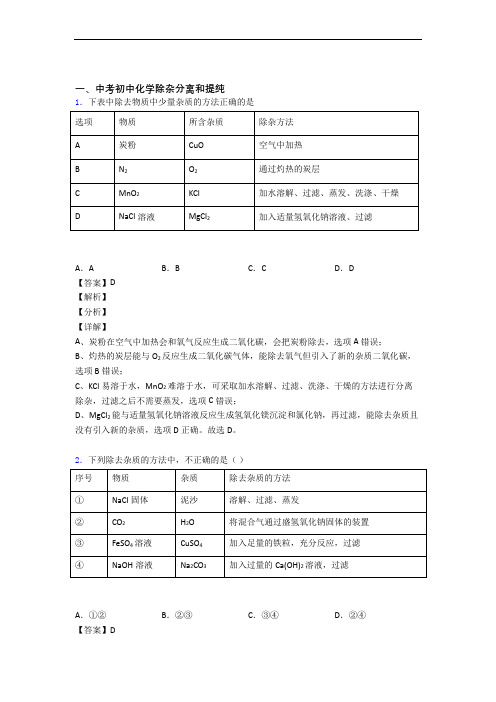
一、中考初中化学除杂分离和提纯1.下表中除去物质中少量杂质的方法正确的是A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、炭粉在空气中加热会和氧气反应生成二氧化碳,会把炭粉除去,选项A错误;B、灼热的炭层能与O2反应生成二氧化碳气体,能除去氧气但引入了新的杂质二氧化碳,选项B错误;C、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,过滤之后不需要蒸发,选项C错误;D、MgCl2能与适量氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,再过滤,能除去杂质且没有引入新的杂质,选项D正确。
故选D。
2.下列除去杂质的方法中,不正确的是()A.①②B.②③C.③④D.②④【答案】D【解析】【分析】【详解】①氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确;②二氧化碳能与氢氧化钠固体反应生成碳酸钠和水,氢氧化钠固体具有吸水性,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误;③铁粉能与CuSO4反应生成硫酸亚铁和铜,再过滤除去不溶物,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确;④Na2CO3能与过量的Ca(OH)2溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质氢氧化钙,不符合除杂原则,故选项所采取的方法错误,故②④方法不正确,故选D。
【点睛】本题为除杂题,是中考的重点,也是难点,解决除杂问题时,抓住除杂的必需条件(加入的试剂只与杂质反应,反应后不能引入新杂质)是正确解题的关键。
3.下表中,除去物质所含少量杂质的方法和反应类型归类均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜和氧气加热生成氧化铜,反应为化合反应,氧化铜和氧气加热不反应,可以除去铜粉,故A正确;B、一氧化碳和氧化铜反应生成铜和二氧化碳,反应不属于置换反应,故B不正确;C、盐酸和氢氧化钠反应生成氯化钠和水,反应类型为复分解反应,故C不正确;D、硫酸钾和硝酸钡反应生成硫酸钡和硝酸钾,引进新杂质硝酸钾,故D不正确。

一、中考初中化学推断题1.现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。
为确定其组成,进行了如下图所示的实验(假设实验过程无损耗)。
请回答:(1)根据实验可以确定白色沉淀是________;原固体粉末中一定含有_____________,它的可能组成有____________种。
(2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是____g,固体粉末由______________(填化学式,下同)组成,其中质量小于10g的是_____________________。
【答案】CaCO3(或“碳酸钙”) Na2CO3(或“碳酸钠”) 3 11.7 CaCO3、CaO、Na2CO3 CaCO3、CaO【解析】【分析】把固体粉末加入水中,得到白色沉淀,根据题给的物质可以判断该白色沉淀为碳酸钙,得到无色溶液与稀盐酸反应生成无色气体,可以判断在无色溶液中含有碳酸钠,而无色气体为二氧化碳,那么X就可能是氯化钠的溶液。
【详解】(1)在白色粉末中能产生白色沉淀,可知该白色沉淀应该为碳酸钙,又得到的无色溶液能够和稀盐酸反应生成气体,可以知道在固体粉末中一定含有碳酸钠,它可能的组合为:①碳酸钠,氧化钙;②碳酸钠,碳酸钙;③碳酸钠,氧化钙,碳酸钙等三种可能的组成;(2)根据(1)的解答可知X溶液为氯化钠溶液其质量为:200g×5.85%=11.7g,根据题意结合化学方程式,可以求出与盐酸反应的碳酸钠的质量为10.6g,进而可以判断出该固体粉末的组成为:CaCO3、CaO、Na2CO3 ,进而可以判断若白色沉淀质量小于10g,则原混合物的组成为氧化钙和碳酸钙,计算过程如下:设碳酸钠的质量为x2322Na CO+2HCl=2NaCl+H O+CO106117x11.7g106 x =117 11.7gx=10.6g这里我们求得的只是和盐酸反应的碳酸钠,总质量为20g,所以假如白色沉淀是固体粉末中的,则只有20g-10.6g=9.4g,而题目中得到的白色沉淀的质量是10g,也就是说白色沉淀并不是完全来自于原固体粉末中,而是有一部分是反应中生成的,即氧化钙和水反应生成了氢氧化钙,而氢氧化钙又和碳酸钠反应生成了碳酸钙沉淀,从而可以判断在混合物中含有氧化钙.故本题答案为:(1)CaCO3(或“碳酸钙”); Na2CO3(或“碳酸钠”); 3;(2)11.7; CaCO3、CaO、Na2CO3;CaCO3、CaO.2.实验室有一包白色粉末,可能含有 Na2SO4、Ba(NO3)2、K2CO3、KOH、CuSO4、Mg(NO3)2和KCl中的一种或几种,为了确定其成分,某化学兴趣小组进行了如下实验探究。

专题六 化学思想方法的应用
一、选择题
1.(2017,菏泽)化学与人类的生活密切相关,下列对化学知识的应用归纳完全正确的一组是( A )
2.(2017,遵义汇仁中学一模)进行化学实验,观测实验现象,通过分析推理得出正确结论是化学学习的方法之
一。
对下列实验事实的解释正确的是( B )
A .高锰酸钾受热后,固体质量减少了,说明化学反应前后各物质的质量总和不相等
B .把铁钉放在硫酸铜溶液中,铁钉上有紫红色的铜生成,说明铁比铜活泼
C .在某化肥中加入碱液,无氨味,说明该化肥一定不是氮肥
D .在紫色的石蕊溶液中通入二氧化碳气体,溶液变红,说明二氧化碳气体显酸性 3.(2017,广东)“如图”的实验设计不能实现其对应实验目的的是( A )
二、非选择题
4.(2017,重庆)“对比实验”是科学探究常用的方法。
根据以下实验回答问题。
(1)图A 中,可观察到__外焰__(填火焰的名称)处火柴炭化最明显。
(2)图B 中__左__(选填“左”或“右”)边试管发烫。
(3)从图C 中可得出燃烧的条件之一是__温度达到可燃物的着火点__,发生反应的化学方珵式为__4P +5O 2=====点燃
2P 2O 5__。
(4)图D 中打开可乐的瓶塞,可观察到大量气泡冒出,说明气体的溶解度与__压强__有关。
5.对比归纳是学习化学的重要方法。
请你参与下列探究活动并回答问题: 实验一:探究影响硫燃烧剧烈程度的因素。
实验二:探究二氧化碳能否与氢氧化钠反应。
一、中考初中化学除杂分离和提纯 1.下列除去杂质(在括号内)选用的试剂(在箭头右侧)不正确的是
A.CO2(CO)→CuO B.CaCl2溶液(HCl)→碳酸钙
C.NaCl(泥沙)→水
D.NaOH溶液(Na2CO3)→稀盐酸
【答案】D 【解析】 【分析】 【详解】 A、CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合
除杂原则,选项A正确; B、HCl能与碳酸钙反应生成氯化钙、水和二氧化碳,碳酸钙不溶于水,过量的碳酸钙可以
采用过滤的方法除去,能除去杂质且没有引入新的杂质,符合除杂原则,选项B正确; C、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,
选项C正确; D、NaOH溶液和Na2CO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不
符合除杂原则,选项D不正确。故选D。
2.除去下列物质中的少量杂质,所选用的试剂和操作方法均正确的是( ) 选项 物质 杂质(少量) 试剂和操作方法 A 氧气 二氧化碳 通入盛有足量氢氧化钠溶液洗气瓶
B 氯化钠 碳酸钠 加入适量稀盐酸 C 铜 氧化铜 加入足量稀硫酸,过滤
D 氯化钾 氯酸钾
加入二氧化锰,加热至不再产生气
过滤,蒸发结晶
A.A B.B C.C D.D 【答案】D 【解析】 【分析】 【详解】 A、CO2能与氢氧化钠溶液反应生成碳酸钠和水,氧气不与氢氧化钠溶液反应,应再进行干
燥,故选项所采取的方法错误; B、碳酸钠能与适量稀盐酸反应生成氯化钠、水和二氧化碳,应再进行蒸发,故选项所采取
的方法错误; C、CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,再过滤、洗涤、干燥,故选
项所采取的方法错误; D、氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,加热至不再产生气体,氯化钾易
溶于水,二氧化锰难溶于水,溶解,过滤,蒸发结晶,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。 故选D。 【点睛】 除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。