反义核酸药物
- 格式:docx
- 大小:38.42 KB
- 文档页数:2

反义寡核苷酸aso的递送系统解释说明1. 引言1.1 概述反义寡核苷酸(antisense oligonucleotide, ASO) 是一种具有广泛应用前景的基因治疗工具,它通过与特定mRNA分子序列互补结合,从而抑制或调控目标基因的表达。
ASO递送系统是将ASO有效地运送到靶位点的关键问题,它包括了手性寡核苷酸的设计、载体选择和优化策略,以及递送机制研究等方面。
1.2 文章结构本文将重点讨论反义寡核苷酸ASO的递送系统。
首先介绍反义寡核苷酸ASO 的概念和作用机制,明确其在基因治疗领域的重要性和应用前景。
接着,详细讨论目前存在的问题和挑战,如ASO递送效率低、稳定性差等。
然后,我们将介绍ASO递送系统的设计与原理,包括手性寡核苷酸设计原理、载体选择和优化策略以及递送机制研究进展。
接下来,在第四部分中探讨了ASO递送系统在遗传病治疗和肿瘤治疗中的应用前景,并探索了其他领域中的可能应用方向。
最后,通过总结和展望,提出未来关于ASO递送系统的研究方向。
1.3 目的本文的目的是全面介绍反义寡核苷酸ASO的递送系统。
通过对手性寡核苷酸设计原理、载体选择和优化策略以及递送机制研究进展的深入探讨,旨在提供关于ASO递送系统设计与优化的重要参考。
此外,本文还将预测ASO递送系统在遗传病治疗、肿瘤治疗以及其他领域中可能的应用前景,为相关领域的科学家和医生提供指导和启示。
最后,我们希望通过文章的撰写能够推动反义寡核苷酸ASO 递送系统领域的发展,并促进其在基因治疗中的应用成果。
2. 反义寡核苷酸ASO的递送系统2.1 反义寡核苷酸ASO简介反义寡核苷酸(Antisense oligonucleotide,ASO)是一种能够通过与靶标RNA 特异性杂交而调控基因表达的短链核酸分子。
ASO具有特异性、可调节性和高度选择性的特点,广泛应用于基因治疗、药物开发和生物学研究等领域。
ASO 的作用机理主要包括:阻断mRNA转录、刺激mRNA降解以及干扰蛋白质合成等。


[12] Mamiya K,Ieiro I ,Shimam oto J ,et al .The effects of ge 2netic polym orphisms of CY P2C9and CY P2C19on phenytoin metabolism in Japanese adult patients with epilepsy :studies in stereoselective hydroxylation and population pharmacoki 2netics[J ].Epilepsia ,1998,39(12):1317-1323.[13] K irchheiner J ,Brockm oller J ,Meineke I ,et al .Impact ofCY P2C9amino acid polym orphisms on glyburide kinetics and on the insulin and glucose response in healthy v olunteers[J ].Clin Pharmcol Ther ,2002,71(4);286-296.[14] Leger F ,Seronie 2Vivien S ,Makdessi J ,et al .Impact ofthe biochemical assay for serum creatinine measurement on the individual carboplatin dosing :a prospective study[J ].Eur J Cancer ,2002,38(1):52-56.[15] Frame B ,Miller R ,Lalonde R L.Evaluation of mixturem odeling with count data using NONME M[J ].J Pharma 2cokinet Pharmacodyn ,2003,30(3):167-184.反义寡核苷酸的药代动力学研究进展尚明美综述 刘秀文,汤仲明,陈惠鹏审校(军事医学科学院放射医学研究所,北京 100850)摘要:反义药物在经历了20年后,又迎来了一个蓬勃的发展阶段。


ASO药物定义1. 简介ASO药物(Antisense Oligonucleotide drug),又称反义寡核苷酸药物,是一种通过干扰基因表达来治疗疾病的新型生物医药产品。
ASO药物是一种定制的、合成的寡核苷酸链,通过与目标RNA序列互补结合,干扰或抑制特定蛋白质的合成,从而达到治疗疾病的目的。
2. 原理ASO药物的工作原理是通过与特定的靶标RNA(mRNA或ncRNA)序列互补结合,形成双链结构,进而干扰或抑制该靶标RNA的正常功能。
具体而言,ASO药物通过与靶标RNA的互补碱基序列结合,可以产生以下效应:2.1. 阻断转录ASO药物结合在mRNA上游,阻断RNA聚合酶的进一步合成,从而抑制靶标RNA的转录过程,减少对应蛋白质的产生。
2.2. 促进mRNA降解ASO药物结合在mRNA中,可以增加RNA内切酶的识别效率,促使mRNA的降解,从而减少对应蛋白质的合成。
2.3. 抑制剪接ASO药物可以与靶标RNA的剪接位点结合,干扰剪接酶的识别,导致正常剪接事件的改变,从而调控基因表达。
2.4. 阻断翻译ASO药物可以与mRNA的翻译区结合,阻断核糖体的附着,抑制蛋白质的合成。
3. 应用领域ASO药物的研究和应用领域非常广泛,可以用于治疗多种疾病,例如:3.1. 罕见遗传性疾病ASO药物可以通过纠正异常基因的表达,治疗罕见遗传性疾病,例如肌萎缩侧索硬化症(ALS)和囊性纤维化等。
3.2. 癌症ASO药物可以通过抑制癌细胞的特定蛋白质合成,抑制癌细胞的增殖和转移,从而达到治疗癌症的效果。
3.3. 心血管疾病ASO药物可以调控与心血管疾病相关的基因表达,例如调控血脂代谢、血管生成等,从而治疗高血压、冠心病等心血管疾病。
3.4. 炎症性疾病ASO药物可以通过抑制炎症相关基因的表达,减少炎症因子的产生,从而治疗炎症性疾病,例如类风湿关节炎、炎性肠病等。
4. 临床前研究与临床研究ASO药物的开发通常经历多个阶段,包括临床前研究和临床研究。



antivirals that inh ibit cytom egalovirus,antivirals that inh ibit herpesvirus and antivirals that inh ibit influenza virus.T h is review discusses their pharm aco logical p roperties,m ain adverse drug reac2 ti ons,therapeutic use and introduces som e advances in the research of antivirals.Key words A ntiviral agents Pharm aco logical p roperties T herapeutic use(收稿:1998207220,修回:1998211209)第二代反义寡核苷酸的研究Ξ朱冬晖 魏东芝(华东理工大学生物反应器工程国家重点实验室 生物化学研究所 上海 200237)摘 要 第一代反义核酸寡核苷酸硫代磷酸酯,是目前研究最广泛、最成熟的反义核酸药物,已进入临床试验阶段,但其具有一定的毒副作用;第二代反义核酸,包括嵌合寡核苷酸、杂合寡核苷酸等,是在硫代寡核苷酸的基础上,再引入其它的修饰基团,从而提高其生物活性,减少毒副作用。
本文着重介绍了第二代反义核酸的生物物理学性质,药动学及其与第一代反义核酸毒性的比较。
关键词 反义寡核苷酸 化学修饰 生物物理学 药物动力学 副作用 反义寡核苷酸通过序列特异地与靶m RNA结合而抑制基因表达,从而可以成为一类理想的、在基因水平调控的治疗药[1,2]。
因具有较好的抗酶解活性,寡核苷酸硫代磷酸酯(p ho spho ro th i oate o ligonucleo tides, PS2ODN s),已成为目前最广泛研究的寡核苷酸类似物之一,并已应用于临床[3]。

核酸药物的研究与应用摘要:核酸药物是各种具有不同功能的寡聚核糖核苷酸(R N A)或寡聚脱氧核糖核苷酸(D N A),主要在基因水平上发挥作用。
一般认为,核酸药物包括A p t a m e r、抗基因(A n t i g e n e)、核酶(R i b o z y m e)、反义核酸(A n t i s e n c e n u c l e i c a ci d)、R N A干扰剂。
由于其具有特异性针对致病基因,也就是说具有特定的靶点和作用机制,因此核酸药物具有广泛的应用前景。
该文就核酸药物的分类简要介绍核酸药物及其研究进展。
关键词:核酸药物定义分类生产应用现状核酸类药物作为抗病毒药物,以低毒性、不生产抗药性等特点,被广泛应用于临床。
用于治疗肿瘤的药物有5-氟尿嘧啶、5-脱氧氟尿嘧啶等。
还有些核酸衍生物具有抗肿瘤和抗病毒双重作用,如合成的阿拉伯糖苷类衍生物中的阿糖胞苷、环胞苷,除抗癌外,还用于抗疱疹病毒感染及治疗疱疹性脑炎。
1核酸药物的定义又称核苷酸类药物。
由某些动物、微生物的细胞中提取出的核酸(包括核苷酸和脱氧核苷酸),或者用人工合成法制备的具有核酸结构(包括核苷酸和脱氧核苷酸结构)同时又具有一定药理作用的物质,称为核酸药物或核酸类生化药物。
广义的核酸药物可包括核苷酸药物、核苷药物及含有不同碱基化合物的药物。
2核酸药物的分类:2.1核酸药物的一般分类(1)具有天然结构的核酸类物质;(2)天然碱基、核苷、核苷酸的类似物或聚合物。
2.2核酸药物具有多种药理作用,按其作用特点可分为:(1)抗病毒剂,代表药物有三氮唑核苷、无环鸟苷和6可糖腺苷等,临床上用于抗肝炎病毒、疱疹病毒及其他病毒;(2)抗肿瘤剂,代表药物有用于治疗消化道癌的氟尿嘧啶以及用于治疗各类急性白血病的阿糖胞苷等;(3)干扰素诱导剂,代表药物为聚肌胞,临床上用于抗肝炎病毒、疱疹病毒等;(4)免疫增强剂,主要用于抗病毒及抗肿瘤的辅助治疗;(5)供能剂,用于肝炎、心脏病等多种疾病的辅助治疗。

nusinersen作用机理
Nusinersen( 诺西那生钠)是一种用于治疗脊髓性肌肉萎缩症( SMA)的药物,其作用机理是通过抑制(SMN2(基因前体(mRNA(的剪切,从而增加功能性(SMN(蛋白的表达。
SMA(是一种遗传性神经肌肉疾病,由于(SMN1(基因的缺失或突变导致(SMN(蛋白表达不足,从而导致肌肉无力和萎缩。
Nusinersen(是一种反义寡核苷酸药物,可以与(SMN2(基因前体(mRNA(结合,从而抑制其剪切,增加功能性(SMN(蛋白的表达。
Nusinersen(的作用机理是基于(RNA(干扰技术,通过特异性地结合(SMN2(基因前体(mRNA(的特定序列,从而抑制其剪切,增加功能性(SMN(蛋白的表达。
这种作用机理可以有效地增加(SMN(蛋白的表达,从而改善(SMA(患者的症状。
Nusinersen(的治疗效果和安全性可能因个体差异而异,因此在使用该药物时需要遵循医生的建议,并进行密切的监测和管理。
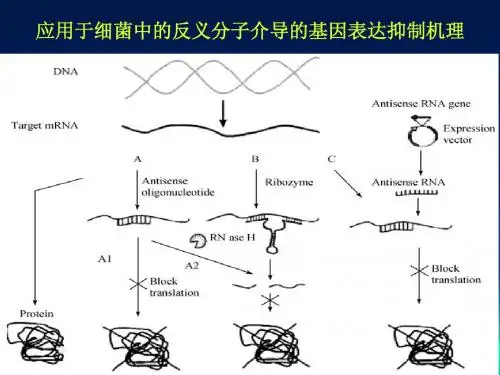
反义核酸药物
的作用原理
反义核酸目前有三种来源:一是利用固相亚磷酰胺法人工合成的短小反义寡聚核苷酸antisense
oligodeoxyncleotides,AON,这是反义核酸最普遍的应用方式,包括未修饰AON
和硫代磷酸酯化PS、磷酸二酯化PO和甲基化等修饰AON二类,其中以PSAON应用最广泛。
ANO设计合成简单,只要其顺序与靶mRNA部分顺序互补即可,而对基因的读码框无要求;
二是更具有实用价值的人工表达载体,包括单个基因和多个基因的联合反义表达载体[3],它是利用基因重组技术将靶基因序列反向插入到载体的启动子和终止子之间,通过转录可
源源不断产生反义RNA分子;三是天然存在的反义核酸分子,但目前分离纯化尚存在困难。
的作用特点
反义核酸作为基因治疗药物之一,与传统药物相比具有诸多优点。
1高度特异性:通过特异的碱基互补配对作用于靶RNA或DNA,犹如“生物导弹”。
2高生物活性、丰富的信息量;反义核酸是一种携带特定遗传信息的信息体,碱基排列顺序可千变万化,不可穷尽。
3高效性:直接阻止疾病基因的转录和翻译。
4最优化的药物设计:反义核酸技术从本质上是应用基因的天然顺序信息,实际上是
最合理的药物设计。
5低毒、安全:反义核酸尚未发现其有显著毒性,尽管其在生物体内的存留时间有长
有短,但最终都将被降解消除,这避免了如转基因疗法中外源基因整合到宿主染色体上的
危险性。
的在寄生虫学中的应用
反义核酸技术的飞速发展和成熟,使其逐渐渗透并应用到寄生虫学领域,丰富和发展
了寄生虫病的基因治疗策略。
反义核酸技术在抗寄生虫病研究的应用主要集中于原虫类,
如疟原虫、锥虫和利什曼原虫等,而且反义核酸中又以AON方面的报道最多。
下面着重就AON在寄生虫方面的研究应用作用一简要阐述。
⒊1 疟原虫
疟原虫嘌呤核苷酸合成具有特殊性,即无从头合成途径,依靠补救合成途径利用体内
游离的嘌呤或嘌呤核苷。
疟原虫的二氢叶酸还原酶dihydrofolate reductase,DHFR和胸
苷酸合酶thymidylate
synthase,TS结合形成双功能蛋白DHFR-TS,这对于维持疟原虫四氢叶酸水平和
DNA合成极为重要[14],此酶也是疟原虫脱氧胸苷酸生物合成唯一通路中必不可少的酶。
抗疟药中的抗叶酸代谢药如乙胺嘧啶,就是通过竞争性抑制DHFR-TS来阻断虫体脱氧胸苷酸生物合成[15]。
然而,随着恶性疟原虫Plasmodium
falciparum多药抗性株的出现和广为传播,疟疾的化疗面临重大挑战,促使人们寻求新的抗疟疗法。
目前,DHFR-TS是AON抗疟作用首选靶基因。
生物大分子进入感染红细胞中的疟原虫,必需穿透三层膜,即红细胞膜、纳虫泡膜和虫体的胞质膜。
研究表明,不能穿透红细胞膜和纳虫泡膜的大分子和葡聚糖、IgG2a抗体和蛋白A等,可经过纳虫微管parasitophorous
duct进入虫体,虫体通过胞吞作用直接从细胞外摄入大分子物质[16]。
因此,对于小分子的AON而言,作用于感染红细胞中的虫体完全成为可能,下述众多研究已充分证明了这一点。
Rapaport等1992研究发现[17],以DHFR-TS为靶21 nt PS
AON能选择性地进入恶性疟原虫感染红细胞,对体外培养的氯喹敏感株和耐药株虫体具有同等的抑制效果,而未感染疟原虫的红细胞则完全为不摄入AON,因此这对应用反义核酸于抗疟治疗非常有利。
诸多研究表明,AON越长,对转译的抑制作用就越强;AON浓度越高,非特异性抑制作用越明显,在低浓度时则呈特异性抑制。
Sartorius和Franklin1991以DHFR-TS的mRNA 为靶合成系列AON,利用兔网织红细胞翻译系统,探讨AON对体外转译的抑制作用[18]。
在DHFR翻译起始位点处合成了6条21-49nt不等长的AON,在TS编码区全成的30nt、39nt和49nt三条AON。
当AON长度为30nt或更长时,呈明显转译抑制作用,抑制率可高达50%以上。
其中,TS编码区的49nt
aONOTS49抑制效果最高,当浓度在45μmlo/L时的抑制率几乎达90%,主要是因为OTS49与DHFR-TS靶mRNA
感谢您的阅读,祝您生活愉快。