金属间化合物的晶体结构资料.
- 格式:pptx
- 大小:177.47 KB
- 文档页数:15

金属间化合物的晶体结构一、经典离子理论根据经典离子理论,金属和非金属之间的化学键是通过电荷间的吸引力形成的。
在金属间化合物中,金属离子以正电荷形式存在,而非金属离子以负电荷形式存在。
这种离子之间的吸引力使得金属离子和非金属离子结合在一起,形成晶体。
二、NaCl型结构NaCl型结构是金属间化合物中最典型的晶体结构之一、它由正交晶系的结构单元组成,其中金属离子和非金属离子交替排列。
每个正电荷的金属离子周围都有6个负电荷的非金属离子,每个负电荷的非金属离子周围也有6个正电荷的金属离子。
这种排列方式使得晶体具有高度规则和紧密堆积的结构。
例如,氯化钠(NaCl)和氟化钙(CaF2)都属于NaCl型结构。
三、CsCl型结构CsCl型结构也是金属间化合物中一个常见的晶体结构。
它由正交晶系的结构单元组成,其中一个金属离子和一个非金属离子位于体心立方(BCC)晶胞中。
这种排列方式使得晶体具有比NaCl型结构更紧密的堆积。
例如,氯化铯(CsCl)和溴化银(AgBr)都属于CsCl型结构。
四、ZnS型结构ZnS型结构是金属间化合物中另一个重要的晶体结构。
它由正交晶系中的结构单元组成,其中一个金属离子和一个非金属离子位于面心立方(FCC)晶胞中。
这种排列方式使得晶体具有更高的密度和更紧密的堆积。
例如,硫化锌(ZnS)和硫化铜(Cu2S)都属于ZnS型结构。
五、其他晶体结构除了上述三种常见的晶体结构,金属间化合物还可以具有其他类型的晶体结构。
例如,磷化锗(GeP)具有立方体结构,亚硫酸铁(FeSO4∙7H2O)具有单斜晶体结构。
这些不同的晶体结构导致了金属间化合物的物理和化学性质的差异。
总结:金属间化合物的晶体结构对其性质具有重要影响。
经典离子理论认为金属离子和非金属离子之间的离子吸引力是形成金属间化合物的化学键。
NaCl型结构、CsCl型结构和ZnS型结构是金属间化合物中最常见的晶体结构。
此外,金属间化合物还可以具有其他类型的晶体结构。
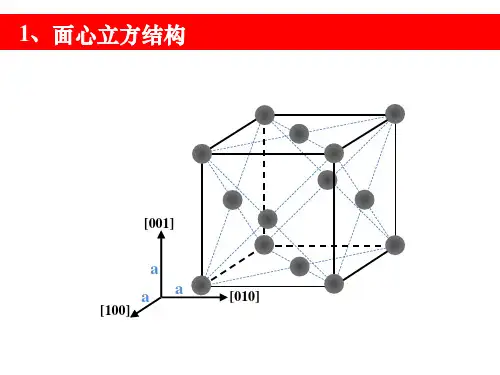
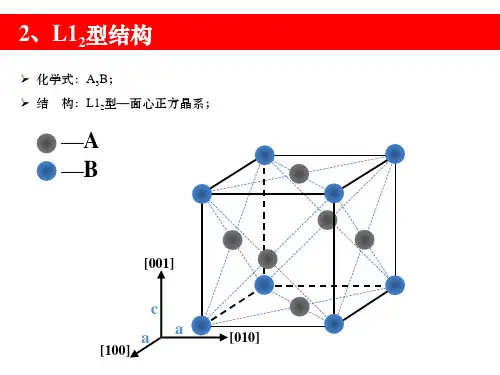




六方钙钛矿结构
六方钙钛矿结构是一种特殊的晶体结构,由钙、钛和其他元素及其官能团在结构上形成的共生关系。
这种结构由六方对称性堆积晶体点状结构组成,其真实结构是由金属间化合物覆盖在晶体表面形成的六方空分子的结构。
钙原子位于晶体表面上方,钛原子位于晶体表面下方,氧原子填充六方体晶体表面中间。
六方钙钛矿结构具有良好的机械性能和电学性能,在几乎所有材料工程领域都有应用。
与多晶硅和其它传统单晶材料相比,由钙钛矿结构构成的晶体表面非常光滑,可以有效地减少高强度的晶体晶粒缺陷,从而改善材料的力学性能和抗热性能。
此外,钙钛矿结构还具有较高的原子密度,可以抑制空间等位原子的迁移,从而使材料的韧性增强并导致抗裂破能力的提高。
六方钙钛矿结构也具有良好的耐腐蚀性和气环境耐受性,因此在高温、高压及危险环境中,可以使材料具有较长的使用寿命和稳定性。
此外,它还具有良好的电学性能和热电性能,可以使电子加热晶体表面和产生脉冲延迟用于无线电电力系统。
不过,六方钙钛矿结构也存在一些缺点,例如材料的裂变容易性,因为他们的结构中有非常细小的有序转换区,相对容易被外界的外力扰乱,从而表现
出裂变的倾向。
但这个缺陷在工程实践中可以通过控制晶体晶粒结构装置和尺寸来解决。
以上内容仅供参考,如需更多信息,建议查阅相关文献或咨询材料学专家。

金属间化合物是指由两个或两个以上的金属元素构成的化合物,它们的原子之间通过共享电子对而形成了化学键。
这些化合物通常具有不同于其组成金属的物理和化学性质。
金属间化合物可以根据它们的晶体结构进行分类,其中一些常见的类型包括:
1. 正常价化合物:这类化合物的形成是由于金属原子之间的电子转
移,以达到稳定的电子结构。
例如,在FeCl2 中,铁原子失去两个电子,而氯原子获得两个电子,形成了具有离子键的化合物。
2. 电子化合物:这类化合物的形成是由于金属原子之间的共享电子
对,以形成稳定的电子结构。
例如,在Al2Cu 中,铝原子和铜原子共享电子对,形成了具有共价键的化合物。
3. 间隙化合物:这类化合物是由较小的金属原子填入较大金属原子
的晶格间隙中形成的。
例如,在Fe3C 中,碳原子填入了铁原子的晶格间隙中,形成了具有复杂结构的化合物。
金属间化合物在材料科学中具有重要的应用,例如在合金设计、催化剂、电子材料和磁性材料等领域。
它们的特殊性质可以通过改变组成元素、晶体结构和制备方法等来调控,以满足不同的应用需求。

金属间化合物的结构引言:金属间化合物是由两种或更多种金属元素形成的化合物,具有特殊的结构和性质。
本文将重点介绍金属间化合物的结构特点,并以几种典型的金属间化合物为例进行详细探讨。
一、晶体结构金属间化合物的晶体结构多种多样,常见的有离子型、共价型和金属型结构。
其中,离子型结构由阳离子和阴离子组成,阴阳离子之间通过离子键结合。
共价型结构则由共价键连接金属原子和非金属原子,形成共价键网络。
金属型结构是金属间化合物中最常见的结构类型,金属原子通过金属键连接形成三维金属晶体结构。
二、NaCl型结构NaCl型结构是金属间化合物中最简单的一种结构类型。
它由阳离子和阴离子以八面体配位方式排列而成。
常见的NaCl型金属间化合物包括氯化钠(NaCl)、氟化钠(NaF)等。
这种结构具有高度的离子性,具有较高的熔点和硬度。
三、CsCl型结构CsCl型结构是一种简单立方结构,其中阳离子和阴离子分别位于晶体的立方体中心和顶点位置。
铯氯化物(CsCl)即为典型的CsCl型金属间化合物。
CsCl型结构具有较高的离子性和较低的对称性,熔点一般较高。
四、锌刚石型结构锌刚石型结构是一种典型的共价型结构,其中金属原子和非金属原子通过共价键连接。
锌刚石型结构的典型代表是硼化硅(SiC),它具有高硬度、高熔点和良好的导热性能。
五、体心立方型结构体心立方型结构是金属间化合物中常见的一种结构类型,其中金属原子位于立方体的顶点和体心位置。
典型的体心立方型金属间化合物包括铁素体、铬铁、镍铁等。
体心立方型结构具有较高的密堆度和较低的对称性。
六、六方最密堆积结构六方最密堆积结构是一种典型的金属型结构,其中金属原子按照最密堆积方式排列。
常见的六方最密堆积金属间化合物有钛(Ti)、锆(Zr)、钨(W)等。
六方最密堆积结构具有高度的对称性和较高的密堆度。
七、其他结构类型除了上述几种典型的金属间化合物结构外,还存在许多其他的结构类型,如六方密堆积结构、简单四方结构、钙钛矿结构等。

金属间化合物的晶体结构金属间化合物是由两种或多种金属元素组成的化合物,具有特殊的晶体结构。
这些化合物通常具有高硬度、高熔点和良好的导电性等特性,因此广泛应用于材料科学和工程领域。
本文将介绍金属间化合物的晶体结构和其形成原因。
1.铜金属间化合物:铜金属间化合物的典型晶体结构是CuAl2或CuZn5等。
在这些化合物中,铜原子通常占据体心或面心位置,形成一个紧密堆积的结构。
在这种结构中,铜原子与其他金属原子之间有共价键和金属键的形成,使得化合物具有高强度和硬度。
2.镍基金属间化合物:镍基金属间化合物通常具有复杂的晶体结构,如Al3Ni2、Ni3Al等。
这些化合物中,镍和铝原子按照一定比例堆积在一起,形成由金属键和共价键组成的三维网络。
这种结构使得镍基金属间化合物具有高熔点、高硬度和良好的抗腐蚀性能。
3.钛金属间化合物:钛金属间化合物的晶体结构种类较多,常见的有TiAl、TiNi等。
在这些化合物中,钛原子和其他金属原子形成各种晶格结构,如体心立方、面心立方等。
这些化合物具有高硬度、高熔点、较低密度和良好的抗腐蚀性能。
4.铁基金属间化合物:铁基金属间化合物的晶体结构也较为复杂,常见的有Fe3Al、Fe2Ti等。
这些化合物中,铁原子和其他金属原子按照一定比例排列在一起,形成复杂的晶格结构。
这种结构使得铁基金属间化合物具有高硬度、高熔点和良好的热稳定性。
1.金属元素之间的原子半径差异:金属原子的半径决定了化合物的晶格结构。
如果两种金属元素的原子半径差异较小,它们可能会形成固溶体,而不会形成金属间化合物。
然而,如果差异较大,它们通常会形成金属间化合物。
2.金属元素之间的电负性差异:金属元素之间的电负性差异也会影响金属间化合物的形成。
如果两种金属元素的电负性相差较大,它们通常会形成金属间化合物,而不是固溶体。
3.金属元素的原子堆积方式:金属原子的堆积方式也影响着金属间化合物的晶体结构。
不同的原子堆积方式会导致不同的晶体结构。

2.3合金相结构[1]虽然纯金属在工业中有着重要的用途,但由于其强度低等原因,因此,工业上广泛使用的金属材料绝大多数是合金。
所谓合金是指由两种或两种以上的金属或金属与非金属经熔炼、烧结或其他方法组合而成并具有金属特性的物质。
组成合金的基本的独立的物质称为组元。
组元可以是金属和非金属元素,也可以是化合物。
例如,应用最普遍的碳钢和铸铁就是主要由铁和碳所组成的合金;黄铜则为铜和锌的合金。
改变和提高金属材料的性能,合金化是最主要的途径。
欲知合金元素加人后是如何起到改变和提高金属性能的作用,首先必须知道合金元素加人后的存在状态,即可能形成的合金相及其组成的各种不同组织形态。
而所谓相是合金中具有同一聚集状态、同一晶体结构和性质并以界面相互隔开的均匀组成部分。
由一种相组成的合金称为单相合金,而由几种不同的相组成的合金称为多相合金。
尽管合金中的组成相多种多样,但根据合金组成元素及其原子相互作用的不同,固态下所形成的合金相基本上可分为固溶体和中间相两大类。
固溶体是以某一组元为溶剂,在其晶体点阵中溶入其他组元原子(溶质原子)所形成的均匀混合的固态溶体,它保持着溶剂的晶体结构类型;而如果组成合金相的异类原子有固定的比例,所形成的固相的晶体结构与所有组元均不同,则称这种合金相为金属化合物。
这种相的成分多数处在A在B中溶解限度和B在A中的溶解限度之间,因此也叫做中间相。
合金组之间的相互作用及其所形成的合金相的性质主要是由它们各自的电化学因素、原子尺寸因素和电子浓度三个因素控制的。
2.3.1固溶体固溶体晶体结构的最大特点是保持着原溶剂的晶体结构。
根据溶质原子在溶剂点阵中所处的位置可将固溶体分为置换固溶体和间隙固溶体两类,下面即来分别加之讨论。
1.置换固溶体当溶质原子溶入溶剂中形成固溶体时,溶质原子占据溶剂点阵的阵点,或者说溶质原子置换了溶剂点阵的部分溶剂原子,这种固溶体就称为置换固溶体。
金属元素彼此之间一般都能形成置换固溶体,但溶解度视不同元素而异,有些能无限溶解,有的只能有限溶解。