塑形性支气管炎CT
- 格式:pptx
- 大小:43.02 MB
- 文档页数:24

慢性阻塞性肺疾病CT影像结合肺功能检测的临床意义慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是一种以进行性气流受限为主要特征的慢性呼吸系统疾病。
其主要表现为慢性支气管炎和肺气肿。
COPD 的诊断主要依靠临床症状、肺功能检测和影像学检查等多种手段。
CT影像结合肺功能检测的联合应用对COPD的诊断和评估具有重要的临床意义。
CT影像在COPD的诊断中起到了重要的作用。
其可以直观地显示肺部的形态和结构变化,包括肺占位性病变、肺气肿、肺囊性变以及中央气道的病变等。
尤其对于轻度的COPD 患者,CT影像能够检测出更早期的肺部病变,从而帮助早期干预和治疗。
CT影像还可以观察到肺部的空气含量、吸气过程等动态变化,能提供更多的信息以帮助临床医生进行判断。
与肺功能检测相比,CT影像能够提供更加直观、全面的结构信息,但不能提供功能方面的评估。
肺功能检测是诊断COPD以及评估其严重程度的重要手段。
肺功能检测能够评估患者的肺功能状态,包括肺活量、呼气流速、肺弹力和通气功能等。
通过肺功能检测,可以判断患者是否存在气流受限,并且可以评估气流受限的程度和类型。
肺功能检测还可以评估肺的弹性、通气功能和氧合能力等,有助于指导治疗和预后评估。
CT影像与肺功能检测的联合应用可以更全面地评估COPD患者的病情和预后。
CT影像通过观察肺部结构变化来判断病变的范围和程度,而肺功能检测则可以评估气流受限程度和类型。
CT影像可以帮助评估并发症的存在和性质,如支气管扩张、肺气肿和肺动脉高压等。
通过CT影像和肺功能检测的综合分析,可以更好地指导COPD患者的治疗决策和预后评估。



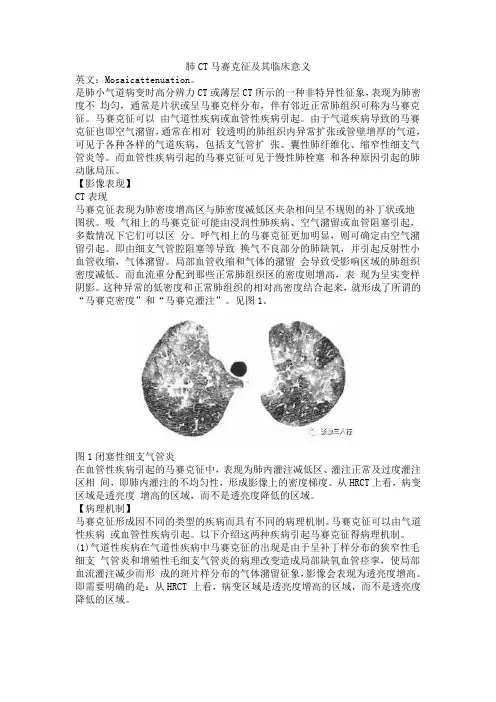
肺CT马赛克征及其临床意义英文:Mosaicattenuation。
是肺小气道病变时高分辨力CT或薄层CT所示的一种非特异性征象,表现为肺密度不均匀,通常是片状或呈马赛克样分布,伴有邻近正常肺组织可称为马赛克征。
马赛克征可以由气道性疾病或血管性疾病引起。
由于气道疾病导致的马赛克征也即空气潴留,通常在相对较透明的肺组织内异常扩张或管壁增厚的气道,可见于各种各样的气道疾病,包括支气管扩张、囊性肺纤维化、缩窄性细支气管炎等。
而血管性疾病引起的马赛克征可见于慢性肺栓塞和各种原因引起的肺动脉局压。
【影像表现】CT表现马赛克征表现为肺密度增高区与肺密度减低区夹杂相间呈不规则的补丁状或地图状。
吸气相上的马赛克征可能由浸润性肺疾病、空气潴留或血管阻塞引起,多数情况下它们可以区分。
呼气相上的马赛克征更加明显,则可确定由空气潴留引起。
即由细支气管腔阻塞等导致换气不良部分的肺缺氧,并引起反射性小血管收缩,气体潴留。
局部血管收缩和气体的潴留会导致受影响区域的肺组织密度减低。
而血流重分配到那些正常肺组织区的密度则增高,表现为呈实变样阴影。
这种异常的低密度和正常肺组织的相对高密度结合起来,就形成了所谓的“马赛克密度”和“马赛克灌注”。
见图1。
图1闭塞性细支气管炎在血管性疾病引起的马赛克征中,表现为肺内灌注减低区、灌注正常及过度灌注区相间,即肺内灌注的不均匀性,形成影像上的密度梯度。
从HRCT上看,病变区域是透亮度增高的区域,而不是透亮度降低的区域。
【病理机制】马赛克征形成因不同的类型的疾病而具有不同的病理机制。
马赛克征可以由气道性疾病或血管性疾病引起。
以下介绍这两种疾病引起马赛克征得病理机制。
(1)气道性疾病在气道性疾病中马赛克征的出现是由于呈补丁样分布的狭窄性毛细支气管炎和增殖性毛细支气管炎的病理改变造成局部缺氧血管痉挛,使局部血流灌注减少而形成的斑片样分布的气体潴留征象,影像会表现为透亮度增高。
即需要明确的是:从HRCT 上看,病变区域是透亮度增高的区域,而不是透亮度降低的区域。

树芽征(tree-in-bud pattern,TIB)是指CT表现为靠近胸膜下区小叶中心直径为3~5 mm的分支状线影和与其相连的细支气管横断面结节影,状如春天里挂满树芽的树,即树芽征。
是细支气管扩张、阻塞的特征影像之一。
1993年由Im等首次报道,最初用来描述肺结核沿终末支气管扩散的征象,后来逐渐用于有类似征象的其它支气管疾病CT尤其是高分辨CT(HRCT)能够很好的显示此征。
树芽征不是一个病,而是一组疾病可能出现的CT征象,胸部X线射片不能发现如此细小的病变。
树芽征树芽征的CT表现由于扩大的细支气管呈分支并有成边缘模糊结节的细支气管周围炎症,它的表现类似发芽或长果子的树。
术语树芽征也用于描述支气管造影上小气道充盈的表现。
以双肺中、下叶多见,一般由直径2~4mm小叶中心结节影及分支状线影两部分组成,结节较大时刻可达6~8mm。
结节边缘清晰,较大时可模糊。
分支状线影常呈树枝状,粗细不均匀,边缘可光整或不光整。
两者相连,状如树芽。
TIB常和肺内其他影像表现同时存在,如支气管扩张时,常和“印戒征”、“轨道征”同时存在;肺结核时可与纤维索条影、片状浸润影、结核空洞及钙化影共存。
如果细支气管内充盈的黏液、脓液等排空,细支气管管腔被空气充盈,那么在看到细支气管扩张的同时,还可以看到细支气管壁的增厚及细支气管周围炎。
树芽征位于肺的周围,正常情况下在肺的周围距胸膜下1cm以内,见不到支气管影像,又因缺乏逐渐变细的特征,而易与正常的小叶中心动脉鉴别。
TIB的病理机制树芽征病理基础为肺泡导管、呼吸性细支气管、终末细支气管被黏液、脓液等阻塞形成,并伴有细支气管管扩张、细支气管壁的增厚及细支气管周围炎。
树芽征的小叶中心结节影和分支状线影是相同病理结果的不同影像表现,二者的病理基础都是细支气管的扩张与阻塞,与CT横断面像平行走向的细支气管表现为分支状线影,与垂直或斜向走行者表现为结节影。
原发或继发于细支气管的病变可导致细支气管管壁增厚、细支气管扩张,当同时伴有分泌物潴留时,支气管“树”状如春天里一棵挂满枝芽的“树”,即树芽征。



支气管扩张指近端中等大小支气管由于管壁的肌肉和弹性成分的破坏,导致其管腔形成异常的、不可逆性扩张、变形。
本病多数为获得性,多见于儿童和青年。
大多继发于急、慢性呼吸道感染和支气管阻塞后,患者多有童年麻疹、百日咳或支气管肺炎等病史。
临床表现主要为慢性咳嗽、咳大量脓痰和(或)反复咯血。
近年来随着急、慢性呼吸道感染的恰当治疗,其发病率有减少趋势。
病理生理早期病变轻而且局限时,肺功能测定可在正常范围。
病变范围较大时,表现为阻塞性通气障碍。
当病变严重而广泛,且累及胸膜时,则表现为以阻塞性为主的混合性通气功能障碍。
肺内动-静脉样分流,以及弥散功能障碍导致低氧血症。
少数患者病情进一步发展,出现肺动脉高压、并发肺源性心脏病。
实验室检查一、X线检查①胸部平片:平片对支气管扩张的敏感性较差。
早期轻症患者常无特殊发现,以后可显示一侧或双侧下肺纹理局部增多及增粗,而典型的X线表现为粗乱肺纹理中有多个不规则的蜂窝状透亮阴影或沿支气管的卷发状阴影,感染时阴影内出现液平面;②CT扫描:普通CT扫描诊断支气管扩张的敏感性和特异性分别是66%和92%,而高分辨CT (HRCT)诊断的敏感性和特异性均可达到90%以上,现已成为支气管扩张的主要诊断方法。
特征性表现为管壁增厚的柱状扩张或成串成簇的囊样改变;③支气管碘油造影:是确诊支气管扩张的主要依据。
可确定支气管扩张的部位、性质、范围和病变的程度,为外科决定手术指征和切除范围提供依据。
但由于这一技术为创伤性检查,现已被CT取代。
二、其它检查有助于支气管扩张的直观或病因诊断。
纤维支气管镜可发现出血、扩张或阻塞部位,还可进行局部灌洗作涂片、细菌学、细胞学检查,也可经纤维支气管镜作选择性支气管造影。
肺功能测定可以证实由弥漫性支气管扩张或相关的阻塞性肺病导致的气流受限。
痰液检查常显示含有丰富的中性粒细胞以及定植或感染的多种微生物。
痰涂片染色以及痰细菌培养结果可指导抗生素治疗。
白细胞总数和分类一般在正常范围,急性感染时白细胞及中性粒细胞增高。


儿童肺炎支原体肺炎诊疗指南(2023年版)肺炎支原体肺炎(mycoplasma pneumoniae pneumonia,MPP)是我国5岁及以上儿童最主要的社区获得性肺炎(community acquired pneumonia,CAP)。
如何早期发现重症和危重症病例、合理救治、避免死亡和后遗症的发生是MPP诊治的核心和关键问题。
为此,国家卫生健康委员会委托国家儿童医学中心(首都医科大学附属北京儿童医院)牵头撰写儿童MPP诊疗指南。
国家儿童医学中心组织了国家呼吸病临床研究中心、全国儿科呼吸、重症、血液、影像、检验、药学等多学科专家,参照现有国内外证据和经验制定了本诊疗指南,以期指导和规范儿科医师对MPP的诊治,减少抗微生物药物的不合理使用,减少后遗症、降低病死率、减轻医疗负担等。
本指南为总体指导性原则,各地各级医院在临床实践中应结合具体情况运用。
一、定义肺炎支原体肺炎(MPP):指肺炎支原体(mycoplasma pneumoniae, MP)感染引起的肺部炎症,可以累及支气管、细支气管、肺泡和肺间质。
难治性肺炎支原体肺炎(refractory mycoplasma pneu-moniae pneumonia, RMPP):指MPP患儿使用大环内酯类抗菌药物正规治疗7d及以上,仍持续发热、临床征象及肺部影像学所见加重、出现肺外并发症者。
大环内酯类药物无反应性肺炎支原体肺炎(macrolide -unresponsive MPP,MUMPP):指MPP患儿经过大环内酯类抗菌药物正规治疗72h,仍持续发热,临床征象及肺部影像学无改善或呈进一步加重的MPP。
原因与MP耐药、异常免疫炎症反应以及混合感染等有关。
临床及时识别MUMPP更有利于早期有效的治疗,减少重症和后遗症的发生。
重症肺炎支原体肺炎(severe MPP, SMPP):指MPP病情严重,符合重症CAP判定标准,详见临床分型。
危重症肺炎支原体肺炎:指患儿病情迅速进展、出现呼吸衰竭或危及生命的肺外并发症,需要进行生命支持治疗的少数SMPP。
弥漫性泛细支气管炎病情说明指导书一、弥漫性泛细支气管炎概述弥漫性泛细支气管炎(diffuse panbronchiolitis,DPB)是以肺部呼吸性细支气管为主要病变区域的特发性、弥漫性、炎性和阻塞性气道疾病。
可表现为慢性咳嗽、多痰和劳力性呼吸困难,并伴有气流受限。
本病是一种慢性和进展性疾病,预后较差。
如果不及时治疗,会导致慢性呼吸衰竭和肺心病的出现。
英文名称:diffuse panbronchiolitis,DPB。
其它名称:无。
相关中医疾病:暂无资料。
ICD疾病编码:暂无编码。
疾病分类:呼吸系统疾病。
是否纳入医保:部分药物、耗材、诊治项目在医保报销范围,具体报销比例请咨询当地医院医保中心。
遗传性:与遗传因素有关。
发病部位:肺脏。
常见症状:持续性咳嗽、咳痰、活动时呼吸困难。
主要病因:人种特异性及遗传因素、慢性气道炎症、免疫系统功能障碍、慢性气道感染机制。
检查项目:体格检查、血常规、C反应蛋白、血沉、灌洗液检查、冷凝集试验、免疫学检查、痰细菌学检查、胸部X线检查、胸部CT检查、鼻窦X线检查、鼻窦CT检查、肺功能测定、支气管镜检查、病理学检查。
重要提醒:患者在出现咳嗽、咳痰、呼吸困难时,应及时就医,查明病因,积极治疗,以免延误病情。
临床分类:按其胸片表现共分5型。
1、Ⅰ型仅有含气量增加所致的肺透亮度增加而无小结节。
2、Ⅱ型除有含气量增加外,尚可见小结节阴影,但仅限于1个肺叶。
3、Ⅲ型小结节阴影分布于全肺野。
4、Ⅳ型除有Ⅲ型改变外,两肺下野尚可见支气管充气和双轨状阴影。
5、Ⅴ型除有Ⅳ型改变外,尚可见大小不等的环形阴影。
二、弥漫性泛细支气管炎的发病特点三、弥漫性泛细支气管炎的病因病因总述:弥漫性泛细支气管炎(DPB)目前病因尚不明确,可能与人种特异性及遗传因素、慢性气道炎症、免疫系统功能障碍、慢性气道感染机制有关。
基本病因:1、人种特异性及遗传基因(1)HLA基因:近年研究表明DPB发病以东亚人(蒙古系人种)居多,有明显的人种差别且部分患者有家族发病倾向。
弥漫性泛细支气管炎诊疗要点一、明确诊断询问病史、体格检查是基本。
因80%以上的DPB患者存在鼻窦炎,建议为疑似DPB者执行鼻部CT。
此外,还需检查肺功能和冷血凝素滴度。
日本厚生省发布了DPB的诊疗指南,其诊断标准见表1。
表1 DPB的诊断标准[2](注:FEV1:一秒用力呼气量;FVC:用力肺活量;PaO2:动脉氧分压)二、识别DPB的胸部CTDPB患者的胸部影像学“辨识度高”,其胸部CT常提示双肺弥漫性小结节(下肺较上肺明显)、以小叶中心分布,可有“Y型结构”和“树芽征”;部分患者存在支气管扩张。
“理论结合实际”—简述DPB的影像学特征一名63岁男性,因咳嗽、咳痰10年就医。
既往有慢性鼻窦炎病史,入院胸部CT提示双上、下肺弥漫性网状结节影,双侧支气管扩张、有“树芽征”及“Y 型结构”。
图1 DPB案例(一)[3]另一男性患者,因咳嗽、气促6月就医。
既往有慢性鼻窦炎、慢性淋巴细胞白血病。
入院胸部CT发现双肺多发分支状小结节、有“树芽征”和支气管扩张。
图2 DPB案例(二)[4]对于疑似DPB者,高分辨率胸部CT(HRCT)还能辅助临床分期、评估病情严重程度。
▲HRCT可将DPB分为4期[5],从第1至4期,病情逐渐加重。
1期:支气管分支末端可见直径约5mm的小结节;2期:可见小叶中心结节、以“Y形结构”与远端分支支气管血管相连,呈现“树芽征”;3期:结节与近端支气管血管束相连并形成高密度环形或导管区域,有囊性支气管扩张;4期:囊性支气管扩张区域增大。
三、治疗DPB患者常因慢性咳嗽、咳痰就医,在部分患者的呼吸道分泌物中检出流感嗜血杆菌、铜绿假单胞菌。
为此,支气管扩张剂、祛痰药、糖皮质激素、β内酰胺抗菌药物曾用于DPB的治疗,但疗效不佳。
直到1982年,一位日本DPB患者服用2年的红霉素(0.6g/d)后病情明显改善、肺部病灶吸收明显。
进一步研究发现,大环内酯类具有以下药理作用[6]:•抗炎、免疫调节,加强宿主防御功能;•减少气道内的流感嗜血杆菌及铜绿假单胞菌的菌落数、抑制细菌生物被膜和毒力因子的产生;•抑制铜绿假单胞菌产生血凝素;•减少痰液分泌。
细支气管疾病和闭塞性细支气管炎1 细支气管疾病的定义及特征所谓“细支气管疾病”是一种非特异性的描述性名称,包括诸多病变,主要累及内径小2mm的气道,包括细支气管和终末细支气管(12~16级),以及呼吸性细支气管,还包括部分内径较小的小支气管(7~11级),以阻塞性病变为特征。
多数患者临床主要症状和体征为呼吸困难、咳嗽、阻塞性通气功能障碍和胸部影像有过度充气。
上述虽然在概念上似乎已较清楚,但在临床上诊断却非常困难。
这是因为在细支气管疾病,许多已有描述的组织病理类型与临床和影像之间缺乏明确的关联,即便存在明确关联者,可能因为有限的病理改变难以转化或解释其影像和不能引起需要临床诊断的症状及功能减退,从而影响临床诊断。
另外,由于在解剖上其连接支气管和肺实质(肺泡),从病因上细支气管疾病常常可能是远端肺间质或近端支气道疾病的一部分,各种感染或非感染性因素均可能损害细支气管导致可逆或不可逆损伤(阻塞),并同时影响支气管和肺实质,如病毒感染、结缔组织病和其他免疫性疾病、吸入性损伤、药物反应、异体移植物移植及许多其他疾病,而一些支气管和肺实质疾病,也常累及细支气管。
同时在判别细支气管病变呼吸功能减退时,还应考虑肺实质病变及支气管受累的影响。
再者,细支气管病无论从临床,影像和病理学均表现的十分复杂、多变。
病程可以为急性,也可以是慢性。
影像既可表现为局限、多发或弥漫性,也可显示为远端小气道病变。
至于病因,虽然可以明确,但大多数不清楚。
2 细支气管疾病分类细支气管疾病的组织病理学分型及临床特征复杂多样,也导致疾病命名不清、词条冗余或概念范畴重叠。
虽然临床医生、病理学家和放射学家等从各自的视角进行了不同的分类,至今尚无一个被人们广泛接受。
通常疾病分类主要是根据组织病理学分型或病因学。
10年前,Wright及其同事提出了关于“小气道疾病” 的权威性综述,其中包括了吸烟、矿物粉尘、移植性细支气管炎、闭塞性细支气管炎以及BOOP。
儿童社区获得性肺炎管理指南完整版肺炎是儿童常见呼吸系统疾病,是全球5岁以下儿童感染性疾病发病和死亡的主要原因。
目前,我国儿童肺炎城市发病率5岁以下为65.8/千人年,高于高收入国家(44.6/千人年),5~9岁17.37/千人年,10~17岁3.07/千人年;病死率为0.32‰~1.09‰,占全病因死亡的8%。
为此,本文将依据最新发布的《儿童社区获得性肺炎管理指南(2024修订)》(作者:中华医学会儿科学分会呼吸学组;通信作者:陆权,上海交通大学医学院附属儿童医院呼吸科;申昆玲,首都医科大学附属北京儿童医院呼吸科),整理出儿童社区性肺炎的诊断、评估以及治疗等内容,详情如下:社区获得性肺炎病原学社区获得性肺炎(简称肺炎)是指原本健康的儿童在医院外获得的感染性肺炎,包括感染了具有明确潜伏期的病原体而在入院后潜伏期内发病的肺炎,是儿童期常见的感染性疾病。
肺炎病原包括病毒、细菌、非典型病原[肺炎支原体(MP)、肺炎衣原体(CP)、沙眼衣原体、嗜肺军团菌]、真菌和原虫等。
年龄可以很好地提示儿童肺炎可能病原。
年幼儿肺炎50%以上由病毒引起;大龄儿童常由MP或细菌感染所致。
图1:不同年龄儿童肺炎的常见病原临床特征1 临床征象(1)发热和咳嗽是肺炎的主要症状,呼吸增快是重要临床表现,判定标准如下(平静时观察1min):呼吸频率<2月龄,≥60次/min;2月龄至1岁,≥50次/min;>1~5 岁,≥40次/min;>5岁,≥30次/min。
肺部听诊可有湿性啰音、管状呼吸音或呼吸音减低,重者可出现呼吸困难、发绀、胸壁吸气性凹陷等体征。
(2)不同年龄、不同病原所致肺炎的临床表现差异较大。
临床特征对病原学有一定提示作用。
(3)病毒性肺炎多见于婴幼儿,有一定的季节性,容易流行或聚集性发病,常见临床特征见图2。
(4)细菌性肺炎感染中毒症状重,多中高热,喘息少见;可有湿啰音和肺实变体征及影像学改变,常见细菌性肺炎的临床特征详见图3。