有机化学立体
- 格式:doc
- 大小:261.50 KB
- 文档页数:5



有机化学立体结构表示方法宝子!今天咱们来唠唠有机化学里立体结构的表示方法呀。
一、楔形式。
这楔形式就像在给分子画小漫画呢。
它用实线表示在纸平面上的键,楔形的粗线表示指向纸面前方的键,虚线表示指向纸面后方的键。
就好像分子里的原子们在一个小舞台上,实线的原子就在舞台平面上,楔形粗线的原子是从舞台前面冒出来的,虚线的原子是躲在舞台后面的。
比如说甲烷的立体结构用楔形式表示,就能很清楚地看到氢原子和碳原子在空间的相对位置啦。
二、锯架式。
锯架式也很有趣哦。
它是从斜侧面看分子的样子。
把分子想象成一个小架子,各个原子和键就像架子上的零件。
这种表示方法能直观地看到相邻原子之间的连接方式和角度关系。
就像搭积木一样,你能看到每个“积木块”(原子)是怎么靠着旁边的“积木块”的。
在研究一些有机反应的时候,锯架式能让我们很好地理解反应过程中原子的空间变化。
三、纽曼投影式。
纽曼投影式就像是给分子拍了个特殊的照片。
它是沿着碳 - 碳键的轴去看分子的。
前面的碳原子用一个点表示,后面的碳原子用一个圆表示,然后把连接在这两个碳原子上的原子和基团画在相应的位置上。
这就好比是从分子内部去窥探它的结构,看那些原子们是怎么围绕着碳 - 碳键排列的。
对于一些构象分析,纽曼投影式可太有用啦。
四、费歇尔投影式。
费歇尔投影式有点像把分子压扁了画在纸上。
它是把碳链竖起来,氧化态高的基团在上面,氧化态低的在下面,然后水平方向的键是伸向纸面前方的,垂直方向的键是伸向纸面后方的。
就像给分子安排了一个特定的“站姿”,这样我们可以方便地比较不同分子或者同一分子不同异构体的结构关系。
这些立体结构表示方法在有机化学里就像不同的魔法工具,帮助我们更好地理解那些微观的分子世界。
它们各有各的妙处,学会了这些,就好像拿到了进入有机化学立体世界的小钥匙,能让我们在有机化学的奇妙天地里畅游呢。

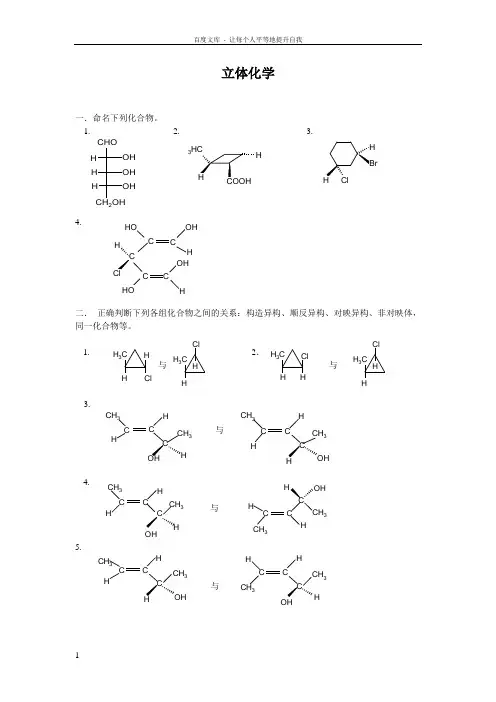
有机立体化学习题及答案立体化学一. 命名下列化合物。
4.二. 正确判断下列各组化合物之间的关系:构造异构、顺反异构、对映异构、非对映体,同一化合物等。
1. 2.与 与3.与4.与C CC CH 3HHCH 3HCCC CH 3HHCH 3OH H 3C H H ClH 3C HH ClH 3C HHCl H 3C HH Cl C CC CH 3H HCH 3HOHC CCCH 3HHCH 3OH与6.与7.与8. 与9.与10.与三.指出下述指定化合物与其他化合物之间的关系(对映体、非对映体或同一化合物)CH 3HOHCH=CH 2CH 3H HBr Cl 3CH 3H HBrCl3CH 2OHCH 3HOHHOH 333 C CCCH 3HCH 3OH CCC CH 3HHCH 3H2OH2OHC CCH 3H HO2OHCH 3HOHCH=CH 21.(a ) (b) (c) (d)2.(a ) (b) (c) (d) (e)四.写出下列化合物的三维结构式。
1. (S )-2-羟基丙酸2. (S )—2—氯四氢呋喃3.(2R,3R )—2,3— 二氯丁烷4. (R )—4—甲基—3—氯—1—戊烯 5.(1S,2R )—2—氯环戊醇 6. (R)—3—氰基环戊酮 7.(R)—3—甲基—3—甲氧基—4—己烯—2—酮 8.(2E,4S )—4—氘代—2—氟—3—氯—2—戊烯9. (2R,3R )—2—溴—3—戊醇 10. (2S,4R )—4—氨基—2—氯戊酸 11. (S )—2—氯—1,4—环己二酮 12. (1S,3S )—3—甲基环己醇 13. (2R,3S )—2—羟基—3—氯丁二酸 14.(2E,4S )—3—乙基—4—溴—2—戊烯15. (1S,3S,5R )—1—甲基—3—硝基—5—氯环己烷 16. (3S,5R )—3,5—二甲基环己酮CH 333五.用Fisher投影式完成下列题目。

有机化学中的立体化学有机化学是研究含碳化合物的化学性质和反应机理的一个重要分支领域。
在有机化学中,立体化学是一个至关重要的概念,它研究的是有机分子中空间构型的特征以及由此带来的化学性质和反应特点。
立体化学的研究不仅深化了对有机化合物结构与性质之间关系的理解,也为合成有机化合物提供了重要的理论指导。
本文将从有机化学中的立体化学角度出发,探讨立体化学的基本概念、立体异构体的分类、手性分子的性质以及立体化学在药物合成和生物活性研究中的应用等方面展开阐述。
立体化学是研究有机分子空间构型的科学,它关注的是分子中不同原子或基团之间的空间排布关系。
在有机化学中,分子的立体构型对其化学性质和反应具有重要影响。
立体异构体是指分子结构相同但空间排布不同的异构体,主要包括构象异构体和对映异构体两种。
构象异构体是由于键的旋转或双键构型不同而导致分子整体结构不同的异构体,如环状分子的椅式和船式构象;而对映异构体则是镜像对称的立体异构体,它们在物理性质上几乎完全相同,但在化学性质和生物活性上却可能有着截然不同的表现。
手性分子是立体化学中一个重要的概念,它是指不能与其镜像重合的分子,即具有手性的分子。
手性分子由手性中心或手性轴引起,具有左右旋性质。
手性分子的对映异构体是非重叠的,它们在化学性质和生物活性上表现出截然不同的特点。
手性分子的研究不仅在有机合成领域有着广泛的应用,还在药物合成和生物活性研究中发挥着重要作用。
许多药物分子都是手性的,对映异构体可能具有不同的药理活性,因此在药物设计和合成过程中需要考虑手性对药效的影响。
立体化学在有机合成中有着重要的应用价值。
通过合理设计手性诱导剂或催化剂,可以有效地控制反应的立体选择性,实现对映选择性合成。
立体选择性合成不仅可以提高合成反应的产率和选择性,还可以减少废弃物的生成,具有重要的环境保护意义。
立体选择性合成在药物合成、天然产物合成以及材料化学等领域都有着广泛的应用,为有机合成化学提供了重要的理论基础和方法支持。


有机化学中的同分异构体与立体异构体有机化学是研究碳和碳之间的化学反应以及有机化合物的结构和性质的学科。
在有机化学中,同分异构体和立体异构体是两个重要的概念。
本文将着重探讨这两个概念,并分析它们在有机化学中的应用。
同分异构体是指分子式相同但结构不同的有机化合物。
由于碳原子可以形成多种键合方式,使得同样的原子可以以不同的方式排列,从而形成不同的同分异构体。
例如,丙酮和丙醇就是一对同分异构体。
它们的分子式都是C3H6O,但结构不同。
丙酮是一个酮,而丙醇是一个醇。
同分异构体的存在使得有机化学变得更加复杂,因为它们具有不同的化学性质和生物活性。
立体异构体是指分子式相同,但空间构型不同的有机化合物。
在立体异构体中,分子的原子排列相同,但它们的空间排列不同。
立体异构体可以分为两种类型:构象异构体和对映异构体。
构象异构体是指分子在空间中可以通过旋转单键或双键而相互转化的异构体。
对映异构体是指分子在空间中存在镜像对称的异构体。
对映异构体之间的空间排列是不可重叠的,就像左手和右手一样。
由于对映异构体的存在,有机化学中的立体化学变得更加复杂,因为它们的化学性质和生物活性可能截然不同。
同分异构体和立体异构体在有机化学中有着重要的应用。
首先,它们可以用于解释化合物的性质和反应。
同分异构体和立体异构体具有不同的化学性质,因为它们的分子结构不同。
通过研究同分异构体和立体异构体之间的差异,我们可以揭示化合物的反应机理和性质。
其次,同分异构体和立体异构体可以用于合成有机化合物。
在有机合成中,合成目标化合物的选择性合成是一个重要的问题。
通过调整反应条件和选择合适的反应试剂,可以选择性地合成同分异构体和立体异构体。
这为有机合成的发展提供了重要的指导。
此外,同分异构体和立体异构体还在药物研发中发挥着重要作用。
药物的立体异构体可能具有不同的生物活性和药效。
通过合成和研究药物的立体异构体,可以优化药物的性能和疗效。
同样,同分异构体也可以用于药物的设计和开发。



有机化学基础知识点立体异构体的烯烃与芳香烃在有机化学的学习中,立体异构体是一个重要的知识点。
立体异构体是指化学结构相同,但是空间构型不同的分子。
烯烃和芳香烃是有机化合物中常见的两类化合物,它们在立体异构体方面也有一些特点和规律。
本文将介绍有机化学基础知识点立体异构体在烯烃和芳香烃方面的研究进展。
烯烃是含有碳碳双键的烃类化合物,具有较高的反应活性和特殊的立体异构体性质。
通过双键位置、单键位置和碳链结构的不同,烯烃可以存在多种不同的立体异构体。
其中最常见的是顺式和反式异构体。
顺式异构体是指双键两侧的取代基在空间上相对排列较为接近,而反式异构体则是指双键两侧的取代基在空间上相对排列较为远离。
这种独特的排列方式使得顺式异构体和反式异构体在物理性质和化学性质上表现出差异。
例如,顺式异构体由于取代基之间的位阻导致分子间相互排斥力增大,使得其熔点和沸点相对较高;而反式异构体则由于双键取代基间的空间隔离,熔点和沸点相对较低。
芳香烃是由苯环结构为基础构建的有机化合物。
芳香烃的立体异构体主要是指苯环上取代基的不同排列方式。
当苯环上存在两个或多个不同的取代基时,它们可以以不同的顺序和位置进行排列,从而形成不同的立体异构体。
在芳香烃的立体异构体中,最常见的是间位异构体、邻位异构体和对位异构体。
其中,间位异构体是指取代基相互之间处于相对的位置;邻位异构体是指取代基相互之间处于相邻的位置;对位异构体是指取代基相互之间处于对称的位置。
这些不同的排列方式导致立体异构体在化学性质和物理性质上表现出差异。
总结一下,有机化学基础知识点立体异构体的研究对于理解烯烃和芳香烃的性质和反应机理具有重要意义。
研究发现,通过立体异构体的控制,可以调控化合物的性质和反应活性,有助于设计和合成更具有特殊功能和应用价值的有机化合物。
立体异构体的研究也为有机化学领域的理论建模和计算提供了一定的指导。
未来的研究工作应该在更深入和细致的层面上探索立体异构体的结构和性质之间的关系,促进有机化学领域的发展和应用。
有机化学中的烯烃的立体化学烯烃是一类重要的有机化合物,其分子结构中存在碳碳双键。
烯烃的立体化学是指双键两侧的立体构型,包括顺式和反式异构体以及立体异构体的构象。
1. 顺式和反式异构体顺式异构体是指双键两侧的取代基或原子位于同一侧,而反式异构体是指双键两侧的取代基或原子位于不同侧。
以丁二烯为例,顺式丁二烯的双键两侧的氢原子位于同一侧,而反式丁二烯的双键两侧的氢原子位于不同侧。
两者的分子结构不同,性质和化学反应也会有所差异。
2. 立体异构体的构象另一种烯烃的立体化学是立体异构体的构象。
立体异构体是指在同一分子中,由于双键的限制性旋转,使得取代基或原子的空间排列存在不同的构象。
以正戊烯为例,其中一个碳原子上存在两个不同的取代基:甲基和乙基。
这两个取代基相对于双键的排列方式不同,分别称为顺式构象和反式构象。
在顺式构象中,甲基和乙基位于双键的同一侧,而在反式构象中,甲基和乙基位于双键的不同侧。
3. 立体异构体的性质差异烯烃的立体异构体具有不同的空间结构,因此在性质和化学反应上表现出差异。
例如,顺式丁二烯由于双键两侧的氢原子位于同一侧,分子结构更加接近线性,容易发生加成反应。
反式丁二烯由于双键两侧的氢原子位于不同侧,分子结构更加扭曲,不容易与其他化合物发生反应。
立体异构体的存在还会影响烯烃的物理性质,如沸点、熔点和溶解度等。
不同的构象会导致分子之间相互作用的差异,进而影响它们在化学反应中的活性和选择性。
4. 研究方法与应用研究烯烃的立体化学需要使用一系列的分析和测定方法,如核磁共振(NMR)、红外光谱(IR)和质谱(MS)等。
这些方法可以帮助确定烯烃分子中取代基的相对位置和构象。
在有机合成领域,烯烃的立体化学研究对于设计和合成拥有特定立体结构的化合物至关重要。
通过控制反应条件,选择适当的立体异构体,可以高效地合成目标化合物。
此外,烯烃的立体化学也在药物研发和生物领域具有重要应用。
了解烯烃分子的立体构型,可以深入研究药物与受体的相互作用,从而设计出具有较高活性和选择性的药物分子。
有机化学反应的立体选择性研究有机化学是研究含碳的化合物的化学性质和反应规律的学科。
其中,有机化学反应的立体选择性研究是探索有机反应过程中所涉及的反应物、催化剂以及反应条件对反应产物立体结构的选择性影响的重要方面。
本文将从不同角度来阐述有机化学反应的立体选择性研究。
一、立体选择性的概念立体选择性指的是化学反应中产物的立体结构相对于反应物的特异性选择。
在有机合成中,常常存在着不同立体异构体的选择性合成问题。
通过对反应物、催化剂、溶剂、温度等不同因素的调控,可以实现特定立体异构体的高选择性合成。
二、立体选择性反应的机制在有机化学反应中,立体选择性的产生与反应中的过渡态结构和活化能有关。
反应的立体选择性可以通过几种机制来解释和研究,比如部分进入与完全进入、无选择性与单一选择性、大立体效应与小立体效应等。
1. 部分进入与完全进入部分进入是指反应物在反应中仅有一部分分子发生反应,产生特定立体异构体的产物。
而完全进入则是指所有反应物分子都能够形成特定立体异构体的产物,具有较高的立体选择性。
2. 无选择性与单一选择性无选择性反应是指反应物在反应中形成多种立体异构体的产物,缺乏立体选择性。
而单一选择性则是指在反应过程中形成一种特定的立体异构体产物。
3. 大立体效应与小立体效应大立体效应是指反应物分子与催化剂或溶剂等因素之间的相互作用能够显著影响反应产物的立体选择性。
而小立体效应则是指这种相互作用对立体选择性的影响较弱。
三、立体选择性研究的方法立体选择性研究是有机化学研究中的重要内容,通常采用以下方法来评价和探索反应的立体选择性。
1. 立体化学方法通过分析产物立体结构的实验数据,比如NMR、X射线衍射等技术,可以对反应过程中产生的立体异构体进行鉴定和定量分析。
2. 立体选择性因素的研究通过对反应物的结构、催化剂的种类和结构、反应条件的调控等因素的研究,可以了解它们对反应立体选择性的影响,并找到合适的条件来控制反应立体选择性。
有机化学基础知识点立体异构体的分类与命名立体异构体,作为有机化学领域中的重要概念,涉及到有机分子空间构型的不同形式。
本文将就立体异构体的分类与命名进行详细阐述。
一、立体异构体的概念立体异构体是指具有相同分子式、分子量相同的有机化合物,在空间构型上有所不同的化合物。
虽然它们的化学性质相同,但由于空间构型的异同,其物理性质可能存在显著的差异。
二、立体异构体的分类根据立体异构体的特点,我们可以将其分为以下两类:构象异构体和立体异构体。
1.构象异构体构象异构体是由于分子内部键的旋转而产生的异构体。
它们的化学键并未破裂,只是由于自由旋转的存在,使得它们的空间构型上存在差异。
构象异构体一般是同分异构体,即同一种化合物的空间构型在旋转键的影响下而改变。
2.立体异构体立体异构体是由于化学键的不同空间排列方式而产生的异构体。
它们的产生是由于化学键的旋转或断裂所引起的。
立体异构体包括两种基本类型:构造异构体和对映异构体。
(1)构造异构体构造异构体是指分子内原子的连接顺序不同所形成的异构体。
分子内原子的原子序数相同,但它们在空间构型上的排布不同,使得它们的化学性质和物理性质也不相同。
(2)对映异构体对映异构体是指分子在空间构型上与其镜像像面不重合的异构体。
对映异构体之间的关系类似于左手和右手的关系,无法通过旋转或平移使其完全重合。
对映异构体之间的主要差异在于对光线的旋光性质。
其中,左旋的异构体被称为“L体”,右旋的异构体被称为“D体”。
三、立体异构体的命名立体异构体的命名主要依据其空间构型的差异来进行。
下面以构造异构体和对映异构体为例进行说明。
1.构造异构体的命名构造异构体的命名主要基于其原子连接顺序的差异。
常用的命名方式有助记命名、系统命名和缩写命名等。
(1)助记命名助记命名是指通过描述分子的结构特点来进行命名。
例如,苯和萘就是两个常见的构造异构体,我们可以通过观察其分子结构特点,给予它们特定的命名。
(2)系统命名系统命名是根据有机化合物的化学式和结构特点来进行命名,以确保命名的准确性和一致性。
有机化学中的立体化学与空间构象有机化学是研究有机物质的结构、性质和反应的一门学科,而立体化学则是有机化学中的重要分支之一。
立体化学研究的是分子的空间构象以及分子之间的相互作用,对于理解有机化学反应的速率和选择性具有重要意义。
在有机化学中,分子的空间构象是指分子在三维空间中的排列方式。
分子的空间构象决定了分子的物理性质和化学性质。
一个分子的空间构象可以通过分子内的原子之间的键角和键长来描述。
例如,碳原子的四个共价键可以形成不同的空间构象,如平面构象、立体构象等。
不同的空间构象会导致分子的性质发生变化,从而影响分子的反应性质。
立体化学研究的一个重要概念是手性。
手性是指分子或物体无法与其镜像重合的性质。
在有机化学中,手性分子是指分子存在两个非重合的镜像异构体,即左旋体和右旋体。
手性分子的手性性质对于药物合成、生物活性和光学性质等方面具有重要的影响。
手性分子的产生通常与立体中心有关。
立体中心是指分子中一个碳原子上的四个不同基团。
当一个分子中存在立体中心时,就会产生手性分子。
手性分子的两个镜像异构体可以通过手性催化剂或手性试剂来分离。
手性分子的分离和合成是有机化学中的重要研究内容之一。
除了手性分子,还有一些其他的立体异构体。
顺式异构体和反式异构体是指分子中两个相邻的取代基的空间排列方式不同。
顺式异构体中相邻的取代基处于同一平面上,而反式异构体中相邻的取代基处于不同的平面上。
这种空间构象的不同会影响分子的性质和反应性质。
在有机化学中,立体异构体的研究对于理解化学反应的速率和选择性具有重要意义。
立体异构体之间的相互作用可以影响反应的速率和选择性。
例如,立体异构体之间的空间阻碍可以影响反应物分子之间的碰撞,从而影响反应的速率。
此外,立体异构体的选择性也会影响反应的产物的生成。
不同的立体异构体可能导致不同的反应产物的生成,这对于有机合成的设计和优化具有重要意义。
总之,有机化学中的立体化学与空间构象是研究分子的空间排列方式和相互作用的重要内容。
有机物的立体性
摘要:立体化学始终贯穿着现代有机化学的整个领域,因而立体化学是有机化学的一个重要组成部分,而立体异构又是立体化学的一个很重要的内容,它包括构象异构、顺反异构(也称几何异构)和旋光异构(也称光学异构包括对映异构和非对映异构),它有机反应有立体选择性。
关键词:构型,构象,异构体
立体异构是指分子中原子或官能团的连接顺序或方式相同,但在空间的排列方式不同而产生的异构,,顺反异构和旋光异构又叫做构型异构,它与构象异构的区别是:构型异构体的相互转化需要断裂化学键,室温下能够分离出异构体;而构象异构体的相互转化是通过碳碳单键的旋转来完成的,不必断裂化学键,室温下不能够分离出异构体(图1)。
立体异构体的类型
1 . 构型异构及其表达式
构型(configuration)是指具有一定构造的分子中原子或基团的固有空间排列,其构型的改变必须依靠共价键的断裂和生成。
分子构造相同而构型不同称为构型异构。
构型通常可用Fischer 投影式、Newman投影式、透视式和楔形式等4种方式表示。
表示构象的Newman投影式、透视式和楔形式也可表示构型,因为分子的构象确定了,构型也就确定了。
它们在表示构象的同时,也表示出了分子的构型。
而Fischer投影式只能表示构型,不能表示构象,因为在Fischer 投影式中,没能表示出由于单键的旋转,形成的分子中各原子或基团在空间的相对位置关系;另外构型确定了,构象还可能有多种,即在同一种构型中,可能有多种不同的构象。
Fischer投影式由于书写简单。
在标记手性碳原子的构型时又十分方便,被广泛采用。
其书写时遵循“碳链竖放,编号小的置于上”和“横前竖后碳居中”的规则(这里不再具体赘述)。
若对Newman投影式、透视式和楔形式直接进行构型标记,因此,常常把分子构型的其它表达式转化为Fischer投影式,又因为Fischer投影式是重叠式构象,其它不同构型的表达式一定要通过σ键的旋转,转换为全重叠式后再进行构型标记。
由图4可以看出,不管是透视式、Newman 投影式还是楔形式都要根据仃键可以绕键轴自由旋转(不会改变其构型)的性质,将它们碳原子处于交叉位置的构象换为处于重叠位置的构象后,才可直接转换为费歇尔投影式,并进行构型标记。
2. 构象异构及其表达式
构象(conformation)是指具有一定构造的分子,由于单键的旋转而使分子中各原子或基团在空间的排布状况,是指一个分子在空间可能采取的姿态。
构象在理论上有无数种,但通常只考虑它的极限构象,即最稳定和最不稳定的构象,其它构象介于二者之间,它研究的是分子采取哪种姿态能量最低的问题。
构象之间的转变通过分子的热运动就能实现,不需要共价键的断裂和生成。
构象通常用Newman投影式、透视式(或称锯架式)和楔形式(或称伞形式)3种方式表示¨J。
构象的3种不同表示方式各有优点:透视式和楔形式能形象、直观、清楚地观察分子中所有的价键,Newman投影式可以很好地表示各原子和基团之间的相对位置关系。
如2,3一二溴丁若绕c:和c,之间的盯单键旋转能产生4种典型的极限构象(用Newman投影式表示,图2);能
量最高的是全重叠式,它是最不稳定的构象;能量最低的是对位交叉式,它是最稳定的构象。
这3种构象表达式之间的转换可以这样描述(图3):把Newman投影式看成是正对观察者的被高度压缩而成的弹簧然后把它弹放出来,同时让c:一C,键与水平面成45角放置后就变成透视式,若让C:一C,键水平放置,实楔线表示在纸平面直线表示在纸平面上,即“实前虚后线平面”,这样就变成楔形式前方,虚楔线表示在纸平面后方。
3. 糖的环状结构的Haworth式
自然界中的单糖普遍是以五、六元环存在的,因此用直立的环状投影式不能反映出各个基团的相对空间关系,所以应把环状结构写成透视式即Haworth式,它能够较真实地反映出单糖分子中各个原子或基团的相对关系。
由Fischer投影式写成Haworth式的规则是:根据欲写出的Haworth式环的大小确定参与成环的--OH,并通过原子或基团互换而不改变分子构型的操作,然后将碳链放成水平状,再将碳链按水平位置弯成六边形,这样C,上的—oH可以与—cH0形成半缩醛形式(形成吡喃环),这样一cHO的碳原子(C。
)就变成的手性碳,那么半缩醛碳上的羟基(C。
上的羟基,称之为苷羟基)若与尾基—CH20H(C,上的羟甲基)在环的异侧称为a型,在
环同侧为B型。
4. 顺/反、cis/trans和Z/E异构体
在构型异构中包括有顺反异构,它是因双键或环不能自由旋转,导致原子或基团在空间结构中排列不同而产生的异构。
为了表示这种不同的异构,最初以cis/trans来区别,即当相同的原子或基团位于双键或环的同侧时为cis式化合物,我们称之为顺式化合物;位于异侧时则为trans式化合物,即反式构型。
这种cis/trans命名方法和我国顺/反命名方法是相对应的,也是一致的,但是在文献中cis/trans还是常用的,这两套命名目前作为俗名看待。
它们的缺点是这两种命名系统只适用于双键或环上至少有一对原子团是相同的情况,假如4个基团或原子团皆不相同,则它们就不适用了。
为解决这一问题IUPAC的有机化学命名委员会使用Z/E命名系统,按次序规则,当次序较高的两个基团处于双键的同侧时为z构型,若在异侧时为E构型。
在大多数情况下,z等于传统的顺式(或cis一),E等于传统的反式(或trans一);但是,顺/反、eis/trans与Z/E也有不一致的情况,即顺式不一定是Z构型,反式也不一定是E构型。
5. 内型(endo一)/外型(exo一)和顺型(syn一)/反型(anti一)异构体
它们分别是描述桥环化合物中原子或基团的相对位置⋯。
取代基位于主桥相反的位置或位于环内障碍较大的位置,则称内型(endo一)异构体,若取代基位于靠近主桥的位置或位于环外障碍较小的位置,则称外型(exo一)异构体;在主桥上的取代基与编号最小取代基所处的环位于同侧称为syn型,位于异侧称为anti型。
一般主桥的确定遵循以下规则:①含杂原子的桥;②含取代基较少的桥;③含最低次序的取代基。
6 .赤式(erythro一)/苏式(threo一)和D型/L型异构体由碳水化合物的命名而来川,用来表述相邻立体中心的相对构型,通常用来专门用于处理含两个不同的手性碳原子的分子的,它源出于赤藓糖(erythrose)和苏阿糖(threose)。
具体指相邻碳上的两个相同(或相似)的原子(团)在Fischer投影式中位于同侧的称为赤式(erythro一),处于异侧的为苏式(threo一);
D/L系统目前主要在碳水化合物和氨基酸的命名上用途较大,其它化合物的命名现在已经被绝对构型(物质的真实构型)R/S命名系统所取代;D/L系列是相对构型,在还没有适当的方法测定旋光物质的绝对构型以前,人们为了研究方便,选择了甘油醛作为标准,人为地规定它们的构型,即甘油醛的Fischer投影式中,——0H在碳链的右侧时标记为D型,在左侧的标记为L型;从D一甘油醛衍生的一系列D型异构体简称为D系列,同样,从L一甘油醛衍生的一系列L型异构体简称为L系列;当化合物中有多个手性碳原子时,一般以最下面的手性碳原子为准;自然界存在的糖类大多是D型的,而天然产的氨基酸主要是L型的。
D/L这种相对构型表示法在使用范围上有其明显的局限性,它要求水平位置必须有一个是氢原子,这样只有仅一羟基酸和n一氨基酸化合物中能达到这一要求,对于其它更普遍的情况已不适用了,同时对于手性碳原子不只一个时常常被绝对构型R/S命名系统所取代。
7. 差向异构体
在分子中存在两个以上手性碳原子,而在反应中,仅仅改变其中一个手性碳原子的构型,这类反应称为差向异构化反应。
经差向异构化后的产物属于两种不同立体构型的化合物,彼此称为差向异构体。
差向异构体之间是非对映体关系。
如葡萄糖和乳糖两者为差向异构体。
(+)一樟脑用硝酸氧化后获得(+)一顺式樟脑酸,后者在酸或碱的作用下发生差向异构化反应,最后获得的差向异构产物(一)一反式樟脑酸,它们的差别只在于C,的构型不同。
以碳碳双键上的加成反应来说明研究立体化学在反应历程研究中的应用.
大家都知道2-丁烯与卤素的加成反应产物分子中有两个手性碳原子,应有四个立体异构体,但是,它们是两个相同的手性碳原子,所以,只有三种异构体。
2-丁烯与稀,冷高锰酸钾的碱性水溶液反应的顺式二羟基化产物的立体化学为
综上所述,我们认识到化合物的立体结构以及立体结构对化学反应产物的生成有重要作用。
参考文献:
[1] 彭梦侠,陈梓云.构型与构象教学的探索[J].嘉应学院学报(自然科学),2006,24(3):49—53.
[2] 来水利.立体化学教学中的有关问题的讨论[J].陕西师范大学学报(自然科学版),2005,33(Sup.):270—272.
[3] 赵郁,刘新宇,杨宇虹,解用虹.构型与构象[J].生命的化学,2004,24(2):170—171.
[4] 刘伯渠.构型异构的判断方法及其应用[J].安庆师范学院学报(自然科学版),2008,14(4):91—93.
[5] 邢其毅,裴伟伟,徐瑞秋,裴坚.有机化学(第3版)[M].北京:高等教育出版社,2005.
[6]Moss,G P.Basic terminology of stereochemistry[J].Pure&Appl.Chem.,1996,68(12):2193—2222.
[7] 曾昭琼.有机化学(第4版)[M].北京:高等教育出版社,2004.
[8]]董恒山.烯烃加成立体化学的讨论[J].教材通讯1987(3).33。