ASP实验指导
- 格式:ppt
- 大小:164.00 KB
- 文档页数:41

计算机网络实验指导书-TCP协议分析及应用层命令实验指导教师:韩家伟孙玉钰实验4TCP报文段分析及应用层命令实验1.实验目的1.掌握使用IRIS工具对TCP与UDP协议进行抓包分析的方法。
2.掌握TCP协议的报文格式及其优缺点。
3.熟悉应用层命令。
2.实验设备与环境1.Iris网络分析软件2.网络数据包捕获3.捕获TCP报文段并分析(一)实验内容1.启动网络嗅探工具,设置好过滤条件,捕获UDP用户数据报和TCP报文段。
2.分析UDP与TCP协议。
(二)TCP协议实验指导传输控制协议(Transmission Control Protocol,TCP)是一种可靠的面向连接的传送协议。
它在传送数据时是分段进行的,主机之间交换数据必须建立一个会话。
它用比特流通信,即数据被作为无结构的字节流。
通过每个TCP传输的字段指定顺序号,以获得可靠性。
它是在OSI参考模型的第4层,TCP是使用IP的网际间互联功能而提供可靠的数据传输,IP不停地把报文放到网络上,而TCP负责确信报文到达。
在协同IP的操作中TCP负责握手过程、报文管理、流量控制、错误检测和处理(控制),并根据一定的编号顺序对非正常顺序的报文给予重新排列顺序。
TCP是面向连接的协议。
在面向连接的环境中,开始传输数据之前,在两个终端之间必须先建立一个连接。
对于一个要建立的连接,通信双方必须用彼此的初始化序列号seq和来自对方成功传输确认的应答号ack(指明希望收到的下一个八位组的编号)来同步,习惯上将同步信号写为SYN,应答信号写为ACK。
整个同步的过程称为三次握手,如图4-1所示。
图4-1 TCP连接的建立对于一个已经建立的连接,TCP使用四次握手来结束通话(使用一个带有FIN附加标记的报文段)。
如图4-2所示。
图4-2 TCP连接的释放TCP每发送一个报文段,就对这个报文段设置一次计时器。
只要计时器设置的重传时间到期,但还没有收到确认,就要重传这一报文段。

金陵科技学院信息技术学院《软件体系结构》实验指导书实验1 多层C/S结构应用设计一、实验目的设计并实现一个基于多层C/S结构的数据库应用,熟悉多层C/S体系结构及其基本处理流程,了解多层结构表现层、业务逻辑层(功能层)、数据访问层所完成的功能,掌握多层C/S结构的数据库应用设计方法,对这三层进行明确分割,并在逻辑上使其独立。
学生通过本实验的训练能够熟练掌握对小型数据库应用系统三层结构层次划分方法及系统实现技术。
二、实验要求(1)记录系统分析及层次结构设计的过程,调试程序要记录调试过程中出现的问题及解决办法;(2)编写程序要规范、正确,上机调试过程和结果要有记录,不断积累编程及调试经验;(3)做完实验后给出本实验的实验报告。
三、实验设备、环境奔腾以上计算机,Windows XP 、Visual Studio 2005、SQL Server 2005四、实验步骤及内容分别采用二层C/S结构和多层C/S结构实现个人通讯录系统。
该系统的设计目标是能够轻松地管理个人的联系人信息,包括添加、修改和删除操作。
联系人信息包括姓名、住址、电话。
整个系统的功能图如下图所示:分析系统需求,完成软件体系结构设计及模块划分、数据库设计,采用Visual C#实现系统功能。
五、讨论、思考题与二层C/S体系结构比较,三层(多层)体系结构有什么有点?采用三层体系结构在系统设计时应该注意哪些问题?金陵科技学院信息技术学院实验2 B/S结构应用设计一、实验目的设计并实现一个基于B/S结构的数据库应用,熟悉B/S体系结构及其基本处理流程,了解B/S结构系统各部分所完成的功能,掌握B/S结构的数据库应用设计方法。
学生通过本实验的训练能够熟练掌握对小型数据库应用系统B/S结构设计及系统实现技术。
二、实验要求(1)记录系统分析及结构设计的过程,调试程序要记录调试过程中出现的问题及解决办法;(2)编写程序要规范、正确,上机调试过程和结果要有记录,不断积累编程及调试经验;(3)做完实验后给出本实验的实验报告。

《云计算,大数据技术及应用》实验指导书《云计算,大数据技术及应用》课程的实验环节意在通过实践使学生对课程内容有更加感性的认识,加深和提高对云计算的理解。
培养学生的实际动手能力,独立解决实际问题的能力,实现“做中学,学中做”的目的。
为帮助学生更好地完成实验考核和实验报告,特作如下说明和要求:(1)做好每个实验的准备工作:需要对每个要做的实验进行预习,了解相关内容、知识点和具体要求,并且复习与课程有关内容和阅读实验指导书,明确实验目的要求、实验内容和实验步骤;(2)认真完成实验的各个环节:每个学生都必须在规定时间到机房做实验,并且遵守实验室的纪律,认真做实验。
在实验中,根据所给的实验内容进行认真的分析和实施,结合课堂知识完成实验,按实验步骤认真完成每步的工作。
实验完成后要做认真的整理和总结,记录重要的结果数据;(3)完成实验报告:做完每个实验后要严格按照实验报告的格式要求,写出实验报告。
实验报告的内容有以下几个部分:实验名称、实验目的、实验内容和要求、以及实验结果。
实验一:Windows Azure云平台搭建和部署云平台服务一:实验目的1.通过微软公司提供的验证码激活账号,登录微软公司的Windows Azure云计算平台;2.把Windows Azure开发环境安装好,为以后的实验作准备;3.在Windows Azure下开发项目并且发布;二:实验设备1.安装Windows 7 Professional Edition or higher的计算机,推荐用个人的电脑;2.稳定高速的High Speed Internet;三:预习要求:1.认真预习本实验的要求与实验任务,做好准备。
2.认真复习第一章和第二章云计算的基本知识;3.认真学习课本第五章有关Windows Azure云计算平台的基本知识;4.要求在做实验之前就对实验的任务和步骤比较清楚;四:实验任务1.通过微软公司提供的验证码激活账号,登录微软公司的Windows Azure云计算平台.然后要按照以下办法在Windows Azure下面创建网站并且发布到Windows Azure云平台上;2.利用提供的Windows Azure Training Kit 的目录:L1 Cloud Introduction,创建一个Windows Azure Web Site网站,然后用FTP客户得到一个运行在云中的ASP Legacy page 网页,记录下Internet上能够访问它的网络链接web link;实验二:学习Windows Azure存储一:实验目的e Blob Service(先做);e Table Service;e Queue Service;二:实验设备1.安装Windows 7 Professional Edition or higher的计算机,推荐用个人的电脑;2.稳定高速的High Speed Internet;三:预习要求:1.认真预习本实验的要求与实验任务,做好准备;2.认真学习课本上第五章《Windows Azure云计算平台》5。

做数据库实验的心得体会范文5篇做数据库实验的心得1持续一个月的数据库实训,让我参与了软件工程化的开发过程。
其中体会最深的便是我们这个实训网的几个之最:一.项目最大:项目大是因为我们这个事业起点网站涉及到用户众多-高校,企业,学生,老师,专家,第二个原因是网站的功能多-用户管理,网上实习,网上竞赛,毕业实习设计,项目管理,人才库管理,人才推荐,搜索项目大很容易造成系统范围的泛滥,在我们的开发初期,由于需求不太明确,功能实现没有重点,造成了需求范围的扩大,给项目开发进度造成了严重的滞后性。
然后我们召开了会议讨论了这个问题,一致认同先把项目的基本功能实现,将网站的基本架构搭建起来,最后再在这个基础上继续增加我们网站的其他功能。
因此在这个过程中,我深刻体会到了软件工程初期阶段的需求分析以及概要设计的重要性,这两个文档是指导我们后期开发的最重要的依据。
二.数据库表最多:如此庞大的系统,就需要庞大的数据库来支持,所以项目大的直接后果就是我们的数据库表特别多,而且表与表之间的依赖关系也复杂,实体类之间的关系众多,设计起来有一定的难度。
数据库的另外一个问题是-数据表的属性,数据表属性的设计完全是依赖于我们刚开始做的需求分析文档,如果需求分析不完整的话,就会造成数据库表属性的缺失,从用户的角度看,就会觉得你的系统提供的数据不够全面,信息量小。
三.开发团队最大:我们团队一共有十四个人,这个对于我们的项目经理来说,是一个相当严峻的问题,毕竟十四个人的团队相当于其他几个小组加起来的人数总和,管理起来有相当大的难度。
对于我们这些小组成员来说,由于沟通渠道太多,造成了我们项目中遇到问题,不知道去跟哪个小组成员沟通。
为了解决这个问题,我们在团队中又选出了三个小组长,小组成员遇到问题,先去咨询小组长,然后小组长提供反馈信息。
四.项目各个模块间藕合度高:网站涉及的各个功能模块之间的联系紧密,模块之间的接口设计的好坏是项目最终集成成功与否的最重要因素。
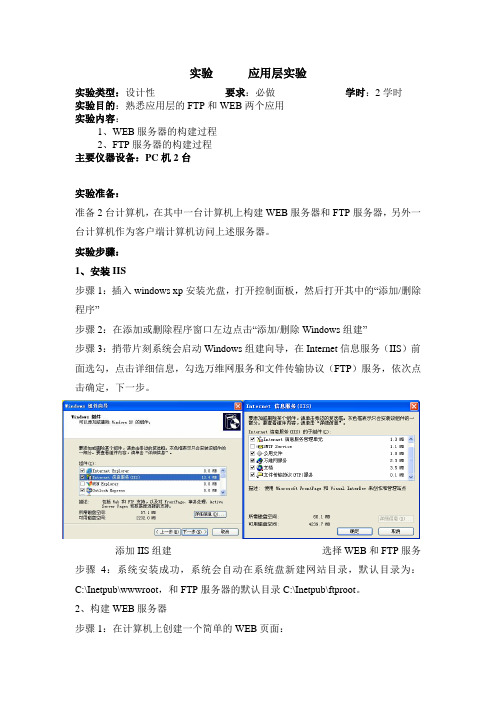
实验应用层实验实验类型:设计性要求:必做学时:2学时实验目的:熟悉应用层的FTP和WEB两个应用实验内容:1、WEB服务器的构建过程2、FTP服务器的构建过程主要仪器设备:PC机2台实验准备:准备2台计算机,在其中一台计算机上构建WEB服务器和FTP服务器,另外一台计算机作为客户端计算机访问上述服务器。
实验步骤:1、安装IIS步骤1:插入windows xp安装光盘,打开控制面板,然后打开其中的“添加/删除程序”步骤2:在添加或删除程序窗口左边点击“添加/删除Windows组建”步骤3:捎带片刻系统会启动Windows组建向导,在Internet信息服务(IIS)前面选勾,点击详细信息,勾选万维网服务和文件传输协议(FTP)服务,依次点击确定,下一步。
添加IIS组建选择WEB和FTP服务步骤4:系统安装成功,系统会自动在系统盘新建网站目录,默认目录为:C:\Inetpub\wwwroot,和FTP服务器的默认目录C:\Inetpub\ftproot。
2、构建WEB服务器步骤1:在计算机上创建一个简单的WEB页面:在Notepad(记事本)中,键入下列文本:<html><head><title>网站在构建中……</title></head><body><h1> 本页面在构建中……</h1><p>更多的信息将在这里发布 </p></body></html>另存为网页文件,例如index.html注意:网站首页一般以default.htm或index.htm保存。
以便让WEB浏览器显示而不需要指定该页面的名字。
并将该文件复制到C:\Inetpub\wwwroot文件夹中或其他指定文件夹中。
步骤2:依次选择“开始”→“设置”→“控制面板”→“管理工具”→“Internet 信息服务”,打开“Internet信息服务”对话框。

网页制作实习报告(6篇范文)【导语】网页制作实习报告怎么写好?本文精选了6篇优秀的网页制作实习报告范文,都是标准的书写参考模板。
以下是小编为大家收集的网页制作实习报告,仅供参考,希望您能喜欢。
【第1篇】网页制作实习报告一实验过程1.资料的搜集。
2.熟悉制作软件。
3.构建站点框架。
打开dremweaver后第一步便是新建站点4设计主页及二级页面。
5实现网页间的链接链接的过程其实很简单,主要是把要链接的文字选择在选择工具栏的链接按钮最后选择自己要链接的网页单击确定便可以了。
6向静太网页插入动态效果具体情况如下:通过这半年的学习实践中和老师的指导下以大量明晰的操作步骤和典型的应用实例,教会我们。
使更丰富全面的软件技术和应用技巧,使我们真正对所学的软件融会贯通。
所以我结合所学专业的内容制作了个人网站,作为实习的成果。
其内容是多样化的。
制作网页用的软件是dreamweaver , banner软件。
dreamweaver大大加速了网络时代电子交易应用中的项目交付。
它提供了网页和表单的动态生成到企业级的解决方案,如电子商店,库存管理系统和企业内部局域网的数据库应用等功能。
例如,网页上很流行的阴影和立体按纽等效果,只需单击一下就可以制作完成。
当然,其最方便之处是,它可以将图象切割,图象映射,悬停按纽,图象翻转等效果直接生成html代码,或者嵌入到现有的网页中,或者作为单独的网页出现。
主图是一个网页的门面,它能体现出这个网页的整体风格。
制作网页,首先是确定主题,经过再三考虑,就做了个关于中国的网站,平时也总是浏览类似的网站,对这些还有些了解,于是确定主题,做一些类似的网站,但考虑到,现在网络上好多类似的网站,但有些内容不适合我们大学生阅读,对于我们来说有点不实际,根据这种情况,最后决定建立一个简单的中国介绍和相关的事迹网站,专门介绍一些即使用,又便宜的小秘笈。
于是网站主题确立。
然后是整体规划,每一版块都有其个性的色彩,清晰明了,便于阅读浏览,大致分几部分,中国简介,中国历史,用户登录注册页面留言,再加入个别网站等,每一部分又分几小部分,内容比较充分,多样。
各种酶活性测定方法第一超氧化物歧化酶SOD测定一、原理超氧物歧化酶〔superoxidedismutase,SOD〕普遍存在于动、植物体内,是一种清除超氧阴离子自由基的酶.本实验依据超氧物歧化酶抑制氮蓝四唑〔NBT〕在光下的还原作用来确定酶活性大小.在有氧化物质存在下,核黄素可被光还原,被还原的核黄素在有氧条件下极易再氧化而产生O2,可将氮蓝四唑还原为蓝色的甲腙,后者在560nm处有最大吸收.而SOD可清除O2,从而抑制了甲腙的形成.于是光还原反应后,反应液蓝色愈深,说明酶活性愈低,反之酶活性愈高.据此可以计算出酶活性大小.二、材料、仪器设备与试剂〔一〕材料;水稻或小麦叶片〔二〕仪器设备:1.高速台式离心机;2.分光光度计;3.微量进样器;4.荧光灯〔反应试管处照度为4000Lx〕;5.试管或指形管数支.〔三〕试剂 1. 0.05mol/L 磷酸缓冲液〔pH7.8〕;2. 130mmol/L 甲硫氨酸〔Met〕溶液:称1.9399gMet用磷酸缓冲液定容至100ml;3.750μmol/L 氮蓝四唑溶液:称取0.06133gNBT用磷酸缓冲液定容至100ml,避光保存;4. 100μmo l/L EDTA-Na2溶液:称取0.03721gEDTA-Na2用磷酸缓冲液定容至1000ml;5. 20μmol/L 核黄素溶液:称取0.0753g核黄素用蒸馏水定容至1000ml避光保存.三、实验步骤1. 酶液提取取一定部位的植物叶片〔视需要定,去叶脉〕0.5g于预冷的研钵中,1ml预冷的磷酸缓冲液在冰浴上研磨成浆,加缓冲液使终体积为5ml.取 1.5~2ml于1000rpm下离心20min,上清液即为SOD粗提液.2. 显色反应取5ml指形管〔要求透明度好〕4支,2支为测定管,另2支为对照管,按下列加入各溶液:试剂〔酶〕用量〔ml〕终浓度〔比色时〕0.05mol/L 磷酸缓冲液1.5130mmol/L Met 溶液0.313mmol/L 750μmol/L NBT溶液0.375μmol/L 100μmol/L EDTA-Na2液0.310μmol/L 20μmol/L 核黄素0.320μmol/L 酶液0.052支对照管以缓冲液代替酶液蒸馏水0.25总体积3.0混匀后将1支对照管置暗处,其它各管于4000Lx日光下反应20min〔要求各管受光情况一致,温度高时间缩短,低时延长〕.3. SOD活性测定与计算至反应结束后,以不照光的对照管做空白,分别测定其它各管的吸光度.四、结果计算已知SOD活性单位以抑制NBT光化还原的50%为一个酶活性单位表示,按下式计算SOD活性.SOD总活性=<A ck-A E>×V/<A ck×0.5×W×V t>上式中,SOD比活力=SOD总活性蛋白质含量式中SOD总活性以每克鲜重酶单位表示;比活力单位以酶单位/mg蛋白表示Ack照光对照管的吸光度AE样品管的吸光度V样品液总体积〔ml〕Vt测定时样品用量〔ml〕W样鲜重〔g〕蛋白质含量单位为:mg蛋白/g鲜重. SOD、POD、CAT、MDA的测定方法-非试剂盒法缩写:SOD:超氧化物歧化酶; CAT:过氧化氢酶; POD:过氧化物酶; MDA:丙二醛;PVP:聚乙烯吡咯烷铜K-30;L-Met:甲硫氨酸;NBT:氮蓝四唑;TBA:硫代巴比妥酸;TCA:三氯乙酸;PBS: 磷酸缓冲液1. SOD的测定方法加样顺序:〔V=3ml〕磷酸缓冲液:1.5ml L-Met: 0.3mlNBT: 0.3mlEDTA-Na2: 0.3ml 核黄素:0.3ml 酶液:0.05ml 蒸馏水:0.25ml试剂配制:<1> 0.05mol/L PBS:pH7.8<2> 130mmol/L L-Met: 1.9399g Met用PBS定容至100ml<3> 750mmol/L NBT: 0.06133g用PBS定容至100ml<避光保存><4> 100umol/L EDTA-Na2: 0.03721g用PBS定容至1000ml<5> 20umol/L核黄素: 0.0753g用蒸馏水定容至1000ml<避光保存>注:〔1〕对照:以加缓冲液、不照光为空白;照光的为最大还原管<2> 照光后至显蓝色要立即避光放置、迅速测定A560值2.MDA的测定方法试剂配制:〔1〕5% TCA: 5g用蒸馏水定容至500ml〔2〕0.5% TBA:2.5g用TCA定容至500ml方法:酶液1ml—3ml0.5%TBA和5%TCA—混合后在100度水浴煮沸15min—迅速冷却,10000r/min 离心10min—用蒸馏水调零分别测定上清液在532nm、600nm处的吸收值3.POD的测定方法试剂配制:〔1〕0.1mol/L的醋酸缓冲液:8.8mlA+41.2mlB得到100mlph5.4的醋酸缓冲液A<0.2mmol/L的HAc溶液>—6ml冰醋酸溶到494ml蒸馏水中〔2〕0.25%愈创木酚溶液—125um愈创木酚溶于50ml 50%乙醇中〔临用前配制〕〔3〕0.75%H2O2溶液:1.25ml 30% H2O2定容至50ml〔临用前配制〕方法:比色杯中依次加入2ml 0.1mol/L的醋酸缓冲液—1ml 0.25%愈创木酚溶液—xml酶液〔5min值为500-800即可〕—0.1ml 0.75%H2O2溶液—迅速巅到混匀把A460调零并开始计时—1次/30s,连续读取3min4.CAT的测定方法试剂配制:<1> 50mmol/L的PBS〔pH7.0〕 <2> 0.3% H2O2—1ml H2O2定容至100ml方法:<1>以不加H2O2的50mmol/L的PBS〔pH7.0〕为空白把A240调零<2>50ul酶液—3ml 50mmol/L的PBS〔pH7.0〕—0.2ml 0.3% H2O2—迅速颠倒混匀,开始计时—1min后在240nm下比色,1次/1min<连续读取5min>.20XX06月22日星期二 19:331 叶绿素含量测定:80%的丙酮液的配制:4L丙酮+ 1L蒸馏水.称0.5g左右的叶片放在50ml的离心管〔做三个重复〕,加入25ml浓度为80%的丙酮液,放在黑暗处浸提大约36小时后取出,稀释4倍后分别在波长663nm、645nm、652nm和470nm 下测定光密度,以80%的丙酮液为空白.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P35~36〕也可用95%乙醇溶液,在665、649、470nm处有最大吸收峰649Cx.c=<1000D470-2.05Ca-114Cb>/2452 抗氧化酶活性的定:〔2.5g样〕0.05mol/L磷酸缓冲溶液<PBS>〔pH=7.8〕溶液的配制:65.5506g Na2HPO4·12H2O + 2.65285g NaH2PO4·2H2O, 定容到4L.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P134〕. 取低温保存的鲜样,称2g左右的叶片〔或根〕放在50ml的离心管,加入20ml浓度为0.05mol/L 磷酸缓冲溶液〔pH=7.8〕〔最好是较冷的磷酸缓冲溶液,防止研磨时温度过高使酶失活〕,研磨〔用磨碎机磨〕,8000r/min的冷冻离心机下离心20分钟,上清液为粗酶液.2.1丙二醛〔MDA〕的测定:20%三氯乙酸〔TCA〕溶液的配制:称200g三氯乙酸,用蒸馏水定容到1000ml.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P124〕;0.5% 硫代巴比妥酸〔TBA〕溶液的配制:称5g硫代巴比妥酸〔TBA〕,用20%三氯乙酸〔TCA〕溶液溶解并定容到1000ml.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P124〕〔先加少量的氢氧化钠1mol/L溶解〕;0.5ml酶液〔对照用0.5ml的0.05mol/L pH=7.8的磷酸缓冲液代替酶液〕〔做三个重复〕+ 3mlTBA――振荡――沸水浴上反应30min――冷却〔至少30min〕――比色〔OD600、OD532、OD450〕.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P124〕2.2超氧化物歧化酶〔SOD〕的测定:NBT<400ml>混合反应液:392mlPBS<Ph=7.8>,+0.0206g NBT+ 0.776g甲硫酸铵+8ml核黄素溶液+0.4ml EDTA-Na溶液〔100mlPBS缓冲溶液中含0.01204g核黄素〕.〔另配〕100ml PBS溶液加EDTA-Na 3.7224gEDTA-Na测试时:取3ml反应液+0.05ml<根>或0.02 ml<叶>粗酶液,于光照培养箱中6-10分钟,OD650下测定吸光度.2.3过氧化物酶〔POD〕的测定:0.05mol/L磷酸缓冲溶液<PBS>〔pH=7.0〕溶液的配制:10.9251g Na2HPO4·12H2O + 3.042975g NaH2PO4·2H2O,定容到1000ml.0.3%H2O2溶液的配制:吸2.5ml 30%H2O2,用0.05mol/L pH=7.0磷酸缓冲溶液<PBS>定容到250ml.0.2%愈创木酚溶液的配制:称0.5g愈创木酚,用0.05mol/L pH=7.0磷酸缓冲溶液<PBS>定容到250ml.2ml 0.3%H2O2溶液+ 0.95ml 0.2%愈创木酚溶液+ 1ml 0.05mol/L pH=7.0磷酸缓冲溶液<PBS> + 0.02ml??〔原来为0.01〕酶液〔根加0.05ml酶液〕〔对照用0.05mol/L磷酸缓冲溶液代替酶液〕〔做三个重复〕,记录470nm处OD降低速度.将每分钟OD增加0.01定义为1个活力单位.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》P121〕比色时加酶液,混合后即刻计时.2.4 脯氨酸的测定标准曲线的制作:编号1234567标准脯氨酸的量〔ml〕00.10.20.40.60.81.0H2O〔ml〕1.00.90.80.60.40.20冰乙酸〔ml〕2222222显色液〔ml〕3333333脯氨酸含量〔µl〕012468100.5ml酶液〔对照用0.5ml 80%乙醇代替〕〔做三个重复〕+ 1ml冰乙酸+ 1.5ml显色液―――混匀,沸水浴15min,冷却后测OD520.2.5可溶性蛋白的测定〔参考赵志杰,史国安,董新纯编的《植物生理学实验指导》〕牛血清白蛋白:配成100µg/ml和1000µg/ml.90%乙醇:90ml乙醇+ 10ml蒸馏水.???85%〔W/V〕磷酸:170ml磷酸+ 30ml蒸馏水.考马斯亮蓝G-250:称0.2g考马斯亮蓝G-250溶于100ml 90%乙醇中,加入85%〔W/V〕磷酸200ml,用蒸馏水定容到2L.常温下可保存一个月.标准曲线的制作:配制0~100µg/ml血清白蛋白血液管号123456100µg/ml牛血清白蛋白<ml>00.20.40.60.81.0蒸馏水量<ml>1.00.80.60.40.20蛋白质含量〔ml〕00.020.040.060.080.10配制0~1000µg/ml血清白蛋白血液管号789101112100µg/ml牛血清白蛋白<ml>00.20.40.60.81.0蒸馏水量<ml>1.00.80.60.40.20蛋白质含量〔ml〕00.20.40.60.81.00.1ml 酶液〔做三个重复〕+ 5ml考马斯亮蓝G-250―――混匀,放置2min后在595nm下比色.2.6过氧化氢酶〔CAT〕的测定:0.3%H2O2溶液的配制:吸5ml 30%H2O2,用0.05mol/L pH=7.0磷酸缓冲溶液<PBS>定容到500ml.1 ml 0.3%H2O2溶液+ 1.9ml H2O + 0.1 ml 酶液,测定240nm处OD降低速度.将每分钟OD 减少0.01定义为1个活力单位.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》P121〕2.7 抗坏血酸〔ASA〕的测定:〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P125〕5%三氯乙酸〔TCA〕溶液的配制:25g三氯乙酸,用蒸馏水定容到500ml.10%三氯乙酸〔TCA〕溶液的配制:25g三氯乙酸,用蒸馏水定容到250ml.150mmol/L NaH2PO4〔pH 7.4〕溶液的配制:100ml.44%H3PO4溶液的配制:250ml.4%2,2-二联吡啶溶液的配制:250ml.3%FeCl3溶液的配制:100ml.首先标制作准曲线.粗酶液的提取:取低温保存的鲜样,称0.5g左右的叶片〔或根〕放在50ml的离心管,加入15m 5%三氯乙酸〔TCA〕溶液〔最好是较冷的三氯乙酸〔TCA〕溶液,防止研磨时温度过高使酶失活〕,研磨〔用磨碎机磨〕,15000r/min的冷冻离心机下离心10分钟,上清液为粗酶液,用于抗坏血酸〔ASA〕含量的测定.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》P125~126〕测定:0.2ml 粗酶液+ 0.2ml 150mmol/L NaH2PO4〔pH 7.4〕溶液+ 0.2ml H2O,混匀〔振荡〕,至少30秒后,再依次分别加入:0.4 ml 10%三氯乙酸〔TCA〕溶液+ 0.4 ml 44%H3PO4溶液+ 0.4 ml 4%2,2-二联吡啶溶液+ 0.2ml 3%FeCl3溶液,混合后在37℃水浴中保温60min,测定OD525处的值.〔参考陈建勋,王晓峰主编的《植物生理学实验指导》P125~126〕2.8 谷胱甘肽的测定:4g新鲜材料+ 2ml 0.3mol/L醋酸汞+ 2ml 30%醋酸钠后研磨匀浆,转移到离心管中,以蒸馏水冲洗残渣,并以玻璃棒搅拌,净置10min,使之充分沉淀,离心后弃去上清液,沉淀以水〔每次10ml〕在摇动情况下冲洗2次.向沉淀中加入10ml 1mol/L盐酸以溶解其中的谷胱甘肽,以玻璃棒搅拌5min后加入1ml 20%的碘化钾溶液,混匀,离心.上清液转入供滴定用的100ml玻璃管中,沉淀在搅动情况下以10ml水冲洗.离心后溶液与第一次离心液合并.向得到的溶液中加入0.5ml淀粉液,用1mmol/L KIO3滴定,直至出现不消失的蓝色为止.1ml 1 mmol/L 的KIO3相当于0.307mg谷胱甘肽.〔参考《现代植物生理学实验指南》,中国科学院##植物生理研究所编〕.2.9天冬酰胺合成酶〔AS〕的测定:2.10 天冬酰胺转氨酶〔AspAT〕的测定:3 硝酸还原酶<NR>的测定采用离体法:〔1g样〕〔参考陈建勋,王晓峰主编的《植物生理学实验指导》,P27~29〕亚硝酸钠标准溶液〔1µg/ml〕:称NaNO2 0.9857g ,定容到1000ml,再吸5ml定容到1000ml.0.1 mol/L pH7.5的磷酸缓冲溶液:30.0905g Na2HPO4·12H2O + 2.4965g NaH2PO4·2H2O,加蒸馏水定容到1000ml.3mol/L HCl:125ml浓盐酸加蒸馏水定容到500ml.1%磺胺溶液:5.0g磺胺溶于500ml 3mol/L HCl中.0.2%a-萘胺溶液:1.0g a-萘胺溶于125ml冰醋酸后用蒸馏水定容到500ml,贮于棕色瓶中.0.1mol/L KNO3溶液:5.055g KNO3溶于500mln 0.1 mol/L pH7.5的磷酸缓冲溶液.0.025mol/L pH8.7的磷酸缓冲溶液:Na2HPO4·12H2O 8.8640g + NaH2PO4·2H2O 0.0570g,加蒸馏水定容到1L.提取缓冲液:1.211g半胱氨酸+ 0.372g EDTA,溶于1L 0.025 mol/L pH8.7的磷酸缓冲溶液. 2mg/ml NADH 溶液:0.5g NADH溶于250ml 0.1 mol/L pH7.5的磷酸缓冲溶液〔临用前配制〕. 首先标制作准曲线:取7支洁净烘干的15ml刻度试管加试剂,即配成0~2.0μg的系列标准亚硝态氮溶液.摇匀后在30℃保温箱或恒温水浴中保温30min,然后在540nm波长下比色.以亚硝态氮〔μg〕为横坐标〔x〕,光密度值为纵坐标〔y〕绘标准曲线或建立回归方程.各试剂加入顺序管号1234567亚硝酸钠标准液<ml>00.20.40.81.21.62.0蒸馏水<ml>2.01.81.61.20.80.401%磺胺溶液<ml>44444440.2%α-萘胺<ml>4444444每管含NO2- <μg>00.20.40.81.21.62.01g 材料+15ml提取缓冲液后研磨匀浆,转移到离心管中于4℃、4000r/min下离心15min,上清液即为粗酶提取液,用于硝酸还原酶<NR>的测定.0.4ml+1.2ml 0.1mol/L KNO3溶液+ 0.4mlNADH溶液后混匀〔对照不加NADH溶液,而以0.4ml 0.1mol/L pH 7.5磷酸缓冲液代替〕,在25℃水浴中保温30min.保温结束后立即加入1ml 磺胺溶液终止酶反应,再加1ml 0.2%a-萘胺溶液,显色反应15min后于4000r/min下离心5min,取上清液在540nm下比色测定吸光度.根据回归方程计算.。
MIS实验指导说明实验背景网络信息系统(MIS:Management Information System)是管理科学、信息技术和数学科学等众多学科的交叉领域,旨在利用现代计算机网络技术,为企事业单位提供高效、可靠、安全的信息化服务,更好地实现信息化管理和决策。
本实验旨在让学生实践网络信息系统的开发与维护,加深对MIS的理解和应用。
实验目的•熟悉MIS的概念、架构和应用范围。
•了解MIS开发的基本流程和技术手段。
•学会使用MIS开发工具(如Access、MySQL、PHP等)。
•掌握MIS系统的基本操作和维护方法。
•设计实现一个简单MIS系统,加深对MIS开发的理解和实践能力。
实验内容实验环境本实验需要在Windows或Linux操作系统下进行,需要安装以下软件:•数据库管理软件:Access或MySQL•Web服务器:Apache或IIS•开发工具:Dreamweaver、Visual Studio、Notepad++等•浏览器:Chrome、Firefox、IE等实验步骤1.设计MIS系统的数据结构和功能模块,包括用户管理、订单管理、库存管理、报表分析等。
可以使用UML图、流程图等工具进行设计。
2.在数据库管理软件中创建相应的数据表,定义字段、数据类型、键、约束等。
通过SQL命令或图形化界面设计表结构。
3.使用开发工具编写系统的前端和后端代码,实现用户登录、信息录入、查询和分析等功能。
前端可以使用HTML、CSS、JavaScript等技术实现界面效果,后端可以使用PHP、等技术实现数据操作。
4.在Web服务器中配置MIS系统的访问权限和安全设置,确保数据传输和存储的安全可靠。
5.对MIS系统进行测试和调试,检查功能是否达到设计要求,让用户体验更好。
6.对MIS系统进行维护和升级,及时修复漏洞和缺陷,改善系统性能,提高用户满意度。
实验效果完成本实验后,学生应该能够熟悉MIS开发的基本流程和技术手段,掌握MIS系统的基本操作和维护方法,同时具备了自主设计和实现一个简单MIS系统的能力。
ASPEN详细算例《化⼯过程数学模型与计算机模拟》课程案例研究之⼀甲醇→⼆甲醚+ ⽔前⾔概念设计⼜称为“预设计”,在根据开发基础研究成果、⽂献的数据、现有类似的操作数据和⼯作经验,按照所开发的新技术⼯业化规模⽽作出的预设计,⽤以指导过程研究及提出对开发性的基础研究进⼀步的要求,所以它是实验研究和过程研究的指南,是开发研究过程中⼗分关键的⼀个步骤。
概念设计不同于⼯程设计,因⽽不能作为施⼯的依据,但是成功的概念设计不但可以节省⼤量的⼈⼒和物⼒,⽽且⼜可以加快新技术的开发速度,提⾼开发的⽔平和实⽤价值。
即使⼀个很普通的单⼀产品的⽣产过程,也可能有104~109个⽅案可供选择。
如何从技术、经济的⾓度把最有希望的⽅案设计出来,是作为强化研究开发⼯作的⽅向,这是⼀种系统化的分级决策过程,也正是概念设计的真谛。
概念设计是设计者综合开发初期收集的技术经济信息,通过分析研究之后。
对开发项⽬作出⼀种设想的⽅案,其主要内容包括:原料和成品的规格,⽣产规模的估计,⼯艺流程图机简要说明,物料衡算和热量衡算,主要设备的规模,型号和材质的要求,检测⽅法,主要技术和经济指标,投资和成本的估算,投资回收预测,三废治理的初步⽅案以及对中试研究的建议。
随着计算技术和计算机技术的发展,化⼯流程过程模拟软件也越来越成熟,计算机辅助设计也⽇趋⼴泛。
在进⾏概念设计时,采⽤流程系统模拟物料衡算和热量衡算,投资和成本估算等问题以及采⽤流程模拟软件进⾏整体优化业越来越普遍。
本⽂采⽤国际上最成功和最流⾏的过程模拟软件之⼀的ASPLEN PLUS作为辅助设计的主要⼯具。
与过程有关的物料和能量的衡算基本上有该软件给出,并从设计流程计算的收敛与否来检验该流程是否可⾏。
本⽂通过概念设计,其⽬标是寻找最佳⼯艺流程(即:选择过程单元以及这些单元之间的相互连接)和估算最佳设计条件。
采⽤分层次决策的⽅法和简捷设计能消去⼤量⽆效益的⽅案。
本⽂按照以下基本步骤进⾏设计计算:1. 间歇对连续;2. 流程图的输⼊输出结构;3. 流程图的循环结构;4. 分离系统的总体结构;a. 蒸⽓回收系统;b. 液体回收系统。