循环伏安法与线性扫描伏安法
- 格式:pptx
- 大小:238.47 KB
- 文档页数:6

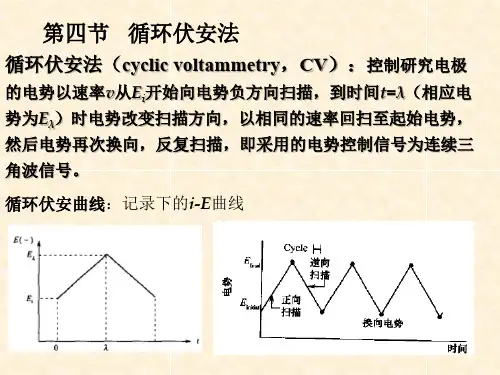
循环伏安法原理:循环伏安法(CV)是最重要的电分析化学研究方法之一。
该方法使用的仪器简单,操作方便,图谱解析直观,在电化学、无机化学、有机化学、生物化学等许多研究领域被广泛应用。
循环伏安法通常采用三电极系统,一支工作电极(被研究物质起反应的电极),一支参比电极(监测工作电极的电势),一支辅助(对)电极。
外加电压加在工作电极与辅助电极之间,反应电流通过工作电极与辅助电极。
对可逆电极过程(电荷交换速度很快),如一定条件下的Fe(CN)63-/4-氧化还原体系,当电压负向扫描时,Fe(CN)63-在电极上还原,反应为:Fe(CN)63-+e-→Fe(CN)64-得到一个还原电流峰。
当电压正向扫描时,Fe(CN)64-在电极上氧化,反应为:Fe(CN)64--e-→Fe(CN)63-得到一个氧化电流峰。
所以,电压完成一次循环扫描后,将记录出一个如图2所示的氧化还原曲线。
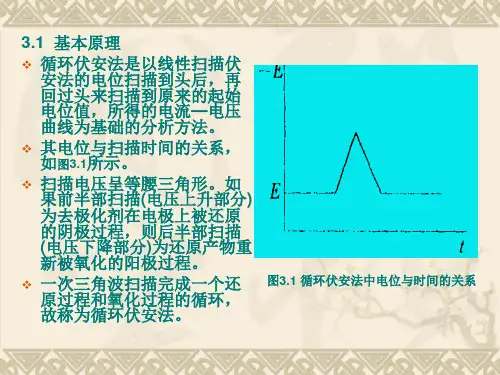
扫描电压呈等腰三角形。
如果前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
应用领域:循环伏安法能迅速提供电活性物质电极反应的可逆性,化学反应历程,电活性物质的吸附等许多信息。
循环伏安法可用于研究化合物电极过程的机理、双电层、吸附现象和电极反应动力学.成为最有用的电化学方法之一。
如通过对未知研究体系的CV研究,可以获研究对象的反应电位或和平衡电位, 估算反应物种的量,以及判断反应的可逆性。
电化学反应中物种反应的量可以依据Faraday定律估算,, 其中m为反应的摩尔量, n为电极反应中的得失电子数,F为图2 氧化还原cv曲线图图1 cv图中电势~时间关系图3 Ag在Pt电极上电结晶过程的CV图0.01mol/LagNO3+0.1mol/LKNO3Faraday常数(96485 C.molmnFidtQt==∫0-1)。

伏安法根据线性扫描伏安法与循环伏安法的基本原理, 采用电化学中典型的K3 [ Fe(CN) 6 ] 电化学可逆系统设计了线性扫描伏安法与循环伏安法实验。
作为应用化学专业高年级学生和研究生学习电化学课程的实验, 收到了非常好的教学效果。
1伏安法:电化学是研究两类导体形成的带电界面现象及其上所发生的变化的科学。
如今已形成了合成电化学、量子电化学、半导体电化学、有机导体电化学、光谱电化学、生物电化学等多个分支。
电化学在化工、冶金、机械、电子、航空、航天、轻工、仪表、医学、材料、能源、金属腐蚀与防护、环境科学等科技领域获得了广泛的应用。
当前世界上十分关注的研究课题, 如能源、材料、环境保护、生命科学等等都与电化学以各种各样的方式关联在一起。
电化学实验技术也在不断的发展, 随着微电子技术和计算机技术的迅猛发展, 线性扫描伏安法和循环伏安法、交流阻抗法和一系列更复杂灵巧的极化程序控制方法已在很大程度上取代了经典极化曲线测量和极谱方法[ 1 - 2 ] 。
本文在参考国内外有关电化学线性扫描伏安法与循环伏安法的基础上[ 3 - 4 ] , 进行了广泛的探索,采用电化学中典型的K3 [ Fe (CN) 6 ] 电化学可逆系统设计了线性扫描伏安法与循环伏安法实验, 得到了适合应用化学专业高年级学生和研究生实验教学的综合研究性实验方案。
教学效果表明, 该实验采用计算机控制的综合电化学测试仪, 实验参数容易控制, 数据测量准确, 实验结果便于计算机处理。
学生通过对实验数据的处理, 自己得出电化学可逆体系的诊断标准, 使学生通过这个综合性研究实验, 加深了对线性扫描伏安法与循环伏安法的特点和基本原理的理解, 掌握线性扫描伏安法的定量分析方法, 熟悉循环伏安法在研究电极机理方面的应用从而达到掌握线性扫描伏安法和循环伏安法实验技术的实验目的。
使用表面静止的液体或固体电极,称为伏安法。
循环伏安法(Cyclic V oltammetry)。

电分析化学循环伏安法电分析化学循环伏安法(cyclic voltammetry, CV)是一种常用的电化学测量方法,主要用于研究电催化反应、电极传感器和电化学反应机理等方面。
本文将对循环伏安法的原理、实验步骤和应用进行详细阐述。
一、原理循环伏安法是利用外加电压的正反向扫描,通过测量电流与电势之间的关系来研究溶液中的电化学反应。
在扫描过程中,电势以一个循环进行周期性变化,通常为从较负的起始电势线性扫描至较正的最大电势,然后再线性扫描回到起始电势。
电流与电势之间的关系可绘制出伏安图。
根据循环伏安曲线上出现的峰电流和峰电势,可以获取溶液中的电极反应的动力学和热力学信息。
峰电流的大小与反应速率成正比,而峰电势则反映了此反应的标准电势。
通过分析伏安图中的特征峰电流和峰电势,可以确定反应是否在电极表面发生,电化学反应的机理以及电极表面的反应活性等信息。
二、实验步骤1.准备实验样品和电化学池:将待测物溶解于合适的溶剂中,配制成一定浓度的电解液。
将工作电极(常用玻碳电极)、参比电极和计时电极放入电化学池中,确保其充分浸泡于电解液中。
2.建立电位扫描程序:选择适当的起始电位、终止电位和扫描速率。
起始电位为一般为较负值,终止电位为较正值。
扫描速率根据实验需求选择,通常为3-100mV/s。
3.进行循环伏安实验:在实验过程中,通常需要稳定电极电势一段时间,直到电流达到平衡。
然后开始正向扫描,直至到达终止电位。
接着进行反向扫描,回到起始电位。
整个循环过程称为一个循环。
4.记录电流-电势数据:记录正反向扫描过程中的电流与电势数据,通常以图形的形式记录,即伏安图。
按照实验需要的精度和时间,可以选择多次重复扫描,以提高实验结果的准确性。
三、应用1.电催化反应研究:循环伏安法可用于研究电催化剂的活性和稳定性,提供电催化反应的动力学和热力学参数。
通过优化电催化剂的结构和组成,可以提高电极催化剂的效能。
2.电极材料评估:通过对循环伏安曲线的分析,可以确定电极材料的氧化还原能力和稳定性。

化学检验工常见电化学催化剂性能测试方法在化学检验工中,电化学催化剂性能测试是一个重要的研究领域。
电化学催化剂可促进化学反应,降低反应能量,提高反应速率。
因此,准确评估电化学催化剂的性能至关重要。
本文将介绍几种常见的电化学催化剂性能测试方法。
一、循环伏安法循环伏安法是一种常用的电化学催化剂性能测试方法,通过在电解质溶液中施加一定的电势来测量电流和电压的变化情况。
该方法可以评估催化剂的氧化还原行为、反应中间体的生成和催化反应的动力学等性能。
二、线性扫描伏安法线性扫描伏安法是另一种常见的电化学催化剂性能测试方法,通过线性地改变电位并测量电流来研究电化学反应的动力学行为。
该方法可用于测定催化剂的活性、稳定性和高效性,广泛应用于燃料电池、电解水和二氧化碳还原等领域。
三、交流阻抗法交流阻抗法是一种用来研究电化学接口阻抗的测试方法。
通过施加交流电势信号,并测量电压和电流信号的响应,可以确定电解质、电极和催化剂之间的界面特性,比如电荷转移电阻、电解质阻抗和电极反应速率等。
四、计时电流法计时电流法是一种基于电化学反应速率的测试方法。
通过记录电解质溶液中的电流变化情况,可以测定催化剂的活性和稳定性。
该方法广泛应用于电解水制氢、二氧化碳还原和电化学合成等领域。
五、电化学质谱法电化学质谱法是一种结合电化学和质谱技术的测试方法。
通过将电极表面的反应产物引入质谱仪进行分析,可以确定催化剂的反应产物和反应机理。
该方法在燃料电池、电解水和电化学催化反应研究中具有重要意义。
六、原位红外光谱法原位红外光谱法是通过将红外光谱技术与电化学测试相结合的方法。
通过在电极表面施加电势,并采集反应体系的原位红外光谱信号,可以研究电化学反应的反应物吸附行为和反应机理。
该方法对于研究催化剂的反应活性和选择性具有重要意义。
综上所述,电化学催化剂性能测试方法对于评估催化剂的活性、稳定性和效率具有重要意义。
循环伏安法、线性扫描伏安法、交流阻抗法、计时电流法、电化学质谱法和原位红外光谱法等常见的测试方法可以提供对催化剂性能的全面评估。


循环伏安法原理及结果分析在电化学研究领域,循环伏安法是一种极其重要的研究手段。
它不仅能提供有关电极反应的丰富信息,还在材料科学、生物化学、环境监测等众多领域发挥着关键作用。
接下来,让我们深入了解一下循环伏安法的原理以及如何对其结果进行分析。
循环伏安法的基本原理基于控制电极电位的线性扫描。
在实验中,工作电极的电位以一定的速率在一个特定的电位范围内进行周期性的线性扫描。
通常,电位从起始电位开始,向一个方向扫描到终止电位,然后反向扫描回到起始电位,如此反复,形成一个循环。
在这个过程中,电极表面会发生氧化还原反应。
当电极电位达到某种物质的氧化电位时,该物质会在电极表面被氧化,产生氧化电流;当电极电位反向扫描到该物质的还原电位时,之前被氧化的物质会被还原,产生还原电流。
通过测量这些电流随电位的变化关系,我们就能够获得有关电极反应的信息。
为了更好地理解循环伏安法的原理,我们可以以一个简单的氧化还原反应为例。
假设在溶液中存在一种可氧化还原的物质 A,其氧化态为 A+,还原态为 A。
当工作电极的电位逐渐升高时,当达到 A 的氧化电位时,A 会被氧化为A+,同时产生氧化电流。
随着电位的继续升高,氧化电流可能会先增大,然后由于扩散控制等因素逐渐减小。
当电位反向扫描时,A+会在电极表面被还原为 A,产生还原电流。
那么,循环伏安法得到的结果通常以电流电位曲线的形式呈现。
在分析这些曲线时,有几个关键的参数和特征需要关注。
首先是峰电位。
氧化峰电位和还原峰电位分别对应着物质的氧化和还原过程中电流达到最大值时的电位。
峰电位的位置可以提供有关反应的难易程度和可逆性的信息。
一般来说,对于可逆反应,氧化峰电位和还原峰电位之间的差值较小;而对于不可逆反应,这个差值较大。
其次是峰电流。
峰电流的大小与参与反应的物质的浓度、扩散系数以及扫描速率等因素有关。
根据 RandlesSevcik 方程,在一定条件下,峰电流与扫描速率的平方根成正比,与物质的浓度成正比。


循环伏安法原理:循环伏安法(CV )是最重要的电分析化学研究方法之一。
该方法使用的仪器简单,操作方便,图谱解析直观,在电化学、无机化学、有机化学、生物化学等许多 研究领域被广泛应用。
循环伏安法通常采用三电极系统,一支工作电极(被研究物质起反应的电极),一支参比电极(监测工作电极的电势),一支辅助(对)电极。
外加电压加在工作电极与辅助电极之间,反应电流通过工作电极与辅助电极。
对可逆电极过程(电荷交换速度很快),如一定条件下的Fe(CN)63-/4-氧化还原体系,当电压负向扫描时,Fe(CN)63- 在电极上还原,反应为:Fe(CN)63-+e - → Fe(CN)64-得到一个还原电流峰。
当电压正向扫描时,Fe(CN)64-在电极上氧化,反应为: Fe(CN)64- - e - → Fe(CN)63-得到一个氧化电流峰。
所以,电压完成一次循环扫描后,将记录出一个如图2所示的氧化还原曲线。
扫描电压呈等腰三角形。
如果前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
应用领域:循环伏安法能迅速提供电活性物质电极反应的可逆性,化学反应历程,电活性物质的吸附等许多信息。
循环伏安法可用于研究化合物电极过程的机理、双电层、吸附现象和电极反应动力学.成为最有用的电化学方法之一。
如通过对未知研究体系的CV 研究,可以获研究对象的反应电位或和平衡电位, 估算反应物种的量,以及判断反应的可逆性。
电化学反应中物种反应的量可以依据Faraday 定律估算,, 其中m 为反应的摩尔量, n 为电极反应中的得失电子数,F 为 图2 氧化还原cv 曲线图图1 cv 图中电势~时间关系图3 Ag在Pt电极上电结晶过程的CV图0.01mol/LagNO3+0.1mol/LKNO3Faraday常数(96485 C.molmnFidtQt==∫0-1)。

在这一节中,将引入两个紧密相关的伏安形式* 线性扫描伏安法* 循环伏安法我们将看到如何进行这些测量以研究电极反应的电子传递机理和传输特性。
一、线性扫描线性扫描伏安法在线性扫描伏安(LSV)中,施加一个电位范围,非常类似于电位阶跃测量。
然而在LSV 中,电位从低限扫描到高限,如下图所示。
电压扫描速度 (v) 从直线的斜率计算,显然,改变扫描范围所用的时间,就可以改变扫描速度。
记录的线性扫描伏安的特性取决于下列因素:(1)、电子传递反应的速度;(2)、电活性粒子的化学反应(3)、电压扫描速度;在LSV测量中,电流响应被作图为电压的函数,而不是时间的函数,这与电位阶跃不同。
例如,如果我们回到Fe3+/Fe2+ 系统随后可以看到一个用只包含单Fe3+的电解液进行的单电压扫描的伏安图。
扫描从电流/电压图的左侧开始,这里没有电流。
当电压向右扫描时(向更加还原值),开始出现电流,最终在下降之前达到一个峰值。
为了理解这个行为,我们需要考虑电压对建立于电极表面的平衡的影响。
如果我们考虑Fe3+到Fe2+的还原,电子传递速度与电压扫描速度相比要快!因此,在电极表面,一个平衡被建立,与热力学预测的相同。
可以从平衡电化学回忆起Nernst方程预测的浓度和电压(电位差)之间的关系,这里E为施加电位差,Eo为标准电极电位。
所以,当电压从V1扫描V2到时,平衡位置从电极表面反应物没有转换的V1移动到全转换的V2 。
伏安行为的确切形式可以通过考虑电压和物质传递效应来理解。
当电位从V1开始扫描时,表面平衡开始改变,电流开始出现:随着电压从初始值继续扫描,电流在增加;平衡位置继续向右移动,有更多的反应物被转换。
峰值出现了,由于在某些点上,电极上部的扩散层已经足够增长,所以向电极方向的反应物流量速度已经不能满足Nernst方程的要求。
在这种情况下,电流开始下降,正如在电位阶跃测量中一样。
事实上,电流的下降服从Cottrell方程所预测的相同行为。
山西大学综合化学实验报告实验名称电化学分析方法学院化学化工学院学生姓名霍雨深蒋康利专业化学学号 2012296013 2012296014 年级 2012级指导教师高春光二Ο一五年四月七日摘要:本实验通过对K3[Fe(CN)6]进行快速循环伏安扫描和线性扫描,了解并掌握利用循环伏安法判定电极的可逆性,扫描速度和浓度对循环伏安图的影响,以及线性扫描中极限峰电流与活性组分浓度关系,掌握循环伏安法于线性扫描法的参数设置。
关键词:循环伏安法,线性伏安扫描法,铁氰化钾溶液,电化学分析1引言:电化学分析方法是仪器分析的一个重要分支,是建立在溶液电化学性质基础上的一类分析方法,或者说利用物质在溶液中的电化学性质及其变化规律分析的一类方法。
电化学性质是指溶液的电学性质(如电导、电量、电流、电位等)与化学性质(如溶液的化学的组成、浓度、形成及其化学变化等)之间的关系。
㈠循环伏安法循环伏安法是一种特殊的氧化还原分析方法。
其特殊性主要表现在实验的工作环境是在三电极电解池里进行。
w为工作电极(即绿色的夹子接铜电极),s为参比电极(即黄色的夹子接饱和氯化钾电极),a为辅助电极(即红色的夹子接铂电极)。
当加一快速变化的电压信号于电解池上,工作电极电位达到开关电位时,将扫描方向反向,所得到的电流-电位(I-E)曲线,称为循环伏安曲线,同样有峰电流ip和峰电位Ep,ip、Ep的表达式也分别相同。
对于可逆电极反应ip=6.25×105n3/2D1/2v1/2Ac 其中:ip为峰电流(A),n为电子转移数,A为电极面积(cm2),D为扩散系数(cm2/s),v 为扫描速度(V/s),c为浓度(mol/L)。
由此可见,ip与v1/2和c都是直线关系。
由于Da和Dc大致相同,对于可逆电极反应ipa/ ipc ≈1铁氰化钾离子[Fe(CN)6]3--亚铁氰化钾离子[Fe(CN)6]4-氧化还原电对的标准电极电位为[Fe(CN)6]3- + e-= [Fe(CN)6]4-φθ= 0.36V(vs.NHE) 电极电位与电极表面活度的Nernst方程式为φ=φθ’+ RT/Fln(C Ox/C Red)在一定扫描速率下,从起始电位(0.110V)正向扫描到转折电位(0.181V)期间,溶液中[Fe(CN)6]4-被氧化生成[Fe(CN)6]3-,产生氧化电流;当负向扫描从转折电位(0.181V)变到原起始电位(0.110V)期间,在指示电极表面生成的[Fe(CN)6]3-被还原生成[Fe(CN)6]4-,产生还原电流。
实验五线性扫描伏安法和循环扫描伏安法一.实验目的1、了解线性扫描伏安法和循环扫描伏安法的特点和基本原理。
2、掌握线性扫描伏安法的定量分析方法。
、3、了解循环扫描伏安法在研究电极机理方面的应用。
二、基本原理1、线性扫描伏安法线性扫描伏安法是在电极上施加一个线性变化的电压,即电极电位是随外加电压线性变化记录工作电极上的电解电流的方法。
记录的电流随电极电位变化的曲线称为线性扫描伏安图。
可逆电极反应的峰电流可由下式表示:Ip=0.4463nFADo1/2Co*(n F v/RT)1/2=5.99*105n3/2Ado1/2v1/2Co*(1)式中n为电子交换数,A为电极有效面积,Do为反应物的扩散数,v为电位扫描速度,Co*为反应物(氧化态)的本体浓度。
也可简化为(A不变时)ip=kv1/2Co* (2)即峰电流与扫描速度的1/2次方成正比,与反应物的本体浓度成正比。
这就是线性扫描伏安法定量分析的依据。
对于可逆电极反应,峰电位与扫描速度无关,Ep=E1/2±1.1RT/nF (3)但当电位反应为不可逆时(准可逆或完全不可逆)。
Ep随扫描速度增大而负(正)移。
2、循环伏安法循环伏安法的原理同线性扫描伏安法相同,该法控制电极电势以不同的速率,随时间以三角波形一次或多次反复扫描,电势范围是使电极上能交替发生不同的还原和氧化反应,并记录电流-电势曲线。
只是比线性扫描伏安法多了一个回归。
所以称为循环伏安法。
循环伏安法是电化学方法中最常用的实验技术。
循环伏安法有两个重要的实验参数,一个峰电位之比,二是峰电位之差。
对于可逆电极反应,峰电流之比iPc/ipa的绝对值约等于1。
峰电流之差约为59.6mv(25℃)。
△Ep=2.22RT/nF (4)三.仪器和试剂1.电化学分析系统2.三电极系统:玻碳电级为工作电极,Ag/Agcl电极为参比电极,铂钛电极为对极。
3.1.0×10-3mol/L铁氰化钾溶液四.实验步骤1.选择仪器实验方法:电位扫描技术——线性扫描伏安法或循环伏安法。
循环伏安法原理:循环伏安法(CV )是最重要的电分析化学研究方法之一。
该方法使用的仪器简单,操作方便,图谱解析直观,在电化学、无机化学、有机化学、生物化学等许多 研究领域被广泛应用。
循环伏安法通常采用三电极系统,一支工作电极(被研究物质起反应的电极),一支参比电极(监测工作电极的电势),一支辅助(对)电极。
外加电压加在工作电极与辅助电极之间,反应电流通过工作电极与辅助电极。
对可逆电极过程(电荷交换速度很快),如一定条件下的Fe(CN)63-/4-氧化还原体系,当电压负向扫描时,Fe(CN)63- 在电极上还原,反应为:Fe(CN)63-+e - → Fe(CN)64-得到一个还原电流峰。
当电压正向扫描时,Fe(CN)64-在电极上氧化,反应为: Fe(CN)64- - e - → Fe(CN)63-得到一个氧化电流峰。
所以,电压完成一次循环扫描后,将记录出一个如图2所示的氧化还原曲线。
扫描电压呈等腰三角形。
如果前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
应用领域:循环伏安法能迅速提供电活性物质电极反应的可逆性,化学反应历程,电活性物质的吸附等许多信息。
循环伏安法可用于研究化合物电极过程的机理、双电层、吸附现象和电极反应动力学.成为最有用的电化学方法之一。
如通过对未知研究体系的CV 研究,可以获研究对象的反应电位或和平衡电位, 估算反应物种的量,以及判断反应的可逆性。
电化学反应中物种反应的量可以依图2 氧化还原cv 曲线图图1 cv 图中电势~时间关系据Faraday 定律估算,, 其中m 为反应的摩尔量, n 为电极反应中的得失电子数,F 为Faraday 常数(96485 C.molmnFidtQt==∫0-1)。
如图3的CV 图中,阴影部分对应的是铂上满单层氢脱附的电量,为210 μC/cm 2。
循环伏安法实验 铁氰化钾在电极上的氧化还原一、实验目的1、学习循环伏安法测定电极反应参数的基本原理2、熟悉伏安法测定的实验技术3、学习固体电极表面的处理方法二、实验原理循环伏安法(CV)是将循环变化的电压施加于工作电极和参比电极之间,记录工作电极上得到的电流与施加电压的关系曲线。
循环伏安法的典型激发信号当工作电极被施加的扫描电压激发时,其上将产生响应电流,以电流对电位作图,称为循环伏安图。
典型的循环伏安图如下:从循环伏安图中可得到几个重要的参数:阳极峰电流(i pa)、阳极峰(E pa )、阴极峰电流( i pc )、阴极峰电位(E pc )扫描电压(V)时间/s对可逆氧化还原电对的式量电位E θ’与E pc 和E pa 的关系为:(1)而两峰之间的电位差值为:(2)对铁氰化钾电对,其反应为单电子过程,ΔE p 是多少?从实验求出来与理论值比较。
对可逆体系的正向峰电流,由Randles –Savcik 方程可表示为:i p = 2.69×105n 3/2AD 1/2υ1/2c (3)其中:i p 为峰电流(A ),n 为电子转移数, A 为电极面积(cm 2), D 为扩散系数(cm 2/s),υ为扫描速度(V / s ), c 为浓度(mol/L)。
根据上式,i p 与υ1/2和c 都是直线关系,对研究电极反应过程具有重要意义。
在可逆电极反应过程中,(4)对一个简单的电极反应过程,式(2)和式(4)是判别电极反应是否可逆体系的重要依据。
三、仪器与试剂仪器 CHI660电化学工作站;三电极系统:铂盘电极为工作电极,Ag/AgCl 电极(或饱和甘汞电极)为参比电极,铂电极为对极(铂丝、铂片、铂柱均可); 试剂 1.0x10-3,2.0 x10-3,4.0 x10-3,6.0 x10-3,8.0 x10-3,1.0 x10-2mol/L K 3[Fe(CN)6](铁氰化钾)溶液(含0.2mol/L KCl )。