安瓿检漏灭菌合同技术参量
- 格式:doc
- 大小:202.94 KB
- 文档页数:17

目的:建立AM-1.2安瓿检漏灭菌柜的操作与维护规程,确保产品质量符合工艺要求。
X围:适用于AM-1.2安瓿检漏灭菌柜的操作与维护全过程。
职责:操作人员、维修人员、工艺员、车间主任、QA现场监控员。
内容:1用途、性能1.1AM-1.2安瓿检漏灭菌装置,采用了先进的门结构装置,传动相当灵活轻捷,维修直观简单,为国内同行业首创。
电器控制系统简洁明了,管路系统气动元件均为国外进口,控制稳定性高。
1.2AM-1.2系列安瓿检漏灭菌是一种高性能、高智能化的安瓿灭菌检漏清洗设备。
主要用于安瓿、口服液、小输液瓶等药品制剂的灭菌和检漏处理。
该设备设计先进、结构合理、控制高档。
灭菌结束后通过真空或真空加色水检漏,最后还可用清水进行清洗处理,保证瓶外壁干净无污染。
1.3主要技术参数1.3.1工作压力:0.21Mpa1.3.2设计压力:0.245 Mpa1.3.3设计温度:139℃1.3.4.工作温度:100-132℃1.3.5.真空度:-0.09 Mpa1.3.6.热均匀度:≤±0.5℃1.3.7.内室容积:1500×750×1100(L×W×H)1.3.8.外形尺寸:1800×131×1900(L×W×H)1.3.9设备重量:1500kg2结构及性能2.1筒体是按国家GB-150《钢制压力容器》标准和《压力容器技术规程》设计制造,AM-1.2安瓿检漏灭菌柜灭菌室采用SUS304不锈钢压制而成,无锈蚀,无污染。
保温层采用性能优良的聚氨酯材质,现场发泡工艺制作。
2.2管路系统由角座式气动阀、过滤器、单向阀、疏水阀、真空泵及各种管件连接而成。
2.3控制系统由日本三菱PLC控制器、日本三菱触摸屏、微型面板打印机、日本TOKYO 压力控制器及其它方式输入的开关量模拟量进行处理,输出不同的控制信号,自动完成控制过程。
2.4喷淋系统采用美国喷雾公司产螺旋式喷嘴,喷出的冷却水环形雾状,密布于整个柜体,无死角,能使安瓿均匀冷却。

目的:建立安瓿检漏灭菌柜标准操作规程,确保该设备正常操作使用。
范围:本规程适用于安瓿检漏灭菌柜的操作。
职责:设备管理员起草;设备部部长审核;质量负责人批准;岗位操作人员执行。
内容:1.概述1.1工作原理为电加热式卧式矩形压力蒸汽灭菌器,是采用饱和蒸汽进行消毒灭菌,利用蒸汽冷凝时释放大量潜热,使被消毒的物品处于高温和潮湿状态,经过一定时间,破坏所有细菌及芽胞组织,达到消毒灭菌的目的。
1.2主要技术参数1.2.1型号:CK-1.5。
1.2.2设计压力:0.17Mpa。
1.2.3工作压力:0.15Mpa。
1.2.4设计温度:129℃。
1.2.5工作温度:126℃。
1.2.6输入功率:动力电源4Kw、380V、50Hz;控制电源:0.5Kw、220V、50Hz。
1.2.7真空度:-0.086pa。
1.2.8蒸汽源压力:0.3~0.5Mpa。
1.2.9压缩空气压力:0.5~0.7Mpa。
1.2.10热均匀度:±1℃。
1.2.11内室尺寸:1870×680×1180(L×W×H)。
1.2.12外型尺寸:2210×1450×2000(L×W×H)。
1.2.13设备重量:约2100Kg。
2.操作2.1操作前准备2.1.1检查“设备状态标识牌”,并更改相应内容,查看“设备日志”,了解上一次设备运行情况,确认无误后方可使用。
2.1.2电源接通状况是否符合设计要求和电气标准。
2.1.3电路系统的连接是否松动,各阀的开启状态是否良好。
2.1.4检查密封门的开关门动作及门密封是否正常。
2.1.5检查循环真空泵和水泵转向是否与标记同向。
2.1.6检查蒸汽、压缩空气、水是否具备能源要求。
2.1.7检查设定压力是否符合额定工作压力。
2.2操作过程2.2.1打开蒸汽旁路阀,放掉公用设施管道中的冷凝水,冷凝水排完后,关闭旁路阀,打开蒸汽阀。
2.2.2打开水源、电源、压缩空气、蒸汽,打开灭菌柜急停键。

《检漏灭菌岗位SOP最详细》灭菌检漏岗位标准操作规程1、目的建立水针车间安瓿灭菌检漏岗位标准操作规程,使操作达到标准化、规范化。
2、适用范围本标准适用于水针车间安瓿检漏灭菌岗位。
3、职责操作人员对本标准的实施负责,车间主任、qa检查员负责监督检查。
4、操作前的检查准备:4.1工序负责人从车间质检人员处领取加盖控制号的空白《灭菌检漏工序生产前检查记录》、《灭菌检漏工序生产记录》、《灭菌检漏工序清场记录》、《灭菌检漏工序日清洗记录》以及空白状态标识。
4.2将以下记录和文件置于工作现场《灭菌检漏岗位标准操作规程》《灭菌检漏工序生产前检查记录》《灭菌检漏工序生产记录》《灭菌检漏工序清场记录》《灭菌检漏工序日清洗记录》《设备使用、维修记录》4.3按顺序检查传递窗、灭菌车架、灭菌柜腔室、灭菌前后区域、暂存间、地漏应无遗留物。
4.4检查洁具、地面、地漏、台面、门窗、内墙、灯罩、顶棚,送回风口应清洁。
4.5灭菌水、色水检查与配置:4.5.1假期后第一天上班,将色水储水罐加满纯化水,然后加入规定级别的染料是色水达到规定颜色。
4.5.2在连续生产情况下生产前应检查色水时期保持规定颜色,储水罐应满罐。
若水位达不到要求应及时补加纯化水至满罐。
4.5.3每天上班前对灭菌水进行检查,应保持满罐,4.6启动压缩机,使压力上升到需要值,然后打开压缩气阀。
4.7将蒸汽管道内的冷凝管排放干净,然后打开与灭菌连接的蒸汽源开关,并检查其压力是否达到规定压力。
4.8打开用户水源、备用水源、去离子水源阀门开关,为程序进行做准备。
4.9打开真空泵水阀,备用电源、去离子水源阀门开关,为程序进行做准备。
4.10检查灭菌柜门封条是否完好,门开关是否正常,收回《设备待用》、《已清洁》标识,换上《设备运行中》,《生产运行中》状态标识。
4.11根据生产计划核对当班的生产品种、规格、批号、数量应与生产传票相符。
4.12将灭菌检漏设备的检查情况写到《设备使用、维修记录》中。


安瓿检漏灭菌器系列使 用 说 明 书连云港千樱医疗设备有限公司LIANYUNGANG SENOH MEDICAL EQUIPMENT CO.,LTD执 行 标 准: Q320700CI01-2003 产 品 名 称: 安瓿检漏灭菌器系列®前言本说明书的用户对象本说明书为安瓿检漏灭菌器系列(以下简称为本设备)的使用说明以及有关参数的设定、操作方法、注意事项、一般的维修方法等,是为以下人员编写:具有一般电气、控制、机械、管道知识的操作人员和维修人员●负责灭菌器选型的人员●负责管理灭菌器的人员●操作本设备的操作人员●负责本设备维修的维修人员注意●在本说明书要求的工作条件和环境下使用。
●本设备请务必在本说明书中的一般规格及性能的范围内使用。
●本设备未经授权,严禁用户对设备部分或全部进行改造。
如有问题,请与本公司的当地办事处或本公司联系。
●请妥善保管本设备的有关资料,以便于随时查阅。
●该说明书适用于等安瓿检漏灭菌器。
声明●本说明书未经许可,不得进行部分或全部复印、复制或提供给他人。
●设备因技术或其它原因发生改动,恕不另行通知。
●本说明书只对说明书配备的产品,如用作指导、操作其它产品引起的后果,本公司无法保证。
●因特殊定货或其它要求而造成与设备不符之处,以实际制造的设备为准。
●本说明书的所有权属于连云港千樱医疗设备有限公司。
本设备的用途●本设备用于对医用、试验用的安瓿类物品。
●如若用于其它类物品的灭菌,应经本公司的技术部门书面许可,否则,可能会引起无法预料的后果。
有关安全的标记在本说明书中,为了更好地使用本设备,注意事项用以下的有关标记和符号表示。
以下为有关的标记和符号所表示的意义和重要程度,请务必遵守。
警告和注意的表示警告表示如果操作错误,可能导致设备的损伤和人员的伤亡。
注意表示应该着重注意的地方。
警告通电时不要擅自拆卸电气元件及接触内部电路,有可能会触电。
通电时,请不要接触端子部分。
维修时,必须切断设备的外部及面板电源、水源和汽源。
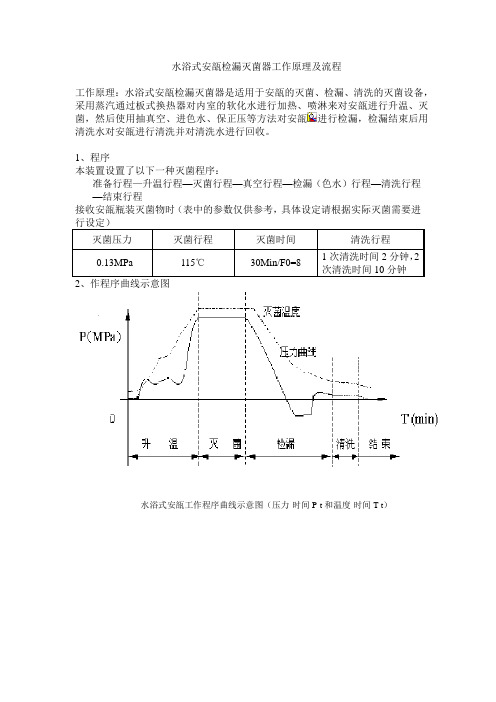
水浴式安瓿检漏灭菌器工作原理及流程工作原理:水浴式安瓿检漏灭菌器是适用于安瓿的灭菌、检漏、清洗的灭菌设备,采用蒸汽通过板式换热器对内室的软化水进行加热、喷淋来对安瓿进行升温、灭菌,然后使用抽真空、进色水、保正压等方法对安瓿进行检漏,检漏结束后用清洗水对安瓿进行清洗并对清洗水进行回收。
1、程序本装置设置了以下一种灭菌程序:准备行程—升温行程—灭菌行程—真空行程—检漏(色水)行程—清洗行程—结束行程接收安瓿瓶装灭菌物时(表中的参数仅供参考,具体设定请根据实际灭菌需要进水浴式安瓿工作程序曲线示意图(压力-时间P-t和温度-时间T-t)工作行程(流程图)-1、准备行程在准备状态进行被灭菌物的放入和有关参数的设定以及准备侧与清洁侧门的闭合,当此阶段完成后便可以按启动开关进入下一工作状态。
在此阶段准备灯亮(受前后开、关状况决定),排泄阀开启,其它状态灯也受前后门开、关状况决定。
-2、升温行程进入升温行程后,状态指示为升温行程、运行灯亮。
-2-1、进入升温行程前,机器前后门槽充气,密封机器的前后门,此后机器的两侧门都不可以打开,直到灭菌程序结束。
-2-2内筒开始补充软水到设定下水位后,停止进软水,快进蒸汽阀开启,循环泵启动,机器开始进入升温阶段,升温阶段中进蒸汽阀受内筒进水温度的调节。
-2-3、当灭菌室到达后,高排口阀转为开启,进蒸汽阀继续打开。
在升温、灭菌行程,进蒸汽阀受压力和温度双重控制。
当温度达到灭菌温度时程序进入下一行程。
-3、灭菌行程进入灭菌行程后,状态指示为灭菌行程、运行灯亮。
高排口阀根据条件脉动打开,并且开始进行灭菌计时。
进蒸汽阀同样受到温度和压力双重控制。
当温度高出灭菌温度0.8℃,则关闭所有进蒸汽阀;当温度降至所设定的灭菌温度+0.3℃时则打开其中的慢进蒸汽阀;如果温度下降幅度过大,则将全部蒸汽阀打开。
当灭菌时间,F0值达到设定值,灭菌行程结束,进入下一行程。
-4、检漏真空行程进入检漏真空行程后,状态指示为真空行程、运行灯亮。
安瓿检漏灭菌柜标准操作、保养规程1、目的:建立装车、灭菌、送物操作规程,以确保灭菌操作正确。
2、范围:使用于装车、灭菌、送物工序。
3、责任者:设备操作维修人员、QA4、内容4.1、准备:检查岗位清场情况、设备完好情况。
4.2、装车:将待灭菌物品放在灭菌车上,堆放完毕推入灭菌室4.3、灭菌:4.3.1、灭菌柜工作条件:水源压力:0.15~0.3Mpa 纯真汽压力:0.4~0.8 Mpa洁净压缩空气压力:0.5~0.8 Mpa 电源:三相四线、AC380V、50HZ、4KW 4.3.2、打开上述能源阀门,确认能源压力在规定范围内;打开蒸汽旁路阀门,排放管道内冷凝水,听到管道内有蒸汽流动声时,可将旁路阀关闭。
4.3.3、打开电源开关,触摸屏界面自动生产。
轻触“华菱”标志下“欢迎”键,进入“操作室”界面。
再轻触“门操作”键,进入“门操作”界面。
然后轻触“开前门”键,使前门开启。
将待灭菌物品推入灭菌柜内,轻触“关前门”键,将门关闭到位。
接着,设定灭菌参数。
在此过程中,设备将自动进行套层预热。
4.3.4、回到“操作室”界面,轻触“自动程序”键,激活自动操作界面,轻触“启动”键,自动转入监控界面。
设备将按下述程序自动运行:升温结束。
脉动真空是柜内通过真空泵抽真空至设定真空度,然后再向柜内补充纯真汽至设定补汽压力,然后再抽真空这样一个循环往复的过程,设定周期为3次,当柜内第3次压力达到与设真空度,则进入升温程序。
升温过程中,柜内压力上升并恒定在所设定的工作压力区间内。
此过程中的热量交换产生的冷凝水由疏水器泄出,使柜内温度逐渐上升到设定的灭菌温度。
灭菌过程中,柜内压力恒定在工作压力区间,温度恒定在灭菌温度。
通过灭菌值的累加,来表达说设定的灭菌效果。
时间的积累和F灭菌完毕进入干燥冷却程序。
在此过程中,柜内先泄放压力至常压,然后进行真空处理,结合套层加温烘干使物品干燥并逐步冷却。
达到设定的干燥时间后停止真的,向柜内补充洁净空压气,至常压即整个程序结束。
安瓿、西林瓶两用检漏、灯检机用户需求标准文件更新日志目录1. 简介 (4)2. 总述 (4)3. 运行要求 (5)3.1. 能力、容量、产能 (5)3.2. 工艺需求 (5)3.3. 工艺控制 (5)3.4. 功能需求 (6)3.5. 数据和安全 (7)3.6. 环境 (8)4. 限制和约束 (8)4.1. 兼容和支持 (8)4.2. 过程约束 (9)4.3. 维护保养 (9)5. 生命周期 (10)5.1. 开发计划 (10)5.2. 测试 (10)5.3. 交付 (10)5.4. 服务支持 (12)6. 术语 (13)7. 参考资料和控制规则 (13)8. 附件 (13)1. 简介本用户需求标准(URS)由有限公司(以下简称A公司)起草并交付于供应商。
本URS描述了对设备的基本需求。
供应商应对本URS的所有章节进行充分确认,对相关技术信息与我方进行充分沟通,确保能够遵循和满足本URS的要求。
双方最终确认的URS将作为采购合同的重要部分。
本URS也是开展后续相关确认或验证工作的基础。
2. 总述本URS适用于A公司生产部用于对安瓿、西林瓶装制品进行检漏和灯检的设备。
设备包括检漏机一台、灯检机一台及两台设备间的自动联机装置,如果能提供检漏、灯检一体机也可。
该设备的设计、构造、材质、安装以及相关文件系统等都必须满足以下标准:本用户仅提出的最低限度的技术要求和设备的最基本要求,并未涵盖和限制卖方设备具有更高的设计与制造标准和更加完善的功能,设备具有更完善的配置、性能更优异的部件和更高水平的控制系统。
卖方应在满足本要求书的前提下提供卖方能够达到的更高标准和功能的高质量设备及其相关服务。
卖方的设备应满足中国有关设计、制造、安全、环保等规程、规范和强制性标准要求。
如遇与卖方所执行的标准发生矛盾时,应按较高标准执行(强制性标准除外)。
3. 运行要求3.1. 能力、容量、产能3.2. 工艺需求3.3. 工艺控制3.4. 功能需求3.5. 数据和安全3.6. 环境4. 限制和约束4.1. 兼容和支持4.2. 过程约束4.3. 维护保养5. 生命周期5.1. 开发计划供应商提供一个质量和项目计划,做为建议的一部分。
福建金山生物制药股份有限公司Y XQ,EAK—1.2安瓿检漏灭菌柜验证方案设备名称:YXQ,EAK—1.2安瓿检漏灭菌柜安装位置:水针车间控制区产品灭菌间验证编号:VP 2003-02(1)-001方案批准:目录一被验证的设备描述 (4)YXQ,EAK—1.2安瓿检漏灭菌柜 (4)1.1 用途 (4)1.2 主要技术指示与参数 (4)1.3 主要工作原理 (5)二再验证目的 (6)三验证小组人员及职责 (6)1验证小组人员 (6)2验证职责 (7)3验证依据 (7)四验证内容 (8)4.1 安装确认 (8)4.2 运行确认 (10)4.3 被验证的设备运行描述 (12)4.4 验证方法 (13)4.5 验证数据的采集和计算 (15)五验证用的仪器 (16)六证检测结果和处理 (16)七验证周期 (16)八附件 (16)一、被验证的设备描述YXQ,EAK—1.2安瓿检漏灭菌柜设备名称:安瓿检漏灭菌柜规格型号:YXQ,EAK—1.2生产厂家:江苏华菱集团医疗设备制造有限公司设备出厂编号:99EAK—06设备出厂日期:1999年11月3日安装位置:水针车间控制区产品灭菌间1.1 用途:YXQ,EAK—1.2安瓿检漏灭菌柜采用PLC全自动程序控制,设自控、手动两套操作系统,并具有F0值预设、显示和打印功能,并与F0控制器相互作用,有效地保证了产品的灭菌效果。
本公司用于灌封后的水针产品最后灭菌。
1.2 主要技术指标与参数本装置主要用于产品的灭菌,采用了实时灭菌时间处理,确保灭菌的可靠性。
安全阀在超压时自动排汽,在超温时报警并开启排汽阀。
1.2.1 灭菌室容积: 1.2m³(1500×750×1050) 1.2.2 设计压力:0.165MPa1.2.3 真空度:-0.08MPa1.2.4 设计温度:129℃1.2.5 工作温度均匀度:+1℃~-1℃1.2.6 蒸汽压力:0.4~0.8Mpa1.2.7 压缩空气: 0.5~0.8Mpa1.2.8 程序周期: 约100分钟1.2.9 电源: 380V, 50Hz, 5KW 1.3 主要工作原理本机采用全过程PLC自动检测控制。
安瓿检漏灭菌柜操作、检修、保养规程安瓿检漏灭菌柜操作、检修、保养规程目的:建立安瓿检漏灭菌柜的操作规程,安全使用设备。
范围:安瓿检漏灭菌柜的操作、检修、保养。
责任:生产部、动力设备部、生产部安瓿检漏灭菌柜的操作工、动力设备部维修工内容:1. 准备:1.1气源:启动压缩机、使压缩空气储罐额定工作压力。
1.2打开蒸汽源旁路阀排放冷凝水直至蒸汽逸出后关闭。
1.3打开冷却水阀并确认其压力正常。
1.4打开电源开关,按“→”进入“操作界面”,根据工艺要求,设定压力、温度、时间等参数。
2. 开门:逆时针方向将门旋开。
3. 装载2.1将待灭菌物品顺序放入灭菌车。
2.2将灭菌车推进灭菌腔。
4. 关门:顺时针方向将门旋紧。
5. 启动运行5.1自动运行5.1.1真空:真空系统运转,抽排柜内的气体5.1.2升温:向柜内输送纯蒸汽,使柜内温度逐渐升高。
5.1.3来菌:到预设温度,转放灭菌程序。
5.1.4检漏:真空检漏5.1.5清洗:把灭菌物品上的色水清洗干净。
5.1.6当柜内压力低度于安全压力时,工作结束。
5.2手动操作:当有物殊的灭菌需求或自控程序出现无法满足灭菌需求时,任何时刻都可以切换到手控操作界面。
5.2.1停止自控程序的运行:在自控界面上按一次“停止”键,然后按“返回”进入操作界面,按一下“手/自动转换”键,便可进入手控操作。
5.2.2真空:按下“真空“操作键,柜内开始抽真空,再按一下停止操作。
5.2.3进汽:按下“进汽”操作键,向柜内进蒸汽,再按一下停止操作。
5.2.4进色水:按下“进色水”操作键,进色水,再按一下停止操作。
5.2.5排色水:按下“排色水”操作键,再按一下停止操作。
5.2.6清洗:按下“清洗”操作键,喷淋系统开启,再按一下停止操作。
5.2.7补气:按下“补气”操作键,补气阀打开,再按一下停止操作。
5.2.8返回:按下“返回”操作键,退出手动控制界面,进入操作界面。
维修与保养:1.各部件各限位开关与门都有机械碰撞,如有移位现象,需及时调整。
湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01安瓿检漏灭菌柜用户需求书项目名称:赛隆药业新厂建设项目类别:工艺设备湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01审批表---- 职务姓名签字日期起草人车间主任曾翔审核人生产技术部经理陈凯审核人设备工程部经理姜跃武审核人副总经理周蓓批准人质量管理部经理/质量受权人侯军湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01目录1. 总则 (4)2. 适用的法规和指南 (4)3. 缩写和定义 (5)4. 设备系统描述 (6)5. 技术要求 (6)6. 文件和培训 (13)7. 参考条件 (16)8. 相关系统 (17)9. 变更历史 (17)湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:011.总则1.1本用户需求书所列技术要求适用于长沙新厂小容量注射剂车间的安瓿灭菌检漏柜的采购。
新引进的设备在设计、制造技术及性能上达到国内外先进水平,符合中国GMP、欧盟GMP及FDA CGMP要求。
1.2 本URS描述了该设备的基本需求,包括:工作性能需求、关键技术参数要求、安全要求、符合中国、欧盟、FDA GMP要求及其他要求。
同时,这份用户要求文件也是开展后续相关验证工作的基础,包括:FAT草案和报告、SAT草案和报告、IQ草案和报告、OQ 草案和报告。
1.3 在本URS中用户仅提出基本的技术要求和设备的基本要求,并未涵盖和限制卖方设备具有更高的设计与制造标准和更加完善的功能、更完善的配置和性能、更优异的部件和更高水平的控制系统。
投标方应在满足本URS的前提下提供卖方能够达到的更高标准和功能的高质量设备及其相关服务。
卖方的设备应满足中国有关设计、制造、安全、环保等规程、规范和强制性标准要求。
如遇与卖方所执行的标准发生矛盾时,应按较高标准执行(强制性标准除外)。
1.4供货范围一台安瓿灭菌检漏柜。
提供能满足两年正常运作要求的备品备件。
2.适用的法规和指南以下为在本用户需求标准URS中所参考的文献标准:1.EN 60204-1机械安全-机械电气设备.2.中国压力容器标准(GB150)3.GAMP 5 –生产自动化管理规范第5版4、中国:药品生产质量管理规范5、美国:CGMP现行药品生产质量管理规范6、欧盟:药品生产质量管理规范7、GEP – Good Engineering Practice. 良好工程管理规范8、21CFR Part 11 电子记录;电子签名.9、(国家质量监督检验检疫总局特种设备许可办公室)相关法规湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:013. 缩写和定义缩写定义BOM Bill of Materials 材料清单BPE Bio-Processing Equipment. 生物加工设备CDA Clean Dry Air. 干燥的洁净空气CIP Clean In Place. 在位清洗COC Certificate Of Conformance. 证书DP Differential Pressure. 压差ETV Electronic Expansion Valve 电子安全阀FAT Factory Acceptance Testing. 出厂验收测试FIT Filter Integrity Test. 过滤器完整性测试FS Functional Specification. 功能标准GA General Arrangement. 总布置图HDS Hardware Design Specification. 硬件设计标准I/O Input / Output. 输入/输出IQ Installation Qualification 安装确认OIP Operator Interface Panel. 人机界面OQ Operation Qualification 运行确认NEMA National Electrical Manufacturers Association. 美国电器制造商协会P&I D Process and Instrumentation Diagram 工艺仪器布局图PLC Programmable Logic Controller. 程序逻辑控制器PW Purified Water 纯化水RTD Resistance Temperature Detector. 电阻式温度检测器SAT Site Acceptance Test. 工厂接受测试SCADA System Control & Data Acquisition System. 数据采集与监视控制系统SDS Software Design Specification. 软件设计标准SIP Sterilization In Place. 在位灭菌SOP Standard Operation Procedure 标准操作规程TBA To Be Agreed. 待同意TBD To be Determined. 待定T/C Thermocouple. 热电偶UPS Uninterrupted Power Supply. 不间断电源湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01缩写定义URS User Requirements Specification. 用户需求标准VIT Vendor Internal Testing. 供应商内部测试WFI Water For Injection. 注射用水4. 设备系统描述4.1 基本描述本设备用于车间2ml安瓿产品的灭菌和检漏。
安瓿灭菌检漏柜为传递式,灌液、密封后的安瓿瓶在一般区装载到托盘后放置到移动小车上的灭菌小车,在一般区灭菌前室打开装载侧门,通过移动小车将灭菌小车推进灭菌柜内,灭菌、检漏完成后,打开一般区灭菌后室的卸载门,将灭菌小车转移到一般区灭菌后室的移动小车上,在一般区进行卸料。
要求每次可灭菌、检漏的产品数量为200000支2ml安瓿瓶。
4.2 工艺设计和原材料性质要求每次可灭菌、检漏的产品数量为200000支2ml安瓿瓶。
4.3 人员数量:1名操作人员。
5. 技术要求5.1 安瓿检漏灭菌柜基本性能要求5.1.1 设备安装在一般区,装载侧门向一般区灭菌前室开启,卸载侧门向一般区后室开启。
装载门和卸载门必须有密封圈。
门密封条需能耐受150℃的温度。
5.1.2 该设备为双端传递式设计。
灭菌检漏柜开门两侧均需要安装仪表板。
仅能由一般区进入灭菌检漏柜的技术区。
所有泵、热交换器、管道、电动和气动装置均安装在技术区内。
5.1.3 带安瓿检漏清洗及清洗后干燥装置和程序,采用倒立式真空检漏。
5.1.4 程序结束后安瓿瓶表面应干燥,表面特性应无损害,安瓿瓶温度不超过40℃。
5.1.5 通过装载含有超过106个嗜热脂肪杆菌芽孢的指示剂进行挑战性试验,必须证明生物负荷至少降低6 个对数单位。
5.1.6 检漏的检出率能达到100%。
5.1.7 设备硬件、管路系统及软件控制系统应有合适措施预防器具灭菌后的二次污染。
湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01 5.1.8 供应商需提供设备的平立面图纸、能源需求及消耗量。
5.1.9 供应商需提供机外车、机内车;需提供产品装载盒的图纸供买方自行加工。
5.2 总体要求5.2.1 设备主体要求序号要求1灭菌腔的内胆、门板的材质应使用经供应商鉴定确认的AISI316Ti不锈钢或其他必须符合FDA注册要求且耐磨、耐高温(135℃)、不脱落颗粒物的材质。
表面经机械抛光处理,光亮滑洁、表面粗糙度为Ra < 0.8um。
2 内胆的所有内角为圆弧型,平滑,无焊渣。
内表面抛光至表面粗糙度<0.4 m。
3框架、外壳、前封板等的材质为AISI304不锈钢或无毒不脱落颗粒的耐腐蚀材质,加强筋为碳钢。
4所有管路、阀门、卡箍的材质根据其内容介质或设计的需求采用相应材质的不锈钢管道,如饮用水、压缩空气、补气管道,真空管道采用AISI304不锈钢管道,纯蒸汽采用AISI316L不锈钢管道等,采用的材质必须为不锈钢或无毒不脱落颗粒的耐腐蚀材质。
所有的管口和管线的连接采用卫生型快接。
所用的阀门为AISI316L不锈钢隔膜阀。
5灭菌柜采用双铰门(机动门),门上装有安全装置,当检测到障碍物时自动停止。
前后门破门密封时,应相互独立,相互之间不影响密封性(如开装载侧门时,卸载侧门应能继续保持密封。
6内胆和夹套形状为长方体,四周圆弧过渡,符合中国压力容器的设计、制造和检测必须根据《钢制压力容器》GB150-1998+2002第一号修改单/《钢制压力容器焊接规程》JB/T4709-2000 /《压力容器安全技术监察规程》/《压力容器无损检测》JB4730-94,或依据中国压力容器监管部门接受的其他标准,并有第三方检测证书。
设计温度不低于135℃,设计压力不低于0.25MPa。
腔体应向排水口有倾斜度,使水和蒸汽冷凝物能完全排出。
底部的排水管与排出阀的距离尽可能短,排水口有一个金属过滤网。
排湖南赛隆药业(长沙)有限公司安瓿检漏灭菌柜URS 版本号:01水口要有空气隔断设施,灭菌柜底部疏水管进口应有防止玻屑及其它异物进入的设施,防止堵塞。
7夹套管道与灭菌室管道分别使用不同管路系统,夹套使用工业蒸汽,灭菌室使用纯蒸汽或过热水;工业蒸汽、纯蒸汽或过热水进入灭菌柜前的末端,安装自动疏水阀及压力表,纯蒸汽压力表应使用卫生压力表。
8纯蒸汽入口管道需使用卫生级的快接和取样阀连接,可进行三项蒸汽测试程序,即无可凝性气体、过热及干燥度。
同时可进行进行冷凝后蒸气的取样。
9 内胆冷凝物排水管路需设置取样阀,用于收集冷凝物样品。
11设备安装有水汽分离器,排水、汽管路与下水管道应有空气隔断,避免下水道污染物倒灌,同时应避免设备短时大量排放水汽导致室内温湿度升高和对下水道产生较大的压力,所有可能存在纯蒸汽冷凝水的管道内冷凝水均能完全排尽。
12水环泵系统与箱体连接的管路、箱体排水管路安装有单向阀,避免因箱体负压而倒吸外界空气或异物,饮用水滤网安装于饮用水管道末端,方便拆卸清洗。
13垫圈、密封硅橡胶和O型圈等密封圈应使用医药/食品级材料。
生理无害,不粘连。
必要时应可提供经FDA批准的有相应证书的(如,CFR-构造证书)密封圈。
14 保温材料应是不含纤维、不含石棉的,并全部用304不锈钢焊接覆盖。
15设备箱体预留验证接口,验证孔至少可以插入16个验证探头。
并提供配套的验证接线器。
16配备的水环真空泵的抽气量应保证可在12分钟内将灭菌腔室内的极限真空抽至60mbar。
真空泵应适用于处理空气/蒸汽冷凝物,或二者以任意比混合。