02-4第二章 化学物质及其变化 章末专题归纳例析
- 格式:ppt
- 大小:1.21 MB
- 文档页数:15

渗析利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
其原理为胶体微粒不能透过半透膜,而溶液中的分子和离子能透过半透膜。
胶体的性质1、丁达尔现象(光学性质)实验:光束分别通过AgI胶体和CuSO4溶液,观察现象。
现象:一束光通过胶体时,从侧面可观察到胶体里产生一条光亮的“通路”。
原因:胶粒直径大小与光的波长相近,胶粒对光有散射作用;而溶液分散质的粒子太小,不发生散射。
应用:鉴别溶胶和溶液。
2、布朗运动(动力学性质)在超显微镜下观察胶体溶液可以看到胶体颗粒不断地作无规则的运动。
原因:溶剂分子不均匀地撞击胶体粒子,使其发生不断改变方向、改变速率的布朗运动。
胶体微粒作布朗运动是胶体稳定的原因之一。
3、电泳现象(电学性质)在外加电场作用下, 胶体粒子在分散剂里向电极(阴极或阳极) 作定向移动的现象, 叫做电泳Fe(OH)3胶体向阴极移动——带正电荷重要胶粒带电的一般规律:带正电荷胶粒带负电荷胶粒金属氢氧化物金属氧化物金属硫化物(如Sb2S3)非金属硫化物(如As2S3)非金属氧化物(如SiO2泥沙)硅酸盐(土壤和水泥)胶粒带同种电荷,相互间产生排斥作用,不易结合成更大的沉淀微粒,这是胶体具有稳定性的主要因素。
五、胶体的凝聚使胶体微粒凝聚成更大的颗粒,形成沉淀,从分散剂里析出的过程叫胶体的凝聚。
胶体为什么能够稳定存在?胶粒带电、布朗运动如何破坏胶体的稳定状态?要使胶体凝聚成沉淀,就要减少或消除胶体微粒表面吸附的电荷,使之减弱或失去电性排斥力作用,从而使胶粒在运动中碰撞结合成更大的颗粒。
(1)加入电解质实例:1.豆浆里加盐卤(MgCl2·6H2O)或石膏(CaSO4·2H2O) ,使之凝聚成豆腐;2.水泥里加石膏能调节水泥浆的硬化速率;3.在江河与海的交汇处形成的沙洲。
(2)加入胶粒带相反电荷的胶体带不同电荷的胶体微粒相互吸引发生电性中和,从而在胶粒碰撞时发生凝聚,形成沉淀或凝胶。




高中化学集体备课《第二章化学物质及其变化》第二章专题复习教案苏教版必修专题复习授课班级课时教学目的知识与技能1、巩固物质的分类及方法,了解胶体的主要性质;2、进一步了解离子反应的本质及离子方程式的书写3、进一步了解氧化还原反应的实质及有关概念过程与方法通过知识归纳总结的教学,让学生学会对所学知识进行归纳总结,引起学生对学习方法的重视。
情感态度价值观通过本次课的学习,让学生找到学习的感觉,重视轻松学习的方法,感受学习的快乐重点离子方程式的本质及离子方程式的书写;难点氧化还原反应的实质及有关基本概念的应用知识结构与板书设计第二章化学物质及其变化专题复习一、本章知识结构梳理1、物质的分类2、物质的化学变化二、本章典型题剖析三、本章专题讲座氧化还原反应的基本规律1、守恒律:化合价有升必有降,电子有得必有失,对于一个完整的氧化还原反应,化合价升高总数 ==降低总数 ==失电子总数 ==得电子总数2、价态律:(1)元素处于最高价,只有氧化性;元素处于最低价,只有还原性,元素处于中间价,既有氧化性,又有还原性。
(2)同种元素不同价态之间发生反应,元素化合价只靠近不交叉,相邻价态间不发生氧化还原反应。
注意:1 元素处于最高价,具有氧化性,但不一定氧化性最强,2 金属元素只有正价无负价, F、 O只有负价无正价3 含同一元素的不同物质,若价态相邻,则不发生氧化还原3、强弱律化合价降低,得电子,被还原氧化剂 + 还原剂== 还原产物 + 氧化产物氧化性:氧化剂氧化产物还原性:还原剂还原产物教学过程教学步骤、内容教学方法、手段、师生活动板书一、本章知识结构梳理讲分类是学习和研究化学物质及其变化的一种常用方法。
分类要有一定的标准,根据不同的标准可以对化学物质及其变化进行不同的分类。
常用的分类方法有交叉分类法和树状分类法。
板书1、物质的分类投影 (1)以分散质粒子大小对分散系分类 (2)以组成为标准对物质进行分类单质金属:Na 、 Mg 、 Al 非金属:S、 N2 、 O2 氧化物酸性氧化物:SO2、 SO3、 P2O5、碱性氧化物:Na2O、 CaO、 Fe2O3 两性氧化物:Al2O3 不成盐氧化物:CO、 NO 按酸根含氧酸:HNO3、 H2SO4 投影主干知识,让学生回忆细节知识。
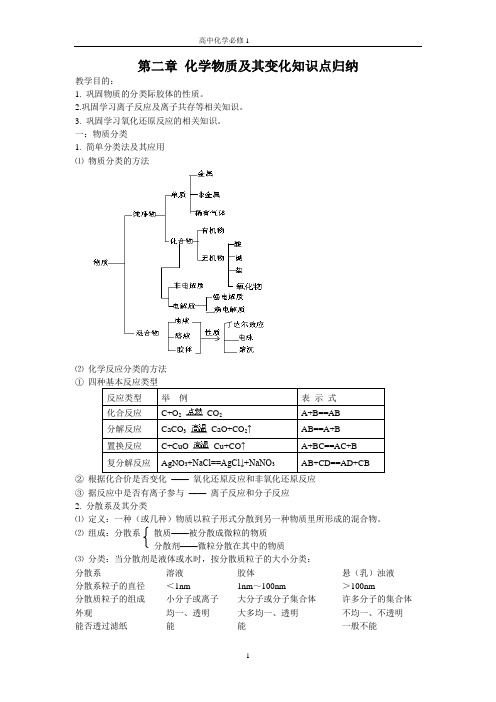
第二章化学物质及其变化知识点归纳教学目的:1. 巩固物质的分类际胶体的性质。
2.巩固学习离子反应及离子共存等相关知识。
3. 巩固学习氧化还原反应的相关知识。
一:物质分类1. 简单分类法及其应用⑴物质分类的方法⑵化学反应分类的方法①四种基本反应类型反应类型举例表示式化合反应C+O2CO2A+B==AB分解反应CaCO3CaO+CO2↑AB==A+B置换反应C+CuO Cu+CO↑A+BC==AC+B复分解反应AgNO3+NaCl==AgCl↓+NaNO3AB+CD==AD+CB②根据化合价是否变化——氧化还原反应和非氧化还原反应③据反应中是否有离子参与——离子反应和分子反应2. 分散系及其分类⑴定义:一种(或几种)物质以粒子形式分散到另一种物质里所形成的混合物。
⑵组成:分散系散质——被分散成微粒的物质分散剂——微粒分散在其中的物质⑶分类:当分散剂是液体或水时,按分散质粒子的大小分类:分散系溶液胶体悬(乳)浊液分散系粒子的直径<1nm 1nm~100nm >100nm分散质粒子的组成小分子或离子大分子或分子集合体许多分子的集合体外观均一、透明大多均一、透明不均一、不透明能否透过滤纸能能一般不能能否透过半透膜能不能不能实例食盐水、糖水淀粉胶体、Fe(OH)3胶体泥水⑷胶体①胶体的制备:Fe(OH)3胶体的制备:______________________②胶体的性质A:丁达尔效应:光束通过胶体,形成光亮的“通路”的现象B:布朗运动:胶体分散质粒子作不停的、无秩序的运动的现象C:电泳现象:在外加电场的作用下胶体微粒在分散剂里做定向移动的现象,叫做电泳。
D:胶体的聚沉:消除胶粒所带电荷,并使其凝集沉降的方法方法1.加电解质溶液(也称盐析):如盐卤点豆腐。
2.加带相反电荷的胶粒;3.加热:如煮鸡蛋。
③胶体介稳定的原因:胶体粒子具有相对较大的表面积,能吸附离子而带电荷,所以胶体粒子带电。
同种胶体粒子带同种电荷,互相排斥;另外,胶体粒子在不停的做布朗运动。
第二章 化学物质及其变化第一讲 物质的组成、性质和分类考点1 物质的组成与分类一、元素、微粒及物质间的关系1.宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
2.元素:具有相同核电荷数(即质子数)的一类原子的总称。
3.元素与物质的关系元素A――→组成⎩⎪⎨⎪⎧单质:只由一种元素组成的纯净物化合物:由多种元素组成的纯净物4.元素在物质中的存在形态(1)游离态:元素以单质形式存在的状态。
(2)化合态:元素以化合物形式存在的状态。
5.混合物和纯净物(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
6.同素异形体(1)同种元素形成的不同单质叫同素异形体。
同素异形体的形成有两种方式:①原子个数不同 ,如O 2和O 3;②原子排列方式不同,如金刚石和石墨。
(2)同素异形体之间的性质差异主要体现在物理性质上,同素异形体之间的转化属于化学变化,但不属于氧化还原反应。
7.元素、微粒及物质间的关系图二、物质的分类1.交叉分类法——从不同角度对物质进行分类(如图为氧化物的分类)2.树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系。
考点2物质的性质与变化一、物质的性质与变化二、单质、氧化物、酸、碱、盐的转化关系1.理解物质转化关系图2.形成转化关系一条线:(氢化物→)单质→氧化物→酸或碱→盐。
三、化学反应的分类化学反应⎩⎪⎪⎪⎨⎪⎪⎪⎧按反应物、生成物种类及数目多少分为⎩⎪⎨⎪⎧化合反应分解反应置换反应复分解反应按反应中有无离子参与分为⎩⎪⎨⎪⎧离子反应非离子反应按反应中有无电子转移分为⎩⎪⎨⎪⎧氧化还原反应非氧化还原反应按反应进行的程度和方向分为⎩⎪⎨⎪⎧可逆反应不可逆反应按反应的能量变化分为⎩⎪⎨⎪⎧吸热反应放热反应四、物质变化中的“三馏”“四色”“五解”和“十八化”归类考点3分散系与胶体一、分散系1.概念:把一种(或多种)物质(分散质)分散在另一种(或多种)物质(分散剂)中所得到的体系。
高考化学 第二章 化学物质及其变化解析【本节学习要点】1.能根据物质的组成和性质对物质进行分类。
2.了解胶体是一种常见的分散系。
重难点一、物质的分类1.物质分类的标准很多,常有:(1)根据物质的组成⎩⎪⎨⎪⎧纯净物⎩⎪⎨⎪⎧单质化合物⎩⎪⎨⎪⎧ 酸碱盐氧化物混合物(2)根据物质的导电性⎩⎪⎨⎪⎧导体绝缘体半导体(3)根据元素的存在方式⎩⎪⎨⎪⎧单质化合物(4)根据物质的溶解性⎩⎪⎨⎪⎧难溶物质微溶物质可溶物质易溶物质(5)根据物质的状态⎩⎪⎨⎪⎧气体液体固体2.一类物质有多种分类方法 如酸的其他分类:(1)按酸强弱⎩⎪⎨⎪⎧强酸:如H 2SO 4、HNO 3、盐酸等弱酸:如碳酸等(2)按酸挥发性⎩⎪⎨⎪⎧难挥发性酸:如H 2SO 4、H 3PO 4等挥发性酸:如盐酸、HNO 3等(3)按酸稳定性⎩⎪⎨⎪⎧稳定性酸:如H 2SO 4等不稳定性酸:如H 2CO 3等(还有其他分类方法) 3.理清交叉分类的关系 如氧化物的分类中:(1)金属氧化物不一定是碱性氧化物,如Mn 2O 7、A l 2O 3等;(2)非金属氧化物不一定是酸性氧化物,如CO 、NO 等; (3)酸性氧化物不一定是非金属氧化物,如Mn 2O 7等; (4)碱性氧化物一定是金属氧化物。
氧化物交叉分类图:重难点二、分散系及其分类 常见三种分散系的比较特别提醒(1)三类分散系的本质区别是分散质粒子的大小,分散系的性质(如是否透明、均一、稳定)都是由它决定的。
同种分散质在不同分散剂中可以得到不同的分散系,如NaCl溶于水得溶液,溶于酒精得胶体。
(2)液体分散系的稳定性质 ①溶液是最稳定的分散系这是因为这类分散系中的分散质(溶质)对于分散剂(溶剂)而言是可溶性的。
溶质以分子、原子或离子(直径<1 nm)的形式自发地分散在溶剂中,形成均一、稳定的混合物。
②浊液是不稳定的分散系因为分散质粒子是大量分子的集合体,分散质粒子容易在重力的作用下沉降或沉淀,故表现出浑浊、不稳定、不透明、不均一的外观特征。