高速逆流色谱仪的优势
- 格式:doc
- 大小:32.50 KB
- 文档页数:4

l 高速逆流色谱是液相色谱的一种新技术,无需载体,从几种色谱原理方法可以清晰说明。
大约50年前,根据对两种液体进行分配的理念,产生了两种相似的方法:逆流分配技术和液-液色谱分配技术,即:逆流色谱和液相色谱。
30年前,日本Sanki Engineering Ltd.利用前一种技术开发出了高性能的逆流色谱仪(HPCPC),它结合了液相色谱中的快速、高效和先进技术。
HPCPC尤其在利用色谱技术进行半制备和全制备的应用中倍受瞩目,它和采用色谱柱技术的液相色谱在四个方面具有显著优势:● 无样品损失:因为流动相和固定相都是液体,样品可以全部回收。
● 大容量和高的分离能力:流动相和固定相的体积比明显很高,从而无需更大的理论塔板数,就可以获得更大的容量和更高的分离能力。
● 十分灵活的两相系统:(两种、三种、四种溶剂混合)为了获得一种纯的化合物,实验中需要比较灵活的更改流动相,HPCPC可以很方便地调整两相的极性。
● 溶剂消耗少:相对于色谱柱制备系统,对于同样的制备量,HPCPC的溶剂消耗量只有十分之一,使用逆流色谱在实验室完成分离后,可以直接放大到生产规模。
● 固定相价格低:另一个显著优点是逆流色谱的固定相是溶剂,相比色谱柱中的填充材料价格低很多;而且固定相可以很容易再生,一些添加的物质如手性选择剂或复杂的配位体可以无损失地回收,国际上出版的论文可以提供十分有用的信息和应用参考。
新型的高速逆流色谱仪HPCPC广泛地应用于化学领域的纯化,如抗生素、缩氨酸、丹宁酸、皂角苷、油脂、药品等,将来的发展可以预见更大规模和产量的HPCPC设备出现,在化学领域将更加广泛地应用,如手性药物分离等。
与传统制备液相的优势● 逆流色谱仪HPCPC十分快速由于固定相溶剂通过离心力保留在分配通道中,可以不用顾及分离精度的高低要求而让流动相的流速保持很高。
● 明显优于传统制备液相由于逆流色谱仪HPCPC不需要固定相,不会出现对十分昂贵的样品产生不可逆转的保留,而在传统色谱柱的液相色谱中,经常出现的变性和分解现象在逆流色谱不会产生,同时保留了原来的生物活性。



高速逆流色谱High Speed Countercurrent Chromatography(HSCCC)逆流色谱是利用溶质在两种互不相溶的溶剂中的分配系数不同,应用色谱层析的方法,将不同溶质分离。
逆流色谱的发展从逆流分配、液滴逆流色谱直至现在的高速逆流色谱,经历了近60年的历程,技术和设备均已日益成熟,现越来越多地应用于中药及天然药物的研究开发。
高速逆流色谱特点:! 无不可逆吸附# 液—液层析系统,无样品与固定相之间的不可逆吸附! 高回收率# 流动相和固定相均为液体,样品可全部回收! 操作简便# 固定相为液体,体系更换、平衡方便、快捷。
高速逆流色谱原理:高速逆流色谱是利用螺旋柱在行星运动时产生的离心力,使互不相溶的两相不断混合,同时保留其中的一相(固定相),利用恒流泵连续输入另一相(流动相),随流动相进入螺旋柱的溶质在两相之间反复分配,按分配系数的次序,被依次洗脱。
在流动相中分配比例大的先被洗脱,反之,在固定相中分配比例大的后被洗脱。
图1是螺旋柱中互不相溶的两相溶剂在行星运动时的流体动力学运动及分配示意图。
上图,在达到稳定的流体动力学平衡态后,柱中呈现两个截然不同的区域:在靠近离心轴心大约有四分之一的区域(混合区)呈现两相的激烈混合。
其余区域(静置区)两溶剂相分成两层:较重的溶剂相在外部,而较轻的溶剂相在内部,两相形成一个线状分界面。
下图,I到IV的展开柱,分别与上图中I到IV位置相对应,每一混合区以跟柱旋转速度相同的速度向柱头端移动(与海面波的运动相似)。
在螺旋柱中任何一部分,两相溶剂都在反复进行混合和静置的分配过程,这一过程频率极高,当柱以800rpm旋转时,频率超过13次/秒,流动相则不断地穿过固定相。
所以高速逆流色谱在一个较宽的流动相流速范围内,仍有相当高的分配效率。
图1 螺旋柱中两溶剂相流体动力学运动及分配高速逆流色谱应用:1. 旋转速度在逆流色谱中,留在柱中固定相的量是影响溶质峰分离度的一个重要因素,一般说来,高保留量会大大改进峰分离度。


高速逆流色谱仪原理特点及应用一、简介高速逆流色谱(HPLC)是一种高效、精准的分析技术,它广泛应用于化学、制药、环保、食品等领域。
高速逆流色谱仪是高速逆流色谱技术的核心设备,能够对各种化合物进行分离和检测。
在本文中,我们将介绍高速逆流色谱仪的原理、特点及应用。
二、原理高速逆流色谱仪使用液相色谱技术,其基本原理是将待测样品溶液经过一定的处理后,注入色谱柱,通过色谱柱内液相的物理化学作用,将各种组分分离出来,并用检测器检测分离出来的化合物。
高速逆流色谱仪相较于其他色谱仪的优势在于可以在极短的时间内完成大量的分离、检测等操作。
高速逆流色谱仪的原理是基于其内部的色谱柱,其内部结构可以细分为装载柱、色谱柱和联接管。
样品通过色谱柱时,每种组分将被一步一步地分离出来,直到达到检测器,最后数据将被转换为电子信号,并通过数据处理软件进行分析和处理。
三、特点1. 高效HPLC技术的一大优势在于其高效性,使用HPLC技术可以在更短的时间内分离出更多的物质成分,从而提高分析效率。
2. 精准由于高速逆流色谱仪的高分辨率和灵敏度,其能够分离出复杂物质的成分,从而提供更加准确的结论。
3. 多种检测方式高速逆流色谱仪可使用不同类型的检测器,如紫外检测器、荧光检测器等,可以检测多种类型的化合物成分。
4. 适用范围广高速逆流色谱仪不仅适用于小分子化合物的分离和检测,也可以用于生物大分子、天然产物、有机和无机化合物等物质的分离和检测。
四、应用高速逆流色谱仪广泛应用于化学、生命科学、环境科学、食品科学等领域,其准确性和高效性为这些领域的研究和实践提供了重要的技术支持。
1. 化学在化学领域中,高速逆流色谱仪通常在合成新药物、分离小分子化合物、分析毒物、研究反应机理等方面有着广泛的应用。
2. 生命科学高速逆流色谱仪在生命科学领域可以用于分析蛋白质、氨基酸、核酸和多糖等生物大分子,可以检测蛋白质含量和组成,研究生物大分子的三维结构,为分子生物学、细胞生物学和基因工程研究提供技术支持。


高速逆流色谱技术1.概述高速逆流色谱(high-speed counter current chromatography,简称 HSCCC),是20世纪70年代由美国国立卫生院(National Institute of Health,简称NIH)Ito博士首创,并且在最近10年之内发展迅速,是一种可在短时间内实现高效分离和制备的新型液-液分配色谱技术,这项技术可以达到几千个理论塔板数的。
它具有操作简单易行、应用范围很广、无需固体载体、产品纯度高、适用于制备型分离等特点。
自1982年第一台仪器问世,就开始了HSCCC的现代化进程。
HSCCC用于天然药物化学成分的分离始于1985年,到1989年达到一个高潮。
自2000年9月起国际逆流研究领域每隔2年举行一次世界逆流色谱学术会议。
近几年, 人们对健康的认识越来越深刻, 更多的人追求天然绿色的健康理念, 故HSCCC 作为一种对提取物污染小的制备技术, 它的应用越来越受到了人们的关注。
鉴于HSCCC的显著特点, 此项技术已被应用于生化、生物工程、医药、天然产物化学、有机合成、环境分析、食品、地质、材料等领域。
目前,HSCCC已从制备型发展到了分析型, 甚至是微量分析型, 应用范围也十分广泛[ 2]。
高速逆流色谱技术在我国的应用较早, 技术水平在国际领域也处于领先地位。
目前, 我国是世界上为数不多的高速逆流色谱仪生产国之一。
我国的深圳同田生化技术有限公司是全球第一家多分离柱高速逆流色谱仪专业生产企业。
公司拥有自主知识产权的高速逆流色谱专利技术, 现已研制并生产出TBE 系列分析型, 半制备型TBE 300,300A, 制备型TBE1000高速逆流色谱仪设备。
2.基本原理高速逆流色谱技术(HSCCC)是一种不用任何同态载体的液-液色谱技术,其分离原理是进行分离纯化时,首先选择预先平衡好的两相溶剂中的一相为固定相, 并将其充满螺旋管柱, 然后使螺旋管柱在一定的转速下高速旋转, 同时以一定的流速将流动相泵入柱内。


高速逆流色谱法的概况及应用高速逆流色谱( High-Speed Countercurrent Chromatography,HSCCC) 是Yoichiro Ito 博士于二十世纪八十年代首先研发、应用并发展起来的一种新型液-液分配色谱技术;HSCCC运用同步多层螺旋管进行行星式离心运动,使得在互不相溶的两相溶剂系统中可以实现样品在短时间内的高效分离,从而制备样品[1,2]。
高速逆流色谱技术不需要固体支撑物,主要根据样品在两相中所具有的不同分配系数进而对样品进行分离,相对于其他色谱技术如高效液相色谱、柱色谱等来说,具有高回收率、无吸附损耗、无峰拖尾等优点。
1、HSCCC法概况1.1 HSCCC法的基本原理HSCCC属于液 -液分配色谱,所以其基本分离原理与其他同类色谱技术相同,即利用物质在两相间分配系数的差别进行分配。
而 HSCCC将两溶剂的分配体系置于高速旋转的螺旋管内 ,建立起一种单向性流体动力平衡体系。
螺旋管的运动形式,是在自身自转的基础上,同时绕一公转轴旋转,成行星运动[3]。
这样 ,加在分配体系上的离心力场不断发生变化,使两相溶剂充分的混合和分配,从而达到洗脱分离目的。
HSCCC技术已经广泛应用于天然产物的分离。
1.2 溶剂系统的选择利用 HSCCC分离物质的关键是溶剂系统的选择。
经查阅多篇文献,总结要点如下。
对用于 HSCCC分离的溶剂体系,应该满足这几方面的要求:1)不造成样品的分解与变性;2)足够高的样品溶解度;3)样品在系统中有合适的分配系数值;4)固定相能实现足够高的保留[4]。
而对于溶剂体系选择的原则,Ito博士本人总结的几个要点是这样描的:1)待分析组分应易溶于溶剂系统 ,并不与之发生反应;2)溶剂体系的各组分应分成体积比例适合的两相,以免浪费溶剂;3)组分在溶剂系统中的分配系数 K应为适当的定值 (0.5≤K≤1);4)固定相的保留值要满足一定要求 (保留值越大峰形越好 )。
高速逆流色谱综述高速逆流色谱(High-speed Countercurrent Chromatography,简称HSCCC),于1982年由美国国立卫生院Ito博士研制开发的一种新型的、连续高效的液液分配色谱技术。
该技术由于不需要固体支撑体,物质的分离依据其在两相中分配系数的不同而实现,因而避免了因不可逆吸附引起的样品损失、失活、变性等问题,具有传统的液-固色谱所不具备的独特优势,特别适合于天然生物活性成分的分离。
而且由于被分离物质与液态固定相之间能够充分接触,使得样品的制备量大大提高,是一种理想的制备分离手段,因此此项技术己被广泛应用于中药成分分离、保健食品、生物化学、生物工程、天然产物化学、有机合成、环境分析等领域[1]。
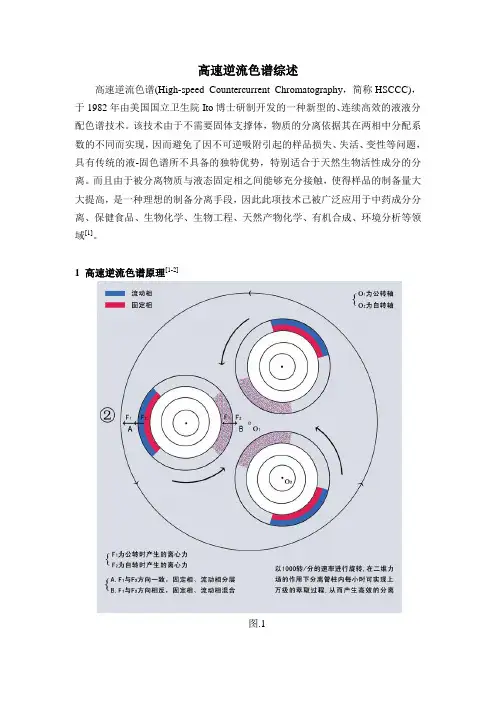
1 高速逆流色谱原理[1-2]图.1高速逆流色谱仪利用螺旋管的自转和公转同步同向行星式运动所产生的变化离心力场将固定相保留在螺旋管中,允许流动相快速流过螺旋管并与固定相进行连续高效的混合和分配,达到一种特殊的流体动力学平衡——单向流体动力学平衡,此时在螺旋柱中任何一部分,两相溶剂都反复进行着混合和静置的分配过程,这一过程频率极高,在800rpm转速下时,混合和分配的频率可以达到13次/s。
大大提高了两相溶剂的混合效率,可以极大地缩短分离时间,这就是高速逆流色谱分离效率高的原因。
如图.1。
2 高速逆流色谱(HSCCC)的特点及与制备型高效液相色谱(prep-HPLC)的比较[3-4]目前制备出高纯度的天然产物的方法中,制备型高效液相色谱是使用最为广泛的。
与其相比,高速逆流色谱具有以下一些突出的优点。
(1)HSCCC回收率高:由于HSCCC不需要固体支撑体,避免了样品在分离过程中的不可逆吸附、分解、变性等问题。
理论上,滞留在柱中的样品可以通过多种洗脱方式予以完全回收;实验中只要调整好分离条件,一般都有很高的回收率。
粗样可以直接上样而不会对柱内固定相造成任何损害。
而prep-HPLC在样品吸附过程中会出现死吸附的现象,在制备高纯品的过程中,必然会以牺牲得率为代价,这是prep-HPLC不可避免的。
⾼速逆流⾊谱分离技术是⼀种不⽤任何载体或⽀撑体的液-液分配⾊谱技术。
该技术分离效率⾼,产品纯度⾼,不存在载体对样品的吸附和污染,具有制备量⼤和溶剂⽔泵少等优点,可⼴泛应⽤于⽣物⼯程、医学、医药、化⼯、⾷品等领域。
上世纪80年代后期,⼴泛应⽤于天然药物成分的分离制备和分析中。
有报道⽤该技术研究⽣物碱、黄酮、蒽醌、⾹⾖素等成分的分离都取得了较好的效果。
⾼速逆流⾊谱分离法不仅适⽤于⾮极性化合物的分离,也适⽤于极性化合物的分离,还可以应⽤于进⾏中药粗提物中各组分的分离或进⼀步的纯化精制。
该技术有望成为中药有效成分质量标准研究、分析的⼀种新⽅法,也会成为中药制剂⽣产的⼀种新型分离技术。
高速逆流色谱技术在植物活性成分分离中
的应用
高速逆流色谱技术是一种新技术,它可以有效地分离并研究植物活性成分。
在植物活性成分分离方面,该技术具有独特的优势,可以解决传统技术不能解决的问题。
首先,高速逆流色谱技术具有很快的分离速度,可以在很短的时间内完成大量植物活性成分的分离。
此外,该技术具有较低的能量消耗,能够有效地降低植物活性成分分离的成本。
此外,由于具有较好的分离精度,能够很好地分离出植物中的复杂活性成分,以得到更加丰富精细的活性物质。
其次,高速逆流色谱技术具有灵活性高的特点,使得植物中不同组分的活性成分能够被准确地分离出来。
此外,该技术具有很好的稳定性,并且可以准确检测到活性成分的微量变化。
除此之外,该技术的建模软件也可以对植物活性成分进行准确的数值描述,从而更准确地确定植物活性成分的结构和性质。
总的来说,高速逆流色谱技术是一种新技术,具备较高的效率和
精度,能有效地分离植物活性成分,并且能进行学术研究和实际应用。
因此,该技术在植物活性成分分离领域有着重要的应用价值。
高速逆流色谱法在中药有效成分分离中的应用研究高速逆流色谱是近几年发展起来的新型色谱技术,由于其独特之处已被广泛应用于各个领域,本文就人们关心的热点中药有效成分的分离,采用新的色谱技术高速逆流色谱技术分离取得的成就进行总结,并展望未来的前景。
标签:高速逆流色谱法;中药有效成分;分离;应用近年来,随着中国经济的高速发展,中草药已经越来越受到人们的关注。
而中药的有效成分复杂,如何获得高效的有效成分,分离效果成为研究的热点。
高速逆流色谱法(high-speed countercurrent chromatography,HSCCC)具有分析能量大、分离效率高、结果重现性好等其他色谱无法替代的优点。
现高速逆流色谱技术这种新型的液-液分配色谱已广泛应用于医药、农林、化工等各领域[1]。
应用新型的高速逆流色谱分离成分复杂的中药有效成分可取得良好的效果,具体总结如下。
1工作原理高速逆流色谱HSCCC是应用不同物质在固液两相中的分配系数不同进行分离。
一台高速逆流色谱仪是由输液泵、分离柱、检测器、工作站、数据采集系统及馏分收集器等组成。
首先选择固定相,是将两相预先平衡好的溶剂中的一相填充满螺旋管柱,将流动相以一定的流速泵入高速旋转的螺旋管柱内。
在有液体流动相流出时,说明体系达到平衡,此时将样品注入高速逆流色谱体系中,螺旋管分离柱将依据不同成分在固液两相中的分配系数不同达到分离,依据工作站和数据采集系统将分离后的结果进行记录并积分处理。
在仪器运行的时候,可调节溶剂、固定相、流动相、样品浓度、柱温、洗脱方式、进样方式、流动相的流速及转速等使分离效果达到最好。
还需要根据所检测样品的特点,选择不同的检测器,UV-VIS(紫外-可见光检测器)、ELSD(蒸发光散射检测器)或者质谱检测器等[2]。
2中药的有效成分各种植物中所含的有效成分分类为生物碱、黄酮、苷、萜、蒽醌、木脂素、香豆素、有机酸等。
3高速逆流色谱分离各类中药有效成分3.1生物碱类中药的有效成分中生物碱是重要的一类化学成分,其中的天然含氮化合物是重要的疾病治疗和药物发展的物质。
高速逆流色谱属于逆流色谱的范畴,逆流色谱是一种新型的分离手段,它的主要分离原理是利用样品在固定相和流动相之间的差异也就是分配比不同而进行分离的,值得注意的是逆流色谱的固定相和流动相都是液体,其主要优点是没有传统色谱的死吸附,样品的回收率高等特点。
逆流色谱源于逆流分溶法,也就是用实验室经常使用的分液漏斗进行连续的液液萃取,根据样品在两种互不相溶的溶剂中分配比不同而进行分离。
逆流色谱早期发展的方法有液滴逆流色谱,旋转小室逆流色谱等。
但是作为一种分离手段,早期发展的逆流色谱不能满足高效快速的分离,分离的周期很长,效率很低。
在70年代,Ito 博士成功开发了一种能够高效快速分离的逆流色谱-高速逆流色谱。
但高速逆流色谱也有很多种设计,经过几十年的发展,现在的高速逆流色谱一般是采用同步行星式的设计,其主要是利用在高速旋转状态产生的二维离心力场的作用下使两种互不相溶的溶剂快速有效的对流或分割----或者说混合或分层,从而使样品能够在短时间内进行成千上万次萃取,根据样品中的物质分配系数的不同而进行分离的一种方法。
HSCCC 有几个突出优点:(1)无不可逆吸附。
聚四氟乙烯管中的固定相无需载体液-液色谱系统,故而消除了气- 液和固- 液色谱中因使用载体而带来的吸附现象,特别适于分离极性物质和生物活性物质;(2)高回收率。
由于流动相和固定相均为液体,样品可全部回收,分离纯化与制备可同步完成,故特别适于制备性分离;(3 )操作简便。
因固定相为液体,体系更换与平衡方便、快捷。
与HPLC 相比,HSCCC 进样量较大,最多可达数克,是HPLC 的数百倍;与常压、低压色谱相比,HSCCC 的分离能力强,有些样品经一次分离即得到1个甚至多个单体,且分离时间短,数小时即可完成,纯度多在98%以上。
高速逆流色谱作为一种比较新颖的分离方法,影响因素主要有溶剂体系的选择,旋转速度,流动相的流速,温度等影响。
溶剂体系选择即条件的摸索,相当于传统色谱摸流动相的条件,不同的是高速逆流色谱条件的摸索主要是指样品在固定相和流动相两者之间的分配的比值,待分离的样品的K值最好在0.6-1.5范围之内,这样才会有一个好分离效果。
高速逆流色谱仪的优势高速逆流色谱(high-speed countercurrent chromatography,简称HSCCC)是一种较新型的液—液分配色谱,由美国国立健康研究院(National Institute of Health, U.S.A.)Ito博土最先研制开发后由北京市新技术应用研究所在国内开展研发和推广工作。
其原理是基于样品在旋转螺旋管内的互不混溶的两相溶剂间分配不同而获得分离,因而无须任何固体载体或支撑体,能达到在短时间内实现高效分离和制备,并且可以达到几千个理论塔板数。
与其他柱色谱相比较,它克服了固定相载体带来的样品吸附、损失、污染和峰形施尾等缺点[3]。
目前此项技术已被应用于生化、生物工程、医药、天然产物化学、有机合成、环境分析、食品、地质、材料等领域[5]。
我国是继美国、日本之后最早开展逆流色谱应用的国家,俄罗斯、法国、英国、瑞士等国也都开展了此项研究。
美国FDA及世界卫生组织(WHO)都引用此项技术作为抗生素成分的分离检定,90年代以来,高速逆流色谱被广泛地应用于天然药物成分的分离制备和分析检定中。
1. 高速逆流色谱仪原理及特点HSCCC利用了一种特殊的流体动力学(单向流体动力学平衡)现象。
具体表现为一根100多米长的螺旋空管,注入互不相溶的两相溶剂中的一相作为固定相,然后作行星运动;同时不断注入另一相(流动相),由于行星运动产生的离心力场使得固定相保留在螺旋管内,流动相则不断穿透固定相;这样两相溶剂在螺旋管中实现高效的接触、混合、分配和传递。
由于样品中各组分在两相中的分配比不同,因而能使样品中各组分得到分离。
2. HSCCC的优点HSCCC主要具有以下几个方面的优点。
2.1 应用范围广,适应性好。
由于溶剂系统的组成与配比可以是无限多的,因而从理论上讲HSCCC适用于任何极性范围的样品的分离,所以在分离天然化合物方面具有其独到之处。
并因不需固体载体,而消除了气液色谱中由于使用载体而带来的吸附现象,特别适用于分离极性物质和其它具有生物活性的物质。
2.2 操作简便,容易掌握。
分离过程中对样品的前处理要求低,仅需一般的粗提物即可进行HSCCC的制备分离或分析。
2.3 回收率高。
由于没有固体载体,不存在吸附、降解和污染,理论上样品的回收率可达100%。
在实验中只要调整好分离条件,一般都有很高的回收率。
2.4 重现性好。
如果样品不具有较强的表面活性作用,酸碱性也不强,那么多次进样,其分离过程稳定性都保持很好、峰的保留相对标准偏差也小于2%,重现性相当好。
2.5 分离效率高,分离量较大。
由于其与一般色谱的分离方式不同,能实现梯度操作和反相操作、亦能进行重复进样,使其特别适用于制备性分离,产品纯度高。
研究结果表明:一台普通的高速逆流色谱仪一次进样可达几十毫升,一次可分离近10g的样品。
因此,在80年代后期被广泛地应用于植物化学成分的分离制备研究文章链接:中国化工仪器网/Tech_news/Detail/49747.html高速逆流色谱仪常用溶剂体系选择方法1. 已知的溶剂体系被分离物质种类基本两相溶剂体系辅助溶剂非极性或弱性物质正庚(已)烷-甲醇氯烷烃正庚(已)烷-乙腈氯烷烃正庚(己)烷-甲醇(或乙腈)-水中等极性物质氯仿-水甲醇,正丙醇,异丙醇乙酸乙酯-水正己烷,甲醇,正丁醇极性物质正丁醇-水甲醇,乙酸2. 分配系数测定法一个稳定的两相溶剂体系是否适合于目标物质的分离,通常要看物质在该溶剂体系中的分配系数是否在一个合适的范围内。
分配系数K=CS/CM或CU/CL。
其中CS指溶质在固定相中的浓度,CM指在流动相中的浓度,CU指溶质在上相中的浓度,CL指溶质在下相中的浓度。
一般而言,对HSCCC最合适的K值范围是0.5~2。
当CS/CM≤0.5时,出峰时间太快,峰之间的分离度较差;当CS/CM≥1时,出峰时间太长且峰形变宽。
而当0.5<CS/CM<2时,可以在合适的时间内,得到分离度较好的峰形。
溶质的分配系数可以采用分析型HPLC来确定。
如果有目标成分的对照品或标准品,当溶质在两个互混溶的液相中分配之后,各组分的浓度即可用HPLC精确测定出来,从而计算出分配系数K值。
如果没有目标成分的标准品,混合物中各组分的分配系数值可以通过下述方法进行简单的计算:即先将一定量的样品溶解在体积为Vu的上层溶液中,然后再用体积为VL的下层进行分配,分别测定分配前和分配后上层溶液中各组分的响应值,然后用图1所示的方法即可计算出分配系数。
同样,也可以采用薄层色谱法来测定各组分的分配系数。
3. HPLC扫描法对于一个未知样品,可以通过HPLC扫描的方法,对样品的复杂程度及其组分的极性程度有一个初步的了解。
具体来讲,可以将样品注入一根15cm长的C18HPLC柱,以乙腈和水为流动相,以1ml/min流速,从100%乙腈梯度洗脱1h,观察样品出峰的位置。
如果绝大部分峰的保留时间都小于15min,也就意味着这些组分是由含量小于25%的乙腈流动相洗脱出来的,在CCC中可以采用极性溶剂体系,如正丁醇-水等;如果峰的保留时间是在15~50min 之间,意味着这些物质具有中等极性,在CCC中可以采用中等极性溶剂;如果绝大部分峰在50min后洗脱出来,也就是由大于80%的乙腈流动相洗脱出来的,那么在CCC分离中应该采用弱极性的容积体系。
4. 薄层色谱法采用薄层色谱(TLC)法也可选择对HSCCC合适的两相溶剂体系。
在硅胶板上作薄层色谱试验,用水饱和的有机层(即两相中的有机相)作展开剂。
如果需要分离的组分的Rf >0.5(低级性溶质),这说明此种条件适用于这些组分混合物的分离,而且弱极性的有机相适用于作流动相。
对于极性较大的溶质Rf<0.5,则极性较强的那一相可作流动相。
这种方法只能给出应选溶剂体系的大体指示,因为TLC本身就包含有分配和吸附两种机理,而CCC 则是纯粹的液-液分配过程。
然而,TLC仍不失为一种简便易行的手段,当小量的样品在溶剂体系的两相之间分配时,TLC仍能用来检查其分布状况。
比如,如果发现样品几乎全分布在一相之中,那么这个溶剂体系是绝对不能用的。
5. 生物活性物质分配比率法这是一种只适合于具有生物活性成分的方法,其原理基于需分离的混合物的生物活性分布规律。
首先振摇溶有样品的两相溶剂体系,然后分别测定上层和下层溶液的生物活性。
在两相中活性分布比较均衡的溶剂体系即可采用。
这一方法的缺点是要获得生物测试的结果往往需要较长的时间。
该方法主要用于抗生素的分离。
6. 分析型HSCCC法用分析型HSCCC法来选择制备型分离时所用的溶剂体系是一种很实用的方法。
由于其柱体积小、所需溶剂量少,在很短的时间内即可获得合适溶剂体系的信息。
溶剂体系的选择和优化是一项复杂而艰巨的工作,目前有关溶剂体系的选择方法和评价体系较多,但是系统性和理论性较差,实际操作起来较为困难。
因此,在实际工作中,溶剂体系的筛选通常更多的是参考已知的溶剂体系,或者根据经验而进文章链接:中国化工仪器网/Tech_news/Detail/49748.html非均相混合物的分离方法非均相混合物通常采用机械的方法分离,即利用非均相混合物中分散相和连续相的物理性质(如密度、颗粒形状、尺寸等)的差异,使两相之间发生相对运动而使其分离。
根据两相运动方式的不同,机械分离可有两种操作方式,过滤和沉降。
1.过滤过滤是流体相对于固体颗粒床层运动而实现固液分离的过程。
过滤操作的外力可以是重力、压差或惯性离心力。
因此,过滤操作又分为重力过滤、加压过滤、真空过滤和离心过滤。
2.沉降沉降是在外力作用下使颗粒相对于流体(静止或运动)运动而实现分离的过程。
沉降操作的外力可以是重力(称为重力沉降),也可以是惯性离心力(称为离心沉降)。
此外对于含尘气体的分离还有过滤净制、湿法净制、电净制等方法。
过滤是分离悬浮液最常用和最有效的单元操作。
过滤与沉降分离相比,过滤操作可使悬浮液分离得更迅速、更彻底。
一、过滤的基本概念1.过滤及过滤推动力过滤是以某种多孔物质作为介质来处理悬浮液的单元操作。
在外力的作用下,悬浮液中的液体通过介质的孔道而固体颗粒被截留下来,从而实现非均相物系的固、液分离。
过滤推动力是过滤介质两侧的压力差。
压力差产生的方式有滤液自身重力、离心力和外加压力,过滤设备中常采用后两种方式产生的压力差作为过滤操作的推动力。
用沉降法(重力、离心力)处理悬浮液,往往需要较长时间,而且沉渣中液体含量较多,而过滤操作可使悬浮液得到迅速的分离,滤渣中的液体含量也较低。
当被处理的悬浮液含固体颗粒较少时,应先在增稠器中进行沉降,然后将沉渣送至过滤机。
在某些场合过滤是沉降的后续操作。
2.过滤方式工业上的过滤操作主要分为饼层过滤和深层过滤。
(1)饼层过滤,过滤时非均相混合物即滤浆置于过滤介质的一侧,固体沉积物在介质表面堆积、架桥而形成滤饼层。
滤饼层是有效过滤层,随着操作的进行其厚度逐渐增加。
由于滤饼层截留的固体颗粒粒径小于介质孔径,因此饼层形成前得到的浑浊初滤液,待滤饼形成后应返回滤浆槽重新过滤,饼层形成后收集的滤液为符合要求的滤液。
饼层过滤适用于处理固体含量较高的混悬液。
(2)深层过滤,过滤介质是较厚的粒状介质的床层,过滤时悬浮液中的颗粒沉积在床层内部的孔道壁面上,而不形成滤饼。
深层过滤适用于生产量大而悬浮颗粒粒径小、固含量低或是粘软的絮状物。
如自来水厂的饮水净化、合成纤维纺丝液中除去固体物质、中药生产中药液的澄清过滤等。
另外,膜过滤作为一种精密分离技术,近年来发展很快,已应用于许多行业。
膜过滤是利用膜孔隙的选择透过性进行两相分离的技术。
以膜两侧的流体压差为推动力,使溶剂、无机离子、小分子等透过膜,而截留微粒及大分子。
工业生产中悬浮液固相含量一般较高(体积分数大于1%),因此本节重点讨论滤饼过滤。
3.过滤介质过滤过程所用的多孔性介质称为过滤介质。
性能优良的过滤介质除能够达到所需分离要求外,还应具有足够的机械强度,尽可能小的流过阻力,较高的耐腐蚀性和一定的耐热性,最好表面光滑,滤饼剥离容易。
工业常用过滤介质主要有织物介质、多孔性固体介质和微孔滤膜等。
(1)织物介质是由天然或合成纤维、金属丝等编织而成的筛网、滤布,适于滤饼过滤,一般可截留的粒径5μm以上的固体微粒。
(2)多孔性固体介质是素瓷、金属或玻璃的烧结物、塑料细粉粘结而成的多孔性塑料管等,适用于含粘软性絮状悬浮颗粒或腐蚀性混悬液的过滤,一般可截留粒径1~3μm的微细粒子。
(3)粒状介质是由各种固体颗粒(砂石、木炭、石棉)或非编织纤维(玻璃棉等)堆积而成。
适用于深层过滤,如制剂用水的预处理。
(4)微孔滤膜,是由高分子材料制成的薄膜状多孔介质。
适用于精滤,可截留粒径0.01μm以上的微粒,尤其适用于滤除0.02~10μm的混悬微粒。