水果中总酸的测定
- 格式:doc
- 大小:46.50 KB
- 文档页数:2

果汁饮料中总酸含量测定的研究一、总酸的概念和意义总酸是指果汁饮料中的有机酸的总量。
主要包括柠檬酸、苹果酸、葡萄酸等有机酸。
总酸的浓度直接影响到果汁饮料的口感、风味和质量,也是果汁饮料营养品质评价的指标之一总酸含量的测定方法可以为酶法、电化学法、光度法等,各种方法各有优缺点。
在实际应用中,根据需要选择合适的方法进行测定。
二、常用的总酸测定方法1.酶法酶法是一种常用的总酸测定方法,主要通过酶类催化有机酸产生的底物和酶促反应进行测定。
比如,通过柠檬酸酶催化柠檬酸和NADH反应生成苹果酸,再通过苹果酸酶催化苹果酸和NADH反应生成乳酸,最后通过乳酸脱氢酶催化乳酸和NADH反应生成丙酮酸来测定总酸。
2.电化学法电化学法主要通过电极测定溶液中的电势变化来进行总酸测定。
常用的电化学法有电位滴定法和电位差滴定法。
这些方法的优点是简洁、高灵敏度,但是需要使用特定的电极和测定设备,操作稍显繁琐。
3.光度法光度法是通过测定溶液中反应物的吸光度来间接反映总酸浓度的方法。
比如,可以利用试剂对有机酸进行比色反应,再通过光度计测定吸收光的强度来计算总酸的浓度。
四、总酸测定方法的优缺点1.酶法的优点是测定结果可靠、操作简便,适用于大批量样品的测定。
但是,该方法的一些试剂和酶催化需要较长的反应时间和反应条件。
2.电化学法的优点是具有较高的灵敏度和准确性,适用于测定较低浓度的总酸。
但是,该方法需要特定的电极和测定设备,成本较高。
3.光度法的优点是简单、迅速,适用于大规模样品的测定,且操作简便。
但是,该方法的准确性和精度受到测定条件的影响较大。
五、研究进展和应用前景随着科学技术的不断发展和进步,对果汁饮料总酸含量测定的研究也越来越深入。
目前,有机酸的分离和定量分析方法正在不断改进,新的测定方法也在不断涌现。
未来的研究可以从以下几个方面进行:1.探索更准确的测定方法:研究者可以尝试引入新的技术,如质谱法、纳米传感器等,来提高测定方法的准确性和灵敏度。

果品总酸度的测定一、实验目的进一步掌握标准碱溶液的配制和标定方法。
学习酸碱滴定法的方法,原理与应用。
二、实验原理水果中富含有机酸,如乙酸、柠檬酸、苹果酸、酒石酸等,它们的结构简式、寓解常数及相对分子质量如下:这些有机酸可以用碱标准溶液滴定,以酚酞为指示剂。
根据所消耗的碱的浓度和体积,即可求出果晶中的总酸度。
总酸度应标明是哪种有机酸。
由于果品中的酸值较低,故应对所用去离子水做空白实验,以扣除影响。
三、仪器与试剂天平(称准至0.01g),烧杯,250mL容量瓶,过滤装置,移液管,碱式滴定管,锥形瓶。
NaOH固体(或标液),滤纸,酚酞指示剂,糊状水果样品。
四、实验步骤1.配制0.05mol/LNaOH标准溶液(参见第三章实验三)。
2.称取制成糊状的果肉约20g(称准至小数点后两位)于洁净干燥的小烧杯中,用适量的去离子水定量地将果品样洗人250mL容量瓶中,定容,棉纱,摇匀。
将滤液用干滤纸(或玻璃纤维、脱脂棉)过滤至另一洁净干燥的烧杯中(弃去最初的约5mL滤液).移取25。
00mL滤液于锥形瓶中,加1~2滴酚酞指示剂,以NaOH标准溶液滴定至溶液呈粉红色且30s内不褪色为终点,屏风,记录消耗NaOH标准溶液的体积(y)。
平行测定2―3次。
另移取25.00mL去离子水,加l~2滴酚酞指示剂,以NaOH标准溶液清定至终点,记录消耗NaOH标液的体积(V1)。
平行测定3~5次。
3.结果计算式中K――有机酸基本单元的式量,乙酸取值60,柠檬酸取值64,苹果酸取值72,酒石酸取值75,琥珀酸取值59,草酸取值45;mx――试样量,s;V――滴定果晶本身所消耗的NaOH标准溶液的体积,mL:V1――滴定蒸馏水(或去离子水)所消耗的NaOH标准溶液的体积,mL。
思考与讨论1.做空白实验的目的是什么?。

【精品】柠檬中总酸度及Vc含量的测定实验目的:1、测定柠檬汁的总酸度。
2、测定柠檬汁中维生素C的含量。
实验原理:1、总酸度的测定常见的柠檬品种中,总酸性成分以柠檬酸为主,其他酸则只是占少数。
所以,测定总酸度,通常是食品标准加以规定的酸称谓,并以柠檬酸为标准。
国家标准(GB/T 5009.158-2016)规定,以柠檬酸的质量分数计算柠檬汁中的总酸含量,也即总酸度。
2、维生素C的测定本实验采用氧化还原滴定法(Iodometric titration)来测定柠檬汁中维生素C的含量。
利用碘和碘化钾催化氧化维生素C还原Fe3+生成Fe2+的过程,来计算样品中维生素C的含量。
实验步骤:1、柠檬汁的制备将柠檬挤压成汁,并去除其中的杂质。
2、总酸度的测定取适量的柠檬汁,加入去离子水,并用磷酸钠标定溶液滴定至黄色至橙色的终点,记录所滴定的体积。
计算总酸度=(所用磷酸钠标准溶液的质量浓度×所用标准溶液体积÷样品重量)×100注意事项:溶液在操作过程中保持恒温,所有使用的仪器均需用去离子水冲洗干净,且在操作过程中尽量避免二氧化碳的吸入。
3、维生素C的测定取适量的柠檬汁,加入足量0.7%的NaOH溶液使其变为淡黄色的透明溶液,加入3%的明胶溶液,加水升至50ml,摇匀,静置放在室温下15分钟,过滤滤液。
将25ml滤液加入250ml锥形瓶中,加上足量的2%醋酸溶液,用50ml去离子水稀释,加入1g异加油醇,摇匀,于2分钟内滴加已调节好的0.02 mol/L碘标准溶液至浅黄色为止,加入淀粉溶液若干,使体系变为淡蓝色,继续滴加0.02 mol/L的碘标准溶液,直到体系变为蓝色,并维持30秒钟,记录滴加的体积,得出维生素C的含量。
计算公式:V1×C1×10×1000/1000/m=mg/100g其中,V1为所滴加的碘标准溶液体积,C1为碘标准溶液的浓度(mol/L),10为维生素C分子量,1000为滤液体积(mL),1000为样品的质量(mg),m为样品所加水的质量。

柑橘果实糖、酸、VC含量的测定方法熊庆娥(农业大学)Eleven手打第一部分测定程序及计算公式建议先通读这些方法几遍,借好仪器,想好人员分配后,再到实验室一、样品制备样品果至少10个。
擦净果皮后,用水果刀在每个果对称位置切取两块。
去皮后,用纱布包裹好果肉,挤压果汁于干燥烧杯中,总量不低于100ml。
样品液混合搅拌均匀后,可供测定可溶性固性物(TSS)、糖、酸、Vc。
二、总酸含量的测定1.用移液管将5ml果汁转入100ml三角瓶,加酚酞1—2滴,用0.1N NaOH (以标定浓度为准)滴至溶液出现粉红色不消失至。
记录滴定所消耗NaOH量。
重复3次。
2.总酸含量(g/100ml)=V:NaOH滴定用量 N:NaOH浓度(标定为准)B:被滴定样品用量(5ml) 0.064:柠檬酸折算系数Eleven补充分析:② N表示mol/L。
② 0.064的来历: 折算系数即1ml氢氧化钠溶液摩尔浓度柠檬酸的质量。
NaOH与柠檬酸的反应中,NaOH与柠檬酸的比例是1:3。
柠檬酸的分子量为192.14。
假设氢氧化钠浓度为A mol/L,即 A mol/ml。
1ml氢氧化钠溶液与柠檬酸反应,则柠檬酸用量为 A mol。
柠檬酸质量为A192.14=0.06405A。
三、Vc含量的测定1.取果汁5ml,用1%草酸稀释,定容至50ml。
即稀释10倍。
用移液管吸取稀释液5ml至50ml三角瓶,通过半微量滴定管滴入2,6D至溶液呈粉红色且30秒不退色。
记录所耗2,6D用量。
重复三次。
2. Vc含量(mg/100ml)=V: 2,6-D滴定用量 A:每毫升2,6-D相当的Vc量(mg)B:滴定所用样品量(5ml) C: 样品稀释倍数(10)Eleven分析补充:抗坏血酸在溶液中易氧化,在整个测定中,操作应迅速。
滴定开始时,染料迅速加入,直至红色不立即消失,而后逐滴加入,并不断摇动锥形瓶直至终点,整个滴定时间不宜超过2.分钟。
所有试剂配制,都需用重蒸馏。

实训一:水果总酸度的测定一、实验目的1、学会水果样品的预处理方法2、掌握用酸碱滴定法测定水果样品中总酸度的原理和方法3、学会合理指定分析项目的顺序,做到合理安排分析时间,合理处理样品。
4、能熟练纸杯实过程中所需要的标准溶液。
5、能规范记录数据并进行数据处理。
二、实验原理• 1. NaOH标准溶液的标定NaOH易吸收水分及空气中的CO2,因此,不能用直接法配制标准溶液。
需需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。
以酚酞为指示剂,当滴定至终点溶液呈浅红色,且30S不褪色时。
反应如下:•KHC8H4O4+NaOH=KNaC8H4O4+ H2O• 2.水果总酸度的测定根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞为指示剂。
当滴定至终点溶液呈浅红色,30s不褪色时,根据滴定时消耗的标准碱溶液的体积,可算出试样中的总酸度。
其反应如下:•HAc+NaOH →NaAc+H2O三、实验仪器及试剂•试剂:0.1000mol/LNaOH标准溶液、邻苯二甲酸氢钾、酚酞指示剂、无CO2的蒸馏水、水果试样(梨)•仪器:洗耳球、玻璃棒、量筒、移液管、电子天平、•水浴锅、锥形瓶、容量瓶、酸碱滴定管、烧杯、小纸片、胶头滴管、干燥的纱布、铁架台四、实验步骤•1、0.1000mol/LNaOH标准溶液的标定:(顾嘉俊王英权)•0.1000mol/lNaoH标准溶液已经配制好,待标定。
•用减量法准确称取0.4—0.45g邻苯二甲酸氢钾三份,分别放入250ml锥形瓶中,加25ml无CO2的蒸馏水溶解。
•然后加1—2d 酚酞指示剂,用NaOH溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。
•记录每次消耗NaOH溶液的体积。
•2、试样的处理:(朱方灵、陈鹏)•取梨试样500g,去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀。
移取梨试样50ml稀释定容为250ml溶液至容量瓶中,然后倒入到烧杯中在75 ~80℃的水浴上加热30分钟。


柑橘果实糖、酸、Vc 含量的测定方法熊庆娥(四川农业大学)第一部分 测定程序及计算公式一、样品制备样品果至少10个。
擦净果皮后,用水果刀在每样果对称部位切取两块。
去果皮后,用纱布包好果肉,挤压果汁于干燥烧杯中,总量不少于100ml 。
样品液混合搅拌均匀后,可供测定可溶性固形物(TSS )、糖、酸、Vc 。
二、Vc 含量的测定1. 果汁5ml ,用1%草酸稀释,定容至50ml ,即稀释10倍。
用移液管吸取稀释液5ml 至50ml 三角瓶,通过半微量滴定管滴入2,6-D ,至溶液呈粉红色30秒内不消失止。
记录所耗2,6-D (ml )。
重复滴定2~3次。
2. Vc 含量(mg/100ml )=C 100V B ⨯A⨯⨯ (1式)V :2,6-D 滴定值(ml ) A :每毫升2,6-D 相当的Vc 量(mg ) B :滴定用样品量(ml ) C :样品稀释倍数三、总酸含量的测定1. 用移液管吸取果汁5ml ,转入100ml 三角瓶,加酚酞1~2滴,用0.1N NaOH (标定浓度为准)滴至溶液出现粉红色不消失止。
记录滴定所耗NaOH 量(ml )。
重复滴定2~3次。
2. 总酸含量(g/100ml )=0.064100V N B ⨯⨯⨯ (2式)V :NaOH 滴定值(ml ) N :NaOH 当量浓度B :滴定用样品量(ml ) 0.064:柠檬酸折算系数四、糖含量的测定1. 还原糖的测定用移液管吸取果汁10ml ,转入100ml 容量瓶,加水稀释定容至刻度,摇匀后装入酸式滴定管。
用移液管分别吸取裴林液A 、B 各5ml 于200ml 三角瓶,摇匀后,加入蒸馏水约30ml ,置电炉上煮至沸腾。
继续保持溶液沸腾,并用样品液滴定至兰色大部分减退,加次甲基兰2滴,继续滴定至溶液刚转砖红色止。
记录样品液滴定值(ml),重复2~3次。
2. 转化糖的测定:用移液管吸取果汁10ml,转入100ml容量瓶,加入6N HCl5ml,置沸水浴上水解15min。

-总酸的测定(滴定法)-一、原理果汁具有酸性反应,这些反应取决于游离态的酸以及酸式盐存在的数量。
总酸度包括未解离酸的浓度和已解离酸的浓度。
酸的浓度以摩尔浓度表示时,称为总酸度。
含量用滴定法测定。
果蔬中含有各种有机酸,主要有苹果酸、柠檬酸、酒石酸、草酸……。
果蔬种类不同,含有机酸的种类和数量也不同,食品中酸的测定是根据酸碱中和的原理,即用标定的氢氧化钠溶液进行滴定。
二、材料、仪器与试剂(一)材料:桃、杏、苹果、蔬菜等(二)仪器:碱式滴定管(20ml)、容量瓶(100ml)、移液管(10ml)、烧杯(100ml)、研钵或组织捣碎机、天平、漏斗、滤纸等。
(三)试剂1.0.1mol/L氢氧化钠:称4.0g氢氧化钠定容至1000ml,然后用0.1mol/L邻苯二甲酸氢钾标定,若浓度太高可酌情稀释。
2.1%酚酞指示剂:称1.0g酚酞,加入100ml 50%的乙醇溶解。
三、操作步骤准确称取混合均匀磨碎的样品10.0g(或吸10.0ml样品液),转移到100ml 容量瓶中,加蒸馏水至刻度、摇匀。
用滤纸过滤,准确吸取滤液20ml放入100ml 三角瓶中,加入1%酚酞2滴,用标定的氢氧化钠滴定至初显粉色在0.5min内不褪色为终点,记下氢氧化钠用量,重复三次,取平均值。
四、计算V C×N×折算系数总酸度(%)=——×————————×100W V1式中:V——样品稀释总体积(ml)V1——滴定时取样液体积C——消耗氢氧化钠标准液毫升数N——氢氧化钠标准液摩尔浓度W——样品重量(g)折算系数:即不同有机酸的毫摩尔质量(g/mmol),食品中的总酸度往往根据所含酸的不同,而取其中一种主要有机酸计量。
食品中常见的有机酸以及其毫摩尔质量折算系数加下:苹果酸——0.067(苹果、梨、桃、杏、李子、番茄、莴苣)醋酸——0.060(蔬菜罐头)酒石酸——0.075(葡萄)柠檬酸——0.070(柑橘类)乳酸——0.090(鱼、肉罐头、牛奶)。

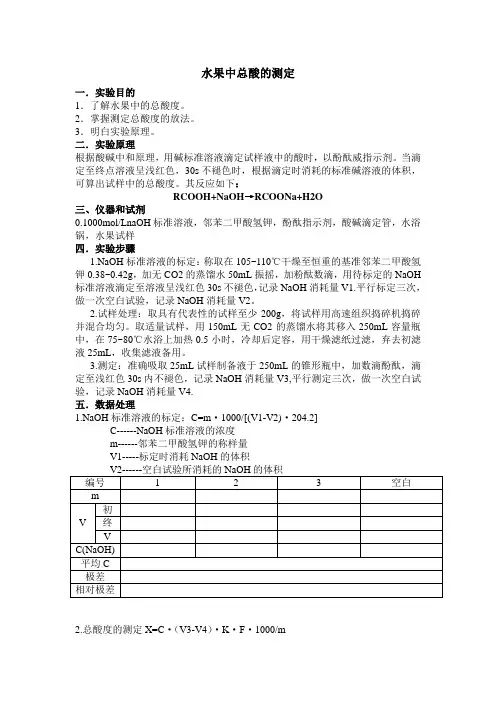
水果中总酸的测定一.实验目的1.了解水果中的总酸度。
2.掌握测定总酸度的放法。
3.明白实验原理。
二.实验原理根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。
当滴定至终点溶液呈浅红色,30s不褪色时,根据滴定时消耗的标准碱溶液的体积,可算出试样中的总酸度。
其反应如下:RCOOH+NaOH→RCOONa+H2O三、仪器和试剂0.1000mol/LnaOH标准溶液,邻苯二甲酸氢钾,酚酞指示剂,酸碱滴定管,水浴锅,水果试样四.实验步骤1.NaOH标准溶液的标定:称取在105~110℃干燥至恒重的基准邻苯二甲酸氢钾0.38~0.42g,加无CO2的蒸馏水50mL振摇,加粉酞数滴,用待标定的NaOH 标准溶液滴定至溶液呈浅红色30s不褪色,记录NaOH消耗量V1.平行标定三次,做一次空白试验,记录NaOH消耗量V2。
2.试样处理:取具有代表性的试样至少200g,将试样用高速组织捣碎机捣碎并混合均匀。
取适量试样,用150mL无CO2的蒸馏水将其移入250mL容量瓶中,在75~80℃水浴上加热0.5小时,冷却后定容,用干燥滤纸过滤,弃去初滤液25mL,收集滤液备用。
3.测定:准确吸取25mL试样制备液于250mL的锥形瓶中,加数滴酚酞,滴定至浅红色30s内不褪色,记录NaOH消耗量V3,平行测定三次,做一次空白试验,记录NaOH消耗量V4.五.数据处理1.NaOH标准溶液的标定:C=m·1000/[(V1-V2)·204.2]C------NaOH标准溶液的浓度m------邻苯二甲酸氢钾的称样量V1-----标定时消耗NaOH的体积2.总酸度的测定X=C·(V3-V4)·K·F·1000/mC------NaOH标准溶液的浓度V3------消耗NaOH的体积V4------空白试验消耗NaOH的体积F------试样的稀释倍数m-------试样质量或体积。

QS NO 2012003 实验报告专业:工业分析与检验课程:食品分析班级:XXXXXXXXXX姓名:XX学号:************实验日期:2012/4/11XXXX职业技术学院化工系实验一:果汁中总酸度及有效酸度的测定实验目的:1)掌握食品中有效酸度及总酸度的概念。
2)掌握并运用测定食品中有效酸度及总酸度的方法。
实验原理:食品中的有机弱酸在用标准碱液滴定时,被中和成盐类,用酚酞作指示剂,当地定制终点(PH8.2,指示剂显红色)时,根据滴定时小号的标准碱液的体积,可计算出样品中的总酸量,其反应式为ORCOOH+NaOH →ROOHNa+H2实验仪器及试剂:仪器:碱式滴定管、锥形瓶、烧杯、水浴锅、量筒、玻璃棒、万方式电炉、PHS-4型酸度计试剂:(1)0.1000mol/LNaOH标准滴定溶液。
配置:称取氢氧化钠110g,溶于100mL无水二氧化碳的水中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮。
取上层清夜5.4mL,用无水二氧化碳的水稀释至1000mL,摇匀。
标定:精密称取0.75g预先于105-110度烘箱中干燥至恒重的基准邻苯二甲酸氢钾,加无水二氧化碳的水50mL,振摇使其溶解,加2滴酚酞指示剂,用配置的NaOH标准溶液滴定至溶液呈红色30s不褪色,同时作空白试验。
计算:22.204)(10000⨯-⨯=v v m c式中C---氢氧化钠标准溶液的摩尔浓度,mol/L ;m --基准试剂邻苯二甲酸氢钾的质量,g ;V 0 -----空白试验所消耗用氢氧化钠标准溶液的体积,mL ;V----标定时所消耗氢氧化钠标准溶液的体积,mL ;204.22--邻苯甲酸氢钾的摩尔质量,g/L ;(2)1%酚酞乙醇溶液:称取酚酞1g 溶解于100mL 95%乙醇中。
实验步骤:(一)食品中总酸度的测定①样品制备液体样品:不含二氧化碳的样品,充分混合均匀,备用;含二氧化碳的样品,至少取200g 样品于500mL 烧杯中,置于电炉上,边搅拌边加热至微沸腾,保持2min ,称量,用煮沸过的水补充至煮沸前的质量,置于密闭玻璃容器内,备用。
实验水果、蔬菜中总酸的测定(学号:030212011031,030212011026 李欣钰和郎琳)【实验目的】1、利用标准液滴定水果蔬菜,测定不同水果蔬菜中总酸度2、练习利用滴定管滴定溶液3、练习移液管的使用4、练习pH计的使用【实验原理】1、水果和蔬菜中含有各种不同的有机酸,主要为苹果酸,柠檬酸,酒石酸,草酸等。
果树的种类不同,含有机酸的种类和数量也不同。
果汁或菜汁的酸性取决于游离态的酸或酸式盐的存在数量。
这些算都是有机弱酸,所以在测定时,有氢氧化钠标准溶液滴定就能测出酸度。
这样测得的数据是总酸度,包含了未离解酸和已离解酸的浓度。
用下式计算:总酸度(%)=(V样/W样)x(V NaOH xc NaOH x折算系数/V取样)x100式子中V样为样品稀释总体积;V取样为滴定时取样体积;W样为样品的质量。
折算系数为不同有机酸的毫摩尔质量2、食品中的总算度往往根据算韩算的不同,而取其中某种主要有机酸计量。
食品中常见的有机酸及其毫摩尔质量折算系数如下苹果酸——0.067(苹果,梨,西红柿)酒石酸——0.075(葡萄)柠檬酸——0.090(柑橘类)【仪器试剂】烧杯(100ml)(3-5只),洗耳球,移液管(25ml),容量瓶(250ml)(3只),滤纸,铁架台,滴定管夹,碱式滴定管,玻璃棒,胶头滴管,电子天平,研钵,酚酞指示剂,NaOH标准溶液(约为0.2mol/l),西红柿,葡萄,橘子(自备),塑料袋若干(自备),小刀(自备)【实验内容】1.准确称取混合均匀磨碎的样品10g2.转移到250ml容量瓶中,加纯水至刻度线,摇匀3.吸取50ml溶液于锥形瓶中,加入两滴酚酞试剂4.用NaOH标准溶液滴定溶液至淡红色,并且在30s内不退色,即到达终点。
5.记下所用的NaOH体积。
重复测定三次取平均值。
6.利用同样的方法测定剩余的两种水果或蔬菜。
并记录实验数据7.用pH计测出样品稀释液的pH8.处理实验数据,比较所测的西红柿,葡萄,橘子的总酸度的不同实验数据处理表。
水果中总酸度的测定一、目的要求:1.学会水果样品的预处理方法2.掌握用酸碱滴定法测水果样品中总酸度的原理和方法3、学会合理制定分析项目的顺序,做到合理安排分析时间,合理处理样品。
4、能熟练制备实训过程中所需要的标准溶液。
5、能规范记录数据并进行数据处理。
二、原理:1. NaOH标准溶液的标定 NaOH 易吸收水分及空气中的 CO2,因此,不能用直接法配制标准溶液。
需要先配成近似浓度的溶液,然后用邻苯二甲酸氢钾为基准物进行标定。
以酚酞为指示剂,当滴定至终点溶液呈浅红色,且 30S不褪色时。
反应如下:KHC8H4O4+NaOH=KNaC8H4O4+ H2O2.水果总酸度的测定根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。
当滴定至终点溶液呈浅红色,且 30S不褪色时,根据滴定时消耗的标准 NaOH 溶液的体积,可算出试样中的总酸度。
其反应如下:HAC+NaOH→NaAc+H2O三、所需仪器、试剂:仪器:酸碱式滴定管、锥形瓶、移液管、量筒、烧杯、容量瓶、胶头滴管、洗耳球、水浴锅、铁架台、电子天平、玻璃棒、小纸片、干燥的纱布试剂: 0.1000mol/L NaOH 溶液、邻苯二甲酸氢钾、酚酞指示剂、水果试样、无CO2的蒸馏水四、实验步骤:1. 0.1000mol/LNaOH 标准溶液的配制和标定称取固体NaOH约2g放置在500mL的烧杯中,先加入100ml溶解,再加水稀释成 500mL 溶液,混匀,放入烧杯中,待标定。
用减量法准确称取0.41~0.45g邻苯二甲酸氢钾3份,分别放入250mL锥形瓶中,加25mL 无CO2蒸馏水溶解。
然后加1~2滴酚酞指示剂,用 NaOH 标准溶液滴定至终点(至粉红色,并保持30s不褪色为终点)。
记录每次消耗 NaOH 溶液的体积。
2.试样处理:取水果试样,需去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀。
准确移取 25mL 水果试样,加100mL无CO2的蒸馏水,稀释定容为250mL溶液。
综合性、设计性实验报告(本科学生)一、实验设计方案:(三).【实验原理】:橘子中含有丰富的有机酸,主要有柠檬酸、苹果酸、烟酸等。
其中柠檬酸为主要的酸。
结构式为:,在水中的解离常数为: K a1=7.4×10-4,K a2=1.7×10-5,K a3=4.0×10-7。
由于柠檬酸相邻解离常数之间相差不大,不能满足分步滴定要求,但是最后一级解离常数并不小,且滴定突跃弱在碱性范围内,因此可以用NaOH标准溶液作滴定剂,用酚酞做指示剂,按多元酸一次进行滴定至终点溶液由无色变为微红色。
反应式为:HOOCCH2C(OH)(COOH)CH2COOH+3NaOH=NaOOCCH2C(OH)(COONa)CH2COONa+3H2O。
再根据消耗NaOH标准溶液的体积V和称取橘子的质量m计算出橘子中总算度的含量。
计算式为:总算度(g/100g)=(K(CV)NaOH×100)/(V试液/250)(其中:K=0.064)。
水果中酸的含量影响水果的色香味,而且人摄入过多的酸对身体不好,因此有必要测水果中的酸含量,而指导人们控制水果的一次摄入量。
(四).【实验内容、步骤】:1.式样预处理:取橘子试样去皮、去柄、去核,切成块状,置于搅拌机中捣碎并混匀,称取100g捣碎试样充分抽滤,将滤液在75~80℃水浴中加热30分钟,冷却后再转入容量瓶中加蒸馏水稀释为250mL备用。
2. 配制0.05mol/LNaOH标准溶液250mL: NaOH的质量m=0.05×250/1000×39.997=0.49g KHP的质量m=0.05×25/1000×204.22=0.25g 称取0.49~0.5 g的氢氧化钠固体于洁净的烧杯中,加蒸馏水溶解后,稀释至250mL。
再准确称取0.25~0.3g的KHP于3只洁净的锥形瓶中,加25mL蒸馏水溶解后,加入2~3滴酚酞指示剂,用NaOH溶液标定至终点溶液由无色变为微红,计算NaOH溶液的准确浓度。
苹果中总酸的测定
实验原理:苹果中的有机酸,用酸碱滴定,被中和生成盐类。
RCOOH+NaOH==RCOONa+H2
一、试剂:1、氢氧化钠标准溶液的配制与标定
在粗天平上称取固体氢氧化钠1克,加蒸馏水溶解并稀释至250毫升,摇匀,备用。
在分析天平上准确与105-110℃至恒重的邻苯二甲酸氢钾0.3-0.5克于250毫升的锥形瓶中,加蒸馏水100毫升溶解,加两滴酚酞指示剂,用配用的氢氧化钠标准溶液滴定至溶液呈微红色,同时做空白试验。
C(NaOH)=m/【(V-V o)*0.2042】
式中;C(NaOH)---氢氧化钠标准溶液的物质的量浓度,mol/L V o---空白试验氢氧化钠标准溶液的用量,ml
M---邻苯二甲酸氢钾的质量,g
0.2042---邻苯二甲酸氢钾的摩尔质量,Kg/mol
2、酚酞指示剂(10g/L)
二、测定方法:
将苹果洗净,取可使用部分切碎,加等量水打碎,与粗天平上称取50g,移入250毫升容量瓶中,约2/3的蒸馏水,摇匀,与75-80℃水浴中浸提30分钟,冷却至室温加水定容到刻度,摇匀,过滤。
用吸管吸取滤液50毫升于250毫升锥形瓶中加2滴酚酞指示剂,用氢氧化钠标准溶液滴定至溶液呈微红色。
三、计算:
总酸(以苹果酸计)%=C*V*0.067*20
式中:C--氢氧化钠标准溶液的物质的量浓度,mol/L
V---氢氧化钠标准溶液的用量,ml
0.067---苹果酸的系数。
四、说明:
1、平行试验结果容许差为0.5%
2、酸度包括总酸(可滴定酸度),有效酸(氢离子活度,即PH值)和挥发酸。
总酸是指所有酸性成分的总量,通常用碱液来滴定,并以样品中所含主要酸的百分数表示。
柑橘果实糖、酸、VC含量的测定方法熊庆娥(农业大学)Eleven手打第一部分测定程序及计算公式建议先通读这些方法几遍,借好仪器,想好人员分配后,再到实验室一、样品制备样品果至少10个。
擦净果皮后,用水果刀在每个果对称位置切取两块。
去皮后,用纱布包裹好果肉,挤压果汁于干燥烧杯中,总量不低于100ml。
样品液混合搅拌均匀后,可供测定可溶性固性物(TSS)、糖、酸、Vc。
二、总酸含量的测定1.用移液管将5ml果汁转入100ml三角瓶,加酚酞1—2滴,用0.1N NaOH (以标定浓度为准)滴至溶液出现粉红色不消失至。
记录滴定所消耗NaOH量。
重复3次。
2.总酸含量(g/100ml)=V:NaOH滴定用量 N:NaOH浓度(标定为准)B:被滴定样品用量(5ml) 0.064:柠檬酸折算系数Eleven补充分析:② N表示mol/L。
② 0.064的来历: 折算系数即1ml氢氧化钠溶液摩尔浓度柠檬酸的质量。
NaOH与柠檬酸的反应中,NaOH与柠檬酸的比例是1:3。
柠檬酸的分子量为192.14。
假设氢氧化钠浓度为A mol/L,即 A mol/ml。
1ml氢氧化钠溶液与柠檬酸反应,则柠檬酸用量为 A mol。
柠檬酸质量为A192.14=0.06405A。
三、Vc含量的测定1.取果汁5ml,用1%草酸稀释,定容至50ml。
即稀释10倍。
用移液管吸取稀释液5ml至50ml三角瓶,通过半微量滴定管滴入2,6D至溶液呈粉红色且30秒不退色。
记录所耗2,6D用量。
重复三次。
2. Vc含量(mg/100ml)=V: 2,6-D滴定用量 A:每毫升2,6-D相当的Vc量(mg)B:滴定所用样品量(5ml) C: 样品稀释倍数(10)Eleven分析补充:抗坏血酸在溶液中易氧化,在整个测定中,操作应迅速。
滴定开始时,染料迅速加入,直至红色不立即消失,而后逐滴加入,并不断摇动锥形瓶直至终点,整个滴定时间不宜超过2.分钟。
所有试剂配制,都需用重蒸馏。
柠檬中总酸度的测定一、实验目的1、了解水果总酸度与食物成熟程度、营养的相关性。
2、学习从水果样品预处理的方法。
3、学会用中和法直接测定酸性物质。
4、掌握水果样品中总酸量测定的原理和方法。
5、掌握强碱滴定弱酸的滴定过程,突跃范围及指示剂的选择原理。
6、进一步规范记录数据并进行数据处理。
二、实验原理水果和蔬菜中含有各种不同的有机酸,主要为苹果酸、柠檬酸、酒石酸、草酸等。
果树的种类不同,含有机酸的种类和数量也不同。
果汁或菜汁的酸性取决于游离态的酸或酸式盐的存在数量。
这些酸都是有机弱酸,所以在测定时,用氢氧化钠标准溶液滴定就能测出酸度。
这样测得的数据是总酸度,包含了未离解酸和已离解酸的浓度。
柠檬富含柠檬酸、维生素C、苹果酸、高量钠元素和低量钾元素,是最有药用价值的水果之一。
其主要成分是柠檬酸和维生素C。
柠檬酸又名枸橼酸,摩尔质量为92.14 g/mol,无色晶体,常含一分子结晶水,易溶于水。
柠檬酸是三元弱酸,故有很强的酸味,各级解离常数分别为:Ka1 = 7.4×10-4,Ka2 = 1.7×10-5,Ka3 = 4.0×10-7。
由于柠檬酸各相邻解离常数之间相差不大,故不能分步滴定,但由于最后一级解离常数并不小,因此可以用NaOH标准溶液作滴定剂,按多元酸一次进行滴定。
用碱标准溶液滴定试样液中的柠檬酸时,以酚酞为指示剂。
当滴定至溶液由无色变为微红色且30 s不褪色时,即达到终点。
反应式为:CH2COOHC-COOH HO-CH2COOH + 3NaOHCH2COONaC-COONaHO-CH2COONa+ 3H2O根据滴定时消耗的标准NaOH溶液积,可算出试样中柠檬酸的总酸度。
三、实验仪器与材料、试剂1、材料、试剂2、仪器:四、实验内容1、NaOH溶液的配制(0.01 M)用50 mL小烧杯在台秤上迅速称取0.1 g NaOH固体,先加入少量蒸馏水溶解,冷却,再稀释到250 mL,倒入干净的细口试剂瓶中,用橡皮塞塞紧,以防NaOH溶液吸收空气中的CO2而改变浓度,贴上标签,备用。
水果中总酸的测定
一.实验目的
1.了解水果中的总酸度。
2.掌握测定总酸度的放法。
3.明白实验原理。
二.实验原理
根据酸碱中和原理,用碱标准溶液滴定试样液中的酸时,以酚酞威指示剂。
当滴定至终点溶液呈浅红色,30s不褪色时,根据滴定时消耗的标准碱溶液的体积,可算出试样中的总酸度。
其反应如下:
RCOOH+NaOH→RCOONa+H2O
三、仪器和试剂
0.1000mol/LnaOH标准溶液,邻苯二甲酸氢钾,酚酞指示剂,酸碱滴定管,水浴锅,水果试样
四.实验步骤
1.NaOH标准溶液的标定:称取在105~110℃干燥至恒重的基准邻苯二甲酸氢钾0.38~0.42g,加无CO2的蒸馏水50mL振摇,加粉酞数滴,用待标定的NaOH 标准溶液滴定至溶液呈浅红色30s不褪色,记录NaOH消耗量V1.平行标定三次,做一次空白试验,记录NaOH消耗量V2。
2.试样处理:取具有代表性的试样至少200g,将试样用高速组织捣碎机捣碎并混合均匀。
取适量试样,用150mL无CO2的蒸馏水将其移入250mL容量瓶中,在75~80℃水浴上加热0.5小时,冷却后定容,用干燥滤纸过滤,弃去初滤液25mL,收集滤液备用。
3.测定:准确吸取25mL试样制备液于250mL的锥形瓶中,加数滴酚酞,滴定至浅红色30s内不褪色,记录NaOH消耗量V3,平行测定三次,做一次空白试验,记录NaOH消耗量V
4.
五.数据处理
1.NaOH标准溶液的标定:C=m·1000/[(V1-V2)·204.2]
C------NaOH标准溶液的浓度
m------邻苯二甲酸氢钾的称样量
V1-----标定时消耗NaOH的体积
2.总酸度的测定X=C·(V3-V4)·K·F·1000/m
C------NaOH标准溶液的浓度
V3------消耗NaOH的体积
V4------空白试验消耗NaOH的体积F------试样的稀释倍数
m-------试样质量或体积。