十八章非金属元素小结
- 格式:ppt
- 大小:958.50 KB
- 文档页数:64

高中化学知识点总结:非金属元素及其化合物(一)非金属元素概论1.非金属元素在周期表中的位置在目前已知的112种元素中,非金属元素有22种,除H外非金属元素都位于周期表的右上方(H在左上方)。
F是非金属性最强的元素。
2.非金属元素的原子结构特征及化合价(1)与同周期的金属原子相比,最外层电子数较多,次外层都是饱和结构(2、8或18电子结构)。
(2)与同周期的金属原子相比较,非金属元素原子核电荷数多,原子半径小,化学反应中易得到电子,表现氧化性。
(3)最高正价等于主族序数(O、F无+6、+7价)‘对应负价以绝对值等于8–主族序数。
如S、N、C1等还呈现变价。
3.非金属单质(1)组成与同素异形体非金属单质中,有单原子分子的He、Ne、Ar等稀有气体;双原子分子的H2、O2、Cl2、H2、Br2等,多原子分子的P4、S8、C60、O3等原子晶体的金刚石,晶体硅等。
同一元素形成的不同单质常见的有O2、O3;红磷、白磷;金刚石、石墨等。
(2)聚集状态及晶体类型常温下有气态(H2、O2、Cl2、N2…),液态(Br2)、固态(I2、磷、碳、硅…)。
常温下是气钵,液态的非金属单质及部分固体单质,固态时是分子晶体,少量的像硅、金刚石为原子晶体,石墨“混合型”晶体。
4.非金属的氢化物(1)非金属氢化物的结构特点①IVA—RH4正四面体结构,非极性分子;VA—RH3三角锥形,极性分子;VIA—H2R为“V”型,极性分子;VIIA—HR直线型,极性分子。
②固态时均为分子晶体,熔沸点较低,常温下H2O是液体,其余都是气体。
(2)非金属气态氢化物的稳定性一般的,非金属元素的非金属性越强,生成的气态氢化物越稳定。
因此,气态氢化物的稳定性是非金属性强弱的重要标志之一。
(3)非金属氢化物具有一定的还原性如:NH3:H2S可被O2氧化HBr、HI可被Cl2、浓H2 SO4氧化等等。
5.最高价氧化物对应水化物(含氧酸)的组成和酸性。


第十八章非金属元素小结预习提纲第18章非金属元素小结第一节非金属单质的结构和性质要求:1、了解非金属单质中的共价键数为8-N(H2为2-N)。
2、第2周期中的O、N为什么易形成多重键?3、第3、4周期的S、Se、P、As等则易形成单键?4、非金属单质按其结构和性质大致可分为哪三类?5、掌握单质Cl2、S、P、Si和B与NaOH反应的方程式。
一、非金属单质的结构和物理性质1. 小分子单质(单原子分子和双原子分子)分子晶体,熔点、沸点都很低。
2. 多原子分子单质(P4、As4、S8 )分子晶体,熔沸点稍高于第一类单质。
3. 大分子单质(金刚石、晶态硅和单质硼)包括过渡型晶体,如石墨、黑磷、灰砷.原子晶体,熔沸点极高,难挥发。
二、非金属单质的化学反应1.活波非金属与金属元素反应2.非金属元素之间反应3.大部分非金属单质不与水反应4.非金属单质一般不与非氧化酸反应,但可与浓硝酸、浓硫酸及王水反应.5.大部分非金属单质可和碱反应,有时是歧化反应第二节分子型氢化物同一周期分子型氢化物从左到右稳定性增强,还原性减弱,水溶液酸性增强同一族分子型氢化物从上到下稳定性减弱,还原性增强,水溶液酸性增强分子型氢化物的热稳定性:与组成氢化物的非金属元素的电负性有关, 非金属与氢的电负性相差越大, 所生成的氢化物越稳定。
分子型氢化物的热稳定性, 在同一周期中从左到右依次增加; 在同一族中, 从上到下依次减小。
分子型氢化物的标准生成自由能或标准生成焓越负,氢化物越稳定。
还原性(An-失电子的能力):除HF外,其它分子型氢化物都有还原性,其变化规律与稳定性的增减的规律相反,稳定性大的氢化物,还原性小。
分子型氢化物的还原性,在同一周期中从左到右依次减小;在同一族中,从上到下依次增加。
因为在周期表中,从右向左,自上而下,元素半径增大,电负性减小,失电子的能力依上述方向递增,所以氢化物的还原性也按此方向增强。
水溶液酸碱性和无氧酸的强度:分子型氢化物在水溶液中的酸碱性和该氢化物在水中给出或接受质子能力的相对强弱有关。

![习题解_非金属元素小结[1]](https://uimg.taocdn.com/30e8c43a31126edb6f1a10ed.webp)
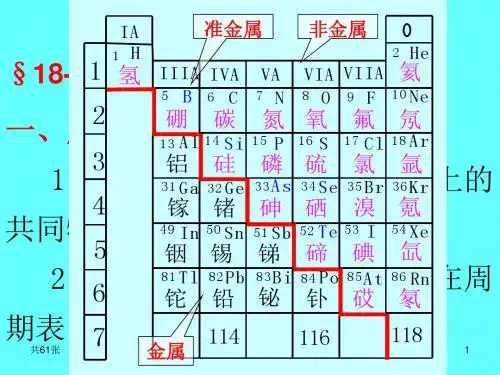
第十八章非金属元素小结18-1 按周期表位置,绘出非金属元素单质的结构图,并分析它们在结构上有哪些特点和变化规律。
解:非金属元素的晶体结构大多数是分子晶体,也有少数原子晶体和过渡型层状晶体。
在分子晶体中又可分为两类:一类是以小分子为结构单元,如单原子分子的稀有气体和双原子分子的H2,卤素(X2),O2、N2等;另一类是以多原子分子为结构单元,如S8、Se8、P4等。
它们在周期表中的位置如图所示:从结构图可知:位于非金属—金属交界线附近的元素,其单质的结构比较复杂,其特点是增大配位数,接近金属的结构,如B—C—Si—As—Te,都是以共价键结合成的无限分子,不论是简单或复杂结构,在单质的结构中非金属元素明显地表现出它们各自固有的共价特征。
18-2 为什么氟和其它卤素不同,没有多种可变的正氧化态?解:因为氟原子价层没有空的轨道,基态只有一个未成对电子,只能形成一个共价单键;再由于氟在所有元素中电负性最大,因此,没有多种可变的正氧化态。
18-3 小结P区元素的原子半径、电离能、电子亲合能和电负性,在按周期表递变规律的同时,还有哪些反常之处?说明其原因。
解:原子半径:r Ga< r Al ,因为Ga是第四周期元素,从Al→Ga,次外层第一次开始出现10个d电子,由于d电子对核电荷屏蔽效应小,导致有效核荷Z*比没有d电子时要大,对最外层电子引力增大,故Ga的半径反常地比Al的小。
电离能:(1)ⅤA族N、P、As的IE1分别大于ⅥA族同周期O、S、Se的IE1,因为前三者价电子层均为半满。
(2)ⅢA第四周期Ga的IE1略大于第三周期的Al,原因和原子半径反常同理。
电子亲合能:(1)第二周期N、O、F的电子亲合能均分别小于第三周期同族的P、S、Cl。
因为第二周期元素原子半径特别小,电子对间排斥作用大。
(2)同一周期从左到右,稀有气体的电子亲合能最小,因为稀有气体价电子层全满。
电负性:按阿莱—罗周电负性标度,第四周期的Ga、Ge、As、Se的x AR均分别比第三周期的Al、Si、P、S要大,其原因和第四周期P区元素Z*和r变化的反常同理。

非金属元素小结在所有的化学元素中,非金属元素占22中,它们被包括在单质、氧化物、酸、盐及配合物中。
在金属与非金属的分界线上,有B、Si、As、Se、Te五种准金属,也是常见的半导体材料。
一、非金属单质的结构和性质1.结构和成键除H、He的价电子层上有1、2个s电子,He以外的希有气体的价电子层结构(除He外)为ns2np6外,III A~VII A族的价电子层结构为ns2np1~ns2np5。
得电子达到8e- 结构的倾向逐渐增强(除B的成键不满8e--)。
并且形成共价键;若以N代表非金属元素在周期表中的族数,则这类元素在单质中的共价键数为8-N(B除外)、H为2-N.希有气体的共价数等于0(8-8),其结构单元为单原子分子,这些单原子分子借范德华引力结合成分子型晶体。
VII A原子的共价数等于1(8-7),每两个原子以一个共价键形成双原子分子,然后分子间借范德华力形成分子晶体。
H的共价数等于1(2-1),也属同一类。
VI A的O、S、Se等共价数为2(8-6)。
V A的N、P、As等的共价数为3(8-5)。
这两族中的N、O处于第二周期,内层只有1s电子,每两个原子之间除了形成σ键以外,还可以形成p-pπ键,所以,它们的单质为重键组成的双原子分子;第三、四周期的非金属元素如S、Se、P、As等,则因内层电子较多,最外层的p电子云重叠形成p-p π键比较困难,而倾向于形成尽可能多的σ键,所以它们的单质往往是一些原子以共价键形成的多原子分子。
如S8、Se8、P4、及As4等,然后这些分子形成分子型晶体。
上述非金属元素是形成具有多重键的双原子分子还是形成只有σ单键的多原子分子?这主要取决于形成多重键或形成σ单键的键焓的大小。
如果△b H0(重键)〉2△b H0(单键),则形成具有重键的双原子分子(如O2,N2);否则,形成只有σ单键的多原子分子(如S8、Se8、P4、As4等)IV A的共价数等于4(8-4)。

高一上学期非金属元素及其化合物重要化学方程式小结1.F2 + H2=2HF (冷暗处爆炸) Cl2 +H2点燃2HCl (光照或点燃)注意:氢气在氯气中燃烧时呈苍白色火焰.硫单质与氢气的化合反应:2.Cl2 +2Na点燃2NaCl(火焰呈黄色,白烟) Cl2+Cu点燃CuCl2(棕色的烟)3Cl2 +2Fe点燃2FeCl3(棕色的烟)3.Cl2+2NaBr=2NaCl+Br2 Cl2 +2KI =2KCl+I2(此反应可用于氯气的检验)4.2O2 +3Fe 点燃Fe3O4 2Fe+3Br2=2FeBr3 Fe+I2△FeI2Fe+S △2Cu+ S△Cu2S 2Na+S=Na2S(研磨或加热)5.S+O2点燃SO2 N2+O2=2NO(放电)6.2C+O2(少量)点燃2CO C+O2(足量)点燃CO2 C+CO2高温2CO7.Cl2+H2O=HCl+HClO 2F2 +2H2O=4HF+O28.Cl2+2NaOH=NaCl+NaClO+H2O9.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O(漂粉精的主要成分与有效成分)10.4HCl(浓)+MnO2△MnCl2+Cl2↑+2H2O(实验室制取氯气的反应原理)11.注意工业上氨的催化氧化制硝酸的反应原理4NH3+5O2催化剂△4NO+6H2O2NO+O2=2NO2(NO是无色气体而NO2是红棕色气体)3NO2+H2O=2HNO3+NO12.NH3+HCl=NH4Cl(白烟) NH3+HNO3=NH4NO3(白烟) 2NH3+H2SO4=(NH4)2SO413.工业合成SO3:2SO2+O2催化剂加热2SO3。
14.工业上合成硫酸的原理:⑴工业上制取SO2有两种方法:一是用FeS2;另一种用硫磺。
⑵SO2催化氧制取SO3:2SO2+O2催化剂加热2SO3⑶溶于水制得硫酸SO3+H2O=H2SO415.2SO2+O2+2H2O=2H2SO4(这是SO2在大气中缓慢发生的环境化学反应)16.SO2使氯水褪色:SO2+Cl2+2H2O=H2SO4+2HCl注:SO2能使氯水、溴水、碘水褪色,显示的是SO2的还原性,而不是漂白性17.2CO+O2点燃2CO2 CO+CuO △Cu+CO218.工业上炼铁的反应原理3CO+Fe2O3△219.SO2+H2O H2SO3 CO2+H2O H2CO320.SO3+H2O=H2SO4 SO3+CaO=CaSO4 SO3 +Na2O=Na2SO4 CO2 +Na2O=Na2CO321.SO3+Ca(OH)2=CaSO4+H2O SO2+Ca(OH)2=CaSO3↓+H2O注:不能用澄清石灰水鉴别SO2和CO2,可用品红、溴水、酸性高锰酸钾溶液鉴别。


第18章非金属元素小结18-1 略18-2为什么氟和其他卤素不同,没有多种可变的正氧化态?解:因为F是电负性最大的元素,在形成化合物时,电子云总是偏向F,而且F处于第二周期,没有空d轨道参与成键,所以,和其他卤素不同,没有多种可变的正氧化态。
18-3 小结p区元素的原子半径、电离能、电子亲和能和电负性,在按周期性递变规律的同时,还有哪些反常之处?说明其原因。
解:p区元素的原子半径、电离能、电子亲和能和电负性,对同一周期,一般是自左向右原子半径依次减小,电离能依次增大,电子亲和能依次增大,电负性依次增大。
对于同一族,一般是从上到下原子半径依次增大,电离能依次减小,电子亲和能依次减小,电负性依次减小。
但第V A族的N、P、As等的第一电离能和电子亲和能出现反常,第一电离能比同周期VIA族的O、S、Se大,电子亲和能比同周期IV A族的C、Si、Ge小,这是由于V A族元素的外层p轨道处于半充满,结构稳定,不易失去电子,也不易接受电子。
另外,F的电子亲和能要小于Cl,O的电子亲和能小于S,N的电子亲和能小于P等,这是由于第二周期p区元素的原子半径太小,电子云密度大,电子之间排斥力很强,以致当加合一个外来电子形成负离子时,因排斥力大使放出的能量减小,导致上述反常结果。
18-4 概括非金属元素的氢化物有哪些共性?解:非金属元素的氢化物都是以共价键结合的分子型氢化物,在通常状况下为气体或挥发性液体,都能与氧、卤素、氧化态高的金属离子以及一些含氧酸盐等氧化剂作用。
18-5 已知下列数据(298K):△f G mӨ[H2S(aq)]= -27.9 kJ·mol-1;△f G mӨ[S2-(aq)]= 85.8 kJ·mol-1;△f G mӨ[H2Se(aq)] = 22.2 kJ·mol-1;△f G mӨ[Se2-(aq)] = 129.3 kJ·mol-1试计算下列反应在298K时的△r G mӨ和平衡常数K,并比较两者中哪一个酸性较强?(1) H2S(aq) -→ 2H+(aq) + S2-(aq)(2) H2Se(aq) -→2H+(aq) + Se2-(aq)解:(1) H2S(aq) -→ 2H+(aq) + S2-(aq)298K △r G1Ө= △f G mӨ[S2-(aq)]-△f G mӨ[H2S(aq)]= 85.8-(-27.9) = 113.7kJ·mol-1由△r G1Ө = - RTlnK1Ө求得:K1Ө = 1.17×10-20(2) H2Se(aq) -→2H+(aq) + Se2-(aq)298K △r G2Ө= △f G mӨ[Se2-(aq)]-△f G mӨ[H2Se(aq)]= 129.3-22.2) = 107.1kJ·mol-1由△r G2Ө = - RTlnK2Ө求得:K2Ө = 1.68×10-19通过(1)、(2)的计算结果可知:H2Se的酸性比H2S的酸性强。