第二章 晶体结构缺陷3
- 格式:ppt
- 大小:1.99 MB
- 文档页数:40



第二章、晶体结构缺陷1缺陷的概念2、热缺陷(弗伦克尔缺陷、肖特基缺陷)热缺陷是一种本征缺陷、高于0K就存在,热缺陷浓度的计算影响热缺陷浓度的因数:温度和热缺陷形成能(晶体结构)弗伦克尔缺陷肖特基缺陷3、杂质缺陷、固溶体4、非化学计量化合物结构缺陷(半导体)种类、形成条件、缺陷的计算等5、连续置换型固溶体的形成条件6、影响形成间隙型固溶体的因素7、组分缺陷(补偿缺陷):不等价离子取代形成条件、特点(浓度取决于掺杂量和固溶度)缺陷浓度的计算、与热缺陷的比较幻灯片68、缺陷反应方程和固溶式9、固溶体的研究与计算写出缺陷反应方程T固溶式、算出晶胞的体积和重量T理论密度(间隙型、置换型)T和实测密度比较10、位错概念刃位错:滑移方向与位错线垂直,伯格斯矢量b与位错线垂直螺位错:滑移方向与位错线平行,伯格斯矢量b与位错线平行混合位错:滑移方向与位错线既不平行,又不垂直。
幻灯片7第三章、非晶态固体1熔体的结构:不同聚合程度的各种聚合物的混合物硅酸盐熔体的粘度与组成的关系2、非晶态物质的特点3、玻璃的通性4、Tg、Tf ,相对应的粘度和特点5、网络形成体、网络改变(变性)体、网络中间体玻璃形成的结晶化学观点:键强,键能6、玻璃形成的动力学条件(相变),3T图7、玻璃的结构学说(二种玻璃结构学说的共同之处和不同之处)8、玻璃的结构参数Z可根据玻璃类型定,先计算R,再计算X、Y 注意网络中间体在其中的作用。
9、硅酸盐晶体与硅酸盐玻璃的区别10、硼的反常现象幻灯片8第四章、表面与界面1表面能和表面张力,表面的特征2、润湿的概念、定义、计算;槽角、二面角的计算改善润湿的方法:去除表面吸附膜(提高固体表面能)、改变表面粗糙度、降低固液界面能3、表面粗糙度对润湿的影响4、吸附膜对润湿的影响5、弯曲表面的效应(开尔文公式的应用)6、界面的分类与特点7、多晶体组织8、粘土荷电的原因,阳离子交换序9、粘土与水的作用,电动电位及对泥浆性能的影响流动性,稳定性,悬浮性,触变性,可塑性10、瘠性料的悬浮与塑化泥浆发生触变的原因,改善方法幻灯片9第五章、相平衡1、相律以及相图中的一些基本概念相、独立组分、自由度等2、水型物质相图的特点(固液界线的斜率为负)3、单元系统相图中可逆与不可逆多晶转变的特点4、S iO2相图中的多晶转变(重建型转变、位移型转变)5、一致熔化合物和不一致熔化合物的特点6、形成连续固溶体的二元相图的特点(没有二元无变量点)7、相图应用幻灯片108、界线、连线的概念,以及他们的关系9、等含量规则、等比例规则、背向规则、杠杆规则、连线规则、切线规则、重心规则。





第⼆章晶体结构与晶体缺陷2-1 (a )MgO 具有NaCl 结构。
根据O 2-半径为0.140nm 和Mg 2+半径为0.072nm ,计算球状离⼦所占有的空间分数(堆积系数)。
(b )计算MgO 的密度。
解:(a )MgO 具有NaCl 型结构,即属⾯⼼⽴⽅,每个晶胞中含有4个Mg 2+和4个O 2-,故Mg 所占有体积为:2233MgO Mg O 3344()344(0.0720.140)30.0522nm V R R ππ+-++===因为Mg 2+和O 2-离⼦在⾯⼼⽴⽅的棱边上接触:22Mg O 2()20.0720.1400.424nm a R R +-++==()=()堆积系数=%=)(=5.68424.00522.033MgOaV(b )37233)10424.0(1002.6)0.163.24(4·0MgO -+?==a N Mn D =3.51g/cm 32-2 Si 和Al 原⼦的相对质量⾮常接近(分别为28.09和26.98),但SiO 2和Al 2O 3的密度相差很⼤(分别为2.65g/cm 3和3.96g/cm 3)。
试计算SiO 2和Al 2O 3的堆积密度,并⽤晶体结构及鲍林规则说明密度相差⼤的原因。
解:⾸先计算SiO 2堆积系数。
每cm 3中含SiO 2分⼦数为:32232234322323222232.65SiO /cm 2.6410/cm(28.0932.0)/(6.0310)Si /cm 2.6410/cm O /cm 2.64102 5.2810/cm +-?+==个=个==个每cm 3中Si 4+和O 2-所占体积为:2-32273Si432273O 4/cm 2.6410(0.02610)30.001954/cm 5.2810(0.13810)30.5809V V ππ-+-====Si 2O 3晶体中离⼦堆积系数=000195+0.5809=0.5829或58.29% Al 2O 3堆积系数计算如下:322323233322223232222332273Al 32273O 32 3.96Al O /cm 2.3410/cm101.96/6.0310Al /cm 2.34102 4.6810/cm O /cm 2.341037.0210/cm 4V /cm 4.6810(0.05310)0.029234V /cm 7.0210(0.1410)0.80703ππ+---+-==个==个==个====Al 2O 3中离⼦堆积系数=0.0292+0.8070=0.8362或83.62%计算时Si 4R +=0.026nmO 2R -=0.138nm (四配位) Al 3R +=0.053nm2O R -=0.14nm (六配位)由于Al 2O 3离⼦堆积系数83.62%⼤于SiO 2晶体总离⼦堆积系数,故Al 2O 3密度⼤于SiO 2。

第二章 晶体结构与晶体中的缺陷1、证明等径圆球面心立方最密堆积的空隙率为25.9%。
解:设球半径为a ,则球的体积为4/3πa 3,求的z=4,则球的总体积(晶胞)4×4/3πa 3,立方体晶胞体积:33216)22(a a =,空间利用率=球所占体积/空间体积=74.1%,空隙率=1-74.1%=25.9%。
2、金属镁原子作六方密堆积,测得它的密度为1.74克/厘米3,求它的晶胞体积。
解:ρ=m/V =1.74g/cm 3,V=1.37×10-22。
3、 根据半径比关系,说明下列离子与O 2-配位时的配位数各是多少? 解:Si 4+ 4; K + 12; Al 3+ 6; Mg 2+ 6。
4、一个面心立方紧密堆积的金属晶体,其原子量为M ,密度是8.94g/cm 3。
试计算其晶格常数和原子间距。
解:根据密度定义,晶格常数)(0906.0)(10906.094.810023.6/(43/13/183230nm M cm M M a =⨯=⨯⨯=- 原子间距= )(0641.02/0906.0)4/2(223/13/1nm M M a r ==⨯=5、 试根据原子半径R 计算面心立方晶胞、六方晶胞、体心立方晶胞的体积。
解:面心立方晶胞:3330216)22(R R a V ===六方晶胞(1/3):3220282/3)23/8()2(2/3R R R c a V =•••=•= 体心立方晶胞:333033/64)3/4(R R a V ===6、MgO 具有NaCl 结构。
根据O 2-半径为0.140nm 和Mg 2+半径为0.072nm ,计算球状离子所占据的体积分数和计算MgO 的密度。
并说明为什么其体积分数小于74.05%?解:在MgO 晶体中,正负离子直接相邻,a 0=2(r ++r -)=0.424(nm)体积分数=4×(4π/3)×(0.143+0.0723)/0.4243=68.52%密度=4×(24.3+16)/[6.023×1023×(0.424×10-7)3]=3.5112(g/cm 3)MgO 体积分数小于74.05%,原因在于r +/r -=0.072/0.14=0.4235>0.414,正负离子紧密接触,而负离子之间不直接接触,即正离子将负离子形成的八面体空隙撑开了,负离子不再是紧密堆积,所以其体积分数小于等径球体紧密堆积的体积分数74.05%。

第二章晶体结构与晶体中的缺陷内容提要:通过讨论有代表性的氧化物、化合物和硅酸盐晶体结构,用以掌握与本专业有关的各种晶体结构类型。
介绍了实际晶体中点缺陷分类;缺陷符号和反应平衡。
固熔体分类和各类固熔体、非化学计量化学化合物的形成条件。
简述了刃位错和螺位错。
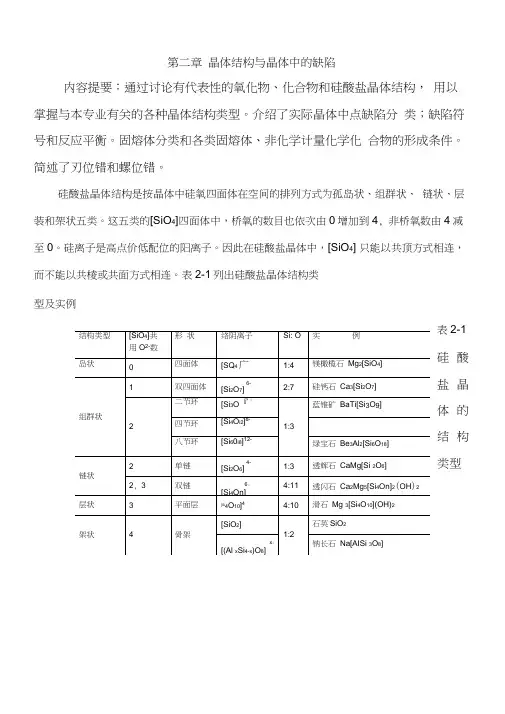
硅酸盐晶体结构是按晶体中硅氧四面体在空间的排列方式为孤岛状、组群状、链状、层装和架状五类。
这五类的[SiO4]四面体中,桥氧的数目也依次由0增加到4, 非桥氧数由4减至0。
硅离子是高点价低配位的阳离子。
因此在硅酸盐晶体中,[SiO4] 只能以共顶方式相连,而不能以共棱或共面方式相连。
表2-1列出硅酸盐晶体结构类型及实例表2-1 硅酸盐晶体的结构类型真实晶体在高于0K的任何温度下,都或多或少地存在着对理想晶体结构的偏离,即存在着结构缺陷。
晶体中的结构缺陷有点缺陷、线缺陷、面缺陷和复合缺陷之分,在无机材料中最基本和最重要的是点缺陷。
点缺陷根据产生缺陷的原因分类,可分为下列三类:(1)热缺陷(又称本征缺陷)热缺陷有弗仑克儿缺陷和肖特基缺陷两种基本形式。
弗仑克儿缺陷是指当晶格热震动时,一些能量足够大的原子离开平衡位置而挤到晶格点的间隙中,形成间隙原子,而原来位置上形成空位,这种缺陷称为弗仑克儿缺陷。
肖特基缺陷是指如果正常格点上原子,热起伏后获得能量离开平衡位置,跃迁到晶体的表面,而在原正常格点上留下空位,这种缺陷称为肖特基缺陷。
(2)杂质缺陷(非本征缺陷)(3)非化学计量化学化合物为了便于讨论缺陷反应,目前广泛采用克罗格-明克(Kroger-Vink)的点缺陷符号(见表2-2)。
表2-2 Kroger-Vink 缺陷符号(以MTX2-为例)缺陷反应方程式书写规则:(1)位置关系。
(2)质量平衡。
(3)电荷守恒。
热缺陷平衡浓度n/N :n/N二exp(- : G t/2kT)其中n——TK时形成n个孤立空位;G t――热缺陷形成自由焓;h――波儿兹曼常数。
第二章晶体结构【例2-1】计算MgO和GaAs晶体中离子键成分的多少。
【解】查元素电负性数据得,则,,,MgO离子键%=GaAs离子键%=由此可见,MgO晶体的化学键以离子键为主,而GaAs则是典型的共价键晶体。
【提示】除了以离子键、共价键结合为主的混合键晶体外,还有以共价键、分子间键结合为主的混合键晶体。
且两种类型的键独立地存在。
如,大多数气体分子以共价键结合,在低温下形成的晶体则依靠分子间键结合在一起。
石墨的层状单元内共价结合,层间则类似于分子间键。
正是由于结合键的性质不同,才形成了材料结构和性质等方面的差异。
从而也满足了工程方面的不同需要。
【例2-2】 NaCl和MgO晶体同属于NaCl型结构,但MgO的熔点为2800℃, NaC1仅为80l℃,请通过晶格能计算说明这种差别的原因。
【解】根据:晶格能(1)NaCl晶体:N0=6.023×1023 个/mol,A=1.7476,z1=z2=1,e=1.6×10-19 库仑,,r0===0.110+0.172=0.282nm=2.82×10-10 m,m/F,计算,得:EL=752.48 kJ/mol (2)MgO晶体:N0=6.023×1023 个/mol,A=1.7476,z1=z2=2,e=1.6×10-19库仑,r0==0.080+0.132=0.212 nm=2.12×10-10 m,m/F,计算,得:EL=3922.06 kJ/mol则:MgO晶体的晶格能远大于NaC1晶体的晶格能,即相应MgO的熔点也远高于NaC1的熔点。
【例2-3】根据最紧密堆积原理,空间利用率越高,结构越稳定,但是金刚石的空间利用率很低,只有34.01%,为什么它也很稳定?【解】最紧密堆积的原理只适用于离子晶体,而金刚石为原子晶体,由于C-C共价键很强,且晶体是在高温和极大的静压力下结晶形成,因而熔点高,硬度达,很稳定。
56第二章 晶体结构缺陷我们在讨论晶体结构时,是将晶体看成无限大,并且构成晶体的每个粒子(原子、分子或离子)都是在自己应有的位置上,这样的理想结构中,每个结点上都有相应的粒子,没有空着的结点,也没有多余的粒子,非常规则地呈周期性排列。
实际晶体是这样的吗?测试表明,与理想晶体相比,实际晶体中会有正常位置空着或空隙位置填进一个额外质点,或杂质进入晶体结构中等等不正常情况,热力学计算表明,这些结构中对理想晶体偏离的晶体才是稳定的,而理想晶体实际上是不存在的。
结构上对理想晶体的偏移被称为晶体缺陷。
实际晶体或多或少地存在着缺陷,这些缺陷的存在自然会对晶体的性质产生或大或小的影响。
晶体缺陷不仅会影响晶体的物理和化学性质,而且还会影响发生在晶体中的过程,如扩散、烧结、化学反应性等。
因而掌握晶体缺陷的知识是掌握材料科学的基础。
晶体的结构缺陷主要类型如表2—1所示。
这些缺陷类型,在无机非金属材料中最基本和最重要的是点缺陷,也是本章的重点。
表2—1 晶体结构缺陷的主要类型2.1 点缺陷研究晶体的缺陷,就是要讨论缺陷的产生、缺陷类型、浓度大小及对各种性质的影响。
60年代,F .A .Kroger 和H .J .Vink 建立了比较完整的缺陷研究理论——缺陷化学理论,主要用于研究晶体内的点缺陷。
点缺陷是一种热力学可逆缺陷,即它在晶体中的浓度是热力学参数(温度、压力等)的函数,因此可以用化学热力学的方法来研究晶体中点缺陷的平衡问题,这就是缺陷化学的理论基础。
点缺陷理论的适用范围有一定限度,当缺陷浓度超过某一临界值(大约在0.1原子%左右)时,由于缺陷的相互作用,会导致广泛缺陷(缺陷簇等)的生成,甚至会形成超结构和分离的中间相。
但大多数情况下,对许多无机晶体,即使在高温下点缺陷的浓度也不会超过上述极限。
缺陷化学的基本假设:将晶体看作稀溶液,将缺陷看成溶质,用热力学的方法研究各种缺陷在一定条件下的平衡。
也就是将缺陷看作是一种化学物质,它们可以参与化学反应——准化学反应,一定条件下,这种反应达到平衡状态。
缺陷种类名称点缺陷瞬变缺陷声子电子缺陷电子、空穴原子缺陷空位填隙原子取代原子缔合中心广泛缺陷缺陷簇切变结构块结构线缺陷位错面缺陷晶体表面晶粒晶界体缺陷孔洞和包裹物第二章晶体结构缺陷我们在讨论晶体结构时,是将晶体看成无限大,并且构成晶体的每个粒子(原子、分子或离子)都是在自己应有的位置上,这样的理想结构中,每个结点上都有相应的粒子,没有空着的结点,也没有多余的粒子,非常规则地呈周期性排列。
实际晶体是这样的吗?测试表明,与理想晶体相比,实际晶体中会有正常位置空着或空隙位置填进一个额外质点,或杂质进入晶体结构中等等不正常情况,热力学计算表明,这些结构中对理想晶体偏离的晶体才是稳定的,而理想晶体实际上是不存在的。
结构上对理想晶体的偏移被称为晶体缺陷。
实际晶体或多或少地存在着缺陷,这些缺陷的存在自然会对晶体的性质产生或大或小的影响。
晶体缺陷不仅会影响晶体的物理和化学性质,而且还会影响发生在晶体中的过程,如扩散、烧结、化学反应性等。
因而掌握晶体缺陷的知识是掌握材料科学的基础。
晶体的结构缺陷主要类型如表2—1所示。
这些缺陷类型,在无机非金属材料中最基本和最重要的是点缺陷,也是本章的重点。
表2—1 晶体结构缺陷的主要类型2.1点缺陷研究晶体的缺陷,就是要讨论缺陷的产生、缺陷类型、浓度大小及对各种性质的影响。
60年代,F.A.Kroger和H.J.Vink建立了比较完整的缺陷研究理论——缺陷化学理论,主要用于研究晶体内的点缺陷。
点缺陷是一种热力学可逆缺陷,即它在晶体中的浓度是热力学参数(温度、压力等)的函数,因此可以用化学热力学的方法来研究晶体中点缺陷的平衡问题,这就是缺陷化学的理论基础。
点缺陷理论的适用范围有一定限度,当缺陷浓度超过某一临界值(大约在0.1原子%左右)时,由于缺陷的相互作用,会导致广泛缺陷(缺陷簇等)的生成,甚至会形成超结构和分离的中间相。
但大多数情况下,对许多无机晶体,即使在高温下点缺陷的浓度也不会超过上述极限。