地中海贫血基因检测-PCR扩增 2(13检本)
- 格式:pdf
- 大小:459.43 KB
- 文档页数:18

α-地中海贫血基因检测操作规程(益生堂)一、目的:对筛查出来的地贫疑似病例和需要进行地贫产前诊断的夫妇提供进一步的确认。
二、适用范围:适用于益生堂PCR扩增、琼脂糖电泳技术等分析的操作。
三、原理:应用特异的PCR引物选择性地扩增不同类型的α-地中海贫血基因,通过琼脂糖凝胶电泳的带型分析,诊断α-地中海贫血基因缺失型。
四、操作规程(一)标本收集、标本保存、标本转运1、静脉采血:从肘静脉或手背静脉抽取静脉血1mL以上,将血液沿管壁缓慢注入加有EDTA或枸橼酸钠的试管内,轻轻混匀,即为抗凝全血。
羊水的采集:由临床医师经腹壁行羊膜穿刺取得。
采集羊水时速度不宜太快,标本抽取量也不宜太多,一般10-15mL即可。
2、标本一经采集,则应尽快送至实验室检测,抗凝全血室温放置不超过4小时,4℃保存不超过一周,-20℃保存不超过半年,应避免反复冻融。
3、标本装入试管密封,再装入塑料袋中,置冰壶或泡沬箱加冰袋密封运输,在运输过程中应避免剧烈震荡。
4、注意事项(1)抗凝时,不能用肝素抗凝。
(2)采集羊水穿刺羊膜要在妊娠16周羊水达到200mL以后才能进行。
(二)全血DNA提取操作规程1、所需试剂及仪器:试剂由益生堂生物技术(深圳)有限公司提供,包含核酸提取试剂、扩增管、模条、无水乙醇,1.5mL离心管.仪器有黑马和博日扩增仪、台式高速离心机、旋涡振荡器、真空旋转干燥仪、电泳仪、电泳槽、分子杂交仪、凝胶成像系统。
2、实验前准备工作2.1、准备好1.5mL无菌离心管及无菌吸头。
2.2、变性液在每次使用前应充分摇匀以保证提取质量。
3、操作步骤(1)在1.5mL离心管中加入250μL充分摇匀的变性液及100μL抗凝全血,充分混匀,室温放置5分钟。
也可选择以下操作步骤,以获得更高质量的DNA:在1.5mL离心管中加入1mL无菌水及100μL抗凝全血,充分混匀,室温放置5分钟以裂解红细胞。
13000rmp离心1分钟,弃上清,保留管底白细胞块。

pcr反向点杂交检测地中海分型报告PCR反向点杂交检测地中海分型报告一、引言地中海贫血是一种常见的遗传性血液病,主要分为地中海贫血(β-地中海贫血)和地中海贫血症(α-地中海贫血)。
PCR反向点杂交(PCR-RFLP)是一种常用的分子生物学方法,可用于检测地中海分型。
本报告旨在详细介绍PCR-RFLP技术在地中海分型检测中的应用。
二、PCR反向点杂交原理1. PCR原理PCR是聚合酶链式反应(Polymerase Chain Reaction)的缩写,是一种通过体外扩增DNA片段的方法。
它利用DNA聚合酶酶活性,在特定条件下,使DNA模板得到高效扩增。
2. 反向点杂交原理反向点杂交是一种基于DNA序列特异性识别的方法。
它通过将目标DNA序列与特异性引物结合,并经过适当处理后,通过电泳或其他方法进行检测。
三、PCR-RFLP技术在地中海分型检测中的应用1. 样本采集和DNA提取需要从受检者身上采集样本,如静脉血或口腔黏膜细胞。
通过常规方法提取DNA,如酚/氯仿法或商用DNA提取试剂盒。
2. PCR扩增使用特异性引物对目标基因进行PCR扩增。
对于β-地中海贫血,通常选择扩增β-地中海贫血突变的片段;对于α-地中海贫血,通常选择扩增α-地中海贫血突变的片段。
3. 酶切反应将PCR产物与适当的限制性内切酶一起进行酶切反应。
限制性内切酶是一种能够识别特定DNA序列并在该序列上切割的酶。
4. 胶电泳分析将酶切产物经过胶电泳分离,并使用合适的染料染色。
在紫外光下观察和记录胶图。
根据不同基因型的特点,可以确定受检者的地中海分型。
四、结果解读根据PCR-RFLP结果,可以得出以下结论:1. 如果在PCR-RFLP分析中观察到明显的限制性内切酶位点差异,即PCR产物经过酶切后出现不同长度的片段,可以判断受检者为地中海贫血(β-地中海贫血)或地中海贫血症(α-地中海贫血)。
2. 通过比对PCR-RFLP结果与已知标准样本的电泳图,可以进一步确定受检者的具体地中海分型。


地中海贫血检测的方法目前,用于地中海贫血检测的方法的代表性技术大体可分为以下两类:检测基因缺失突变的单管多重跨越断裂点PCR技术和多重连接探针扩增技术(MLPA);检测基因点突变的反向点杂交技术(RDB)、变性高效液相色谱技术(dHPLC)]和DNA序列分析技术等。
此外,最近发展的基于实时荧光PCR平台的新技术,如用于α地贫缺失拷贝数定量的实时荧光PCR直接检测技术、以及用于检测β地贫点突变的基于探针熔解曲线的基因分型技术(PMCA),可能是下一步更新换代的技术选择。
上述胛p PCR、RDB和MLPA等为地贫检测的主流技术。
1.Southern 印迹法优点:分析缺失型α-地中海贫血分子缺陷的可靠技术缺点:操作繁冗,不宜作为常规手段2.联合检测平均红细胞参数(MCV、MCH)+红细胞脆性检测+Hb(血红蛋白)电泳MCV:平均红细胞容积 MCH:平均红细胞血红蛋白量3.PCR-RDB法(PCR/寡核苷酸探针反向斑点杂交法)检测中国南方常见的17种β地贫突变:CD41~42(-TCCT)、IVS-2 nt654 C →T、-28 A→G、CD71~72(+A)、CD71~72(+T)、CD17 A→T、CD26 G→A、CD31(-C)、CD27~28(+C)、CD43 G→T、-32 C→A、-29 A→G、-30 T→C、CD14~15(+G)、CAP、Int及IVS-1 nt5 G→C4.α地中海贫血的基因诊断依据Gap-PCR原理采用单管四重PCR法(多重PCR技术)对其基因组DNA进行扩增,同时检测-α3.7、-α4.2、--SEA和正常对照4种等位基因型,采用1.2%琼脂糖凝胶电泳分离扩增产物,通过片断大小判断患者的基因型。
5.采用PCR-RFLP方法检测非缺失型α地贫Hb Constant Spring(HbCS)。



文章编号(Article ID):1009-2137(2004)04-0472-03·论著·多重PCR用于缺失型α2地中海贫血的基因检测吴洁莹,廖灿,李坚,黄以宁广州市妇婴医院优生围产研究所,广州510180摘要 为了探讨多重PCR技术在检测我国南方常见缺失型α2地中海贫血中的临床应用,观察缺失型α2地中海贫血的基因分布频率,采用单管多重DNA扩增的方法(M2PCR)对经血红蛋白定量分析初步诊断为标准型和静止型α2地中海贫血及血红蛋白H(HbH)病的145例患者进行基因检测。
扩增产物经1.2%琼脂糖凝胶电泳,出现1.3及1.8kb条带者,提示为22SEA/αα;1.6及1.8kb条带者为2α4.2/αα;1.8及2.0kb条带者为2α3.7/αα;1.3及1.6或2.0kb条带,提示为缺失型HbH病(22SEA/2α4.2或22SEA/2α3.7)。
结果表明,145例受检者中发现100例22SEA/αα(68.9%), 15例2α3.7/αα(10.3%),8例2α4.2/αα(5.52%),2例2α3.7/2α4.2(1.38%),2α3.7及2α4.2纯合子各1例(0.69%);14例22SEA/2α3.7(9165%),2例22SEA/2α4.2(1.38%);另有2例患者产前诊断证实为Bart水肿胎儿。
结论:运用多重PCR 技术可以准确、简便、快速地检测我国南方地区常见的2α3.7、2α4.2、22SEA3种缺失型α2地中海贫血,这一技术对α2地中海贫血的大人群筛查及携带者的检出是一种较为理想的方法。
关键词 多重PCR;α2地中海贫血;缺失型α地中海贫血;基因缺失中图分类号 R556161文献标识码 AMultiplex PCR for Detecting G enotypes of Deletionalα2ThalassemiaW U Jie2Yi ng,L IA O Can,L I Jian,HUA N G Yi2N i ngInstit ute of Eugenics and Peri natalogy,Guangz hou M aternal and Neonatal Hospital,Guangz hou510180,Chi naAbstract To investigate the clinical application of multiplex PCR in detecting genotypes of deletionalα2thalassemia in S outh China and observe the distribution frequency ofα2globin gene deletion,145patients with silent carrier,alpha tha2 lassemia trait or HbH were identified by M2PCR and1.2%agarose gel electrophoresis.There are1.3,1.6,1.8and2.0kb bands which indicate22SEA,2α4.2,ααand2α3.7,respectively.The results showed that among145patients,100pa2 tients with22SEA/αα(68.9%),15with2α3.7/αα(10.3%),8with2α4.2/αα(5.52%),2with2α3.7/2α4.2(1.38%),1 with2α3.7/2α3.7(0.69%),1with2α4.2/2α4.2(0.69%),14with22SEA/2α3.7(9.65%),2with22SEA/2α4.2(1.38%)were found.Two patients prenatal diagnosed were confirmed with Bart′s hydrops fetuses.In conclusion,M2PCR analysis is a simple,rapid and accurate method for detection ofα2thalassemia gene deletion.This technique is helpful in screening,car2 rier identification and prenatal diagnosis of deletionalα2thalassemia.K ey w ord Multiplex2PCR;α2thalassemia;deletionalα2thalassemia;gene deletionJ Ex p Hem atol2004;12(4):472-474α2地中海贫血(α2thalassemia)是因珠蛋白基因缺失或突变使血红蛋白的4条珠蛋白肽链合成障碍而引起的溶血性贫血,是世界上最常见的人类单基因遗传病之一1,也是我国长江以南各省发病率最高、影响最大的遗传病之一。

地中海贫血基因报告单
姓名: 性别:
年龄: 出生日期:
检测日期:
1. 基因检测结果
您的基因检测结果显示,您携带了地中海贫血症状的致病基因。
该基因是使人体不产生足够的血红蛋白,增加贫血的风险。
2. 发病风险
由于您携带了地中海贫血症状的致病基因,因此您的发病风险
高于正常人口。
如果您计划要生育或者已经怀孕,你的子孙也有
可能携带该致病基因并且有发生地中海贫血的风险。
我们建议您
谨慎考虑生育计划,避免将地中海贫血基因遗传给孩子。
3. 预防措施
虽然目前没有特效治疗地中海贫血的方法,但借助一些有效的措施你可以远离地中海贫血的风险。
生活中,尽可能避免暴曝在紫外线照射下,合理运动及饮食,增强体质。
如果您是地中海贫血的患者,应该避免饮酒和吸烟。
虽然您携带地中海贫血基因,但是请不要过分担心。
我们提供的检测以及预防措施可以帮助你预防地中海贫血疾病的发生。
如有任何问题可随时咨询我们,我们将竭尽所能为您提供帮助。

地中海贫血基因检测实验步骤地中海贫血(Mediterranean anemia),又称为地中海型家族性小红细胞性贫血,是一种常染色体隐性遗传病。
该病是由珠蛋白基因缺陷引起的,导致血红蛋白结构异常,造成红细胞携氧能力减弱。
地中海贫血的基因检测通常涉及以下几个步骤:1. 样本采集:- 采集患者的血液样本或使用拭子采集口腔黏膜细胞。
2. DNA提取:- 从血液或细胞样本中提取DNA。
这通常涉及破坏细胞膜和核膜,然后使用化学试剂纯化DNA。
3. PCR扩增:- 利用聚合酶链反应(PCR)技术,特异性地扩增珠蛋白基因的特定片段。
这通常涉及设计针对基因突变热点区域的引物,并通过循环加热和退火步骤使目标DNA片段指数级增长。
4. 凝胶电泳:- 将PCR产物通过凝胶电泳进行分离,根据大小将不同长度的DNA片段分开。
这有助于识别是否存在特定的突变。
5. 基因测序:- 对PCR产物进行测序,以识别可能的基因突变。
测序可以揭示DNA序列中的碱基替换、插入或缺失,这些改变可能与地中海贫血的发生有关。
6. 突变分析:- 将测序结果与已知的突变数据库进行比对,以确定是否存在与地中海贫血相关的特定基因突变。
7. 数据解读:- 根据突变分析的结果,结合患者的临床症状和家族史,医生或遗传顾问将解释检测结果,并提供遗传咨询服务。
8. 报告编写:- 编写一份包含检测结果和相关解释的报告,供医疗专业人员和患者参考。
基因检测对于诊断地中海贫血非常重要,它不仅可以帮助确诊患有该病的个体,还可以为家族成员提供风险评估和遗传咨询。
随着科技的进步,新的检测技术(如芯片基因分型和下一代测序)正在使地中海贫血的基因检测变得更加快速和精确。

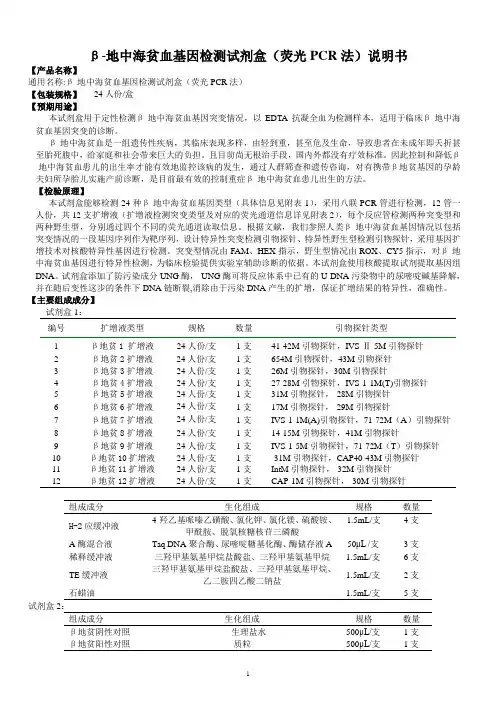
β-地中海贫血基因检测试剂盒(荧光PCR法)说明书【产品名称】通用名称:β-地中海贫血基因检测试剂盒(荧光PCR法)【包装规格】24人份/盒【预期用途】本试剂盒用于定性检测β-地中海贫血基因突变情况,以EDTA抗凝全血为检测样本,适用于临床β-地中海贫血基因突变的诊断。
β-地中海贫血是一组遗传性疾病,其临床表现多样,由轻到重,甚至危及生命,导致患者在未成年即夭折甚至胎死腹中,给家庭和社会带来巨大的负担。
且目前尚无根治手段,国内外都没有疗效标准。
因此控制和降低β-地中海贫血患儿的出生率才能有效地监控该病的发生,通过人群筛查和遗传咨询,对有携带β地贫基因的孕龄夫妇所孕胎儿实施产前诊断,是目前最有效的控制重症β-地中海贫血患儿出生的方法。
【检验原理】本试剂盒能够检测24种β-地中海贫血基因类型(具体信息见附表1),采用八联PCR管进行检测,12管一人份,共12支扩增液(扩增液检测突变类型及对应的荧光通道信息详见附表2),每个反应管检测两种突变型和两种野生型,分别通过四个不同的荧光通道读取信息。
根据文献,我们参照人类β-地中海贫血基因情况以包括突变情况的一段基因序列作为靶序列,设计特异性突变检测引物探针、特异性野生型检测引物探针,采用基因扩增技术对核酸特异性基因进行检测。
突变型情况由FAM、HEX指示,野生型情况由ROX、CY5指示,对β-地中海贫血基因进行特异性检测,为临床检验提供实验室辅助诊断的依据。
本试剂盒使用核酸提取试剂提取基因组DNA。
试剂盒添加了防污染成分UNG酶,UNG酶可将反应体系中已有的U-DNA污染物中的尿嘧啶碱基降解,并在随后变性这步的条件下DNA链断裂,消除由于污染DNA产生的扩增,保证扩增结果的特异性,准确性。
【主要组成成分】试剂盒1:编号扩增液类型规格数量引物探针类型1 β地贫1 扩增液24人份/支1支41-42M引物探针,IVS-Ⅱ-5M引物探针2 β地贫2扩增液24人份/支1支654M引物探针,43M引物探针3 β地贫3扩增液24人份/支1支26M引物探针,30M引物探针4 β地贫4扩增液24人份/支1支27-28M引物探针,IVS-1-1M(T)引物探针5 β地贫5扩增液24人份/支1支31M引物探针,-28M引物探针6 β地贫6扩增液24人份/支1支17M引物探针,-29M引物探针7 β地贫7扩增液24人份/支1支IVS-1-1M(A)引物探针,71-72M(A)引物探针8 β地贫8扩增液24人份/支1支14-15M引物探针,41M引物探针9 β地贫9扩增液24人份/支1支IVS-1-5M引物探针,71-72M(T)引物探针10 β地贫10扩增液24人份/支1支-31M引物探针,CAP40-43M引物探针11 β地贫11扩增液24人份/支1支IntM引物探针,-32M引物探针12 β地贫12扩增液24人份/支1支CAP-1M引物探针,-30M引物探针组成成分生化组成规格数量H-2应缓冲液4-羟乙基哌嗪乙磺酸、氯化钾、氯化镁、硫酸铵、甲酰胺、脱氧核糖核苷三磷酸1.5mL/支4支A酶混合液Taq DNA聚合酶、尿嘧啶糖基化酶、酶储存液A 50μL /支3支稀释缓冲液三羟甲基氨基甲烷盐酸盐、三羟甲基氨基甲烷 1.5mL/支6支TE缓冲液三羟甲基氨基甲烷盐酸盐、三羟甲基氨基甲烷、乙二胺四乙酸二钠盐1.5mL/支2支石蜡油 1.5mL/支5支试剂盒2:组成成分生化组成规格数量β地贫阴性对照生理盐水500μL/支1支β地贫阳性对照质粒500μL/支1支注:本试剂盒由试剂盒1和试剂盒2组成。
地贫基因检测报告单
尊敬的用户:
您好!感谢您选择本机构进行地贫基因检测。
根据您提供的样本,我们已完成检测并生成了检测报告单,现将结果详细通知如下:
一、检测结果。
1. 地贫基因检测结果,阴性。
2. 检测方法,PCR扩增技术。
3. 检测时间,2022年10月15日。
二、结果解读。
根据我们的检测结果,您的地贫基因检测为阴性,即您并未携带地贫基因。
这意味着您在遗传上并不具有地贫症的风险,也不会将地贫基因传递给下一代。
这对于您个人和家庭来说都是一个好消息。
三、建议和注意事项。
虽然您的地贫基因检测结果为阴性,但我们仍建议您保持良好的生活习惯,包括均衡饮食、适量运动、定期体检等。
此外,如果您计划要孩子,我们也建议您在孕前进行全面的遗传咨询和检测,以确保孩子的健康。
四、关于地贫基因。
地贫是一种常见的遗传性疾病,患者因体内血红蛋白合成障碍而导致贫血。
地贫症主要由地中海贫血、遗传性珠蛋白病等引起,患者常出现贫血、黄疸等症状。
地贫基因主要通过父母遗传给子女,因此对于有地贫家族史的人群,进行地贫基因检测是非常有必要的。
五、结语。
感谢您选择本机构进行地贫基因检测,并信任我们的专业技术。
如果您对检测结果有任何疑问或需要进一步咨询,欢迎随时联系我们的专业医生团队,我们将竭诚为您解答疑惑。
最后,祝愿您和您的家人健康幸福!
此致。
敬礼。
地贫基因检测中心敬上。
第1篇一、实验背景地中海贫血(Thalassemia)是一种由于珠蛋白基因缺陷引起的遗传性溶血性贫血病。
根据珠蛋白基因突变的不同,地中海贫血可分为α-地中海贫血和β-地中海贫血两大类。
本实验旨在通过分子生物学技术对疑似地中海贫血患者进行基因检测,以确定其基因型,为临床诊断和治疗提供依据。
二、实验目的1. 确定疑似地中海贫血患者的基因型。
2. 为临床诊断和治疗提供科学依据。
三、实验材料1. 样本:疑似地中海贫血患者的血液样本。
2. 试剂:DNA提取试剂盒、PCR试剂盒、DNA测序试剂盒等。
3. 仪器:PCR仪、电泳仪、测序仪等。
四、实验方法1. 样本DNA提取:采用DNA提取试剂盒提取疑似地中海贫血患者的血液样本DNA。
2. PCR扩增:根据α-地中海贫血和β-地中海贫血的基因突变位点,设计特异性引物,进行PCR扩增。
3. PCR产物检测:通过琼脂糖凝胶电泳检测PCR产物,观察条带情况。
4. DNA测序:对扩增产物进行DNA测序,确定基因突变位点。
5. 基因型分析:根据测序结果,分析疑似地中海贫血患者的基因型。
五、实验结果1. 样本DNA提取:成功提取疑似地中海贫血患者的血液样本DNA。
2. PCR扩增:成功扩增出α-地中海贫血和β-地中海贫血的基因片段。
3. PCR产物检测:电泳结果显示,扩增产物大小与预期相符。
4. DNA测序:测序结果显示,疑似地中海贫血患者的基因存在突变。
5. 基因型分析:根据测序结果,确定疑似地中海贫血患者的基因型为α-地中海贫血杂合子。
六、讨论与分析1. α-地中海贫血是一种常染色体隐性遗传病,主要由于α-珠蛋白基因缺陷引起。
本实验通过PCR和DNA测序技术,成功检测出疑似地中海贫血患者的基因突变,为临床诊断提供了依据。
2. α-地中海贫血的基因型可分为纯合子和杂合子。
本实验结果显示,疑似地中海贫血患者的基因型为α-地中海贫血杂合子,提示其可能表现为轻型α-地中海贫血或无症状携带者。
地中海贫血基因检测报告单怎么看尊敬的客户:
感谢您选择我们的地中海贫血基因检测服务。
检测报告单中包
含了您基因检测的具体结果和相关解释,本文将为您详细介绍报
告单的各项内容。
1.个人信息
在报告单的顶部,您能看到个人信息的栏目,这一栏中列出了
您的姓名、出生日期、性别等个人信息,方便您快速辨认。
2.样品信息
接下来这一部分将提供样品信息,其中包括样品编号、检测日
期等信息。
这些信息将有助于查找和追踪样本的来源和检测过程。
3.基因检测结果
在报告单的核心部分,我们提供了详细记录您基因检测结果的信息表格。
这张表格中第一列列出了与地中海贫血相关的11种基因突变,第二列将显示每种突变在您的基因中的状态。
基因会有两个拷贝,一份来自母亲,一份来自父亲,分别对应第三列和第四列。
我们将所有可能的基因状态进行解释和分类,以便您更好地了解您的基因情况。
4.检测建议
报告单的最后一部分是检测建议,我们将对您检测结果进行评估和分类,并给出适当的建议。
此建议并非诊断结果,仅作为一个参考,如果您需要进一步的诊断和治疗信息,请咨询专业医生的建议。
总结:
基于个人成因的地中海贫血检测是一种安全、快捷、准确的诊断方法。
通过检测报告单中的各项数据,您可以更好地了解自己的基因信息并得出适当的诊断建议。
如果您有任何关于报告单中数据的提问,或者需要进一步地了解我们的检测服务,可以随时联系我们的专业团队。
再次感谢您的选择和信任。
地中海贫血检查报告单报告日期:_______________
报告编号:_______________
受检者基本信息:
姓名:_____________ 性别:_____________ 年龄:_____________
联系方式:__________________________
检测项目:
地中海贫血基因检测
检测结果:
受检者_____________基因筛查结果如下:
□ α0型□ α+型□ β0型□ β+型□ 总体特缺□ 无异常
检测人员:
检测机构:__________________________
报告说明:
地中海贫血是一种遗传性疾病,通常由父母双方至少携带其中一种基因而遗传给子女。
本次检测结果显示,受检者
_____________基因筛查结果为_____________。
特别是β0型和α0型地中海贫血基因是几乎不产生血红蛋白的严重型,患者会有严重的贫血、黄疸、脾大、肝大、发育不良等,常常在幼年时期就发现症状。
受检者或代理人应仔细阅读本报告,如有疑问请咨询医师或遗传咨询师,建立完善的个人和家庭遗传史档案,采取科学有效的措施。
建议在孕前咨询医生,进行基因检测和遗传咨询,减少地中海贫血的遗传风险。
此报告仅基因检测报告,仅供参考。
如需更加全面的检测结果,需结合其他化验结果及医疗检查结果来判断。
签字:__________________________
注:本报告一式两份,一份为受检者保存,一份为检测机构存档。
一、实验背景地中海贫血(Thalassemia),又称地中海型贫血,是一种遗传性血红蛋白合成障碍的疾病。
该病主要发生在地中海沿岸、东南亚以及我国南方等地区。
地中海贫血患者由于血红蛋白合成不足,导致红细胞形态异常、寿命缩短,严重者可引发贫血、肝脾肿大、骨骼变形等并发症,甚至危及生命。
近年来,随着分子生物学技术的不断发展,地中海贫血的基因诊断技术逐渐成熟。
本研究旨在通过实验,探究地中海贫血基因诊断方法,为临床诊断和治疗提供理论依据。
二、实验目的1. 掌握地中海贫血基因诊断的基本原理和操作步骤;2. 了解地中海贫血基因突变类型及其对血红蛋白合成的影响;3. 评估不同基因诊断方法在临床应用中的优势和局限性。
三、实验材料与方法1. 实验材料(1)实验样本:选取10份地中海贫血患者样本和10份正常对照样本;(2)试剂:PCR试剂盒、DNA提取试剂盒、限制性内切酶、DNA连接酶、Taq DNA聚合酶等;(3)仪器:PCR仪、电泳仪、凝胶成像系统等。
2. 实验方法(1)DNA提取:采用酚-氯仿法提取实验样本中的基因组DNA;(2)PCR扩增:针对地中海贫血基因突变位点设计特异性引物,进行PCR扩增;(3)限制性内切酶酶解:将PCR产物进行限制性内切酶酶解,观察酶切产物条带;(4)电泳分析:将酶切产物进行琼脂糖凝胶电泳,观察条带变化,判断是否存在突变。
四、实验结果与分析1. DNA提取结果实验成功提取了10份患者样本和10份正常对照样本的基因组DNA,A260/A280比值在1.8-2.0之间,符合实验要求。
2. PCR扩增结果通过PCR扩增,成功扩增出地中海贫血基因的突变位点。
10份患者样本均出现异常条带,而10份正常对照样本则无异常条带。
3. 限制性内切酶酶解结果对PCR产物进行限制性内切酶酶解,发现10份患者样本酶切产物与正常对照样本存在差异。
患者样本酶切产物条带数量、位置和大小均与正常对照样本不同。
4. 电泳分析结果电泳结果显示,患者样本与正常对照样本在特定位置出现差异条带。