2020ASCO胰腺癌最新研究进展(强烈推荐)
- 格式:pptx
- 大小:11.70 MB
- 文档页数:63


胰腺癌是一种少见的恶性肿瘤,虽仅占所有癌症病例的2%~3%,却是7%的癌症死亡的罪魁祸首。
2020年美国估计将有57 600例胰腺癌新病例,这种疾病现在是仅次于肺癌和结肠癌的第三大癌症死亡原因。
据估计,到2030年,胰腺癌将超过结肠癌,成为第二大致死原因。
胰腺癌唯一的根治方法是手术切除,但大多数患者在发病时就已无法切除或发生转移。
因此,系统性治疗对大多数患者是必要的选择。
本文对当前转移性胰腺癌的治疗选择进行介绍,并展望了有前景的研究。
两个1类推荐的一线化疗方案,如何抉择?对于适合积极治疗的转移性胰腺癌患者,有两种1类推荐的一线治疗方案。
具有最强生存获益证据的方案是5-氟尿嘧啶(5-FU)、亚叶酸钙、伊立替康和奥沙利铂(FOLFIRINOX)。
在Ⅲ期PRODIGE试验中,对东部肿瘤协作组(ECOG)体能状态评分为1或更低的初治患者随机分配,给予FOLFIRINOX方案或吉西他滨单药治疗。
中位总生存(OS)明显支持FOLFIRINOX 方案(11.1个月vs. 6.8个月)。
此外,FOLFIRINOX组的中位无进展生存期(PFS)更好(6.4个月vs. 3.3个月)。
虽然FOLFIRINOX与吉西他滨相比有更多的不良事件,但在后续的研究中,采用减少剂量强度和积极的支持治疗,包括常规的生长因子支持治疗,结果显示,FOLFIRINOX方案的耐受性得以改善。
而且,尽管FOLFIRINOX方案毒性增加,但治疗6个月后患者的生活质量下降仅为31%,而吉西他滨组为66%。
另一个1类推荐的化疗方案是吉西他滨+白蛋白结合型紫杉醇。
Ⅲ期MPACT试验的数据比较了吉西他滨+白蛋白结合型紫杉醇与吉西他滨单药疗法在Karnofsky 功能状态评分≥70%的初治患者中的疗效。
吉西他滨+白蛋白结合型紫杉醇组的OS改善(8.7个月vs. 6.6个月)。
靶向治疗进展:一路高歌虽然目前转移性胰腺癌的一线系统治疗推荐已经建立,但近年来后续治疗的格局已经发生变化,现在的重点是靶向治疗。


美国临床肿瘤学会ASCO2020早期临床研究速递美国临床肿瘤学会ASCO 2020 早期临床研究速递2020年美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)年会已于6月初落下帷幕,会议期间公布了多项早期临床研究结果。
免疫治疗仍是本次会议的热点,改良的免疫治疗、免疫联合治疗、双免疫特异性靶点抑制剂、嵌合抗原受体T细胞免疫疗法(chimeric antigen receptor T-cell immunotherapy,CAR-T)等早期临床研究层出不穷,在头颈鳞癌、血液肿瘤获得初步结果,也在消化道肿瘤进行了初步探索。
新靶点的药物治疗同样有闪光点。
现将创新性比较突出的几个药物简评如下以供参考。
1 免疫治疗免疫治疗是目前抗肿瘤治疗最重要的突破口之一,以程序性死亡蛋白-1(programmed death-1,PD-1)/程序性死亡蛋白配体1(programmed death ligand-1,PD-L1)、细胞毒性T细胞相关蛋白-4(ytotoxic T lymphocyte associate protein-4,CTLA-4)为靶点的免疫检查点抑制剂在治疗晚期肺癌、黑色素瘤、霍奇金淋巴瘤、微卫星高度不稳定结直肠癌等肿瘤中取得了巨大成功。
但是获益人群仍然有限,研发的重点方向是如何扩大受益人群、逆转耐药。
PROBODY是一类完全重组的单克隆抗体,其原理是将药物的抗原结合位点利用抗体掩蔽技术进行封闭,在正常组织中保持惰性,而在肿瘤微环境中药物能被肿瘤特异的蛋白酶切割从而被选择性激活,暴露出抗原结合位点发挥功能,从而减小药物脱靶效应的产生。
CX-072是一种靶向PD-L1的PROBODY型免疫检查点抑制剂[1],最早亮相于2018年ASCO年会。
在2020年ASCO会议上,共3篇摘要对CX-072 Ⅰ期和Ⅰ/Ⅱ期临床研究结果进行了报道(3005,3108,3602)。

MSS魔咒⼜破除!pMMR胰腺癌患者获益K药+乐伐,PD1+多靶药持续打破MSSpMMR免。
MSI/MMR是免疫治疗的预测指标,在消化道癌种中检出率较⾼。
按对免疫治疗的疗效,分为免疫⾮常敏感的MSI-H/dMMR型,但这类患者的占⽐⾮常低,5%-10%左右;以及对免疫疗效极差的MSS/pMMR稳定型,此类占据了肿瘤患者中的主体,有多差,部分研究中显⽰,单药免疫去治疗MSS型结直肠癌,有效率为0,即使PDL1阳性也不能缓解。
因此,如何攻破此类免疫“冷”肿瘤的免疫僵局,运⽤好PD1/PDL1如此好的药物,成为了长久以来研究的重点。
幸运的是,今年曝出了⼏例通过联合⼿段成功处理的案例,免疫⽆效禁锢有望攻破!真实案例:p M M R胰腺癌患者从K药联合乐伐替尼获益2017年3⽉,1位55岁⼥性出现间歇性腹痛,有⾼⾎压病史(⼝服⾮洛地平缓释⽚),胃溃疡1年,痔疮多年。
腹部彩超提⽰可能为胰腺癌,CT提⽰多发肝转移、肺转移。
患者被诊断为胰腺癌cT4N1M1(伴肝肺转移)。
免疫组化提⽰MLH1 (+), MSH2 (+), MSH6 (+++), PMS2 (++),即pMMR(免疫⽆效型)。
针对患者腹痛情况,⾸先进⾏了腹部放疗联合化疗。
胰腺病灶⾏70Gy/15f,肝右叶的2个⼤转移灶⾏60Gy/15f和50Gy/15f。
联合GS化疗(吉西他滨1000mg/m2 d1、8;S-1 100mg/d1-14 qid 21d)2个周期。
放化疗后,患者腹痛减轻,但因Ⅱ级⾎⼩板减少和疲乏⽽拒绝进⼀步的化疗。
测了基因检测提⽰ERBB2扩增(20%)和19外显⼦突变(0.14%)和20外显⼦突变(0.12%),TMB(14.9mut/Mb)远远⾼于平均值(2.5mut/Mb)。
针对基因检测中HER2扩增的情况,患者随后接受了4次的曲妥珠单抗(第⼀次8mg/kg d1 Q21d,之后6mg/kg)联合厄洛替尼100mg/Qd治疗,治疗过程中,CA19-9⽔平有所下降。


不可切除胰腺癌的分子靶向药物治疗进展胡润,李俊蒽,姚沛,桂仁捷,段华新湖南师范大学附属第一医院,湖南省人民医院肿瘤科,长沙 410005通信作者:段华新,****************(ORCID: 0000-0001-9596-5013)摘要:胰腺癌作为消化系统最常见的恶性肿瘤之一,其发病率及死亡率正逐年上升,大多数胰腺癌患者因分期较晚而失去了手术机会。
尽管以吉西他滨、氟尿嘧啶为主的化疗方案在一定程度上延长了患者的生存期,但仍有部分患者因无法耐受化疗而失去治疗机会。
随着精准医疗时代的来临,分子靶向药物治疗展现出的优异疗效使其成为对抗肿瘤的重要治疗手段之一,但由于胰腺癌高度的异质性及复杂的免疫微环境,针对胰腺癌的分子靶向治疗并未取得显著效果,因此亟需探寻新的治疗靶点及药物攻克这一难题。
本综述基于胰腺癌常见分子靶点及肿瘤免疫相关靶点探究在不可切除胰腺癌中分子靶向药物治疗研究的最新进展,为胰腺癌患者提供新的治疗策略。
关键词:胰腺肿瘤;分子靶向治疗;免疫疗法基金项目:湖南省自然科学基金(2020JJ8084)Advances in molecular-targeted therapy for unresectable pancreatic cancerHU Run,LI Junen,YAO Pei,GUI Renjie,DUAN Huaxin.(Department of Oncology,The First Affiliated Hospital of Hunan Normal University, Hunan Provincial People’s Hospital, Changsha 410005, China)Corresponding author: DUAN Huaxin,****************(ORCID: 0000-0001-9596-5013)Abstract:Pancreatic cancer is one of the most prevalent malignant tumors of the digestive system, and its incidence and mortality rates are increasing year by year. Most patients with pancreatic cancer are unable to receive surgery due to the advanced stage. Although chemotherapy regimens based on gemcitabine and fluorouracil have prolonged the survival time of patients to some extent,some patients cannot tolerate chemotherapy and hence lose the opportunity for treatment. With the advent of the era of precision medicine, molecular-targeted therapy has exhibited an excellent therapeutic efficacy and has thus become one of the most important treatment techniques for tumors; however, due to the high heterogeneity of pancreatic cancer and its complicated tumor microenvironment, molecular-targeted therapy for pancreatic cancer has not achieved notable results. Therefore, it is imperative to seek new therapeutic targets and medications to overcome this issue. This article reviews the latest advances in the research on molecular-targeted therapy for unresectable pancreatic cancer based on common molecular targets and tumor immunity-related therapeutic targets, in order to provide new treatment strategies for patients with pancreatic cancer.Key words:Pancreatic Neoplasms; Molecular Targeted Therapy; ImmunotherapyResearch funding:Natural Science Foundation of Hunan Province of China (2020JJ8084)胰腺癌是一种起病隐匿、进展迅速、疗效及预后极差的恶性肿瘤,大多数患者确诊时已经属于晚期。


美国临床肿瘤学会《局部进展期不可切除胰腺癌临床实践指南》解读(最全版)摘要绝大多数胰腺癌病人在诊断时已处于疾病的晚期,其中局部进展期不可切除胰腺癌病人例数众多,但国内外却缺乏具有充足循证医学证据的权威性指南来指导临床实践。
最近,美国临床肿瘤学会针对局部进展期不可切除胰腺癌提出了基于随机对照研究的临床实践指南,指出局部肿瘤控制及提高病人生活质量应是局部进展期不可切除胰腺癌的诊治核心。
关键词胰腺癌;局部进展期胰腺癌胰腺癌是一种恶性程度极高、预后极差的消化系统肿瘤,且绝大多数病人在诊断时已处于疾病的晚期[1]而丧失了根治性手术的机会。
大量的临床研究表明,R0 切除对于胰腺癌病人的远期生存至关重要[2-6]。
虽然可能治愈的胰腺癌(potentially curable pancreatic cancer)和局部进展期胰腺癌(locally advanced pancreatic cancer,LAPC)均存在周围血管的侵犯包绕,但可能治愈的胰腺癌尚存在R0 切除的可能,LAPC 由于侵犯范围更广、对血管的包绕更紧密,即使完成血管的切除重建也难以实现R0 切除[7]。
然而临床工作中,LAPC 病人例数众多且多伴有症状,对于这部分病人如何控制局部肿瘤进展、提高病人生活质量、减轻症状则成为处理LAPC 的核心。
美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)2016 年8 月发布了《局部进展期不可切除胰腺癌临床实践指南》(以下简称ASCO 指南)及相应的推荐(表1)。
ASCO 指南由多学科专家组通过系统性回顾2002 年4 月至2015 年6 月的26 个Ⅲ期随机对照研究制定,旨在帮助临床决策的制定。
本文对其予以介绍并解读。
1 治疗前的初始评估(推荐1)影像学在胰腺癌的诊断及分期中有重要的地位,尤其是CT、MRI 及内镜超声(EUS)[8]。
CT 具有更易判断及少受操作者水平影响的特点,结合多期成像能更好地评估肿瘤与周围血管的关系,而胸部CT 可以排除肺内转移。
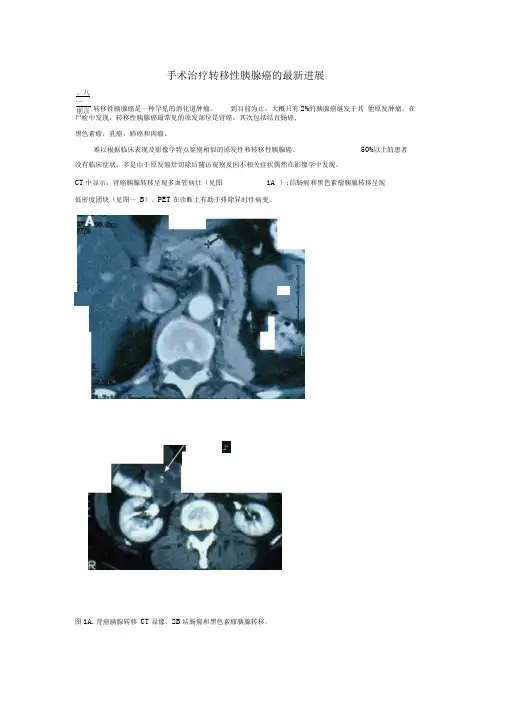
手术治疗转移性胰腺癌的最新进展转移性胰腺癌是一种罕见的消化道肿瘤。
到目前为止,大概只有2%的胰腺癌继发于其 他原发肿瘤。
在尸检中发现,转移性胰腺癌最常见的原发部位是肾癌,其次包括结直肠癌, 黑色素瘤,乳癌,肺癌和肉瘤。
难以根据临床表现及影像学特点鉴别相似的原发性和转移性胰腺癌。
没有临床症状:多是由于原发癌灶切除后随访观察及因不相关症状偶然在影像学中发现。
CT 中显示,肾癌胰腺转移呈现多血管病灶(见图 1A );结肠癌和黑色素瘤胰腺转移呈现低密度团块(见图一 B )。
PET 在诊断上有助于排除异时性病变。
图1A.肾癌胰腺转移 CT 显像,2B 结肠癌和黑色素瘤胰腺转移。
、八—刖言 50%以上的患者r图2.黑色素瘤胰腺颈部和左肺转移 PET/CT 增强显像。
转移性胰腺癌可发生两种不同临床病理表现,一种为严重扩散的病变, 另一种是胰腺上孤立的团块。
只有少部分显示出有手术切除可能的孤立癌灶, 但大部分已经出现了大面积的转移。
在大规模医院,转移性胰腺癌手术的患者越来越多, 可能是由于对此病的重视及无症状患者影像学检查的普及。
通常认为,胰腺切除可导致高发病率和死亡率。
但是近几年证据表明,在大规模医院实行胰腺切除是一种安全及可行的手术;这同样暗示了胰腺转移灶行手术切除的可行性。
此篇回顾了关于常见肿瘤胰腺转移的文献并分析手术的早期和长期的疗效。
资料与方法:在pubmed 上系统性收集了 2013年10月之前的相关文献。
搜索词包括:原发或转移性肿瘤,胰腺切除术,肾细胞癌,乳癌,黑色素瘤,结直肠癌,肉瘤和肺细胞癌。
使用 相关文献”这个功能扩展了检索范围,同时录入了所有的摘要,研究及引用。
文献纳入标准: 的报道。
研究结果将分别概述:1. 肾细胞癌(1)英文的,有摘要的及相关人类研究的文献(2)相关的罕见肿瘤文献剔除标准: 按照最初标准检索出 原发肿瘤是肾,38 是肺癌。
(1)模糊不清的结果及感兴趣参数(2)无法从中提取数据。
胰腺癌化疗新突破!这种新型化疗方案,可显著延长生存期胰腺癌是一种恶性程度很高的消化道肿瘤,其病程短、进展快和预后差,是发病率和死亡率最接近的恶性肿瘤之一,被称为“癌中之王”。
即便是1期胰腺癌,患者的5年生存率也只有14%;一旦进展到3期或4期,5年生存率更是锐减到3%和1%。
据估计,全球每年新确诊的胰腺癌病例超过33.7万例。
那些曾经活跃在身边的名字,一旦成为胰腺癌的猎物,便再难幸免。
诺贝尔奖获得者斯坦曼、《人鬼情未了》中的男星帕特里克、著名男高音帕瓦罗蒂、香港胖姐沈殿霞……不过,好消息是,对于这种预后极差的癌症,最近一项关于新化疗的研究结果却引起医生和患者们的广泛关注。
日前,法国洛林大学洛林癌症研究所Conroy等报告,胰腺癌术后,改良的FOLFIRINOX 方案(mFOLFIRINOX)辅助治疗较吉西他滨单药可显著延长生存期,不过,不良事件发生率较高。
该研究发表在权威期刊《新英格兰杂志》。
新化疗方案含有4种不同的化疗成分,包括:奥沙利铂(oxaliplatin)、亚叶酸钙(leucovorin)、伊立替康(irinotecan)、以及5-氟尿嘧啶(5-fluorouracil)。
为比较mFOLFIRINOX 方案相对吉西他滨用于胰腺癌术后患者辅助治疗的疗效和安全性,该研究入组493例胰导管腺癌术后患者,随机分入mFOLFIRINOX方案组或吉西他滨组。
主要终点为无疾病生存期(DFS),次要终点包括总生存期(OS)和安全性。
结果显示,中位随访33.6个月,mFOLFIRINOX组和吉西他滨组患者的中位无疾病生存期分别为21.6个月和12.8个月,3年无疾病生存率分别为39.7%和21.4%。
中位总生存期分别为54.4个月和35.0个月,3年总生存率分别为63.4%和48.6%。
新方案3~4级不良事件发生率分别为75.9%和52.9%;吉西他滨组有1例死于毒性反应(间质性肺炎)。
其实,早在去年年中,美国临床肿瘤学会(ASCO)也对新的化疗方案进行过专题报道。
2020年胰腺癌研究进展回顾(全文)全球胰腺癌总体发病率和死亡率逐年攀升。
作为“癌中之王”,胰腺癌早期诊断率仅5%,5年生存率仍不足10%。
现有胰腺癌治疗方案存在诸多未满足的需求,手术切除率低且手术切除后生存率不佳;吉西他滨单药一线治疗生存改善不明显,FOLFIRINOX治疗方案仅对合并症少、年龄<65岁、体能状态良好的部分患者有益;二线治疗率低,一线治疗进展后仅43%的患者接受二线治疗。
胰腺癌的致密间质及其肿瘤微环境,是药物治疗效果差的重要原因,该环境为癌细胞营造了足够的缺氧环境,便于肿瘤侵犯与转移。
80%的肿瘤供血血管被厚层的周细胞包裹,阻碍药物在瘤体内沉积,导致治疗失败。
虽然胰腺癌的肿瘤微环境将治疗药物“拒之瘤外”,但却未能阻挡科学家们在胰腺癌治疗领域前行的脚步。
化疗研究进展01转移性胰腺癌(mPC)二线化疗:脂质体伊立替康成为焦点,亚洲人群获益更多纳米脂质体伊立替康(nal-IRI)突破瘤体屏障,成就NAPOLI-1研究的出色成果NAPOLI-1是首个探索脂质体伊立替康用于一线治疗后进展的胰腺癌患者的全球性Ⅲ期研究,该研究在全球14个国家、76个中心开展非盲、随机、III期临床试验,旨在探索脂质体伊立替康单药或联合5-氟尿嘧啶+亚叶酸(nal-IRI+5-FU/LV)治疗既往基于吉西他滨(GEM)化疗方案失败的转移性胰腺癌患者的有效性和安全性。
主要终点为总生存(OS),次要终点包括无进展生存(PFS)、客观缓解率(ORR)、糖类抗原199(CA199)应答率和安全性等。
结果显示,与5-FU/LV 方案相比,脂质体伊立替康联合方案ORR提高15%,CA199应答率提高20%,中位OS时间延长1.9个月(HR=0.67;95%CI:0.49-0.92;P=0.012),且PFS获得双倍延长(3.1个月∶1.5个月;HR=0.56;95%CI:0.41-0.75;P=0.0001)。
经过1年随访,脂质体伊立替康联合方案使mPC患者OS率提高10%。