P53及其信号通路在肿瘤耐药分子机制中的研究进展
- 格式:pdf
- 大小:174.52 KB
- 文档页数:5


p53信号通路在肿瘤发展中的作用研究近年来,肿瘤已经成为全球范围内健康和生命的一大威胁。
与此同时,随着分子生物学和细胞生物学的发展,越来越多的研究集中在了某些关键信号通路的控制上,这些信号通路的异常状态已经被证明与肿瘤的发展和预后密切相关。
p53信号通路就是其中一个最为重要的信号通路,它不仅影响肿瘤的形成和发展,而且还与肿瘤治疗的效果有关。
p53是一个蛋白质,常被认为是“癌细胞中最常见的基因失活突变”。
p53信号通路被广泛认为是细胞凋亡、细胞周期和DNA修复的重要调控器。
它在细胞生长和凋亡中起到关键作用,尤其在肿瘤细胞的凋亡过程中发挥了重要作用。
在正常情况下,p53蛋白的稳定性在细胞中得到控制,它的半衰期很短,只有20-30分钟。
当细胞受到显著的细胞应激或DNA损伤时,p53蛋白的半衰期会显著增加,从而使其在细胞中的水平增加,促进p53信号通路的激活,从而有助于修复损伤的DNA或使细胞转为凋亡状态。
p53信号通路在肿瘤发展中的作用日益受到重视。
p53的缺失或失活在肿瘤形成和发展中扮演了重要角色,而p53信号通路的异常状态则是导致这种失活的重要原因。
研究表明,在约50%的人类实体肿瘤中,p53基因发生了突变,而在剩余类型的肿瘤中,p53信号通路也常常出现异常。
这与肿瘤的发生和发展密切相关,而且有助于理解肿瘤的基本生物学机制。
p53信号通路中的一些基因也被证明在肿瘤的治疗中具有重要意义。
例如,p21Waf1/Cip1是一个CDK抑制剂,可以通过抑制细胞周期的进程,从而促进肿瘤细胞的凋亡。
而Mdm2是一个p53的负向调节因子,可以通过调节p53的稳定性来调控p53信号通路的活性。
近期的一些研究表明,一些Mdm2抑制剂可以恢复失活的p53信号通路并抑制肿瘤的发展。
总之,p53信号通路在肿瘤的形成、发展和治疗中发挥了重要作用,是一项对现代生物学、医学和肿瘤学的重要研究领域。
随着技术的不断进步和研究的深入,相信这些研究成果将在未来为我们提供治疗肿瘤的新思路和新方法。

P53及其信号通路在肿瘤耐药分子机制中的分析研究目的:讨论P53及其信号通路在肿瘤耐药分子機制中的应用,为日后的临床研究提供参考。
方法:在本次研究中,首先对P53自身稳定性与肿瘤耐药性展开分析,将得到的结果作为基础部分,深入开展P53及其信号通路在肿瘤耐药分子机制中的作用分析。
同时,对P53及其信号通路在肿瘤耐药分子机制中的应用进行相应的论述。
结果:P53自身稳定性与肿瘤耐药性集中在P53的自身降解、P53磷酸化等几个方面,经过大量的研究与分析,认为P53及其信号通路在肿瘤耐药分子机制中的作用非常重要。
结论:要想更好的治疗肿瘤患者,必须对肿瘤耐药分子机制展开研究。
经过长久的探究和分析,发现P53在肿瘤的发生发展中占有重要地位,研究P53及其信号通路在肿瘤耐药分子机制中的应用,具有较大的积极意义,日后可深入研究。
标签:P53分子;信号通路;降解;磷酸化;基因突变;肿瘤耐药性近年来,越来越多的医学人员注意到,P53对肿瘤细胞的耐药性具有较大的影响,通过了解P53及其信号通路在肿瘤耐药分子机制中的应用,可进一步制定抵抗耐药性的方案,帮助患者提升治疗效果,减少痛苦。
经过大量的医学研究,已经证实,半数以上的癌症,都存在P53的基因突变,这种现象很可能与P53参与的细胞周期调控以及凋亡有很大关系。
在此,本次研究主要对P53及其信号通路在肿瘤耐药分子机制中的应用展开分析,现做如下综述。
1资料与方法1.1一般资料在本次研究中,首先对P53自身稳定性与肿瘤耐药性展开分析,将得到的结果作为基础部分,深入开展P53及其信号通路在肿瘤耐药分子机制中的作用分析。
同时,对P53及其信号通路在肿瘤耐药分子机制中的应用进行相应的论述。
1.2方法在P53自身稳定性与肿瘤耐药性的研究方面,主要是通过研究P53的自身降解、P53磷酸化、P53基因突变等三个方面来完成。
而在P53及其信号通路在肿瘤耐药分子机制中的应用方面,主要是结合现阶段的医疗情况和需求来完成。

中药调控p53信号通路干预肺癌的作用机制研究进展马倩;李亚;马艺钊;陈锴;王元元;张海龙【期刊名称】《中国药房》【年(卷),期】2024(35)11【摘要】肺癌是最常见的恶性肿瘤,其发病机制复杂、恶性程度高,严重威胁了患者的生命健康。
p53信号通路是影响肺癌进程的重要通路,被众多研究者视为肺癌靶向治疗的潜在靶点之一。
近年来,已有较多研究深入探讨了中药调控p53信号通路干预肺癌的可行性。
基于此,本文系统总结了中药调控p53信号通路干预肺癌的作用机制研究进展,发现清金得生片、调气消积汤、补肺通络解毒方、健脾补肾方及益气扶正解毒方等中药复方及制剂可通过激活p53信号通路,促进肺癌细胞自噬及凋亡,抑制肺癌细胞生长及转移,增强机体免疫功能,发挥抑癌作用;拟人参皂苷Rh2、柴胡皂苷D、重楼皂苷Ⅶ、石斛碱、槐定碱、藤黄酸、雷公藤甲素及雷公藤甲素丁二酸单酯YJ-4等中药单体可通过激活p53信号通路,促进肺癌细胞凋亡,抑制肺癌细胞增殖,调控肺癌细胞周期,发挥抑癌作用。
【总页数】5页(P1403-1407)【作者】马倩;李亚;马艺钊;陈锴;王元元;张海龙【作者单位】河南中医药大学第一附属医院呼吸与危重症医学科;河南中医药大学第一临床医学院;河南中医药大学呼吸疾病中医药防治省部共建协同创新中心/河南省中医药防治呼吸病重点实验室【正文语种】中文【中图分类】R965;R285.5【相关文献】1.中药调控NF-κB信号通路治疗哮喘作用机制的研究进展2.中药调控Toll样受体4信号通路干预心肌缺血作用机制研究进展3.中药调控NF-κB信号通路防治子宫内膜异位症作用机制的研究进展4.中药调控JAK/STAT信号通路干预心肌缺血再灌注损伤作用机制研究进展5.中药调控NF-κB信号通路干预椎间盘退行性变的作用机制因版权原因,仅展示原文概要,查看原文内容请购买。

X raydiffraction(XRD)andenergydispersespectroscopy(EDS)wereemployedtoanalyzetheingredientsandel ementsdistributionofscaffold,respectively.Additionally,thecompressionstrengthofthescaffoldwastestedbymechanicaluniversaltestingmachine.Thebiocompatibilityofthescaffoldandthecellviabilityresearchwerechar acterizedviaCCK 8assayandLive/Deadstaining,respectively,andthecelladhesionwasstudiedbyDPAI/Phal loidinefluorescencestaining.qRT PCRwasemployedtoinvestigatetheexpressionlevelofosteogenic relatedgenesuchasBMP2,RUNX2andCOL1.ALPstainingwascarriedouttomeasuretheosteogenicdifferentiationeffectofBMSCs.Results TheCS β TCPscaffoldwascomprisedofbulkparallel,alignedandthinlamellaswithmanypor ousstructures.β TCPparticleswereevenlydistributedoverCSframeworklayersandtheCS βTCPscaffoldpos sessexcellentelasticpropertyandbiocompatibility,moreover,thecellseededonscaffoldrevealedhighcellviabili tyandcontinuousproliferation.qRT PCRandALPstainingresultsdemonstratedthattheCS β TCPscaffoldcouldinduceosteogenicdifferentiationofBMSC.Conclusion Tosumup,theCS β TCPscaffoldexpresseddesiredme chanicalandbiologicalproperties,andcouldinduceBMSCdifferentiateintoosteoblast,thecompositescaffoldpro videdapromisingstrategyforbonedefectregeneration.Keywords Chitosan;β TCP;compositescaffold;bidirectionallyophilizationtechnique;osteogenicdifferentia tion网络出版时间:2022-06-289:49 网络出版地址:https://kns.cnki.net/kcms/detail/34.1065.r.20220624.1741.020.html基于miR 15a 5p/P53信号通路探讨EMT与肺癌细胞阿霉素耐药的关系魏 东1,辛运超2,刘 博3,容 宇1,李彦明1,郝雁冰1摘要 目的 探讨miR 15a 5p在肺癌细胞对阿霉素(DOX)耐药中的作用,并阐明其与DOX耐药之间的功能和机制联系。
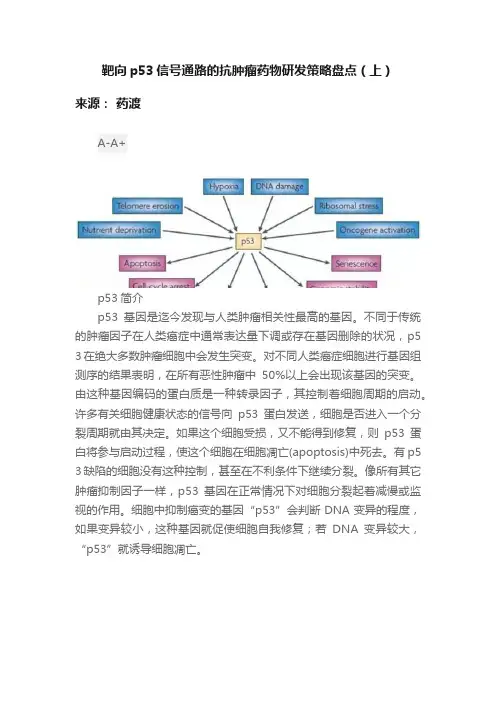
靶向p53信号通路的抗肿瘤药物研发策略盘点(上)来源:药渡A-A+p53简介p53基因是迄今发现与人类肿瘤相关性最高的基因。
不同于传统的肿瘤因子在人类癌症中通常表达量下调或存在基因删除的状况,p5 3在绝大多数肿瘤细胞中会发生突变。
对不同人类癌症细胞进行基因组测序的结果表明,在所有恶性肿瘤中50%以上会出现该基因的突变。
由这种基因编码的蛋白质是一种转录因子,其控制着细胞周期的启动。
许多有关细胞健康状态的信号向p53蛋白发送,细胞是否进入一个分裂周期就由其决定。
如果这个细胞受损,又不能得到修复,则p53蛋白将参与启动过程,使这个细胞在细胞凋亡(apoptosis)中死去。
有p5 3缺陷的细胞没有这种控制,甚至在不利条件下继续分裂。
像所有其它肿瘤抑制因子一样,p53基因在正常情况下对细胞分裂起着减慢或监视的作用。
细胞中抑制癌变的基因“p53”会判断DNA变异的程度,如果变异较小,这种基因就促使细胞自我修复;若DNA变异较大,“p53”就诱导细胞凋亡。
Structure of p53 family members作为转录因子的一员,p53 蛋白结构域分布包括序列特异的DNA 结合结构域,位于氨基酸100-300位间;核定位信号NLS位于氨基酸残基316-325;四聚体寡聚化结构域,定位于氨基酸残基334-356;C-末端非专一DNA调节结构域,同时在碰到DNA损伤时,p53 可以招募其它蛋白质到损伤部位,提供DNA损伤信号。
p53蛋白主要分布于细胞核浆,能与DNA特异结合,其活性受磷酸化、乙酰化、甲基化、泛素化等翻译后修饰调控。
正常的p53蛋白在细胞中易水解,半衰期为20分钟,突变性p53蛋白半衰期为1.4-7小时不等。
Upstream and downstream of p53 signal pathway在某些特定类型的肿瘤细胞亚型中,p53蛋白的突变率尤其高,如卵巢浆液性癌,鳞状细胞癌及三阴性乳腺癌等。

P53通路激活剂的筛选及作用机制研究P53通路激活剂的筛选及作用机制研究引言:P53是一种重要的肿瘤抑制基因,在细胞的DNA损伤和其他应激情况下起到关键作用。
P53通路的异常激活与许多肿瘤的发生和发展密切相关。
因此,研究如何激活P53通路并阻止肿瘤的发生具有重要的临床意义。
本文将探讨P53通路激活剂的筛选方法以及作用机制的研究进展。
一、P53通路激活剂的筛选方法目前,有许多方法可以筛选和鉴定P53通路激活剂,如下: 1. 化学筛选:通过建立化学小分子库,使用细胞模型进行高通量化学筛选,以发现具有激活P53通路的化合物。
其中,Mdm2抑制剂是最常用的筛选对象之一,因为Mdm2是P53的主要负调控因子之一。
2. 基因筛选:通过基因干扰技术(如RNA干扰)或基因敲除技术(如CRISPR/Cas9)对大规模的基因进行筛选,识别与P53通路激活相关的关键基因。
3. 蛋白质筛选:通过蛋白质组学技术,如质谱分析和蛋白质亲和纯化技术,筛选与P53通路激活相关的蛋白质。
二、P53通路激活剂的作用机制P53通路的激活是一个复杂的过程,涉及多种信号分子和调控因子的参与。
1. Mdm2抑制:Mdm2是P53的主要负调控因子,能够结合P53并抑制其活性。
P53通路激活剂的一种常见作用机制是通过抑制Mdm2来释放P53,并从而激活其下游基因的转录。
2. 稳定化P53蛋白:P53通路激活剂还可以通过抑制P53蛋白的降解或增强其稳定性来激活P53通路。
这是通过抑制P53通路的负调控机制,如抑制MDM2或增加PPM1D等方式实现的。
3. 转录调控:激活P53通路的关键步骤是P53进入细胞核并与DNA结合,从而启动下游基因的转录。
P53通路激活剂可以通过促进P53进入细胞核或增强其与DNA结合的能力来增加P53下游基因的转录。
4. 诱导细胞周期停滞和凋亡:P53通路的激活能够引导细胞周期停滞和凋亡,从而抑制肿瘤细胞的生长。
P53通路激活剂可以通过提高P53的活性,增强其在细胞周期调控和凋亡调节中的作用来实现这一效果。


P53基因功能及相关研究进展1979年科学家们首先发现并报道p53基因,并将其定义为一个致癌基因,然而当10年后科学家们揭开p53基因肿瘤抑制子的准确特性后,导致了p53研究的急剧升温。
如今,对p53生物的研究已经持续了30多年,在这30多年里,人们对P53基因有了更深入的了解,但是,人们对其作用以及与癌症的关系却产生了更多的疑问。
对P53功能的研究也成为人们试图攻克肿瘤的一个靶点。
1 P53基因功能1.1 细胞周期调控细胞内P53对各种可能引起肿瘤的异常情况起零耐受作用,可有效地防止细胞的恶性转化。
在DNA受损伤后,细胞分裂被延迟,在细胞周期中从G1-S、G2-M的延迟在大多数机体发生,其中G1期关卡的存在可防止以损伤的DNA为模板进行复制,允许损伤的DNA在关键的细胞功能发生之前修复,可增加细胞存活时间,限制带有可遗传的基因损伤的细胞增殖。
如果损伤的细胞处于G1期早期,P53触发细胞周期限制点,及阻止细胞由G1-S,该限制点抑制细胞周期的作用是通过P21WAF1/CIP1完成,P53蛋白具有与WAF1/CIP1基因启动子序列结合的特性,启动WAF1/CIP1转录,促P21WAF1/CIP1合成,抑制CDK-cyclin复合物,抑制细胞生长,与PCNA结合能抑制PCNA的活性,通过阻止DNA复制的延伸阶段干扰细胞周期的进展,控制S期。
[1]P21WAF1/CIP1还可在细胞周期的后期与cyclinA及B复合物结合,进而阻止进入有丝分裂期。
1.2 P53与细胞凋亡P53触发细胞凋亡,调节一些凋亡相关基因。
肿瘤发生和凋亡之间的联系可由bcl-2的特性看出。
Bcl-2和Bax为同源蛋白,研究表明bcl-2有抑制大部分凋亡途径的特性,而Bax加速细胞凋亡,Bcl-2和Bax可在细胞内形成异源二聚体,Bax本身可形成同源二聚体,细胞凋亡主要取决于同源二聚体和异源二聚体的比例,如Bax/ Bcl-2大于Bcl-2 /Bax细胞就发生凋亡,如Bax/ Bcl-2小于Bcl-2 /Bax细胞凋亡被抑制,bax启动子存在P53结合位点,P53能直接作用于bax基因促进其转录。

恶性肿瘤研究肿瘤耐药机制的研究进展和逆转策略恶性肿瘤是世界范围内一种常见而严重的疾病,其主要特征是肿瘤细胞的无限增殖和侵袭能力。
然而,随着医学的进步,越来越多的癌症患者在接受化疗或靶向治疗后表现出耐药性,这给治疗带来了巨大的挑战。
因此,研究肿瘤耐药机制以及逆转策略成为了当前肿瘤研究的热点领域。
一、肿瘤耐药机制的研究进展肿瘤耐药机制的研究主要包括细胞内信号通路异常和肿瘤微环境对药物的影响。
在细胞内信号通路异常方面,一些基因突变或表达异常导致了细胞凋亡途径的抑制,从而使肿瘤细胞对化疗药物产生耐药性。
此外,肿瘤细胞通过调节DNA修复功能和泵运输蛋白的活性来逃避药物的杀伤作用。
而肿瘤微环境则通过增加血管生成和诱导免疫抑制等方式改变了治疗的疗效。
二、肿瘤耐药机制的逆转策略逆转肿瘤耐药机制是战胜肿瘤耐药性的重要手段之一。
一种常见的逆转策略是靶向特定信号通路或分子,以恢复细胞的凋亡功能。
例如,Biopterin在乳腺癌化疗中起到抗耐药作用。
此外,还可以通过联合用药的方式延缓耐药性的产生,如将化疗药物与有效的免疫治疗相结合。
最近,免疫治疗被广泛研究,并取得了一定的突破。
三、新兴研究领域除了传统的耐药机制和逆转策略之外,还有一些新兴的研究领域值得关注。
比如,肿瘤免疫治疗的发展将重点放在了治疗肿瘤转移和提高复发患者的生存率上。
此外,一些新的诊断方法和技术的出现,如基因组学、转录组学和蛋白质组学的应用,有助于对个体化的治疗进行精准匹配。
这些研究的出现为我们深入了解肿瘤耐药机制和开发逆转策略提供了新的思路和方法。
总结:肿瘤耐药机制的研究和逆转策略的探索是当前肿瘤研究的重点之一。
通过了解肿瘤耐药机制,我们可以针对不同的耐药机制提出相应的逆转策略,从而提高患者的疗效和生存率。
此外,新兴的研究领域的出现为我们解决肿瘤耐药方面的问题提供了更多的可能性。
相信随着科学技术的不断发展,我们能够逐渐攻克恶性肿瘤耐药问题,为患者带来更好的治疗效果。

p53信号通路在乳腺癌中的作用研究乳腺癌是世界范围内最常见的恶性肿瘤之一,占女性恶性肿瘤总发病数的15%-20%。
尽管乳腺癌的发病原因目前尚不完全清楚,但是长期以来,有许多研究表明,p53信号通路的异常活化与乳腺癌的发生及恶化密切相关。
本文将主要从p53信号通路在乳腺癌中的作用机制进行深入探讨。
p53是一种核心转录因子,在人类细胞中广泛存在,并在许多基本的细胞生物学过程中起着非常重要的作用。
p53的主要作用是识别并修复DNA的损伤,当DNA发生严重损伤或受到强化的致癌物质作用时,p53被激活,促进细胞周期的停滞并尽可能避免受损的细胞进一步增殖。
然而,如果p53的信号通路受到致癌因子的干扰,p53的功能将被削弱,从而导致癌症的发生。
近年来许多研究表明,在乳腺癌中,p53信号通路的异常活化起着至关重要的作用。
p53信号通路在乳腺癌中的失调p53的抑癌作用来自于其对细胞周期的控制能力。
正常情况下,p53可以通过促进周期的停滞和DNA修复来防止已损伤的细胞进一步复制。
但是,在乳腺癌细胞中,p53通常被致癌因子的突变,改变成为一个失活态,导致细胞周期不受控制,从而促进癌症的进展。
这种失活态的p53不仅阻碍正常的DNA修复和细胞周期控制,而且还具有促进诱导凋亡和稳态性的“垃圾邮件”基因表达的能力。
实际上,有人发现,在72%的混合型或低级别的乳腺癌中,p53基因发生突变,但有时也会在高级别乳腺癌中出现。
p53信号通路在乳腺癌中的作用p53属于转录因子家族,在细胞周期控制和DNA损伤修复中都扮演着重要角色。
乳腺癌细胞中的p53信号通路失调导致乳腺癌的发生和恶化。
这种失调的作用方式与肾上腺皮质激素,白三烯类化合物和雌激素等外源性因素的作用密切相关。
p53信号通路在乳腺癌中的作用方式是通过促进细胞周期的停滞和DNA损伤修复来防止细胞不受控制的分裂。
一旦乳腺癌细胞的DNA受到致癌物质的损伤或突变,p53将被激活并注入细胞周期,这有助于防止其继续复制和扩散。
p53调控信号通路的研究进展在人类细胞生长、分裂和死亡的过程中,有一种信号通路被广泛认为是最为重要的,那就是p53调控信号通路。
虽然这种通路的基本原理已经被研究了几十年,但是仍然存在许多未知的问题。
近年来,一些新的研究方法和技术的出现,使得p53调控信号通路的研究进展得以快速推进。
p53是一个常见的蛋白质,它在正常的细胞分裂、DNA损伤和其他应激情况下发挥重要作用。
当p53被刺激时,它会通过一系列机制调控其他蛋白的表达,其中最为重要的就是调控细胞周期的基因表达。
具体来说,p53可以抑制细胞周期蛋白的表达,从而在DNA损伤过程中使细胞进入稳态停滞以便进行修复。
此外,p53还可以诱导细胞凋亡或细胞老化,以防止受到严重损伤的细胞进一步扩散。
尽管p53已经被研究了几十年,但是其调控机制目前仍然不十分清楚。
多数情况下,p53的活性是通过蛋白磷酸化调控的。
当p53被磷酸化时,其活性会被激活,从而开始调节目标基因的表达。
然而,p53可以被多个不同的蛋白磷酸化,每种磷酸化情况可能都会对其调控效果产生不同的影响。
因此,研究p53的磷酸化在p53调控信号通路的研究中是十分重要的。
近年来,一些新的研究方法和技术的出现,使得p53调控信号通路的研究进展得以加快。
例如,一些研究人员利用高通量技术筛选了一系列与p53功能密切相关的因子,从而更深入地了解了p53的调控模式。
此外,其他研究人员在细胞中人为诱导p53的活性,从而实现了对p53调控效应的研究。
尽管p53调控信号通路仍然存在许多未知的问题,但是各种新的研究方法和技术的出现为其研究提供了更多的可能性。
相信在不久的将来,我们将深入了解p53调控信号通路的更多细节,从而更加深入地了解细胞的生长、分裂和死亡过程。
p53及耐药相关基因的表达与非小细胞肺癌化疗耐药性的研究孙超;时会云;袁东朋【摘要】目的探讨p53突变与耐药相关基因表达的相关性及其与肺癌化疗耐药的关系.方法免疫组化检测60例非小细胞肺癌组织的p53和耐药相关蛋白P-gp、MRP、LRP、GST-π的表达并分析其相关性及其与肺癌化疗耐药的关系.结果 P-gp、MRP、LRP、GST-π、p53阳性率分别为53.3%、50.0%、75.0%、73.3%、68.3%.LRP在腺癌中表达最高,p53在鳞癌中表达最高.p53的表达与肿瘤细胞分化程度、有无淋巴结转移和TNM分期密切相关,其余4种耐药相关蛋白表达差异均无统计学意义(P>0.05).p53和一种或一种以上耐药相关蛋白共表达率达94.8%,且p53与P-gp、GST-π的表达存在正相关性(P均<0.05).p53蛋白的表达与化疗疗效显著相关,p53阴性化疗有效率(60.5%)明显高于p53阳性者(28.3%,P<0.05).结论肺癌组织p53突变与耐药相关蛋白的表达有相关性,p53结合耐药相关蛋白检测可以预示患者的化疗耐药性,对个体化化疗方案的制定具有指导意义.【期刊名称】《海南医学》【年(卷),期】2010(021)014【总页数】4页(P45-48)【关键词】非小细胞肺癌;免疫组织化学;p53基因突变;耐药相关基因【作者】孙超;时会云;袁东朋【作者单位】东海县人民医院胸外科,江苏,东海,222300;东海县人民医院胸外科,江苏,东海,222300;东海县人民医院胸外科,江苏,东海,222300【正文语种】中文【中图分类】R734.2化疗是肺癌非手术治疗的一线选择,研究证实以顺铂为基础的联合化疗是治疗进展期非小细胞肺癌(NSCLC)的基本方案,但有效率亦仅 25%-30%,化疗反应率低与肿瘤细胞对联合化疗产生原发或继发性耐药有关[1]。
随着对肿瘤发生及联合化疗分子机制的认识,已证实一些肿瘤分子标志的改变与化疗敏感性有关,如:P-糖蛋白 (P-glycoprotein,P-gp)、多药耐药相关蛋白 (Multidrug resis-tance-associated protein,MRP)、肺耐药相关蛋白(Lung resistance-associated protein,LRP)、谷胱甘肽转移酶(Glutathione-S-transferase-pi,GST-π)等多种耐药相关的酶和蛋白。
靶向p53的抗肿瘤药物研究进展
张明玲;刘珊;刘彦杰;王树林
【期刊名称】《国际药学研究杂志》
【年(卷),期】2018(45)2
【摘要】编码蛋白P53(肿瘤蛋白53,TP53)的基因具有控制细胞周期、细胞凋亡及控制新生血管形成等功能.该基因的突变发生于>50%癌症患者中,在一些特定的肿瘤细胞亚型中,该基因突变频率尤高.p53基因突变能明显促进恶性肿瘤的发生发展,从而显著增加患癌风险,因此,p53已成为癌症研究中一个很有吸引力的药物靶点.针对p53基因突变的药物研究主要有两方面:直接作用于突变型p53基因(恢复
p53野生型活性及诱导突变型P53蛋白的降解);间接作用于突变型P53蛋白.本文主要讨论p53的研究现状,靶向p53的抗肿瘤药物研究进展及面临的困难.
【总页数】6页(P88-93)
【作者】张明玲;刘珊;刘彦杰;王树林
【作者单位】266003青岛,中国海洋大学医药学院;266061青岛,青岛海洋生物医药研究院;266003青岛,中国海洋大学医药学院;266003青岛,中国海洋大学医药学院
【正文语种】中文
【中图分类】R341
【相关文献】
1.癌症中p53失活的分子机制和靶向p53的抗癌药物研究进展 [J], 周建林
2.分子靶向抗肿瘤药物皮肤不良反应研究进展 [J], 石艾秀;曹双林
3.蛋白酶激活受体在肿瘤血管生成中的作用及其靶向抗肿瘤药物研究进展 [J], 王明;张亮;毕谆;肖婷;杨诚
4.质子泵抑制剂对口服靶向抗肿瘤药物吸收影响的研究进展 [J], 徐银莹;陆子红;李琪;陆牡丹;姜孙旻
5.靶向突变型p53的抗肿瘤药物研究进展 [J], 丁笠;张新跃
因版权原因,仅展示原文概要,查看原文内容请购买。
肿瘤多药耐药机制的研究进展肿瘤多药耐药(MDR)是指肿瘤细胞同时对多种化疗药物产生耐药性的现象。
这种现象使得肿瘤疾病难以根治,严重影响了治疗效果和患者的生存率。
因此,研究肿瘤多药耐药的机制对于开发新的治疗策略和提高疗效具有重要意义。
本文将介绍肿瘤多药耐药的研究进展。
一、肿瘤多药耐药机制的分类1. 药物外排泵:细胞膜上的多种蛋白质泵,如肿瘤相关蛋白(P-gp)、多药抗性相关蛋白(MRP)、肿瘤抑制基因相关蛋白(BCRP)等,通过主动转运药物分子,将其从细胞内排出。
这些泵的过度表达导致药物浓度降低,从而减少了药物的疗效。
2.路径逃逸:肿瘤细胞通过启动细胞生存途径,如PI3K/AKT、MAPK和NF-κB等信号通路,以逃避化疗药物诱导的细胞凋亡。
在这些逃逸通路中,关键信号分子的过度表达或异常激活可以降低化疗药物对细胞的杀伤作用。
3.DNA损伤修复:肿瘤细胞通过激活DNA损伤修复系统,修复化疗药物引起的DNA损伤,从而减少细胞对药物的敏感性。
这种机制包括核苷酸顺式修复(NER)和核苷酸不匹配修复(MMR)等。
4. 细胞凋亡抑制:肿瘤细胞通过下调或缺失凋亡相关基因(如P53)来抑制化疗药物引起的细胞凋亡。
此外,一些细胞凋亡抑制蛋白(如Bcl-2家族蛋白)的过度表达也可以阻碍细胞凋亡的发生。
1.肿瘤多药耐药基因组学:利用高通量技术如基因芯片、全基因组测序和单细胞组学等,揭示了肿瘤多药耐药相关基因的变异和表达模式。
这些研究为深入理解肿瘤多药耐药的机制和寻找新的治疗靶点提供了重要的依据。
2. 靶向肿瘤多药耐药的新型药物:目前,研究人员正在开发一系列靶向肿瘤多药耐药机制的新型药物。
例如,研究人员发现通过抑制P-gp和MRP泵的表达或活性,可以增强化疗药物的疗效。
此外,靶向途径逃逸、DNA损伤修复和细胞凋亡抑制等机制的药物也在不断研究中。
3.免疫治疗:免疫治疗作为一种新型的治疗策略,已经显示出在肿瘤多药耐药中具有潜在的应用前景。
P53基因的研究进展P53基因是人类体内最重要的抑癌基因之一,也是最早被发现和研究的基因之一、它的发现和研究为我们深入了解癌症的发生和发展提供了重要线索。
近年来,对P53基因的研究取得了一系列重要的进展。
本文将对这些研究进展进行综述,并展望未来的研究方向。
首先,研究人员对P53基因的结构和功能进行了深入的研究。
P53基因编码的蛋白质是一种转录因子,能够调控许多基因的表达,从而影响细胞的增殖、凋亡和修复等生命活动。
研究人员发现,P53蛋白质的活性和表达水平在机体受到DNA损伤或其他外界刺激时会显著上调,以保护细胞免受进一步的损伤。
此外,研究人员还发现,P53蛋白质的突变与多种肿瘤的发生和发展密切相关。
通过深入了解P53基因的结构和功能,我们可以更好地理解癌症的发生机制,为癌症的预防和治疗提供理论依据。
其次,研究人员对P53基因与其他基因的相互作用进行了研究。
P53蛋白质能够与许多其他蛋白质相互作用,形成复合物,从而调控细胞的生命活动。
研究人员发现,P53基因与一些肿瘤抑制基因(如BRCA1和BRCA2)之间存在着相互作用,这些基因调控细胞的DNA修复过程。
这些发现揭示了P53基因在维持细胞的基因稳态和DNA完整性方面的重要作用。
此外,研究人员还对P53基因在肿瘤的治疗中的应用进行了深入研究。
由于P53基因在多种肿瘤中发生突变,导致了P53蛋白质功能的丧失,因此针对P53的治疗策略成为了一个研究热点。
目前,研究人员已经开发了多种针对P53的治疗手段,包括基因治疗、小分子药物和免疫疗法等。
这些新的治疗方法有望为那些患有P53突变的肿瘤患者提供更有效的治疗选择。
最后,对P53基因的研究还面临一些挑战。
一方面,由于P53基因的复杂性和多样性,对其进行研究需要耗费大量的时间和资源。
另一方面,P53的功能和调控机制尚未完全阐明,对其进一步的研究仍然具有挑战性。
综上所述,P53基因的研究已经取得了一系列重要的进展。