NCCN恶性胆管癌的诊治
- 格式:ppt
- 大小:2.04 MB
- 文档页数:17

NCCN胆道癌临床实践指南2020.1版更新解读星期五2020年3月27日不忘初心,砥砺前行!致医生同行:欢迎订购《指南解读》医生会员致通情达理的癌症家庭:【肿瘤管家】全程协助患者抗癌!注:有咨询需求者,请加《指南解读》主编黄医生微信30842121;经济困难者酌情减免!胆道癌指南更新解读目录2020年3月23日,美国国立综合癌症网络更新了《NCCN肝胆癌临床实践指南》,《指南解读》创始人、主编黄志锋医生率先对其中的“胆道癌”更新内容进行解读(有关肝细胞肝癌更新解读内容,请点击蓝色字体查阅),与大家分享,具体如下:胆道癌“胆道癌篇”进行了广泛的修改和更新。
每个章节的标题都进行了修改,分别标注为“胆道癌——胆囊癌/肝内胆管癌/肝外胆管癌”,并且将原来各个章节中的一些内容移动、合并和压缩进入新增的3个章节(影像学检查原则[BIL-A]、放射治疗原则[BIL-B]和系统治疗原则[BIL-C]),这些章节包含胆囊癌、肝内胆管癌和肝外胆管癌的治疗建议。
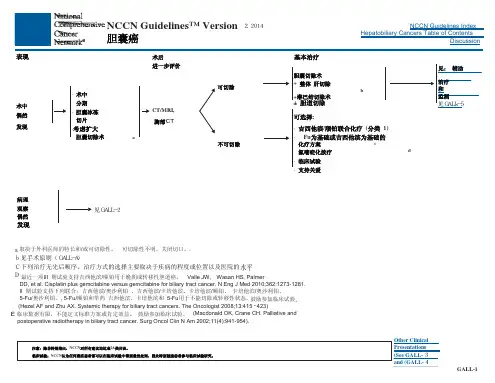
1.影像学检查原则(BIL-A)●PET/CT检测区域淋巴结转移的灵敏度有限,但具有高度的特异性。
对于CT扫描或MRI检查中无法明确的病变,可以考虑行PET/CT 检查。
PET/CT的敏感性有限,但特异性高;如果检查结果模棱两可,可以考虑行PET/CT检查。
●新增1条:当怀疑或证实肝内胆管癌的诊断时,首选延迟期成像。
●新增1篇参考文献:Lamarca A, Barriuso J, Chander A, et al. 18F-fluorodeoxyglucose positron emission tomography (18FDG-PET) for patients with biliary tract cancer: Systematic review and meta-analysis. J Hepatol 2019 Jul;71(1):115-129.2.放射治疗原则(BIL-B)●新增1条:姑息性EBRT适用于控制症状和/或预防转移性病灶(例如骨转移或脑转移)导致的并发症。

肝外胆管癌和胆襄癌临床诊疗指南(2024〉胆道恶性肿瘤(BTC)是一种起源于胆逍的高度俀袭性的恶性肿瘤。
它包括肝内胆管癌(ICC�肝外胆管痉(ECC)以及胆衮癌(GC),在消化道恶性肿瘤中约占3%。
尽笸在肿瘤学领域取句了显茗进展,但由于这些肿瘤发现时多为晚期且具有忘度侵袭性,因此预后通常较差。
BTC常在早期就出现肿瘤转移,其发病率和死亡率均呈上升趋势.对于那些局部病灶可切除的患者,手术往往能提供品佳的治疗效果.然而,即使接受根治性手术,其术后复发的风险依然很高因此,BTC患者越来越多地采用多模式的治疗策略,包括手术切除系统治疗(如分子靶向药物、静脉化学治疗、免疫治疗)以及与局部治疗组合的方案等.鉴于治疗的复杂性和外科诊疗技术的不断进步,本文特别解读了品新实践指南中关千BTC(尤其是ECC 和GC)外科治疗的要点以及图手术期治疗的注怠幸项.1、BTC的评估要点1.1 ECC的诊断与分期ECC按解剖位岂分为肝门部胆管癌(pCCA)或远端胆官癌(dCCA),其中起源千肝总管的pCCA亦称Klatskin肿瘤,dCCA则始千胆哀管汇合部以下的胆总管。
鉴于ICC和ECC在生物学特性上存在差异,它们应作为独立痉种进行治疗.ECC患者通常因胆道梗阻而表现出腹痛和黄疽.dCCA可通过胰十二指肠切除术治疗,而pCCA则通常需要更大范图的肝切除和肝外胆管切除.对pCCA患者而言,术前胆道引流有助千恢复肝功能并降低术后并发症的发生率.如果在大范图肝切除术前未进行胆道引流的相关治疗,其术前胆红素水平的升忘可能会增加术后并发症的发生率和死亡率.在考虑pCCA 行大范图肝切除术时,术前引流对将来保证足够的FLR尤为重要。
欧洲肿瘤内科学会(ESMO)指南过议:在引流前蒂完成影像学诊断,因为支架或引流笸可能干扰对病变范国的判断.美国国立综合癌症网络(NCCN)指南建议:当临床医生担心FLR不足或患者蒂要门静脉栓室时应进行术前引流。

胆管癌的诊断与介入治疗胆管癌是除肝细胞癌外的肝脏第二大恶性肿瘤。
从组织学类型上说主要表现为腺癌。
从组织形态上分为肿块型、管内浸润型和管周生长型肿块型较为常见。
根据肿瘤位于胆管的位置不同,分为肝内胆管癌(Intrahepatic cholangiocarcinoma)、肝门胆管癌(Hilar cholangiocarcinoma)和肝外胆管癌(Extrahepatic cholangiocarcinoma)。
肝内胆管癌位于肝内左右肝管二级及二级以上分支;肝门胆管癌位于肝内的左右肝管的一级分支或肝总管;肝外胆管癌位于胆总管,分别占胆管癌的10%,50%和40%。
在临床上,肝内胆管癌发现时常常表现为较大的肿块,在其早期不引起相关临床症状;肝外胆管癌常在其早期出现黄疸,病灶多且较小。
在传统观念中,外科切除和肝移植在治疗没有血管侵犯和淋巴结转移的患者中具有优先性。
因为其是可治愈该病的方法。
外科切除达到治愈要满足以下条件:肿块全部切除,切缘阴性,并且梗阻缓解和胆肠吻合顺畅。
部分肝内胆管癌,不需要考虑胆汁的因素,直接彻底损毁肝内肿块,可达到治愈肿瘤的目的。
病因胆管癌常常不像肝细胞癌那样有明确的病因,又与肝细胞癌的病因相似,表现为散发。
近来,病毒性肝炎和肝硬化被认为是形成胆管癌的风险因素。
在西方国家,丙型病毒性肝炎流行,而在亚洲国家,乙型病毒性肝炎流行。
来自国外的有关研究显示丙型肝炎与肝内胆管癌有较强的相关性,而来自国内有关研究则显示乙型肝炎与肝内胆管癌有较强的相关性。
这些研究中都显示肝硬化是形成胆管癌的风险因素。
但总体上说病毒性肝炎和肝硬化是肝内胆管癌的致病因素,但不是那么强烈。
原发性硬化性胆管炎(Primary sclerosing cholangitis)与胆管癌之间有着比较确切的关系。
在原发性硬化性胆管炎患者的一生中有5%到10%的机会患胆管癌。
并且有50%的患者是在诊断为原发性硬化性胆管炎24个月的时候进展为胆管癌的。

胆管癌的诊断与术前评估胆管癌是少见恶性肿瘤。
胆管癌的诊断与术前评估需要完整的临床资料,包括:肝胆影像学检查、肿瘤标志物和组织学检查。
手术完全切除病灶是胆管癌治愈的唯一机遇,其结果依托于精湛的技术和病人的选择,可是能够手术切除的患者较少。
胆管癌的最正确处置方法涉及术前精准的诊断、临床分期和评估。
1 胆管癌的分类依照解剖位置,胆管癌可分为肝内或肝外胆管癌。
那个分类是合理的,因为二者在临床、病理和流行病学方面存在不同。
但是,大约有60%~70%的胆管癌起源于肝门部,这种肿瘤被描述为肝门部胆管癌(klatskin tumors);20%~30%来自胆总管远侧;5%~10%起源于肝实质周边的肝内胆管[1]。
国际疾病分类(ICD)编码将起源于肝内小胆管的肝内胆管癌与肝细胞性肝癌一同归类于原发性肝癌[2,3]。
1975~1999年流行病学调查说明:92%的Klatskin肿瘤被归类为肝内胆管癌[4]。
目前,胆管癌按解剖学可分为肝内、远侧肝外或肝门部。
肝门部病变采纳Bismuth分型描述为以下5类:Ⅰ型:左右肝管汇合以下;Ⅱ型:位于左右肝管汇合部;Ⅲa、Ⅲb型:阻塞总肝管及右肝管或左肝管;Ⅵ型:呈多中心发生或侵犯汇合部和左右肝管[5]。
2 胆管癌的分子机制及其标志物在胆管癌中已发觉一些肿瘤基因和抗癌基因突变[6]。
21%~100%的病例K-ras癌基因异样表达,在受累患者的胆汁和胰液中也已检测到K-ras和P53突变体[7,8]。
在胰、胆管肿瘤的诊断中,K-ras 和P53突变分析并非比常规细胞病理学优越,但二者结合分析能增加组织活检和胆汁标本的灵敏性[7,8]。
已有报导原癌基因Bcl-2的过表达能够降低胆管癌细胞系的凋亡,尽管人胆管癌不表达Bcl-2,但能表达其他一些抗凋亡蛋白如Mcl-1和Bcl-xl[9]。
已经在原发性硬化性胆管炎(PSC)相关的胆管癌中检测到点突变引发的细胞周期调剂因子P16INK4a和P14ARF启动子甲基化[10]。

中国抗癌协会胆道恶性肿瘤靶向及免疫治疗指南(2023)要点胆道恶性肿瘤包括肝内胆管癌、肝外胆管癌及胆囊癌,约占所有消化道恶性肿瘤3%,近年来发病率呈上升趋势。
50%的胆道恶街中瘤病人在确诊时已为进展期生存期<1年。
仅有10%左右的病人就诊时具有手术机会,术后1年内的转移复发率高达67%,5年生存率为5%〜15%o第一部分分子诊断篇1胆道肿瘤病理组织学分类胆道恶性上皮性肿瘤构成了胆道恶性W瘤的主要类型(表1),胆管腺癌或胆囊腺癌占主要部分。
2019年WHO病理学分类标准中将胆囊及胆管系统腺瘤、囊腺瘤、乳头状瘤等良性肿瘤归于癌前病变。
2胆道恶性W瘤分子病理学研究进展2.1 胆管系统不同区域起源上皮性W瘤间的分子特征存在较显著差异2.2 起源同区域的胆道恶性W瘤之间分子特征存在差异2.3 流行病学因素对胆道恶性肿瘤分子特征的影响2.4 疾病进程对胆道恶性肿瘤分子特征产生的影响3胆道恶,的中瘤潜在治疗获益的分子靶点研究进展截至2023-12-01,已有多个药物在我国获批应用于胆道恶性W瘤或其他实体肿瘤的临床靶向治疗。
胆道恶街中瘤靶向治疗相关分子靶点变异频率及检测方法总结见表2o4胆道恶性W瘤免疫治疗响应相关生物标记物目前,包括程序性死亡配体-1(PD-11履白表达、肿瘤突变负荷(TMBX错配修复缺陷(dMMR)和微卫星不稳定性(MSI)等在内的多种生物标记物已被证实与实体肿瘤免疫治疗获益相关,在胆道恶性肿瘤方面也有多项研究评估免疫治疗相关分子标记物的报道。
4.1 MS1和dMMR4.2 PD-11表达4.3 TMB5肿瘤高通量分子检测要点按照我国《医疗机构临床基因扩增检验实验室管理办法》(卫办医政发〔2010〕194号),对我国境内肿瘤人群实施高通量基因测序的相关机构需通过省级卫生行政部门相应技术审核和登记备案后,方可开展肿瘤高通量基因测序工作。
肿瘤高通量基因测序全流程管理每个环节,包括样本质控或质量保证、样本预处理、接头连接、预扩增、基因组合靶区的捕获、靶区纯化、扩增文库构建质控定量后行高通量基因测序等,均应有标准的操作规程和完整的操作记录。


胆道系统恶性肿瘤NCCN最新指南解读单钰莹;于茜;陆才德【期刊名称】《现代实用医学》【年(卷),期】2017(029)007【总页数】4页(P843-846)【作者】单钰莹;于茜;陆才德【作者单位】315041宁波,宁波市医疗中心李惠利东部医院;315041宁波,宁波市医疗中心李惠利东部医院;315041宁波,宁波市医疗中心李惠利东部医院【正文语种】中文【中图分类】R735.8美国国立综合癌症网络(NCCN)指南是临床医生进行肿瘤诊断、制定治疗方案和手术管理的重要依据。
2017版NCCN胆道系统恶性肿瘤指南对外科术中处理、术后治疗等进行了一些修改,着重强调了切缘阴性的重要性和多学科团队(MDT)在临床上诊断复杂疾病时起到的重要作用。
本文旨在对胆道系统恶性肿瘤NCCN最新指南进行解读,现报道如下。
胆囊癌在所有胆道癌中最常见,绝大多数是腺癌,发病率随年龄的增长而不断增加。
女性比男性更容易发病,伴有慢性炎症的胆囊结石是胆囊癌发病的危险因素,且其危险度随胆囊结石的增大而增加。
胆囊癌的特征是易于发生局部组织侵袭和血管侵犯,广泛的区域淋巴结转移和远处转移。
比起肝门胆管癌,胆囊癌中位生存时间、肿瘤复发时间、复发后生存期都更短。
由于胆囊癌病情复杂多变,预后差,新版指南多处强调MDT在诊治决策中的作用。
1.1 诊断由于胆囊癌侵袭性高,进展迅速,诊断时往往已达晚期。
胆囊癌症状与胆绞痛及慢性胆囊炎的临床表现类似,早期诊断困难,往往是因良性胆囊疾病或胆囊结石行胆囊切除术的术后病理学检查时意外发现。
其他可能的临床表现包括超声检测到可疑的肿块或胆道梗阻伴有黄疸或慢性右上腹痛。
胆囊癌患者出现黄疸通常提示预后不良,出现黄疸与无黄疸患者相比,疾病特异性生存期明显缩短(6个月vs 16个月,<0.05),可切除率低(7%),手术切缘阴性(5%)概率更低。
出现胆囊肿块或疑似胆囊癌患者的初步处理应包括肝功能检查和肝储备功能评估。
推荐使用胸部、腹部和盆腔的B超、CT或磁共振成像(MRI)来评估肿瘤是否穿过胆囊壁、是否存在淋巴结和远处的转移及转移程度,并检测肿瘤直接侵袭其他器官/胆道系统或主要血管的程度。

胆管癌治疗方案胆管癌是一种恶性肿瘤,常常给患者和家庭带来了巨大的压力和困惑。
治疗胆管癌需要综合考虑多个因素,如患者的健康状况、癌症的分期和类型等。
下面将探讨一些常见的胆管癌治疗方案。
手术是胆管癌治疗的主要方法之一。
根据癌症的分期和位置,手术的范围可以从局部切除到全面切除胆管和肝脏。
对于早期胆管癌,局部切除手术往往可以达到良好的治疗效果。
但对于晚期或复发的胆管癌,全面切除手术可能是更合适的选择。
手术后,常常需要化疗或放疗来杀灭残留的癌细胞。
化疗是胆管癌治疗中常用的辅助疗法之一。
通过给予患者抗癌药物,化疗可以杀灭或抑制癌细胞的生长。
在胆管癌治疗中,常用的化疗药物包括顺铂、卡培他滨和氟尿嘧啶等。
化疗可以在手术前或手术后进行,也可以单独作为一种局部治疗方法。
然而,化疗往往伴随着一系列的副作用,如恶心、呕吐和免疫系统的抑制等。
放疗是另一种常见的辅助治疗方法,在胆管癌治疗中也被广泛应用。
通过高能射线或其他形式的辐射,放疗可以杀死癌细胞或阻止其生长。
放疗通常会在手术前或手术后进行,以增加手术的成功率或降低复发的风险。
然而,放疗也可能导致一系列的副作用,如疲劳、皮肤炎症和口腔炎等。
靶向治疗是近年来进展迅速的一种治疗方法,在胆管癌治疗中也有着重要的应用。
通过抑制乳突状胰凝乳酶样胰蛋白酶-4(MEP3K)等靶点,靶向药物可以干扰癌细胞的生长和扩散。
目前,一些靶向药物已经得到了FDA的批准,如索拉非尼和厄洛替尼等。
虽然靶向治疗对于一些患者来说可能是有效的选择,但其疗效仍存在一定的局限性。
免疫治疗是近年来备受关注的一种治疗策略,在胆管癌治疗中也被研究和应用。
免疫治疗通过增强患者免疫系统的抗癌能力,来抑制癌细胞的生长和扩散。
目前,一些免疫检查点抑制剂已经在临床试验中显示出一定的活性和疗效。
然而,免疫治疗在胆管癌治疗中的地位仍在探索中,并需要进一步的研究和临床实践来明确其作用和潜力。
综上所述,胆管癌治疗方案多样化,需要根据患者的具体情况和医生的建议来选择合适的方法。
