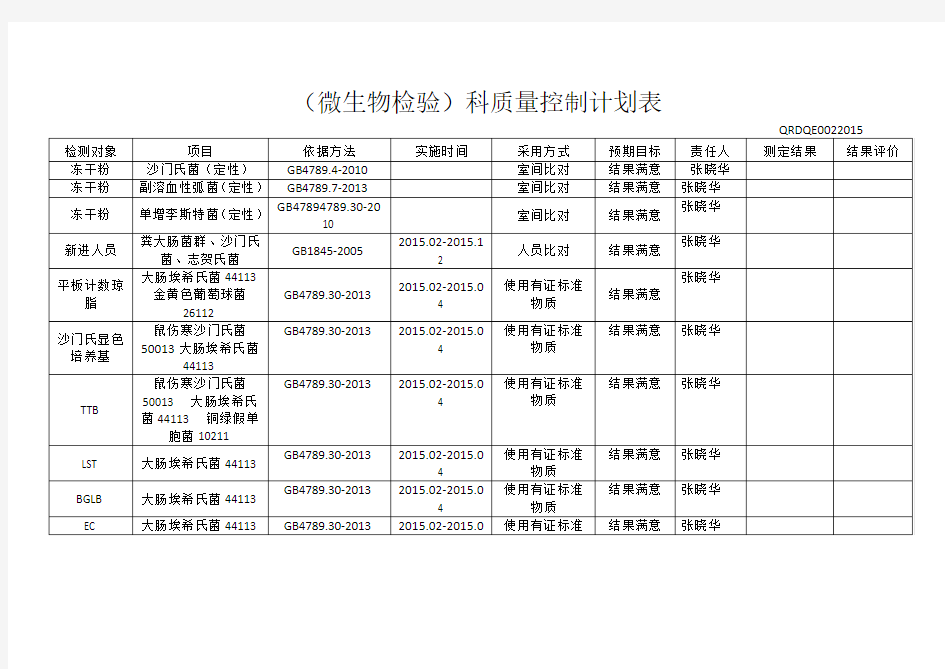

(微生物检验)科质量控制计划表
备注:1、采用方式包括:、室间比对、质控图、使用有证标准物质、留样再测、人员比对、平行样、加标回收等
2、预期目标:结果满意。
要求:
1、各相关科室质量控制计划应当具有针对性,覆盖专业的各子领域,参加能力验证的领域范围、频次应当满足有关资质认定和认可考核要求(参见CNAS-RL02《能力验证规则》)。
2)、质控方式(能力验证、室间比对、质控图、使用有证标准物质、留样再测、人员比对、平行样、加标回收等)尽量多样性。3)、各科室要对实验试剂、耗材(实验用水、培养基等)进行实验前验收、质控。
4)、各科室要制定的质控项目结果判定要符合标准/规范。5)、如测定结果不符合预期目标(结果满意)要进行原因分析,并进行整改,重新测定,直至结果满意。
6)、各科室年终要对质控项目、方式、结果进行汇总、分析、评价,并形成报告,以确定明年质控重点
7)、2月1日前《科室质量控制计划表》上报质管科
9203药品微生物实验室质量管理指导原则 药品微生物实验室质量管理指导原则用于指导药品微生物检验实验室的质量控制。 药品微生物的检验结果受很多因素的影响,如样品中微生物可能分布不均匀、微生物检验方法的误差较大等。因此,在药品微生物检验中,为保证检验结果的可靠性,必须使用经验证的检测方法并严格按照药品微生物实验室质量管理指导原则要求进行检验。 药品微生物实验室质量管理指导原则包括以下几个方面:人员、培养基、试剂、菌种、环境、设备、样品、检验方法、污染废弃物处理、检测结果质量保证和检测过程质量控制、实验记录、结果的判断和检测报告、文件等。 人员 从事药品微生物试验工作的人员应具备微生物学或相近专业知识的教育背景。 实验人员应依据所在岗位和职责接受相应的培训,在确认他们可以承担某一试验前,他们不能独立从事该项微生物试验。应保证所有人员在上岗前接受胜任工作所必需的设备操作、微生物检验技术等方面的培训,如无菌操作、培养基制备、消毒、灭菌、注平板、菌落计数、菌种的转种、传代和保藏、微生物检查方法和鉴定基本技术等,经考核合格后方可上岗。 实验人员应经过实验室生物安全方面的培训,保证自身安全,防止微生物在实验室内部污染。 实验室应制定所有级别实验人员的继续教育计划,保证知识与技能不断的更新。 检验人员必须熟悉相关检测方法、程序、检测目的和结果评价。微生物实验室的管理者其专业技能和经验水平应与他们的职责范围相符,如:管理技能、实验室安全、试验安排、预算、实验研究、实验结果的评估和数据偏差的调查、技术报告书写等。 实验室应通过参加内部质量控制、能力验证或使用标准菌株等方法客观评估检验人员的能力,必要时对其进行再培训并重新评估。当使用一种非经常使用的方法或技术时,有必要在检测前确认微生物检测人员的操作技能。
浅析生活饮用水微生物检验质量控制 发表时间:2018-05-07T09:54:06.903Z 来源:《健康世界》2018年4期作者:孙菡昕 [导读] 探讨并研究生活饮用水微生物检验质量影响因素 孙菡昕 香坊区卫生监督所 150030 摘要:目的探讨并研究生活饮用水微生物检验质量影响因素,并提出质控措施。方法选取2017年1—12月期间在疾病预防控制中心进行的960件生活饮用水微生物检验为研究对象,回顾分析检测报告,分析影响检测结果的因素,并提出针对性的质量控制措施。结果生活饮用水微生物检验影响因素主要包括环境因素、实验设备因素、人为因素。结论分析生活饮用水微生物检验质量影响因素,并采取有效地措施加强对生活饮用水微生物检验质量控制,具有重要的意义。 关键词:生活饮用水;微生物检验;影响因素 [Abstract] Objective To explore and study the factors affecting the quality of microbiological test in drinking water,and to put forward the quality control measures. Methods from 2017 to December,960 microbiological tests of drinking water in the center for Disease Control and prevention from 1 to December were selected as the research objects. The test reports were analyzed retrospectively,and the factors influencing the detection results were analyzed,and the targeted quality control measures were put forward. Results the factors affecting the microbial test of drinking water mainly include environmental factors,experimental equipment factors and human factors. Conclusion it is of great significance to analyze the influencing factors of microbiological inspection quality of drinking water and take effective measures to enhance the quality control of microbial testing for drinking water. [Key words] drinking water;microbial test;influencing factors 生活飲用水与人类生活、健康息息相关,通过科学、有效的微生物检测,可确保生活饮用水水质合格、水处理符合标准[1]。然而在生活饮用水微生物检验过程中,存在一些影响因素,会影响微生物检验结果。生活饮用水是微生物的载体,如果人饮用了质量不合格的生活饮用水,极易受到微生物的侵害,从而导致疾病的发生。所以,研究生活饮用水微生物检验影响因素,并提出可行、有效的质量检验控制措施,具有至关重要的作用。结合2017年1—12月期间在该中心进行的960件生活饮用水微生物检验结果,分析生活饮用水微生物检验质量控制措施,进一步为检验人员提供参考依据。现报道如下。 1 资料与方法 1.1 一般资料 选取2017年1—12月期间在该中心进行的960件生活饮用水作为研究对象。 1.2 方法 1.2.1样本采集选取具有代表性的地点取样,采集过程必须严格执行无菌操作要求,确保水样采集、运输、储存等过程不受污染,且确保在采集4 h内进行检验,以免因放置时间过长造成水样变化或污染。若当天不能检测,应冷藏4℃下,并于24 h内完成检测。 1.2.2材料按照《生活饮用水标准检验方法》(GB /T 5750—2006)要求[2],配制培养基并经121℃灭菌15 min。培养基制成平板以后,置于培养箱37℃培养24 h,若无菌落生长,证明培养基无菌,符合实验要求。将含有大肠埃希氏标准菌株的菌液接种在培养基上,若大肠埃希氏菌能够正常生长,证明培养基的成分能够满足细菌生长的条件,符合实验要求。 1.2.3实验仪器水浴箱、恒温培养箱、高压灭菌器等。 1.2.4检验方法按照《生活饮用水标准检验方法》(GB /T 5750—2006)要求,依据检验微生物类型,选择最适宜、最准确、最科学的实验检验方法。 2 结果 2.1 不同季节水样微生物检测情况 第一季度合格率最高为97.91%,第三季最低为83.33%。 2.2 不同存放时间水样微生物检测结果 存放24 h的水样菌落总数最多(13 MPN/100 mL),总大肠菌群也最多为(1.8×103)CFU/mL。 2.3 不同体积水样微生物检测结果 100 mL的水样菌落总数与总大肠菌群多于1 mL水样。 2.4 不同培养温度水样微生物检测结果 36℃为最适宜菌落为大肠菌群生长的温度。 3 讨论 3.1 影响生活饮用水微生物检验因素 3.1.1环境因素通过以上分析认识到微生物检测结果容易受到外部环境的影响,并且其操作环境必须在无菌环境进行。若无菌环境遭到破坏,生活饮用水微生物检验结果可能存在误差,影响检验质量。 3.1.2实验设备因素由于实验设备长期使用,若日常维护和保养不到位,可能会导致实验检测结果存在误差。特别是恒温培养箱,需要检定内部不同角落温度是否符合检测需求。细菌的培养温度对其生长效果影响极大。 3.1.3人为因素①若操作技术不规范,可能影响检测结果;②微生物样品被接收之后需要立即进行检测,避免其遭到破坏或者发生变化。样品存放时间越长,菌落总数的检测结果越高。③检测过程中取样体积、检测方法和标准限值的不同,检测结果可能出现不符合规律现象。 3.2 生活饮用水微生物检验质量控制措施 3.2.1控制实验环境加强对实验室环境的控制,依据实验实际需求和性质,检测环境采用超净工作台或洁净间,避免生活饮用水受到
微生物检验规程 1.实验注意事项 1.1无菌操作要求 1.1.1 接种细菌时必须穿工作服、戴工作帽。 1.1.2专用的工作服、帽及拖鞋,应放在无菌室缓冲间,工作前经紫外线消毒后使用。 1.1.3 接种样品时,应在进无菌室前用肥皂洗手,然后用75%酒精棉球将手擦干净。 1.1.4 进行接种所用的吸管,平皿及培养基等必须经消毒灭菌,打开包装未使用完的器皿,不能放置后再使用,金属用具应高压灭菌或用95%酒精点燃烧灼三次后使用。 1.1.5 从包装中取出吸管时,吸管尖部不能触及外露部位,使用吸管接种于试管或平皿时,吸管尖不得触及试管或平皿边。 1.1.6 接种样品、转种细菌必须在酒精灯旁操作,接种细菌或样品时,吸管从包装中取出后及打开试管塞(即硅氟胶塞)都要通过火焰消毒。 1.1.7 接种环和针在接种细菌前应经火焰烧灼全部金属丝,必要时还要烧到环和针与杆的连接处。 1.1.8 吸管吸取菌液或样品时,应用相应的橡皮头吸取,不得直接用口吸。1.2无菌间使用要求 1.2.1 无菌间内应保持清洁,工作后用消毒溶液消毒,擦拭工作台面,不得存放与实验无关的物品。 1.2.2无菌间使用前后应将门关紧,打开紫外灯,照射时间不少于30min,使用紫外灯,应注意不得直接在紫外线下操作,以免引起损伤,灯管每隔两周需用酒精棉球轻轻擦拭,除去上面灰尘和油垢,以减少紫外线穿透的影响。 1.2.3处理和接种样品时,进入无菌间操作,不得随意出入,如需要传递物品,可通过小窗传递。 1.3消毒灭菌要求 1.3.1灭菌前准备 (1)所有需要灭菌的物品首先应清洗晾干,玻璃器皿用纸包装严密,如用金属筒应将上面通气孔打开。 (2)装培养基的三角瓶,内容物不应超过总体积的2/3(例如500mL的三角瓶最好装300~350mL培养基,以防再次加热融化时爆沸)。 (3)无菌室内使用的毛巾、脱脂棉球用纸包裹,进行湿热灭菌。
2015版中国药典微生物项变化的应对策略—菌种 上一篇使用大篇幅说了培养基,也是真正揭开这次连载的一些实施细节,得到了一些蒲友和同行业友人的正面反馈,非常感谢大家对我的鼓励!其实写这个连载的目的是希望大家不要对药典微生物项升级那么多内容抓狂,而是真正静下心来想想其背后的意义和对于我们今后的工作会带来什么。梳理那么多内容的时候我并没有烦躁或是感觉是在应付一周一篇的交稿,反而有种释然的感觉,能总结那么多说明我们实验室实实在在的做了很多,收获很多同时也进步很多,心里很感慨也对实验室小伙伴们的努力很感动。谢谢大家能够支持我前面四篇的连载,我会继续加油!废话太多不说了!原本是想将培养基和菌种一起写的,写到后来发现如果写在一篇,确实有些内容会讲的不够细,所以将培养基和菌种拆开了,这次我们就来谈谈我们顽皮的菌种君吧! 1、检验用菌种的选择 在药典第三次征订意见稿《9203 药品微生物实验室质量管理指导原则》的“菌种”项下有这么一句话“药品微生物检验用的试验菌应来自认可的国内或国外菌种保藏机构的标准菌株,或使用与标准菌株所有相关特性等效的可以溯源的商业派生菌株”。这句话写明了中国药典对检验用菌种的挑选原则,感觉上可以使用CMCC(中国医学微生物菌种保藏管理中心)、ATCC(美国典型菌种保藏中心)、NCTC(英国典型菌种保藏中心)等等,最近还有供应商给我推荐CICC(中国工业微生物保藏中心)的菌种。但是我们作为遵循中国药典的企业来说,中国药典微生物限度及无菌检查项下的菌种是明确写明仅可使用CMCC的菌种,所以大家没有必要去挑战权威性,如果你使用ATCC的菌种,检查官到时候问你ATCC和CMCC的区别,我相信我们这种等级的肯定是说不清的,这个项目是中检所在做的研究,所以我们不去做这样的挑战,乖乖的选择符合我国国情的CMCC菌种即可,免去一系列无意义的解释。 当然有些企业的产品需要出口,要符合出口国的药典标准,国外相对来说就放宽很多,但是也有一部分国家不太承认我们的CMCC菌种。在我的工作经历中,发现国内的审计官员对微生物方面了解的甚少,但是有次我们企业请了一名国外资深专家来我们公司全面审计的时候,他一看我们检出的环境菌种就娓娓道来,让我很吃惊,我不知道是不是国外对于微生物这块的重视程度和我国还有一定差距还是什么,他们的药典中对于检验菌种的挑选也不止一种,认可范围更加宽泛。现在迎审过程中,我们微生物实验室更多的是解释而非探讨,我们也希望国内的检查团队中能多一些对微生物了解的老师来给我们帮助和指导。 2、检验用菌种的管理 我们实验室对于菌种的管理也历经了不少波折,现在的管理模式和使用下来的效果还是比较令人满意的,菌种其实最怕就是其活力消退或变异。有些外企的管理模式真的非常方便,使用定量菌株直接实验,可能现在还不太适用于我们大部分国内企业,因为他们使用的定量菌株是ATCC等授权的国外企业制造并供货的,确实非常精准,特别是M家的首席产品,我就不多说了以免有广告嫌疑,国内应运而生的定量菌株我个人还是保留意见。出去培训时还是会发现有很多国内企业对于菌种的管理方式特别是保藏方法存在一定问题,菌种死亡变异的事件还是时有发生。以下我就介绍下我们企业的菌种管理模式,并介绍2种比较方便的菌种保藏方法。
微生物检验标本检验前的质量控制分析 发表时间:2018-11-21T09:53:24.757Z 来源:《世界复合医学》2018年第09期作者:王巍 [导读] 对微生物检验前进行质量控制,可提高检验准确率及治疗效果。 哈尔滨市疾病预防控制中心黑龙江哈尔滨 150010 摘要:目的:总结微生物检验标本前开展质量控制的具体方法及应用效果。方法:选取2016年5月至2017年5月我中心收治的78例呼吸道感染病例作为观察对象,根据随机分配的原则分为观察组(n=39)和对照组(n=39),两组均进行微生物病原学和药敏试验,并给予对症治疗,观察组在微生物检验前实施质量控制,对照组进行常规检验,观察检验结果和治疗结果。结果:药敏试验后,进行抗生素治疗,观察组总有效率92.31%,高于对照组74.36%(P<0.05);经质量控制后进行微生物检验,观察组检出病原菌种类更多,且检出率更高,与对照组比较(P<0.05)。结论:对微生物检验前进行质量控制,可提高检验准确率及治疗效果。 关键词:微生物检验;质量控制;应用效果 Microbiological test specimen quality control before inspection Abstract: Objective: To summarize the specific methods and application effects of quality control before microbiological test specimens. Methods: 78 cases of respiratory infections admitted to our hospital from May 2016 to May 2017 were selected as observation subjects. According to the principle of randomization, they were divided into observation group (n=39) and control group (n=39). Microbial pathogens and drug susceptibility tests were carried out, and symptomatic treatment was given. The observation group was subjected to quality control before microbiological examination, and the control group was subjected to routine examination to observe the test results and treatment results. RESULTS: After the drug sensitivity test, antibiotic treatment was performed. The total effective rate of the observation group was 92.31%, which was higher than that of the control group (74.36%) (P<0.05). After quality control, the microbial test was performed. The observation group detected more pathogens and examined. The rate of outflow was higher than that of the control group (P<0.05). Conclusion: Quality control before microbiological testing can improve the accuracy of the test and the therapeutic effect. Key words: microbiological test; quality control; application effect 微生物检验标本的质量控制过程包括检验前、检验期间及检验后3个阶段,现在大部分实验室都存在完善的检验期间和检验后质量控制制度与措施,因为检验前阶段涉及到其他科室的工作人员、患者和标本运送等环节,以及标本的采集、留取、储存及运输等,属于检验全程质量控制的薄弱环节和难点。本研究以2016年5月至2017年5月收治的78例呼吸道感染病例作为观察对象,分析微生物检验标本前开展质量控制的具体方法及应用效果,现报道如下。 1.资料与方法 1.1一般资料 选取2016年5月-2017年5月我院收治的78例呼吸道感染病例作为观察对象,所有患者经痰培养,结果均呈阳性,对所有标本进行微生物检验,根据随机分配的原则分为观察组和对照组,每组39例,观察组微生物检验前进行质量控制,其中女20例、男19例,年龄12-47岁、平均(29.5±2.3)岁;对照组行常规微生物检验,其中女18例、男21例,年龄13-44岁、平均(28.5±2.1)岁,2组患者基线资料均衡性高(P>0.05)。 1.2方法 对照组进行常规微生物检验,包括常规标本采集、保存、转送、镜检,实施病原分离培养、药敏试验等,在此期间不开展质量控制措施。观察组在微生物检验前实施质量控制,制定标准监管制度以及检验流程,分别从检验人员、培养基、检验仪器及操作等方面进行质量控制。检验人员应该具备扎实的检验操作技能,必须经过严格考核合格后才能上岗操作;培养基应贴有制作时间以及有效期,保证其使用前的无菌性,且该培养基应保证pH颜色、成分以及配制体积均能达到检验要求;确保检验仪器工作正常,保证检验结果的准确性;检验人员应严格按照检验流程执行,并规范操作,若在操作过程中有偏差,则立即上报,重检。同时还应:强化临床各科室间的沟通,听取意见和建议,不断完善检验工作流程,严格按照程序进行,以防违规操作;严格评估检验结果,分析其准确性,认真核实不合格的检验结果;设立咨询服务台,通知制定标本采集知识手册,对患者进行微生物检验的应用价值、标本采集要求与注意事项、准备工作等相关知识的教育;加强对检验人员进行培训,全面提升检验人员的业务水平;做好不合格标本的记录工作,一发现不合格标本立即向临床科室汇报;强化卫生管理,对微生物检验的各个流程进行质检。 2.结果 经质量控制后进行微生物检验,观察组检出病原菌种类更多,且检出率更高,与对照组比较(P<0.05)。 对标本进行药敏试验后,采用抗生素对症治疗,观察组总有效率92.31%,高于对照组的74.36%,两组比较(P<0.05)。
检验员培训考试试题(微生物) 部门职位姓名分数 一、填空(40分,每空1分) 1. 微生物限度检查应在不低于D级背景下的B级单向流空气区域内进行。 2. 微生物限度检查法中需氧菌检查所用培养基为胰酪大豆胨琼脂培养基,培 养温度为30-35 ℃;霉菌,酵母菌检查所用培养基为沙氏葡萄糖琼脂培养基培养温 度为20-25 ℃。 3. 具抑菌活性的供试品,常用消除抑菌活性的方法有:增加稀释液或培养基体积,加入适宜的中和剂或灭活剂,薄膜过滤法。 4. 采用薄膜过滤法,滤膜孔径应不大0.45μm,直径一般为50mm。 5. 供试液制备若需加温时,温度不应超过45℃。供试液从制备至加入检验用培养基,不得超过1小时。 6. 制备的菌液若在室温下放置,应在 2 小时内使用,若保存在2~8℃, 可在24小时内使用。 7.计数培养基适用性检查和供试品计数方法适用性试验,需氧菌总数计数所用试验菌株为金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉;霉菌和酵母菌总数计数所用试验菌株为白色念珠菌、黑曲霉。 11.计数方法适用性试验中,采用平皿法或薄膜过滤法时,试验组菌落数减去供试品对照组菌落数的值与菌液对照组菌落数的比值应在0.5-2 。 12. 检查大肠埃希菌时,应做阴性对照试验和阳性对照试验。
13. 配制培养基时,要填写培养基配制记录,记录内容包括:名称、配制量、配方、灭菌条件、配制日期、配制批号、配制者、PH值 14.在收到检定菌后,保管员要在保存菌种容器外加贴标签,内容为名称、编号、购买日期,同时还要填写菌种接收记录。 二、判断题(5分,每题1分) 1.平皿法操作时应先注入培养基,再加入1ml供试液。(×) 2.以稀释液代替供试液进行阴性对照试验,阴性对照试验应无菌生长。如果阴性对照有菌生长,应进行偏差调查(√) 3.从菌种保藏中心获得的干燥菌种为0代,试验用菌株的传代次数不得超过5 代(√) 4.控制菌检查用培养基促生长能力检查、抑制能力检查接种不大于100cfu试验菌于被检培养基和对照培养基中。(×) 5.纯化水的微生物限度质量标准为每lml供试品中需氧菌总数不得过lOOcfu。(√) 三、选择题(5分,每题1分) 1. 进行供试品控制菌检查时,阳性对照试验的加菌量为( C ) A、不大于50cfu B、50~100cfu C、不大于100cfu
1. 目的:建立非无菌药品微生物限度检查检验标准操作规程,规范检验操作,确保检验结果准确。 2. 适用范围:适用于本公司所有采用非无菌药品微生物限度检查法测定的供试品。 3. 责任者:QC检验员、QC经理。 4. 正文: 4.1 非无菌产品微生物限度检查:微生物计数法 4.1.1 简述 微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数。 当本法用于检查非无菌制剂及其原、辅料等是否符合规定的微生物限度标准时,应按下述规定进行检验,包括样品的取样量和结果的判断等。除另有规定外,本法不
适用于活菌制剂的检查。 本检查法可采用替代的微生物检查法,包括自动检测方法,但必须证明替代方法等效于药典规定的检查方法。 微生物计数试验应在受控洁净环境下的局部洁净度不低于B 级的单向流空气区域内进行。检验全过程必须严格遵守无菌操作,防止再污染,防止污染的措施不得影响供试品中微生物的检出。单向流空气区域、工作台面及环境应定期进行监测。 如供试品有抗菌活性,应尽可能去除或中和。供试品检查时, 若使用了中和剂或灭活剂,应确认其有效性及对微生物无毒性。 供试液制备时如果使用了表面活性剂,应确认其对微生物无毒性以及与所使用中和剂或灭活剂的相容性。 4.1.2 计数方法 计数方法包括平皿法、薄膜过滤法和最可能数法(Most-Probable-NumberMethod,简称MPN 法)。MPN 法用于微生物计数时精确度较差,但对于某些微生物污染量很小的供试品,MPN 法可能是更适合的方法。 供试品检查时, 应根据供试品理化特性和微生物限度标准等因素选择计数方法,所选的方法必须具备检测充足样品量的能力,以保证所获得的试验结果能够判断供试品是否符合规定。所选方法的适用性须经确认。 4.1.3 计数培养基适用性检查和供试品计数方法适用性试验 供试品微生物计数中所使用的培养基应进行适用性检查。 供试品的微生物计数方法应进行方法适用性试验,以确认所采用的方法适合于该产品的微生物计数。 若检验程序或产品发生变化可能影响检验结果时,计数方法应重新进行适用性试
微生物检验实验室质量控制 发表时间:2015-09-16T14:26:19.763Z 来源:《医药前沿》2015年第18期供稿作者:杨再东 [导读] 贵州省黎平县疾病预防控制中心微生物实验室检验是防御疾病、诊断治疗疾病、控制疾病以及卫生监督的主要技术支撑,是疾病防治和卫生执法的主要手段。 杨再东 (贵州省黎平县疾病预防控制中心贵州黎平 557300) 【摘要】随着我国生物医学的不断发展,研究方法和研究技术的不断提高,逐渐加深了对微生物的研究。微生物种类繁多,由微生物感染而引起的疾病不胜枚举。科学家在实验室中对微生物进行研究和探索,而微生物检验的实验结果则是防御疾病、诊断治疗疾病、控制疾病以及卫生监督的主要依据。本文主要阐述了微生物实验室质量检测的措施和微生物检验实验室质量控制的影响因素和对策。 【关键词】微生物检验;实验室;质量控制 【中图分类号】R446 【文献标识码】A 【文章编号】2095-1752(2015)18-0322-02 引言 微生物实验室检验是防御疾病、诊断治疗疾病、控制疾病以及卫生监督的主要技术支撑,是疾病防治和卫生执法的主要手段。微生物检验实验室质量控制直接能够影响正常的实验工作的进度,因此要加强对微生物检验实验室的质量控制,避免检验结果出现偏差,确保检验结果的正确性。对检验实验室的质量控制检验包括多方面检验:全面的质量管理、室间质量控制和室内质量控制。全面质量管理是相关部门通过建立质量管理体系对实验室进行全方位的检验;室间质量控制是指实验室与实验室之间通过相互校准检验、实验室的操作和结果来进行对实验室检验微生物能力的验证;室内质量控制是指实验室内部采取对比分析、跟踪以及相关方法,对检验质量进行自我控制的过程。 1.微生物检验实验室质量控制的重要性 1.1 微生物的概念 微生物包括:细菌、病毒、真菌以及一些小型的原生生物、显微藻类等在内的一大类生物群体,它个体微小,与人类关系密切。涵盖了有益跟有害的众多种类,广泛涉及食品、医药、工农业、环保等诸多领域[1]。 1.2 实验室的质量控制 实验室质量控制的目的是为了提高微生物的检验质量,通常是彻底消除影响检验质量的因素。所谓实验室质量控制管理就是对检验人员、检验方法、所用的仪器设备、用到的相关检验试剂等进行有效的控制,以保证质量控制工作能够正常的进行。通过建立完善的质量管理系统,可以检测整个检验过程的质量并且随时发现问题,及时对检测工作中出现的问题进行处理,确保检测实验质量控制工作能够顺利的进行,因此对实验室质量进行控制管理很重要。 2.微生物检验实验室的质量控制 2.1微生物检验实验室的室内质量控制 (1)技术人员素质要求。 微生物实验室技术人员的能力和素质是保障微生物检验实验室质量控制的关键因素之一。从事微生物检验的技术人员应该有扎实的专业基础,对微生物学、医学以及生物学要有专业理论基础。当技术人员掌握了基础理论知识以后,把相关的理论知识合理的运用到微生物检验中。要严格训练技术人员的检验技术,以便于技术人员能够熟练掌握实验方法并且能够应对实验中的突发事件。技术人员应该具有高度的责任心和严格的无菌观念,对检验对象进行认真检测,降低检测实验中的人为误差。技术人员要经过严格的考核获取岗位资格证以后才能正式上岗。实验室要对技术人员定期培训,不断提高技术人员的实验能力,让技术人员掌握先进的微生物检验技术。此外由于该工作是精密工作,所以对于长期从事微生物实验的技术人员都要对其定期进行健康体检[2]。 (2)微生物实验室检测仪器设备及设施 对微生物进行实验时要保证实验所用的各个仪器设备和设施都处于性能良好并和洁净程度达标的状态。实验室要对仪器设备以及设施定期进行定期检查校正,确保所使用的仪器性能都能达到检测标准。对不同的仪器设备和设施采用不同的检测方法,比如灭菌器,可以使用嗜热芽胞杆菌或者化学方法来测试灭菌效果,洁净室用平皿计数法等等[3]。 (3)检验方法的要求。 微生物检验实验室的方法必须经过相关行业鉴定之后才能使用。在没有可行性检测方法的情况下,应该尽量选择具有权威性技术组织公布的文献或者与国家标准的科技文献中选取一个合理的检测方法,以确保实验结果的准确性和可靠性。 (4)培养基的质量控制 要选择背景雄厚的厂家进行微生物实验室培养基的选择,并且要对培养基进行感官、PH以及生物学指标检定,将被检培养基与相应细菌进行细菌生长率、菌落大小以及生长特征的检测,实验验证合格以后这个培养基才能使用。在配制培养基时要做好培养基的配制的数量、分装情况、灭菌方法、无菌试验检查、配制时间、有效时间等的实验记录,在使用培养基的时候一定要在确认记录完全合格的情况下才可使用[4]。 2.2 微生物检验实验室的室间质量控制 对微生物实验室进行室间的质量控制是指在每一个实验室都能做好室内质量控制的基础上进行的。通过选取两个或者更多的条件相同的实验室相互比较,比较每个实验室的管理能力和技术水平,采用这样的方法对实验室的室间质量控制进行评价。最后由上级质量控制中心的检验机构对实验室进行考核。对各个实验室进行对比考核,是为了了解各个实验室的检验管理能力和技术水平,有助于随时发现问题,及时制定解决方案,不断提高实验室的检验技术水平。 3.总结 现阶段,我国不断的加强教育事业的建设,不断的学习研究新技术,逐渐将探索的对象由宏观物体拓展到了微观世界。而生物医学是一项重要的研究领域,微生物是生物医学中最常见的生命体,也是疾病感染的根源。为此相关人员不断的对微生物进行研究。其中用于微
【摘要】注射剂是一种直接进入人体血液循环而发生作用的药品,为此要严格控制注射液微生物污染。因此本文从注射剂选择适应的灭菌参数、f0值灭菌应用、灭菌效果验证方面进行探究注射剂生产过程中微生物的质量风险控制,以此保障灭菌过程均匀完善,提高注射液的安全性、稳定性、有效性。在探究后总结,注射剂生产过程中微生物的质量风险控制主要还是保证生产过程中应用适当的灭菌工艺,并且严格执行gmp管理,以此保障良好的无菌生产体系,这就要求注射液在生产的各个环节应采取有效措施严格控制微生物污染,确保无菌安全,避免微生物风险,在生产过程中尽可能的完全灭菌,以此保证注射液产品的无菌安全。 【关键词】注射剂;生产过程;微生物;质量风险控制 注射剂是一种直接进入人体血液循环而发生作用的药品,为此要严格控制注射液微生物污染,就显得尤为重要。因此全部生产过程中的灭菌成为保障该注射液药品质量安全的关键工序,同时灭菌过程均匀完善程度直接关系到注射液的安全性、稳定性、有效性[1]。 1注射剂选择适应的灭菌参数 要根据药物的理化性质、稳定性和生物学特性及临床用药的顺应性来保证制剂无菌水平。一般湿热灭菌条件采用121℃×15min、121℃×30min、116℃×40min的程序,以此必须保证邪君后的微生物存活率≤10-6,即没100万个注射剂中存活微生物不得超过1个,以此保证灭菌后制剂的无菌保证水平。 注射剂生产过程中,为保证灭菌效果,应在密闭的制剂灭菌容器内,进行加压高温灭菌,若压力和灭菌时间不当,则不能有效杀死所有芽孢和细菌繁殖体。对于含糖类注射剂和氨基酸类营养性注射液,高温灭菌条件会影响药物产生不稳定性,因此注射剂选择适应的灭菌参数时,要保障高温灭菌的安全性,也要保障注射剂的稳定性,以此能够即可有效去除微生物,确保药剂治疗的稳定性。若灭菌方式方法不当,灭菌温度低、灭菌时间短,达不到灭菌目的;灭菌温度高、时间长,注射剂会产生杂质。因此,要正确选择适当的灭菌温度,保证注射剂质量[2]。 2 f0值灭菌应用 f0值是灭菌周期验证中所应用的术语。高温高压灭菌程序中,121℃下的等效灭菌时间,是标准灭菌时间,是一个可靠的灭菌参数。f0值的计算直接作用于生产灭菌过程的设计和灭菌效果。通常包装材料性能等因素会引起不同的升温速度,包括容器大小、形状及热穿透系数;灭菌产品溶液的粘稠度和容器的填充量;容器在灭菌器中的数量和分布。溶蚀由于f0值会随上述因素温度变化而呈现出的指数也不同,也就是说温度即使有很小的差别也会影响f0值,由此测定灭菌物的实际温度有利于灭菌器和灭菌技术的验证。 3灭菌效果验证 为控制注射剂生产过程中微生物的质量风险,必须进行全效可行的灭菌效果验证,高温高压灭菌时,需要对灭菌器的空载、满载分布进行试验、热穿透试验、生物指标试剂挑战试验,同时,再采用蒸汽灭菌生物指示剂进行验证。 3.1空载、满载分布试验空载、满载分布试验是为了检查灭菌器内腔的热分布情况,检查灭菌器内腔是否有冷点,达不到高温高压灭菌的目的。试验中,将温度探头均匀分布在灭菌器内腔各处,再进行灭菌操作,操作过程中,记录各个温度点[3]。 3.2热穿透试验热穿透试验是在热分布基础之上,确定灭菌器内腔中的“最低温度点”,检查该点f0值是否在无菌保证值之上。试验中,按照注射液的工艺灭菌温度进行操作,检测出“最低温度点”,将此点与注射液接触,监测其温度,记录数据作为热穿透试验数据。 3.3生物指示剂试验生物指示剂能够有效确认监控的灭菌效果。根据热分布试验和热穿透试验的结果,通过生物指示剂试验,对灭菌器内腔中的“最低温度点”进行验证,以此检查确认灭菌效果。通过灭菌器内腔中的“最低温度点”进行灭菌,灭菌后再进行无菌过滤,
疾控系统微生物检验质量控制程先俊 发表时间:2018-05-18T11:21:36.103Z 来源:《基层建设》2018年第2期作者:程先俊 [导读] 摘要:我国作为经济发展中国家,科学技术在不断的提高,国民法律意识越来越强,对于微生物的检验疾控系统的要求也更高,疾控系统作为为行政、司法、社会公益活动、仲裁和经济贸易关系人提供有效的证明和依据,其结果的正确性和有效性是极其重要的。 普洱市西盟县疾控中心 摘要:我国作为经济发展中国家,科学技术在不断的提高,国民法律意识越来越强,对于微生物的检验疾控系统的要求也更高,疾控系统作为为行政、司法、社会公益活动、仲裁和经济贸易关系人提供有效的证明和依据,其结果的正确性和有效性是极其重要的。所以,目前我国对疾控系统的质量要求越来越高,大力发展疾控系统的高效精准性作为目前实验室检验的重要事务,能大大提高微生物检验技术,促进疾控系统的稳定发展。 关键词:疾控系统;微生物检验;质量控制 前言:目前,现代化技术的不断更新发展,造成环境的极大污染,各样的病毒微生物越来越多,所以对于人类、动植物来讲,各种传染性极强的疾病冲击着整个社会环境。所以,我国对实验室微生物疾控系统的要求也越来越高,一个检验结果高效精准的疾控系统对各项微生物的检测异常重要,对快速有效的找出解决疾病的办法具有重要意义。本文针对疾控系统微生物检验质量的方法进行研究和探讨,找出一套行之有效的疾控系统。 一、强化资质认定,全面运行质量管理体系 通常,在微生物实验室检验时,有许多复杂的步骤,例如:标本采集、运送、保存、处理、日常管理、实验人员培训、消毒处理、报告输送试剂的要求、各种仪器要求和工作条件等等,这些每一步看似简单的事项都影响着检验的成功,如果每一步不按照严格的标准操作程序进行,检验的结果就会或大或小的出现问题。在检验完成成功之后也并不代表实验就结束了,后续工作也是非常重要的,根据实验室管理的质量手册要求来填写原始数据、检验报告的发放、实验室中每种仪器、试剂、培养基的使用步骤和方法等;针对出现的问题要及时纠正解决,对于实验室相关工作人员要进行专业培养,完善全面的运行质量管理体系。 二、重视继续教育,培养高素质的检验队伍 一个优秀负责的实验室检验团队对实验室的持续发展具有重要意义,所以,在健全完善实验室各方面的设备时,提高整体检验工作人员的素质是非常有必要的。微生物检验具有的特点是专业性强、步骤复杂、手工操作和定性试验,所以,在检验工作人员进行试验之前要进行专业培训和实习操作,不能直接上岗工作,而且检验的工作还要求工作人员必须具有高度的责任心、耐心和严谨的工作态度,在上岗之前,要对每位实习工作人员进行考核,对考核通过的人员才能允许其进入实验室工作。在进入实验室工作的人员在工作中丝毫不能懈怠,对于实验室日常管理中,要制定相关条款,要求相应的时间段对检验工作人员进行考核,对于考核不通过的人员给予惩罚,严重的可以辞退;对于表现优秀的也可以给予奖励制度,这种制度有利于提高工作人员的积极性和责任感,有效促进检验试验的大力发展。 三、精心准备,切实做好实验前的质控 3.1检验方法的核实和确认 对于实验室的检测方法不能一直使用老旧的检验方法,要根据实际情况的需求,不定时的更新改变检验方法。但是,在每次使用新的检验方法之前,要对其精准性和准确性核实,不能贸然使用新的检验方法,通过取一定的样本进行实验得出一定的指标,在进行讨论看这个方法是否符合使用标准。 3.2环境设施的监控 环境设施的合理分配对微生物检验的成功起着重要作用,对于实验每个区域放置的物品要有合理的安排,不能随拿随放,一个良好的环境对检测实验具有促进作用。一个实验室的选择,首先要安排好每个区域要摆放的物品,对其进行相应的装饰,对于无菌室、超净工作台、生物安全柜和层流洁净室要进行定期检查和消毒。做好环境设施的准备,离检测实验的成功就近了一步。 3.3培养基、试剂的监测 对于实验用到的培养基和试剂,必须选择三证齐全的供货商,切忌使用三无产品。在确定购买之前,可以根据外观、批号、选择性来初步判断物品的好坏,再根据具体的标准对比进一步选择需要购买的培养基和试剂。对于购买回来的实验物品必须要在有效期内使用,不能为了节省材料而使用过期商品,否则会对实验的结果精准性造成影响。每个培养基有与之对应的试剂相匹配,所以在实验时,不能随意使用培养基和试剂,同一批号一起使用。在配制培养基时,要标注好相应的记录,例如:培养基名称、配制日期、有效期、灭菌、分类、贴标等。 3.4仪器的监护和监测 对于实验的仪器,要进行定期养护和检查,精准的仪器才能带来准确的实验结果。对于仪器的管理应该选择专业的管理人员进行管理,并定期记录以便查看。第一、冰箱的温度通常低于4℃,并定期清洁化化霜;第二、水浴箱温度在35℃-37℃;第三、对于称量天平、移液器、生化分析仪、酶标仪等都要定期检验,合格后贴绿标识,方可使用。 四、扎实工作,重视实验中的质控和完善措施 实验的质量决定实验结果成功与否,所以,切实做好实验中的质量监测,针对不合格的事项要严格把关,规范实验步骤。在收到收样单后,要按照相应的要求,规范实行实验流程,阴性、阳性和空白对照是每次实验之前都必须进行的步骤,样品类型的不同也要用不同的处理方法。每次实验都是一次复杂的工作,所以要想做到实验的完整和精准也是不容易的,因此对于检验人员的实验步骤:标本的编号、信息录入、仪器操作、检验结果和审核等都要严格把关,要想做到每一步都不出错,只能是一步一步实行,每进行一步就仔细认真的分析和核实,才能得到理想的结果。第一、对于送检单的核实检验人员一定不能忽视,认为这是一个简单的小问题,只有确保样品的合格对之后的工作才能安全进行;第二、样品检验时每一步的数据和现象都要做详细的记录,便于后面的检查;第三、对于检验报告单的签收要有专人负责运送,而且要做好交接记录,将所有原始记录保存归档便于查阅。 五、加强联系,充分发挥信息沟通的作用 目前,我国是一个信息化的大国,生活中每个问题都离不开信息沟通,在微生物的检测实验技术上也是相同,顺畅的信息沟通为检测
微生物检验实验室质量控制 摘要】随着我国生物医学的不断发展,研究方法和研究技术的不断提高,逐渐 加深了对微生物的研究。微生物种类繁多,由微生物感染而引起的疾病不胜枚举。科学家在实验室中对微生物进行研究和探索,而微生物检验的实验结果则是防御 疾病、诊断治疗疾病、控制疾病以及卫生监督的主要依据。本文主要阐述了微生 物实验室质量检测的措施和微生物检验实验室质量控制的影响因素和对策。 【关键词】微生物检验;实验室;质量控制 【中图分类号】R446 【文献标识码】A 【文章编号】2095-1752(2015)18-0322-02 引言 微生物实验室检验是防御疾病、诊断治疗疾病、控制疾病以及卫生监督的主 要技术支撑,是疾病防治和卫生执法的主要手段。微生物检验实验室质量控制直 接能够影响正常的实验工作的进度,因此要加强对微生物检验实验室的质量控制,避免检验结果出现偏差,确保检验结果的正确性。对检验实验室的质量控制检验 包括多方面检验:全面的质量管理、室间质量控制和室内质量控制。全面质量管 理是相关部门通过建立质量管理体系对实验室进行全方位的检验;室间质量控制 是指实验室与实验室之间通过相互校准检验、实验室的操作和结果来进行对实验 室检验微生物能力的验证;室内质量控制是指实验室内部采取对比分析、跟踪以 及相关方法,对检验质量进行自我控制的过程。 1.微生物检验实验室质量控制的重要性 1.1 微生物的概念 微生物包括:细菌、病毒、真菌以及一些小型的原生生物、显微藻类等在内 的一大类生物群体,它个体微小,与人类关系密切。涵盖了有益跟有害的众多种类,广泛涉及食品、医药、工农业、环保等诸多领域[1]。 1.2 实验室的质量控制 实验室质量控制的目的是为了提高微生物的检验质量,通常是彻底消除影响 检验质量的因素。所谓实验室质量控制管理就是对检验人员、检验方法、所用的 仪器设备、用到的相关检验试剂等进行有效的控制,以保证质量控制工作能够正 常的进行。通过建立完善的质量管理系统,可以检测整个检验过程的质量并且随 时发现问题,及时对检测工作中出现的问题进行处理,确保检测实验质量控制工 作能够顺利的进行,因此对实验室质量进行控制管理很重要。 2.微生物检验实验室的质量控制 2.1微生物检验实验室的室内质量控制 (1)技术人员素质要求。 微生物实验室技术人员的能力和素质是保障微生物检验实验室质量控制的关 键因素之一。从事微生物检验的技术人员应该有扎实的专业基础,对微生物学、 医学以及生物学要有专业理论基础。当技术人员掌握了基础理论知识以后,把相 关的理论知识合理的运用到微生物检验中。要严格训练技术人员的检验技术,以 便于技术人员能够熟练掌握实验方法并且能够应对实验中的突发事件。技术人员 应该具有高度的责任心和严格的无菌观念,对检验对象进行认真检测,降低检测 实验中的人为误差。技术人员要经过严格的考核获取岗位资格证以后才能正式上岗。实验室要对技术人员定期培训,不断提高技术人员的实验能力,让技术人员 掌握先进的微生物检验技术。此外由于该工作是精密工作,所以对于长期从事微
美国FDA药品质量控制微生物实验室检查指南1993年 I.导言 《药品质量控制实验室检查指南》主要涉及许多有关药品实验室分析的化学方面的问题,对微生物实验室的检查仅提供了有限的指导,而本指南则是微生物分析检查过程的指导。本指南建议,如同对任何实验室检查—样,在检查微生物实验室时,应有—名熟悉检验的分析学家(微生物学家)参与。 II.非无菌药品的微生物检验 由于种种原因,局部药品、滴鼻剂和吸入剂存在许多微生物污染方面的问题.美国药典‘‘微生物属性”章(1111)指出“应该从药品用法、药品性质及时患者的潜在危害等方面评价微生物在非无菌药品中的重要性”,除此之外,没有提供具体的指导。美国药典还建议应对某些种类的非无菌药品做常规的总菌数检验及某些特定的污染指示微生物的检验:例如:植物、动物和某些矿物质中的沙门氏菌属;口服液体中的大肠杆菌;局部用药品小的金黄色倘萄球菌和绿脓杆菌污染;以及:自肠、尿道、阴道用药中的酵母菌和霉菌:大量的专题文章还沦及厂微生物的限度。 作为非无菌药品受微生物污染的可接受程度和类型的—般性指导,美国食品和药品管理局药品分局的邓尼根博士曾强调其对健康的危害问题。1970年他提出被革兰氏阴性细菌污染的局部制剂可能引起中度至重度的健康危害:文献和调查表明,许多感染都源于这种局部药品的革兰氏阴性细菌污染。几年前马萨诸塞州的—家医院就报道过—宗络合碘(Povidonelodine)被洋葱假恤孢菌(Pseudomonas cepacia)污染的典型病例。 因此,每家公司都希望为自己的非无菌药品制订出一种关于微生物限度的标准,美国药典中“微生物限度”(USP61)提供了检验几种指示微生物的方法,但并末涉及所有有害微生物。例如医药界普遍认为,洋葱假中孢菌在局部药品或滴鼻剂斗,大量存在是有害的,但美国药典没有提供证明这种微生物存在的检验方法。 间羟异丙肾上腺素硫酸盐吸入剂溶液的收回就是这方面的—个例子。美国药典第XⅫ版各论部分没有要求对这种药品进行微生物检验。药品管理局将其列为一级收回,因为此药受到了洋葱假单孢菌污染。健康危害评估表明,这种微生物对肺部感染的风险很大,特别是对某些患有慢性气管阻塞、囊性纤维变性和免疫缺陷等病的患者具有潜在的生命危险。此外,药典的微生物限度部分所描述的检验程度不能鉴别这些微生物。 现行美国药典在“微生物限度”部分(61)做了复检的规定,但是许多建议要求取消这种复检条款。类似于其他检验,初次检验结果应予以审查与研究。微生物污染并不是均匀地分布在一批药品或样品中的。如果在一个样品中发现污染而在另—次取样样品中没有发现,则不应忽视初次发现的结果。复检的结果应予以审查与评估,并且应特别注意进行复检的逻辑性和合理性。 为了分离出特定的微生物污染物,FDA实验室和制药工业的许多实验室,使用某些自钝化剂如吐温或卵磷脂的营养培养基,这对于钝化药品中常有的防腐剂的作用是非常必要的,还能为受损的或生长缓慢的微生物提供更好的基质;其他生长参数包括降低培养温度以及延长培养时间(至少5天),因为它们可以为这类微生物提供良好的生存条件。 例如:在《细菌学分析手册》(BAM)第Ⅵ版中,FDA实验室采用化妆品的检验方法鉴别非无菌药品中的污染物。这项检验包括将样品置于改良Letheen肉汤中培养。培养结束后,再用血琼脂平皿和麦球凯琼脂平皿进一步鉴定,然后再鉴别分离出的菌落。FDA微生物学家用这种方法使所有潜在的病原体的复活达到最佳,并且测定复活的微生物数量及其类别。FDA分析学家使用这种方法的另—个重要方面就是要确定所有用过的培养暴促进微生物生长的性能。 选择适当的中和剂很大程度上取决于防腐剂的性质和被评价药品所智的配方:如果在营养肉汤出现微生物生长,那么下一步的鉴别就可将样品转到更有选择性的琼脂培养基或适当的增菌琼脂上。 微生物检验可包括对在需氧菌总数检验小发现的菌落的鉴定。另外上述鉴定不应仅限于美国药典中的指示微生物。 鉴别从微生物总数检验或(和)富集培养检验中分离的各种菌落的重要性,将取决于药品的种类及共其