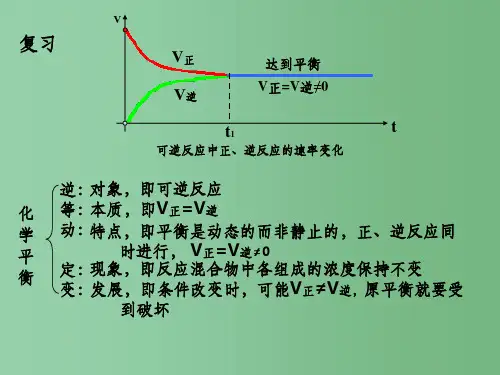
(5)变:条件改变,原平衡被破坏,在新 的条件下建立新的平衡。
在425℃时,在1L密闭容器中进行反应: H2+I2 2HI, 达到平衡,分别说明下列各图所示的涵义。
浓度/mol·L-1
浓度/mol·L-1
同2.0:0 化学平衡的建立与途径无2关.00,只要H条I 件相同, 某1.5一8 可逆HI反应无论是从正反应1开.58始还是从逆反应开
2、什么是饱和溶液?
在一定温度下,在一定量的溶剂里,不 能再溶解某种溶质的溶液,叫做这种溶质 的饱和溶液。
? 饱和溶液中溶质的溶解 过程完全停止了吗? 没有!
3、溶解平衡的建立
饱和硫酸 铜溶液
开始:溶解速率 > 结晶速率 一段时间后:溶解速率= 结晶速率
硫酸铜 晶体
达到溶解平衡,形成硫酸铜饱和溶液
始1.0,0 最终均可达到同一平衡状1态.00。
H2或I2
0.21
0.21
H2或I2
0.00
t1 时间/s
从正反应开始
0.00
t2 时间/s
从逆反应开始
相当于
1molH2+1mol I243; O2
2SO3反应
而言,平衡状态是指( B )
A. SO2 , O2 , SO3分子个数比是2:1:2
D. 反应容器内总物质的量不随时间而 变化
【例3】下列说法可以证明反应
N2+3H2
2NH3
已达平衡状态的是( AC )
A.1个N≡N键断裂的同时,有3个H-H键形成
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有6个N-H键断裂
D.1个N≡N键断裂的同时,有6个N-H键形成
1molO2,能发生什么反应?