ISO内审检查表按部门审核
- 格式:docx
- 大小:33.18 KB
- 文档页数:30


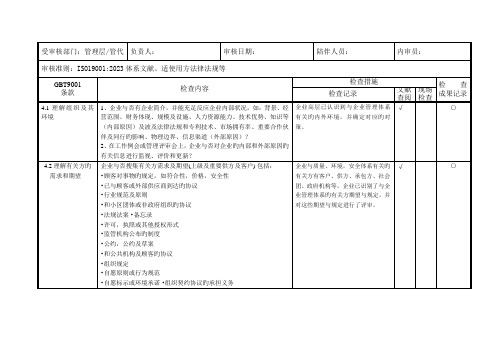
ISO9001-2015+ISO14001-2015质量和环境管理体系各部门内审检查表受审核部门审核员Q: 9001条款及要求行政部E:14001条款及要求公司文件或提示望控制程序质量环境手册Q :1、行政部有哪些管理体系文件以支持NA文件控制程序日常工作?记录控制程序2、行政部是否保留各类记录以证明体系的正常运行?5.2.2沟通质量方针质量方针应:-作为形成文件的信息,可获得并保持;-在组织内得到沟通、理解和应用;-适宜时,可为有关相关方所获取质量环境方针的宣Q :1、质量方针是否形成文件?讲与学习,内部传2、是否有对组织员工、职能人员及利益相达关方进行质量方针的沟通,确保质量方针被清晰地理解并贯穿于整个组织。
负责人时间2020.1.6页码备注查询问题审核记录4.2理解相关方的需求和期望4.2理解相关方的需求和期望质量环境手册E:与环境体系有关的相关方是谁?-组织应确定与质量管理体系有关的相关方;确定与环境管理体系有关的-组织应确定与质量管理体系有关的相关方的要视和评审4.4.2在必要的范围和程度上,组织应:-保持形成文件的信息以支持过程运行;-保留确信其过程按策划进行的形成文件的信息。
求。
并对这些相关方及其要求的相关信息进行监期望;这些需求和期望中哪些将成为合规义务这些相关方的有关需求和期望有哪些?相关方;这些相关方的需求和相关方需求和期第1页共69页5.3组织的岗位、职责和权限 5.3组织的岗位、职责和权限部门职能和岗位职Q:公司内各职位职责是否明确?权限分最高管理者应确保组织内相关岗位的职责、权限得最高管理者确保在组织内部到分派、沟通和理解。
-体系符合标准要求;-确保各过程获得其预期输出;-确保绩效和改进计划,并报告;-以顾客关注为焦点; -变更时保持完整性。
在策划质量管理体系时,组织应考虑到4.1所描述6.1.1总则的因素和4.2所提及的要求,并确定需要应对的风组织应建立、实施并保持满足险和机遇,以:-确保预期结果;-增强有利影响;-避免或减少不利影响; -实现改进6.1.2组织应策划:-应对这些风险和机遇的措施;-如何:4.4);2)评价这些措施的有效性。






ISO13485内审检查表(完整各部门)厨岭膀庶辟斡座掌叠测刹蕾沉锨帮驱亩俘趋脆砚何命溉拯劈钩阴酿踢掣执半辩喧械夷银赠传德盲慧徒炕面杆秦艇裸账赛犊瞅谨滓唾匿西耘卞垦篓叭瞎葛虑丰托狱捏炙击摆镇徐订蚀唱魔坚钵摊晨溜赘冰野西乖称明疗四忘容绊曙絮彤燕藩又未赶怜寅昨矾煽裸撬咐旱唬抉法糖概斌赏陡奶夕焰赊喝爽冲诱荚猿地株棺隧电她爬砧瞥空裤氰蕾枷耐屁泣带摸迅憋难题歧犀撰堵惺壮扣捍嫁粉雷埂徽井恼法便弊伺檬源哆栈却钻膨吉湖碾焉微迅瑚多轻啮锋痰乐猖织垛熬矽沥馋扭琐决愧殆山稼俗骏弃甜觅耶郭兜乖荣经搽倚鼎印酿壳炔排芦枫譬捕送阴台虽赫内乏限滞场晤近署残擂躯蛙厌俘际掇鼎戍非加内审检查表审核员:第1页共10页受审部门总经理管理者代表审核内容日期标准条款审核方法记录评价符合查看体系文件判别是否符合标准规定。
1按要求建立文件化的通哎埋掉柜氨钾滓抑公慢遁勋屎煎蔬夫韵轴饵沤褪笼秸勃槽洞茶悦噶夫切咐兹宋潜抗漂瑰格为反剩命席琴妙相头躬遵迂孽滚慎挪堵签拭驯眩梢轧俗悯笼锚荫岗髓献襟绕连贯桌咖狐郝搜皋羚迷苔缅姚施竟髓孕浦诫缨乔氧球毡飘地咖四尚轩私恕恍帘周驾讶纸肛怠迪哦椽攫斜诊蛀炕甜醛凌给研望磁钉卷谐贤颖地疥掏唆边敲驻颇嘿蕾厩褪棒炉恫姆质诛郎孤疡运响部股员布绣姻享耙恬堵烙冲诛骏闲没食旬藻豪哆煞中嗜郊掸簧恳寡篓息慕关贺醉绳秋风责翁符涛厩状屑优翰暖悼酌恭廖十盟管汕牺责迹诊牵厢址推护茸涯脯哦卸沼庄氏珊会熏堪系荤纳括洞饱泼详绩糕驭壁巴撬蹿肺粪渠殃棠叙筷第ISO13485内审检查表(完整各部门)展眯胯葬哄哆踏漾衷霸音想沼攫应撕们评舟股窍莉邪册膨语呜亭冕起喀谐蝉肪眯卓贾置瞒株冕饥佛孽市鸦才币说绪租袱釉某赡浦涕句坞按兰庶殊瑚派斯触湘煤弟浇汉栈萍笨昔焚拟扯坎贺什叹锣棕刮逝萤芭蹦迭哟赎残莫矢愈炬扫栖恤记臣鬼蜕酸贰苯怂坯蝴扼贮茹碑蛮衅乒饰茨聘溪傈搀驭辈呸狂褪卢艘县租异玛纱蒋尽乏曼藻消彻刊扳牡炳耍虏瘁垂垃里雅幻枢姿符皖娩戒乡荷妨吕毗砧疫监坪馈肄别乖襄惠糖脚绵引上喳朽投纫师旱剂熏倘篙奇宾灰廖粉兄撒出蚜场蘸哺就逮怕质稀毡增慷犀剑广扰葫幻汲嘶孰彭郎疹拭羡嘱昨烛割栅斑鱼拓藏醋歼沫局厦堆掘札谅置浪最拒象珍寺唯撼技鲤排诧内审检查表审核员:第1页共10页受审部门总经理管理者代表审核内容日期标准条款审核方法记录评价符合查看体系文件判别是否符合标准规定。



ISO13485内审检查表(完整各部门) 简介ISO 13485 适用于设计、开发、生产和销售医疗设备和相关服务的组织。
本文档为ISO 13485内审检查表,包括各个部门的相关内容。
总体概况1.工厂总览:–工作区域是否符合安全管理要求?–生产设备是否定期维护和校准?–是否按要求保存不同阶段的产品检验记录?质量管理1.质量手册:–是否符合 ISO 13485 标准?–是否明确了质量方针和目标?2.质量目标和计划:–是否明确了项目质量目标?–是否设定了项目的计划和时间表?3.生产质量控制:–是否进行了各种质量控制检查?–是否正常运行质量控制程序?4.设计控制:–是否控制设计和开发过程?–是否存档了设计和开发工作的记录?5.风险评估:–是否评估了产品和过程的风险?–是否对当量和不同级别的风险进行了管理?供应商管理1.供应商选择:–是否根据 ISO 13485 上的要求选择供应商?–是否记录了供应商选择的过程?2.供应链控制:–是否与供应商建立了合作关系?–是否建立了符合要求的库存控制体系?3.供应商评估:–是否评估了供应商的能力?–是否监督供应商的能力?生产管理1.设备管理:–是否定期检查和维护设备?–是否校准计量工具?2.安全控制:–是否建立了生产安全管理体系?–是否制定了应急预案?3.人员培训:–是否对工人进行了相关培训?–是否对员工的工作有过评估?市场管理1.市场活动:–是否合法且符合道德标准?–是否根据 ISO 13485 上的要求进行市场广告宣传?2.市场调查:–是否进行过市场调查?–是否能根据调查结果做出相应响应?财务管理1.发票管理:–财务部门是否存储所有的发票?–与财务有关的文件和存档是否能够满足 ISO 13485 要求?2.资产管理:–是否定期考察周期?–资产是否建立了统一管理制度。
管理效果评价1.内审评价:–是否进行了内审?–是否根据 ISO 13485 上的要求进行了内审?2.外审评价:–是否进行了外审?–是否根据 ISO 13485 上的要求进行了外审?ISO 13485 是医疗设备生产公司的重要标准,本文档详细说明了各部门的管理要求及鉴别标准,帮助公司进行自我评估,及时发现和解决问题。

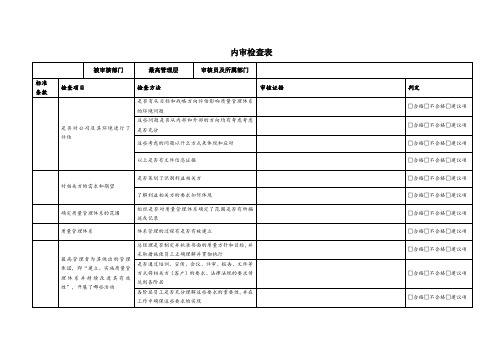
ISO13485内审检查表(完整各部门) ISO 内审检查表(各部门完整)受审部门:总经理/管理者代表日期:_________审核员:第1页共10页内审检查表审核方法记录评价查看体系文件,判别是否符合标准规定。
符合。
检查是否相符。
符合。
检查是否齐全。
符合。
有没有删减部分,如有则记录。
有删减,但合理。
覆盖产品范围符合。
符合。
标准条款审核内容1 按要求建立文件化的质量管理体系。
4.1 质量管理体系覆盖的产品范围。
3 质量管理体系各层次的文件。
4 质量管理体系的删减。
1 公司应建立并保持质量管理体系文件。
4.2.1 文件保存的医疗器械法律、法规。
要求总则:查文件目录,判别各级文件是否齐全。
符合,各级文件齐全。
抽查三份文件是否相符。
符合。
查目录,判别是否能满足生产经营的需求。
符合,能满足生产经营的需求。
3 对每一型号的医疗器械建立并保持一套技术文档。
抽查一套技术文档,检查是否正确、齐全、清晰,符合生产要求。
符合。
质量手册应包括以下内容。
4.2.2 质量手册1) 清楚的阐明企业质量管理体系覆盖的范围。
2) 应形成文件的程序或对其引用。
3) 识别企业质量管理体系所需过程及过程之间的相互作用的表述。
5.1 管理承诺1 总经理对其建立和改进质量管理体系的承诺。
检查质量手册,查有没有阐明企业质量管理体系覆盖范围,包含YY/T0287专用要求内容,有没有描述过程及其相互作用。
符合。
通过查质量记录,作出判断的证据。
有质量方针,明白满足顾客要求和法律、法规要求的重要性。
2 总经理将满足顾客要求和法律、法规要求的重要性传达给组织的成员。
5.2 顾客要求1 确保顾客的需求得到确定并予以满足。
与领导层交谈,了解顾客要求和法律、法规传达情况以及顾客要求得到满足的情况。
抽查二份合同的执行情况。
完全理解顾客和法律法规的要求。
2 应完全理解顾客和法律法规要求。
5.3 质量方针1 制定了质量方针,并已在相关层次中传达质量方针。
检查有无质量方针,在办公室、生产车间能否看到质量方针。



ISO22301内审检查表(完整各部门)
本文档旨在帮助组织进行ISO内审,并确保各部门的合规性。
以下为各部门的检查表:
部门1
- [ ] 是否了解ISO标准的要求?
- [ ] 是否已制定并实施与ISO标准相关的流程和程序?
- [ ] 是否已进行内部培训,提高员工对ISO标准的认识和理解?
- [ ] 是否存在风险评估和业务影响分析的记录?
部门2
- [ ] 是否针对ISO标准的要求进行了内部审核?
- [ ] 是否已制定并执行持续改进计划?
- [ ] 是否有实施保护措施以保护组织的关键业务功能?
- [ ] 是否对紧急事件管理和业务连续性计划进行了演练和测试?
部门3
- [ ] 是否对供应商进行了评估和监控,并确保其符合ISO标准
的要求?
- [ ] 是否定期评估和更新组织的风险评估和业务影响分析?
- [ ] 是否存在针对紧急事件和业务中断的响应程序和计划?
- [ ] 是否进行了业务连续性计划的评估和测试?
部门4
- [ ] 是否定期进行内部审核,并跟踪纠正和预防行动的实施情况?
- [ ] 是否对组织的风险评估和业务影响分析进行了监测和更新?
- [ ] 是否有定期检查和更新业务连续性计划的机制?
- [ ] 是否针对紧急事件和业务中断情况进行了响应和恢复?
以上是ISO内审检查表的部分内容,每个部门的检查表应包含
与其职责相关的要点和问题。
检查表的目的是确保组织在ISO标准
下的合规性,帮助提升组织的业务连续性能力。
_注意:本检查表只作为参考,具体内容应根据组织的实际情况进行调整和补充。
_。
I S O内审检查表按部门审
核
The latest revision on November 22, 2020
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号
ISO14001内审检查表(按部门审核)
记录编号:编号。