2021年乙醇乙酸知识点
- 格式:doc
- 大小:752.50 KB
- 文档页数:10

高中化学知识点:乙醇和乙酸1. 乙醇的性质和制备方法乙醇是一种有机化合物,化学式为C2H5OH。
它是常见的酒精,常用作溶剂和消毒剂。
乙醇具有以下性质:•乙醇是一种无色、具有刺激性气味的液体,在常温下易挥发。
•它可与水混溶,形成不同浓度的醇溶液。
•乙醇具有酸碱性,可与碱反应生成乙醇盐。
乙醇的制备方法主要有两种:1.1 从蔗糖发酵制备乙醇蔗糖(C12H22O11)在酵母的催化下发生发酵反应,生成乙醇和二氧化碳。
这是制备乙醇的常见方法,也是酿酒的过程。
反应方程式:蔗糖 + 酵母→ 乙醇 + 二氧化碳1.2 从乙烯水合制备乙醇乙烯(C2H4)与水在催化剂存在下进行加成反应,生成乙醇。
这是一种工业上常用的制备乙醇的方法。
反应方程式:乙烯 + 水→ 乙醇2. 乙酸的性质和制备方法乙酸是一种无色液体,化学式为CH3COOH。
它是一种常见的有机酸,常用作食品添加剂和工业原料。
乙酸具有以下性质:•乙酸具有刺激性气味,并有酸味。
•它是一种极易挥发的液体,在常温下能与空气快速溶合。
•乙酸可溶于水,形成酸性溶液。
乙酸的制备方法主要有两种:2.1 从乙醇氧化制备乙酸乙醇通过催化剂的氧化反应,生成乙酸和水。
这是一种常见的制备乙酸的方法。
反应方程式:乙醇 + 氧气→ 乙酸 + 水2.2 从乙烯羧化制备乙酸乙烯与过氧化物反应,生成乙酸。
这是另一种制备乙酸的方法。
反应方程式:乙烯 + 过氧化物→ 乙酸3. 乙醇和乙酸的应用3.1 乙醇的应用乙醇具有广泛的应用领域:•作为溶剂:乙醇是一种常用的溶剂,在化学实验室和工业生产中被广泛使用。
•化妆品和个人护理产品:乙醇常用于制造香水、口红和洗手液等化妆品和个人护理产品。
•燃料:乙醇可以用作燃料,例如乙醇汽油用于汽车等内燃机的燃料。
•酿酒:乙醇是酒精的主要成分,用于酿造各种酒类。
3.2 乙酸的应用乙酸也有广泛的应用:•食品添加剂:乙酸可用作食品的酸味剂和防腐剂。
•化学品生产:乙酸是合成其他有机化合物的重要原料,例如合成纤维素醋酸纤维。

乙醇和乙酸知识点乙醇和乙酸是我们日常生活中常见的化学物质。
乙醇是一种有机化合物,也被广泛应用于医学、工业和消费品中。
乙酸是一种酸性物质,常用于食品加工和制药工业。
在本文中,我们将详细了解乙醇和乙酸的性质、用途以及其它相关知识点。
乙醇1. 乙醇的分子结构乙醇的化学式为C2H5OH,它由两个碳原子、六个氢原子和一个氧原子组成。
乙醇的分子结构使其具有一些特殊的性质。
2. 乙醇的性质乙醇是一种透明、无色的液体,具有独特的气味。
它具有一定的挥发性和可燃性。
乙醇可与水混溶,并且与许多有机和无机物质反应。
3. 乙醇的用途乙醇在医学、工业和消费品中有广泛的应用。
•医学应用:乙醇是一种常见的消毒剂,可以用于清洁伤口和消毒工具。
它还被用作某些药物的溶剂。
•工业应用:乙醇是许多工业过程中的重要原料。
它被用于生产塑料、颜料、溶剂等。
•消费品应用:乙醇也是许多消费品的成分之一,如香水、洗发水和口香糖等。
乙酸1. 乙酸的分子结构乙酸的化学式为CH3COOH,它由两个碳原子、四个氢原子和两个氧原子组成。
2. 乙酸的性质乙酸是一种具有刺激性气味的液体,呈无色或微黄色。
它是一种弱酸,可与碱反应生成盐和水。
乙酸还可以发生酯化反应,生成乙酸酯。
3. 乙酸的用途乙酸在食品加工和制药工业中有广泛的应用。
•食品加工:乙酸被用作食品酸化剂和防腐剂。
它在酱料、果酱和果汁等食品中被广泛使用。
•制药工业:乙酸是制药工业中的重要原料之一。
它被用于合成药物、染料和涂料等。
乙醇和乙酸的差异尽管乙醇和乙酸的化学式非常相似,但它们在性质和用途上有一些明显的差异。
•性质:乙醇是一种醇类物质,而乙酸是一种酸类物质。
乙醇具有挥发性和可燃性,而乙酸是一种刺激性液体。
乙酸是一种弱酸,而乙醇不具有酸性。
•用途:乙醇主要用于医学、工业和消费品中,而乙酸主要用于食品加工和制药工业。
在我们的日常生活中,乙醇和乙酸扮演着重要的角色。
我们可以在消毒、食品加工和制药等方面看到它们的应用。

乙醇和乙酸知识点总结一、乙醇1.1 物理性质乙醇的化学式为C2H5OH,是一种无色、有甜味的液体。
乙醇在室温下呈无色透明的液体,密度为0.789g/cm³。
其沸点为78.3℃,熔点为-114.1℃,易挥发,具有刺激性气味。
乙醇可溶于水和许多有机溶剂,与水混合后呈中性溶液。
1.2 化学性质乙醇是一种重要的有机溶剂,在有机合成和日常生活中有着广泛的应用。
它可以被用作食品添加剂、工业原料、燃料、药剂等。
此外,乙醇还是酒精的主要成分,是一种具有麻醉作用的药物,长期饮用会对人体的健康产生不良影响。
1.3 制备乙醇可以通过自然发酵、合成醇和乙烯水合等方法进行生产。
自然发酵是利用某些微生物(如酵母菌)在无氧条件下将含糖物质发酵成酒精。
合成醇是通过水和一定量的乙烯在催化剂的作用下生成乙醇。
乙烯水合是将乙烯与水在阳离子交换树脂的催化剂作用下生成乙醇。
1.4 应用乙醇在医药、化工、食品、饮料等领域都有着广泛的应用。
在医药领域,乙醇可作为一种抗菌消毒剂,用于清洁伤口和器械。
在化工领域,乙醇可用作有机溶剂、原料和裂化剂。
在食品饮料领域,乙醇可用作食品添加剂,用于调味和防腐。
1.5 安全注意事项乙醇有毒,长期接触或吸入会对身体健康产生危害。
在使用乙醇时,应注意避免接触皮肤和眼睛,并确保通风良好。
另外,乙醇易燃,使用过程中应远离火源和高温,避免发生安全事故。
二、乙酸2.1 物理性质乙酸的化学式为CH3COOH,是一种有刺激性气味的无色液体。
乙酸在室温下呈无色透明的液体,密度为1.049g/cm³。
其沸点为118.1℃,熔点为16.6℃,易挥发,具有刺激性气味。
乙酸可溶于水和许多有机溶剂,与水混合后呈中性溶液。
2.2 化学性质乙酸是一种重要的有机酸,具有强烈的腐蚀性。
乙酸可以被用作有机溶剂、食品添加剂、医药原料、工业原料等。
此外,乙酸还是醋的主要成分,具有食用和药用价值。
然而,乙酸也具有一定的毒性,长期接触或吸入会对身体健康产生危害。

高考化学常见有机物知识点:乙醇、乙酸的性质乙醇结构简式CH?CH?OH或C?H?OH,化学式C?H?O,是最常见的一元醇,下文整理了高考化学常见有机物知识点:乙醇、乙酸的性质,希望可以帮助到大家!乙酸物理性质:乙酸在常温下是一种有强烈刺激性酸味的无色液体.乙酸的熔点为16.6℃(289.6 K).沸点117.9℃(391.2 K).相对密度1.05,闪点39℃,爆炸极限4%~17%(体积).纯的乙酸在低于熔点时会冻结成冰状晶体,所以无水乙酸又称为冰醋酸.乙酸易溶于水和乙醇,其水溶液呈弱酸性.乙酸盐也易溶于水.下为中华人民共和国关于工业乙酸的国家标准.乙醇物理性质:乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率.例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度.乙酸化学性质:1、铁、镁和锌,反应生成氢气和金属乙酸盐.2、同样,乙酸也可以成酯或氨基化合物.如乙酸可以与乙醇在浓硫酸存在并加热的条件下生成乙酸乙酯(本反应为可逆反应,反应类型属于取代反应中的酯化反应).3、乙酸的酸性促使它还可以与碳酸钠、氢氧化铜、苯酚钠等物质反应等等.乙酸鉴别:乙酸可以通过其气味进行鉴别.若加入氯化铁(III),生成产物为深红色并且会在酸化后消失,通过此颜色反应也能鉴别乙酸.乙酸与三氧化砷反应生成氧化二甲砷,通过产物的恶臭可以鉴别乙酸.乙醇化学性质:1、乙醇分子中含有极化的氧氢键,电离时生成烷氧基负离子和质子.2、乙醇的酸性很弱,但是电离平衡的存在足以使它与重水之间的同位素交换迅速进行.CH3CH2OH+D2O→(可逆)CH3CH2OD+HOD3、因为乙醇可以电离出极少量的氢离子,所以其只能与少量金属(主要是碱金属)反应生成对应的醇金属以及氢气4、消去反应5、乙醇可以与空气中氧气发生剧烈的氧化反应产生燃烧现象,生成水和二氧化碳.6、乙醇可以在浓硫酸和高温的催化发生脱水反应,随着温度的不同生成物也不同7、乙醇具有还原性,可以被氧化成为乙醛.酒精中毒的罪魁祸首通常被认为是有一定毒性的乙醛,而并非喝下去的乙醇.小编为大家提供的高考化学常见有机物知识点:乙醇、乙酸的性质大家仔细阅读了吗?最后祝大家可以考上理想的大学。

乙醇乙酸的知识点总结一、乙醇乙酸的化学性质1. 乙醇乙酸的化学式为C4H8O2,是一种无色、有毒的液体。
2. 乙醇乙酸是一种饱和脂肪酸,属于羧酸类化合物。
3. 乙醇乙酸是一种具有药物效果的化合物,可以用于制药工业及医药领域。
4. 乙醇乙酸是一种重要的化工原料,广泛应用于合成酯类化合物、溶剂、香料等。
5. 乙醇乙酸是一种具有腐蚀性的化合物,应注意其安全使用和储存。
6. 乙醇乙酸的密度为1.049 g/cm3,沸点为141°C,熔点为16.6°C。
二、乙醇乙酸的制备方法1. 乙醇乙酸可以通过乙烯氧化法制备,将乙烯与氧气经过催化剂的作用,生成乙醇,再通过氧化反应生成乙醇乙酸。
2. 乙醇乙酸还可以通过乙醇氧化法制备,将乙醇经过氧气氧化反应生成乙醇乙酸。
3. 乙醇乙酸还可以通过醋酸酐和乙醇反应生成,醋酸酐与乙醇反应生成乙酸乙酯,再通过水解反应生成乙醇乙酸。
三、乙醇乙酸的应用领域1. 乙醇乙酸是一种重要的工业原料,在化工领域广泛用于合成其他化合物,如醋酸丁酯、醋酸乙酯等。
2. 乙醇乙酸在医药领域具有抗菌、杀菌的功效,常用于制药工业生产药物。
3. 乙醇乙酸可以用作有机溶剂,在涂料、油墨、香料等行业有重要应用。
4. 乙醇乙酸也被广泛应用于食品添加剂领域,用作食品酸化剂和防腐剂。
四、乙醇乙酸的安全性及注意事项1. 乙醇乙酸是一种有毒化合物,长期暴露或高浓度接触可能对人体造成伤害,并且会对环境产生一定的危害。
2. 在使用乙醇乙酸时应注意其防护措施,避免接触皮肤和眼睛,同时避免吸入其蒸气。
3. 乙醇乙酸应储存在阴凉、干燥、通风的仓库中,远离火源和氧化剂,避免高温或直接阳光照射。
4. 在使用乙醇乙酸时应注意其蒸气的排放,避免对周围环境造成污染。
五、乙醇乙酸的环境影响及处理方法1. 乙醇乙酸对环境会产生一定的危害,长期暴露会导致土壤酸化、水源污染等问题。
2. 在工业生产和使用乙醇乙酸时,应采取相应的环保措施,减少其对环境造成的影响。

知识点23:乙醇和乙酸(06-11-28)班级:____________姓名:____________【默写内容】①硫酸铝和氨水反应的离子方程式:_________________________________________________________②氢氧化铝和烧碱溶液反应的离子方程式:__________________________________________________③氢氧化铝受热分解:____________________________________________________________________④碳酸氢钠受热分解:____________________________________________________________________⑤碳酸钠和盐酸反应:____________________________________________________________________ 【高考考点】①乙醇和乙酸的结构和性质;②乙醇和乙酸在生活中的应用。
【要点填空】⑴乙醇的分子式___________,结构式_________________,结构简式______________或_____________,乙醇俗名_________,是____色、有特殊香味的_____体,密度比水_____,沸点_________,_____挥发,能够溶解多种有机物和无机物,能与水以____________互溶。
在医院里经常用来___________________。
⑵乙醇的化学性质:乙醇分子结构中含有—OH基团,称为______基,从而乙醇和乙烷的性质大相径庭。
①乙醇与金属钠反应:▓▓____________________________________________________________▓▓★比较★水与钠反应:▓▓____________________________________________________________▓▓★说明★1、水、乙醇、钠三者密度由大到小顺序是____________________________2、乙醇中—OH上的氢原子________水中的氢原子活泼②乙醇的氧化反应:a、在氧气中燃烧▓▓_________________________________________________________________▓▓b、在Cu或Ag做催化剂的条件下被空气中氧气氧化为______(______________),此过程中Cu先在酒精灯上灼烧生成_________,再插入乙醇中生成______,所以Cu或Ag反应前后的质量_______。

高考乙醇乙酸知识点一、引言高考化学中的乙醇和乙酸是重要的有机化合物,学好它们的相关知识点,对于理解有机化学的基本概念和原理具有重要意义。
本文将重点介绍高考化学中与乙醇和乙酸相关的知识点。
二、乙醇的基本性质乙醇,化学式C2H5OH,是一种醇类化合物。
以下是乙醇的一些基本性质:1. 物理性质:(1)无色液体,具有特殊的酒精气味;(2)沸点约为78℃,密度约为0.79 g/mL;(3)可与水混溶,与很多有机物互溶;2. 化学性质:(1)乙醇可以被氧化,生成醛、酸等产物;(2)乙醇可以被还原,生成乙烷;(3)乙醇可发生酯化反应,生成乙酸乙酯等酯类产物。
三、乙酸的基本性质乙酸,化学式CH3COOH,是一种有机酸。
以下是乙酸的一些基本性质:1. 物理性质:(1)无色液体,具有刺激性气味;(2)沸点约为118℃,密度约为1.05 g/mL;(3)可与水混溶,生成酸性溶液;2. 化学性质:(1)乙酸具有酸性,可以与碱反应生成乙酸盐;(2)乙酸可以与醇反应,生成酯类物质;(3)乙酸可以被氧化,生成二氧化碳和水。
四、乙醇和乙酸的相关反应1. 醇的氧化反应:醇可以被氧化为酮、醛或羧酸。
乙醇氧化的反应方程式如下:C2H5OH + [O] → CH3CHO + H2OC2H5OH + 2[O] → CH3COOH + H2O2. 酸酐的酯化反应:酸酐可以与醇发生酯化反应,生成酯。
乙酸酐与乙醇酯化的反应方程式如下:CH3COOC2H5 + C2H5OH → CH3COOC2H5 + H2O3. 酯的水解反应:酯可以被酸性、碱性水解为醇和酸盐。
乙酸乙酯水解的反应方程式如下:CH3COOC2H5 + H2O → CH3COOH + C2H5OHCH3COOC2H5 + NaOH → CH3COONa + C2H5OH五、乙醇和乙酸在生活中的应用乙醇和乙酸在日常生活中有广泛的应用,例如:1. 乙醇:(1)用作消毒剂,可用于伤口消毒;(2)制备香精、饮料等;(3)作为溶剂,用于印刷、染料等行业。


有机化学基础专题讲解(乙醇和乙酸)一、 乙醇的物理性质和重要用途: 物理性质:1、乙醇俗称酒精,是酒的主要成分。
它是无色透明,具有特殊香味的液体,密度比水小,沸点为78.5度,易挥发,能与水任意比互溶。
重要用途:作燃料、有机溶剂、消毒剂、酿酒、化工原料。
甲醇CH 3 CH 3OH ,医用乙醇浓度为75%。
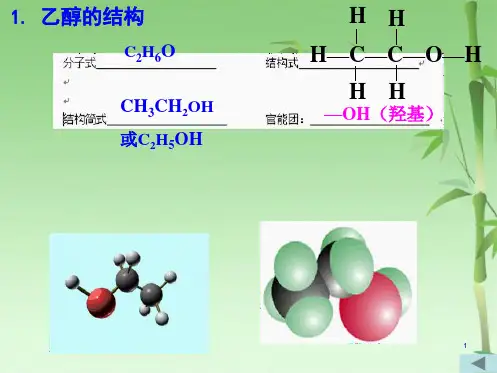
二、乙醇的分子结构: 分子式C 2H 6O结构简式CH 3 CH 2 OH 三、乙醇的化学性质:1、 取代反应: 2CH 3CH 2OH +2Na 2CH 3CH 2ONa + H 2↑CH 3CH 2OH + HBr CH 3CH 2Br + H 2O2CH 3CH 2OHCH3CH 2OCH 2CH 3 +H 2O (分子间脱水) CH 3COOH +CH 3CH 2OHH 2O + CH 3COOC 2H 5 (酯化反应)2、 消去反应(脱水)的反应条件: —邻碳有氢,浓硫酸,170℃CH 3CH 2OH H 2O + CH 2=CH 2 ↑3、氧化反应(脱氢重键式)的反应条件: —邻碳有氢,Cu 、Ag 催化,加热2CH 3CH 2OH + O 2 2CH 3CHO + 2H 2O三、乙醇的工业制法:发酵法:C 6H 12O 6 2CH 3CH 2OH+2CO 2↑乙烯水化法: CH 2=CH 2+H 2O CH 3CH 2OH浓硫酸△△浓H 2SO 4 140℃浓H 2SO 4 170℃Cu △醇的分类(1)根据醇分子里羟基的数目,醇可分为:(2)根据与羟基连接的烃基种类分:题1乙醇分子结构中各化学键如图所示。
关于乙醇在各种反应中断键的说法不正确的是()A. 和金属钠反应时①键断裂B. 乙醇燃烧时断裂②和⑤键C.在银催化条件下与O 2反应时断裂①和③键 D. 和浓H 2SO 4、乙酸共热时断裂①键,其他键不变化题2 用分液漏斗可以分离的一组混合物是 ( )A. 乙醇和水B. 乙酸和水C. 溴苯和水D. 乙酸和乙醇题3. 下列物质不能从溴水中萃取溴的是( ) A. 乙醇 B. 苯 C. 四氯化碳 D. 戊烷题4. 下列物质,都能与Na 反应放出H 2,其产生H 2的速率由快到慢的顺序是( ) ①C 2H 5OH ②CH 3COOH (aq ) ③NaOH (aq )A. ①>②>③B. ②>①>③C. ③>①>②D. ②>③>① 醇一元醇:如 CH 3OH (甲醇)、CH 3CH 2OH (乙醇) 二元醇:如 CH 2―CH 2 (乙二醇) OH OH三元醇:如 CH 2―CH ―CH 2 (丙三醇)醇 脂肪醇:烃基为链烃基,如 CH 3CH 2CH 2OH 脂环醇:烃基为脂环烃基,如 芳香醇:烃基中含苯环,如 OHCH 2OH题5. 某有机物的结构简式为:,下列关于该有机物的叙述不正确的是()A. 能与金属钠发生反应并放出氢气B. 能在催化剂作用下与H2发生加成反应C. 能发生银镜发应D. 在浓H2SO4催化下能与乙酸发生酯化反应题6、甲醇、乙二醇、丙三醇中分别加入足量的金属钠产生等体积的氢气(相同条件),则上述三种醇的物质的量之比是( )A.2∶3∶6B.3∶2∶1C.4∶3∶1D.6∶3∶2题7.酒后驾车是引发交通事故的重要原因。

高一乙醇乙酸知识点总结乙醇与乙酸是我们日常生活中常见的有机化合物之一,它们具有一定的重要性和应用价值。
在高一化学学习中,对于乙醇和乙酸的了解是非常重要的。
本文将对乙醇与乙酸的相关知识点进行总结,以帮助同学们更好地理解和掌握这两种有机化合物。
一、乙醇的性质与应用1. 乙醇的结构和化学式乙醇的结构式为CH3CH2OH,化学式为C2H5OH,由于其中含有羟基(OH)官能团,因此乙醇也可以被称为醇类有机物。
2. 乙醇的物理性质乙醇是一种无色、气味芳香的液体,在室温下易挥发,可与水混溶。
乙醇的密度约为0.79 g/cm³,沸点约为78.5℃。
3. 乙醇的化学性质乙醇是一种具有醇的特性的有机化合物,具有醇的通性。
例如,乙醇可以与酸发生酯化反应,与碱发生醇化反应。
此外,乙醇还可被氧化剂如酸性高锰酸钾氧化为乙醛或乙酸等化合物。
4. 乙醇的应用乙醇在工业、医药、化妆品等领域具有广泛的应用。
它可以作为溶剂、消毒剂和燃料等。
此外,乙醇还可以用于制备醋酸乙酯、氯仿等有机化合物。
二、乙酸的性质与应用1. 乙酸的结构和化学式乙酸的结构式为CH3COOH,化学式为C2H4O2,乙酸是一种含有羧基(COOH)官能团的有机化合物。
2. 乙酸的物理性质乙酸是一种具有刺激性气味的无色液体,密度约为 1.05 g/cm³,沸点约为118℃。
乙酸可与水混溶,但不能与非极性溶剂如石油醚混溶。
3. 乙酸的化学性质乙酸是一种弱酸,可与碱发生酸碱中和反应生成对应的盐和水。
乙酸也可以发生酯化反应,与醇类反应生成相应的酯。
4. 乙酸的应用乙酸广泛应用于化学工业、食品工业等领域。
它可以作为食品酸味剂的添加剂,也可以用于制备乙酸乙酯、乙酸纤维素等化合物。
此外,乙酸还可以用于制取醋酐、染料等。
三、乙醇与乙酸的相互转化1. 乙醇转化为乙酸乙醇经过氧化反应可以转化为乙醛,再进一步氧化则转化为乙酸。
常见的乙醇氧化剂有酸性高锰酸钾等。
2. 乙酸还原为乙醇乙酸在适当条件下可以被还原为乙醇。
乙醇乙酸知识点方程式乙醇乙酸是一种常见的有机化合物,它的化学式为C4H8O2。
它由乙醇和乙酸酐反应而成,下面我们一步一步地来探讨乙醇乙酸的相关知识和化学方程式。
1.乙醇乙酸的结构乙醇乙酸是由两个碳原子、六个氢原子和两个氧原子组成的有机分子。
它的结构可以表示为CH3CH2COOH。
在这个分子中,醇基(-OH)与酸基(-COOH)相连。
2.乙醇与乙酸酐的反应乙醇乙酸的合成可以通过乙醇和乙酸酐的酯化反应进行。
乙酸酐是乙酸与酸酐化剂(如酸氯化剂)反应得到的产物。
酯化反应的化学方程式如下:CH3CH2OH + CH3COOCCH3 -> CH3CH2COOH + CH3COOCH3在这个反应中,乙醇与乙酸酐反应生成乙醇乙酸和乙酸乙酯。
3.化学性质乙醇乙酸是一种酸性物质。
它可以与碱反应生成相应的盐。
例如,与氢氧化钠反应可以生成乙酸乙酸钠:CH3CH2COOH + NaOH -> CH3CH2COONa + H2O此外,乙醇乙酸还可以与一些金属反应生成相应的金属盐。
4.物理性质乙醇乙酸是一种无色液体,具有特殊的酸味。
它在常温下具有较低的沸点和熔点,可溶于水和大多数有机溶剂。
5.应用乙醇乙酸在工业上具有广泛的应用。
它常被用作溶剂、媒染剂和防腐剂。
此外,乙醇乙酸还可以用于合成其他有机化合物。
总结:乙醇乙酸是一种常见的有机化合物,由乙醇和乙酸酐反应而成。
它具有酸性,可与碱反应生成相应的盐。
乙醇乙酸是一种无色液体,具有特殊的酸味。
在工业上,乙醇乙酸被广泛应用于溶剂、媒染剂和防腐剂等领域。
这篇文章介绍了乙醇乙酸的结构、合成反应、化学性质、物理性质以及应用。
希望对你对乙醇乙酸有更深入的了解。
期末复习乙醇乙酸考点一、乙醇—、乙醇的结构与性质L 乙醇的结构特点:(L )乙醇分子中有C — 、 C ―、C —0, □—H 4种化学键:(2}官能团为短基,且轻基氨最活泼总的化学力程式:ZCH M CH/WS —^―>2CH 3ClfO * 21^0 反阀中钳(也可用银)作借化剂•补充:(1)乙醇可被其他强氧化剂氧化:能被酸性高锰酸钾溶液或酸性重铬酸钾溶液所氧化,被直接氧化 成乙酸(使酸性高锰酸钾的紫色褪去) 。
(2) 乙醇与钠的反应可以验证乙醇中有一个氢原子与其他氢原子不同。
(3)— OH 与0H -的区别与联系羟基(一OH ) 氢氧根(OH -)电子式—0H ; ■ O 1 H (有年电匚叮:「「6 ;电性 电中性带负电的阴离子存在形式 不能独立存在 能独立存在与溶液或离子化合物中稳定性 不稳定,能与Na 等发生反应 较稳定,即使与 Fe3+等发生反应,也是整体 参与的,OH —并未遭破坏. 相同点组成兀素相冋【典例1】比较乙烷和乙醇的分子结构 ,下列说法中错误的是 ( )A. 两个碳原子均以单键相连B. 分子里都含6个相同的氢原子C •乙基与一个氢原子相连就是乙烷分子 D.乙基与一个羟基相连就是乙醇分子 【典例2】乙醇分子中的各种化学键如图所示 ,下列关于乙醇在各种反应中断裂键的说法中不正确的是 ( )的剤昼插 人乙皿申1 ------- —*«化学反应 键的断裂 反应方程式反应类型 与钠的反应断①键 2CH 3CH 2OH+2Na 2CH 3CH 20Na+H 21置换反应 燃烧 断①②③④⑤键点燃CH 3CH 2OH+3O 2 -------------- J 2CO 2+3H 2O氧化反应 催化氧化断①③键2CH3CH2OH+O2—忑2CH 3CHO+2H 2O氧化反应与乙酸反应 断①键{ 0CH3 CTH+H LoCj 耳十呼酯化反应2.化学键的断裂(1 )乙醇反应时的断键情况(2)举例(乙醇的倦化氧化):WIJ12Cu+<h-^-2CuO铜代由红色恋为怩色-f —G —^C —O —⑤』血占…③'厂――7仝.艇状的兩11—、:—|A.和金属钠反应时键①断裂B. B.在铜或银催化共热下与 Q 反应时断裂①和③C. 在铜或银催化共热下与 Q 反应时断裂①和⑤D. 在空气中完全燃烧时断裂①②③④⑤考点二、乙酸在发生化学反应时,乙酸的主要新嚥方式有;CH -C +O +H—阴性 1---- 酯化反应⑴乙酸具有明显的酸性,在水溶液里能部分电离,电离方程式 CfCOOH ■ CH3COO_+H ■。
乙醇乙酸知识点总结一、乙醇的化学性质1. 密度和沸点:乙醇的密度为0.7893g/cm³,沸点为78.4℃,比水的沸点略高。
2. 溶解性:乙醇是一种极性分子,能够与许多有机物和无机物发生相互作用,因此在水中具有良好的溶解性。
3. 燃烧性:乙醇是一种易燃易爆的物质,能够燃烧释放大量热量和二氧化碳,因此常被用作燃料。
4. 氧化性:乙醇可以被氧化为乙醛和乙酸,发生还原反应时则可还原为乙醛和乙醇。
5. 酸碱性:乙醇呈现微弱酸性,可被氢氧根离子和碱性氧化剂中和生成乙醇盐。
二、乙醇的制备方法1. 天然发酵:通过天然发酵方法可以将含糖、淀粉或纤维素的植物原料转化为酒精。
2. 化学合成:乙醇也可以通过化学合成方法制备,通常通过乙烯水合反应或乙醛还原反应得到。
三、乙醇的用途1. 饮料加工:乙醇是制备酒精饮料的主要原料,如啤酒、白酒、红酒等。
2. 药品制备:乙醇是许多药品和药物的溶剂和合成原料,也被用作外科手术前的消毒。
3. 工业用途:乙醇在化工领域广泛用于制备乙醛、醋酸、酯类等有机化合物。
4. 燃料制备:乙醇可以用作燃料,被加入汽油中作为车用燃料,也可用于生物柴油的生产。
四、乙醇的危害1. 毒性:乙醇是一种有毒的物质,过量摄入或长期饮酒会对肝脏、大脑等器官造成损害。
2. 燃烧性:乙醇是一种易燃易爆的物质,若使用不当可能会引发火灾或爆炸事故。
3. 环境污染:乙醇的工业生产和使用会产生大量的废水和废气,对环境造成污染。
4. 非法使用:乙醇被用于非法酿造酒精饮料,严重影响社会治安和人民健康。
五、乙酸的化学性质1. 密度和沸点:乙酸的密度为1.05g/cm³,沸点为118.1℃,比水的沸点高。
2. 酸碱性:乙酸是一种弱酸,能够与碱性物质发生中和反应生成乙醋盐。
3. 溶解性:乙酸是一种极性分子,能够与水和有机溶剂发生溶解作用。
4. 氧化性:乙酸可以被氧化为二氧化碳和水,具有一定的还原性。
六、乙酸的制备方法1. 生物发酵:通过对含糖物质或纤维素进行发酵或醋酸发酵可以得到乙酸。
乙醇乙酸知识点
乙醇乙酸是一种常见的有机化合物,广泛应用于化工、医药、日用化工等行业。
它具有一系列特殊的性质和用途,下面我们将逐步介绍乙醇乙酸的相关知识点。
1.乙醇乙酸的化学式和结构:乙醇乙酸的化学式为C4H8O2。
它由两个
碳原子、六个氢原子和两个氧原子组成。
乙醇乙酸的结构式如下所示:
CH3CH2COOH
2.乙醇乙酸的性质:乙醇乙酸是一种无色液体,有特殊的酸味。
它可以
溶于水和多种有机溶剂,如乙醚、醇类等。
乙醇乙酸是一种具有较高沸点和闪点的有机酸。
3.乙醇乙酸的制备方法:乙醇乙酸可以通过乙醇的氧化反应得到。
常见
的制备方法有碱催化法和氧化剂氧化法。
碱催化法是将乙醇与氧气在碱的催化下反应生成乙醇乙酸。
氧化剂氧化法是将乙醇在氧化剂的作用下氧化为乙醛,然后再进一步氧化得到乙醇乙酸。
4.乙醇乙酸的用途:乙醇乙酸在工业上具有广泛的用途。
它常被用作溶
剂、媒染剂、调味剂等。
在医药领域,乙醇乙酸可用于制备多种药物原料和合成药物。
此外,乙醇乙酸还可用于生产醋酸纤维和涂料等。
5.乙醇乙酸的危害性:乙醇乙酸是一种有机酸,具有一定的腐蚀性和刺
激性。
长期接触乙醇乙酸可能对皮肤和黏膜造成伤害。
因此,在使用乙醇乙酸时应注意防护措施,避免直接接触。
以上是有关乙醇乙酸的一些基本知识点。
通过了解其化学式、结构、性质、制
备方法、用途和危害性,我们可以更好地理解和应用乙醇乙酸。
在使用乙醇乙酸时,我们需要注意其安全性,并遵循相关操作规范,以确保工作和生活的安全。
①加热,主要目的是提高反应速率,其次是使生成的乙酸乙酯挥发而收集,使平衡向正反应方向移动,提高乙醇、乙酸的转化率。
.乙酸的填充模型为.乙酸分子中所有原子均位于同一平面上.乙酸的填充模型为,故.乙酸分子中含有甲基,因此所有原子不可能共平面,故不能说明硫酸亚铁已变质,故A 错误;B .钠和乙醇反应生成乙醇钠和氢气,在乙醇中加入一小块钠,钠沉入底部并观察到气泡产生,说明钠的密度大于乙醇的密度,故B 正确;C .NaHCO 3溶液和CaCl 2不反应,故C 错误;D .向Cu(NO 3)2溶液中加入含淀粉的KI 溶液,发生反应,溶液变222Cu 4I 2CuI +I +-+=↓蓝色,生成白色沉淀是CuI ,故D 错误;选B 。
3.关于实验室制备乙酸丁酯的实验,下列叙述错误的是A .不能用水浴加热B .长玻璃管起冷凝回流作用C .加入过量乙酸可以提高1-丁醇的转化率D .提纯乙酸丁酯需要用水、氢氧化钠溶液洗涤【答案】D【解析】A .制备乙酸丁酯的温度为120℃左右,故不能使用水浴加热,A 正确;B .长玻璃导管其冷凝回流作用,增大反应物的转化率,B 正确;C .加入过量的乙酸可以使反应正向进行,提高丁醇的转化率,C 正确;D .乙酸丁酯能与氢氧化钠反应,不能用氢氧化钠洗涤,D 错误;故选D 。
4.乙酸分子的球棍模型如下图所示。
下列关于乙酸分子的说法中,不正确的是A .分子式为B .官能团为羧基242C H O C .结构简式为D .分子中的所有原子位于同一平面内3CH COOH 【答案】D【解析】A .根据乙酸分子的球棍模型可得知,乙酸分子的结构简式为CH 3COOH ,其分子式为C 2H 4O 2,A 正确;B.根据乙酸分子的球棍模型可得知,乙酸分子的结构简式为CH3COOH,其官能团为羧基,B正确;C.根据乙酸分子的球棍模型可得知,乙酸分子的结构简式为CH3COOH,C正确;D.根据乙酸分子的球棍模型可得知,乙酸分子中含有甲基,则所有原子不能位于同一平面内,D错误;故选D。