V320-高中化学-第五讲:烃的衍生物(一)
- 格式:pdf
- 大小:129.87 KB
- 文档页数:2



高一化学烃的衍生物知识点讲解
高一化学烃的衍生物知识点讲解
以下是查字典化学网为大家整理的关于《高一化学烃的衍生物知识点讲解》的文章,供大家学习参考!
烃的衍生物
①乙醇:
a、物理性质:无色,有特殊气味,易挥发的液体,可和水以任意比互溶,良好的溶剂
b、分子结构:分子式C2H6O,结构简式CH3CH2OH或C2H5OH,官能团羟基,OH
c、化学性质:ⅰ、与活泼金属(Na)反应:
2CH3CH2OH+2Na 2CH3CH2ONa+H2
ⅱ、氧化反应:燃烧:C2H5OH+3O2 2CO2+3H2O
催化氧化:2CH3CH2OH+O2 2CH3CHO+2H2O
ⅲ、酯化反应:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
d、乙醇的用途:燃料,医用消毒(体积分数75%),有机溶剂,造酒
②乙酸:
a、物理性质:无色,,有强烈刺激性气味,液体,易溶于水和乙醇。
纯净的乙酸称为冰醋酸。
b、分子结构:分子式C2H4O2,结构简式CH3COOH,官能团羧基,COOH
c、化学性质:ⅰ、酸性(具备酸的通性):比碳酸酸性强。

高中化学《烃的衍生物》精品教案一、教学目标1. 让学生了解烃的衍生物的概念,理解其与烃之间的关系。
2. 掌握烃的衍生物的分类方法,了解不同类型的烃的衍生物的结构特点和性质。
3. 能够运用结构决定性质的观念,分析判断烃的衍生物的性质。
4. 培养学生的实验操作能力,提高学生的科学探究素养。
二、教学重点1. 烃的衍生物的概念及分类。
2. 不同类型的烃的衍生物的结构特点和性质。
3. 结构决定性质的观念在烃的衍生物中的应用。
三、教学难点1. 烃的衍生物的概念的理解。
2. 各类烃的衍生物性质的判断。
四、教学方法1. 采用问题驱动法,引导学生探究烃的衍生物的概念和性质。
2. 利用案例分析法,分析不同类型的烃的衍生物的结构与性质的关系。
3. 运用实验教学法,培养学生的实验操作能力和科学探究素养。
五、教学过程1. 导入:以生活中的实例引入烃的衍生物的概念,激发学生的学习兴趣。
2. 新课导入:讲解烃的衍生物的概念,引导学生理解其与烃之间的关系。
3. 案例分析:分析不同类型的烃的衍生物的结构特点和性质,让学生理解结构决定性质的观念。
4. 课堂练习:让学生运用所学知识分析判断烃的衍生物的性质,巩固所学内容。
5. 实验教学:安排学生进行实验操作,培养学生的实验操作能力和科学探究素养。
6. 课堂小结:总结本节课所学内容,强调重点和难点。
7. 作业布置:布置适量作业,巩固所学知识。
六、教学评价1. 评价学生对烃的衍生物的概念的理解程度。
2. 评价学生对不同类型的烃的衍生物的结构特点和性质的掌握程度。
3. 评价学生运用结构决定性质的观念分析判断烃的衍生物的性质的能力。
4. 评价学生的实验操作能力和科学探究素养。
七、教学资源1. 教学PPT:包含烃的衍生物的概念、分类、性质等知识点。
2. 实验器材:用于进行烃的衍生物相关实验。
3. 案例分析材料:包含不同类型的烃的衍生物的结构和性质的实例。
八、教学进度安排1. 第1-2课时:讲解烃的衍生物的概念和分类。

高中化学烃的衍生物知识点化学是我们生活中广泛应用的学科,也是高中学业中流程科目之一。
其中烃是很重要的一个化学分支,包括一类由碳和氢原子组成的有机化合物。
烃的衍生物非常广泛,有很多在生活中被广泛使用,下面就介绍一下高中化学中关于烃衍生物的知识点。
一、烃的衍生物简介烃的衍生物是由烃分子中的一个或多个氢原子被其他原子或分子所取代的化合物。
根据取代基的不同,烃的衍生物可以分为醇、酚、醛、酮、羧酸、酯、胺、腈、卤代烃、烷基卤化物以及芳族烃等多种。
这些化合物在工业化学及日常生活中应用广泛,如酒精、羧酸类化合物、氨、麻醉剂等。
二、醇醇是烃的一种衍生物,它的分子中含有一个或多个羟基(-OH)。
醇以它的羟基而得名,例如甲醇、乙醇和丙醇等。
醇有许多性质和功能,其中最常见的是作为饮料或用于生产其他有机化合物,比如酯。
三、酚酚是一种由苯环上的一个氢原子被羟基所取代的有机化合物,化学式为C6H5OH。
酚可以作为消毒剂、防腐剂和颜料等方面的原料,同时也可制成不少药品,例如阿司匹林、麻醉剂。
但由于酚具有剧烈的腐蚀性和毒性,过度使用会引起严重的健康问题。
四、醛与酮醛和酮都是由烃分子中的碳氢键被氧原子所取代的化合物。
它们之间的区别是醛分子中有一个羰基(C=O),而酮分子中有两个羰基。
常见的醛包括甲醛和乙醛,可以用于杀菌、熏蒸等方面;酮则包括丙酮、己酮等,可以用于催化反应、制作绝缘材料。
五、羧酸羧酸分子中含有一个羧基(-COOH),能够与醇或胺形成酯或酰胺。
羧酸可以分为饱和脂肪酸和不饱和脂肪酸。
饱和脂肪酸存在于许多生物中,例如麻油、黄油、椰子油等,而不饱和脂肪酸则分布在水生和陆生动物中,例如鱼油、坚果等。
六、酯酯分子中含有一个羧酸和一个醇分子中的氢原子被取代掉了,能够用于制备香料、溶剂等。
酯可以按是否含有羰基分为二元酯和酸酐。
二元酯是指含有一个酸基和一个醇基的酯,例如甲酸乙酯、乙酸丙酯等。
而酸酐是由两个酸分子的羧基进行结合形成的,例如醋酸酐。




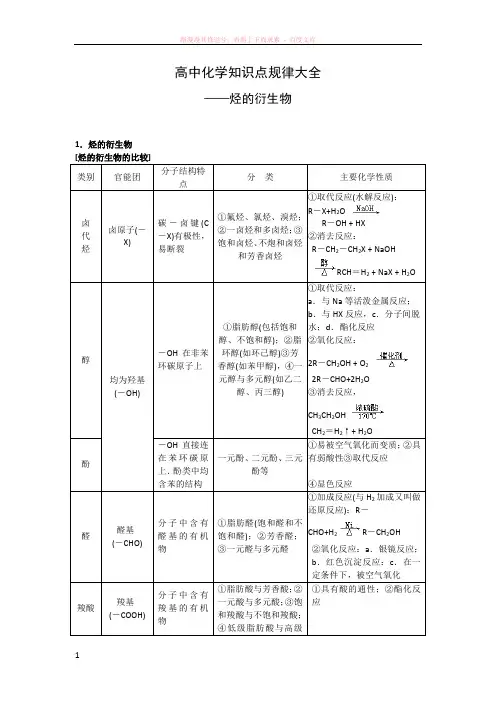
高中化学知识点规律大全——烃的衍生物1.烃的衍生物类别官能团分子结构特点分类主要化学性质卤代烃卤原子(-X)碳-卤键(C-X)有极性,易断裂①氟烃、氯烃、溴烃;②一卤烃和多卤烃;③饱和卤烃、不炮和卤烃和芳香卤烃①取代反应(水解反应):R-X+H2OR-OH + HX②消去反应:R-CH2-CH2X + NaOHRCH=H2 + NaX + H2O醇均为羟基(-OH) -OH在非苯环碳原子上①脂肪醇(包括饱和醇、不饱和醇);②脂环醇(如环己醇)③芳香醇(如苯甲醇),④一元醇与多元醇(如乙二醇、丙三醇)①取代反应:a.与Na等活泼金属反应;b.与HX反应,c.分子间脱水;d.酯化反应②氧化反应:2R-CH2OH + O22R-CHO+2H2O③消去反应,CH3CH2OHCH2=H2↑+ H2O酚-OH直接连在苯环碳原上.酚类中均含苯的结构一元酚、二元酚、三元酚等①易被空气氧化而变质;②具有弱酸性③取代反应④显色反应醛醛基(-CHO)分子中含有醛基的有机物①脂肪醛(饱和醛和不饱和醛);②芳香醛;③一元醛与多元醛①加成反应(与H2加成又叫做还原反应):R-CHO+H2R-CH2OH②氧化反应:a.银镜反应;b.红色沉淀反应:c.在一定条件下,被空气氧化羧酸羧基(-COOH)分子中含有羧基的有机物①脂肪酸与芳香酸;②一元酸与多元酸;③饱和羧酸与不饱和羧酸;④低级脂肪酸与高级①具有酸的通性;②酯化反应脂肪酸羧酸酯酯基(R为烃基或H原子,R′只能为烃基)①饱和一元酯:CnH2n+lCOOCmH2m+1②高级脂肪酸甘油酯③聚酯④环酯水解反应:RCOOR′+ H2ORCOOH + R'OHRCOOR′+ NaOHRCOONa + R'OH(酯在碱性条件下水解较完全)反应类型定义举例(反应的化学方程式)消去反应有机物在一定条件下,从一个分子中脱去一个小分子(如H2O、HBr等)而生成不饱和(含双键或叁键)化合物的反应C2H5OH CH2=H2↑+ H2O苯酚的显色反应苯酚与含Fe3+的溶液作用,使溶液呈现紫色的反应还原反应有机物分子得到氢原子或失去氧原子的反应CH≡CH + H2CH2=H2CH2=H2 + H2CH3CH3R—CHO + H2R-CH2OH氧化反应燃烧或被空气中的O2氧化有机物分子得到氧原子或失去氢原子的反应2CH3CH2OH + O22CH3CHO + 2H2O2CH3CHO + O22CH3COOH 银镜反应CH3CHO + 2Ag(NH3)2OHCH3COONH4+2Ag↓+ 3NH3↑+ H2O红色沉淀反应CH3CHO + 2Cu(OH)2CH3COOH +Cu2O↓+ 2H2O取代反应卤代烃的水解反应在NaOH水溶液的条件下,卤代烃与水作用,生成醇和卤化氢的反应R-CH2X + H2O RCH2OH + HX 酯化反应酸(无机含氧酸或羧酸)与醇作用,生成酯和水的反应RCOOH + R'CH2OHRCOOCH2R′+ H2O酯的水解反应 在酸或碱存在的条件下,酯与水作用生成醇与酸的反应 RCOOR ′+ H 2O RCOOH + R'OHRCOOR ′+ NaOH → RCOONa + R'OH3.有机物的分离和提纯方法(1)有机物的分离与提纯的原则:分离是把混合物各组分经过化学变化而设法分开,得到混合前的物质.提纯是除去物质中混有的少量杂质. ①加入试剂时,不容易引入新的杂质;②所用试剂最好只与杂质起反应,而不与所需提纯的物质起反应; ③反应后的其他生成物必须和所需提纯的物质易分离; ④有机物的分离与提纯不能用合成转化的方法. (2)常见有机物的分离、提纯方法:①洗气法.将气体混合物中的杂质气体用溶液吸收除去.例如,除去气态烷烃中混有的气态烯烃(或炔烃),可将混合气体通过盛有溴水的洗气瓶.②分液法.根据有机物在水中的溶解性、酸碱性等性质上的差异,把两种相互混溶的有机物中的一种转变为可溶于水的物质,另一种仍不溶于水,从而达到分离与提纯的目的.a .若杂质易溶于水而被提纯物不溶于水,则直接加入水后用力振荡,使杂质转入水层中,用分液漏斗分离.b .若杂质与被提纯物都不溶于水,则先使杂质与某种试剂反应,使其转化为易溶于水的物质后再分离. ③蒸馏(分馏)法.a .对沸点差别大的有机物,可直接进行蒸馏提纯与分离;b .混合物中各组分的沸点相差不大时,则加入某种物质,使其中一种组分转化为高沸点、难挥发性物质后再进行蒸馏.例如,分离乙醇与乙酸的混合液时,先向其中加入固体NaOH ,使乙酸转化生成高沸点的CH 3COONa ,蒸馏出乙醇后,再加入浓H 2SO 4,使CH 3COONa 转化为CH 3COOH ,再经蒸馏得到乙酸. 4.有机物的燃烧规律[烃的含氧衍生物燃烧的通式] ①完全燃烧时(O 2充足):CxHyOz + (x +y /42/z -)O 2 →x CO 2 + y / 2H 2O ②不完全燃烧时(O 2不充足):CxHyOz + (242zy x a -++)O 2 →a CO 2 + (a x -)CO + y / 2H 2O[不同有机物完全燃烧时耗O 2量的比较](1)物质的量相同时,等物质的量的烃(通式为CxHy )、烃的衍生物(通式为CxHyOz )完全燃烧时,耗O 2量的比较.方法一:直接根据“1 mol 烃消耗(x +y /4) mol O 2,1 mol 烃的衍生物消耗(242zy x a -++) mol O 2”相比较.方法二(较简便):根据“1个C 耗1个O 2,2个H 耗1个O ”的原理,先将CxHyOz 改写为z O H z y CxH )()2(2⋅-。
