无机化学实验第四版实验二十一:ds区金属(铜,银,锌,镉,汞)
- 格式:doc
- 大小:86.50 KB
- 文档页数:5

2020无机化学实验报告文档Contract Template无机化学实验报告文档前言语料:温馨提醒,报告一般是指适用于下级向上级机关汇报工作,反映情况,答复上级机关的询问。
按性质的不同,报告可划分为:综合报告和专题报告;按行文的直接目的不同,可将报告划分为:呈报性报告和呈转性报告。
体会指的是接触一件事、一篇文章、或者其他什么东西之后,对你接触的事物产生的一些内心的想法和自己的理解本文内容如下:【下载该文档后使用Word打开】无机化学实验报告1Ds区元素(铜、银、锌、镉、汞)【学习目标】认知目标:掌握铜、银、锌、镉、汞的氢氧化物或氧化物的酸碱性,硫化物的溶解性及配位性。
技能目标:掌握Cu+\Cu2+及Hg22+\Hg2+相互转化条件,正确使用汞;思想目标:培养学生观察现象、思考问题的能力。
【教学安排】一课时安排:3课时二实验要点:1、铜、银、锌、镉、汞氢氧化物或氧化物的生成和性质;2、锌、镉、汞硫化物的生成和性质;3、铜、银、锌、汞的配合物;4、铜、银、汞的氧化还原性。
【重点、难点】Cu+\Cu2+及Hg22+\Hg2+相互转化条件;这些元素的氢氧化物或氧化物的酸碱性,硫化物的溶解性及配位性。
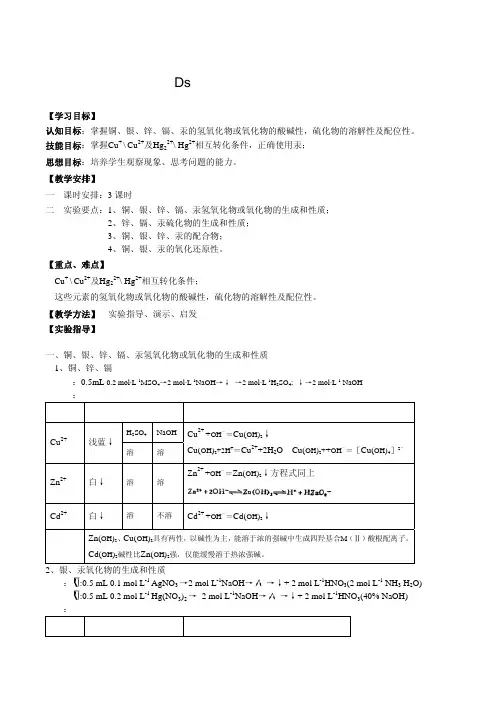
【教学方法】实验指导、演示、启发【实验指导】一、铜、银、锌、镉、汞氢氧化物或氧化物的生成和性质1、铜、锌、镉操作:0.5mL0.2mol·L-1MSO4→2mol·L-1NaOH→↓→2mol·L-1H2SO4;↓→2mol·L-1NaOH指导:离子Cu2+实验现象H2SO4NaOH溶解释及原理Cu2++OH-=Cu(OH)2↓Cu(OH)2+2H+=Cu2++2H2OCu(OH)2++OH-=[Cu(OH)4]2-Zn2++OH-=Zn(OH)2↓方程式同上溶溶浅蓝↓溶Zn2+Cd2+结论白↓白↓溶不溶Cd2++OH-=Cd(OH)2↓Zn(OH)2、Cu(OH)2具有两性,以碱性为主,能溶于浓的强碱中生成四羟基合M(Ⅱ)酸根配离子。

无机化学实验报告-DS区元素实验11 ds 区元素(铜、银、锌、镉、汞)的性质一、实验目的1、掌握铜、锌氢氧化物的酸碱性;2、掌握铜、银、锌、汞的配合物的生成和性质; 6、掌握铜、银、锌、汞离子的分离与鉴定方法。
二、实验原理IB IIBCu Zn Cu (+2,+1) Zn(+2) Ag Cd Ag (+1) Cd(+2) Au Hg Au (+1,+3) Hg(+2,+1) 蓝色的Cu(OH)2呈现两性,在加热时易脱水而分解为黑色的CuO 。
AgOH 在常温下极易脱水而转化为棕色的Ag 2O 。
Zn(OH)2呈两性,Cd(OH)2显碱性,Hg(I, II)的氢氧化物极易脱水而转变为黄色的HgO(II)和黑色的Hg 2O(I)。
易形成配合物是这两副族的特性,Cu 2+、Ag +、Zn 2+、Cd 2+与过量的氨水反应时分别生成[Cu(NH 3)4]2+、[Ag(NH 3)2]+、[Zn(NH 3)4]2+、[Cd(NH 3)4]2+。
但是Hg 2+和Hg 22+与过量氨水反应时,如果没有大量的NH 4+存在,并不生成氨配离子。
如:HgCl 2 + 2NH 3 = Hg(NH 2)Cl↓白+ 2 NH 4Cl Hg 2Cl 2 + 2NH 3 = Hg(NH 2)Cl↓白+ Hg↓黑+NH 4Cl(观察为灰色)Cu 2+具有氧化性,与I -反应,产物不是CuI 2,而是白色的CuI :Cu2++ I - = 2CuI↓白 + I 2将CuCl 2溶液与铜屑混合,加入浓盐酸,加热可得黄褐色[CuCl 2]-的溶液。
将溶液稀释,得白色CuCl 沉淀:Cu + Cu2++ 4Cl - = 2[CuCl 2]-[CuCl 2]-←稀释→CuCl↓白 + Cl -卤化银难溶于水,但可利用形成配合物而使之溶解。
例如:AgCl + 2NH 3 = [Ag(NH 3)2]++ Cl -红色HgI 2难溶于水,但易溶于过量KI 中,形成四碘合汞(II)配离子:HgI 2 + 2I -= [HgI 4]2-黄绿色Hg 2I 2与过量KI 反应时,发生歧化反应,生成[HgI 4]2-和Hg :Hg 2I 2+ 2I - = [HgI 4]2-+ Hg↓黑三、实验内容 1、氧化物的生成和性质(1) C u 2O 的生成和性质Cu 2+ + 2OH - =Cu(OH)2↓ 蓝色 Cu(OH)2 + 2OH - = [Cu(OH)4]-2- 蓝色2[Cu(OH)4]2-+ C 6H 12O 6 (葡萄糖) =Cu 2O↓(红) + 4OH -+C 16H 12O 7+2H 2O或:2Cu 2+ + 5OH - +C 6H 12O 6 = Cu 2O↓+ C 6H 11O 7- + 3H 2O (须加热)分析化学上利用此反应测定醛,医学上利用此反应检查糖尿病。

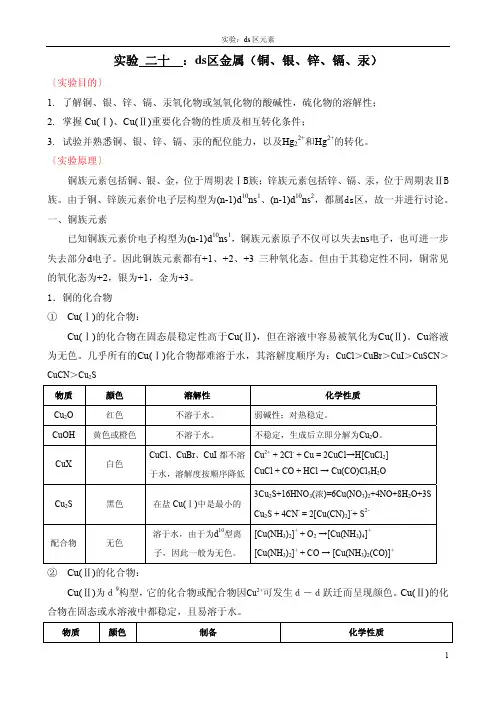
实验二十:ds区金属(铜、银、锌、镉、汞)〔实验目的〕1.了解铜、银、锌、镉、汞氧化物或氢氧化物的酸碱性,硫化物的溶解性;2.掌握Cu(Ⅰ)、Cu(Ⅱ)重要化合物的性质及相互转化条件;3.试验并熟悉铜、银、锌、镉、汞的配位能力,以及Hg22+和Hg2+的转化。
〔实验原理〕铜族元素包括铜、银、金,位于周期表ⅠB族;锌族元素包括锌、镉、汞,位于周期表ⅡB 族。
由于铜、锌族元素价电子层构型为(n-1)d10ns1、(n-1)d10ns2,都属ds区,故一并进行讨论。
一、铜族元素已知铜族元素价电子构型为(n-1)d10ns1,铜族元素原子不仅可以失去ns电子,也可进一步失去部分d电子。
因此铜族元素都有+1、+2、+3三种氧化态。
但由于其稳定性不同,铜常见的氧化态为+2,银为+1,金为+3。
1.铜的化合物①Cu(Ⅰ)的化合物:Cu(Ⅰ)的化合物在固态晨稳定性高于Cu(Ⅱ),但在溶液中容易被氧化为Cu(Ⅱ)。
Cu溶液为无色。
几乎所有的Cu(Ⅰ)化合物都难溶于水,其溶解度顺序为:CuCl>CuBr>CuI>CuSCN>CuCN>Cu2S物质颜色溶解性化学性质Cu2O 红色不溶于水。
弱碱性;对热稳定。
CuOH 黄色或橙色不溶于水。
不稳定,生成后立即分解为Cu2O。
CuX 白色CuCl、CuBr、CuI都不溶于水,溶解度按顺序降低Cu2+ + 2Cl- + Cu = 2CuCl→H[CuCl2] CuCl + CO + HCl → Cu(CO)Cl5H2OCu2S 黑色在盐Cu(Ⅰ)中是最小的3Cu2S+16HNO3(浓)=6Cu(NO3)2+4NO+8H2O+3SCu2S + 4CN- = 2[Cu(CN)2]-+ S2-配合物无色溶于水,由于为d10型离子,因此一般为无色。
[Cu(NH3)2]+ + O2→[Cu(NH3)4]+ [Cu(NH3)2]+ + CO → [Cu(NH3)2(CO)]+②Cu(Ⅱ)的化合物:Cu(Ⅱ)为d9构型,它的化合物或配合物因Cu2+可发生d-d跃迁而呈现颜色。

实验 ds 区金属(铜、银、锌、镉、汞)一、实验目的:1、了解铜、银、锌、镉、汞的氧化物或氢氧化物的酸碱性、硫化物的溶解性。
2、掌握Cu(Ⅰ)、Cu(Ⅱ)重要化合物的性质及相互转化条件。
3、试验并熟悉铜、银、锌、镉、汞的配位能力,以及Hg2 2+ 和Hg 2+ 的转化。
二、实验用品:仪器:试管、烧杯、离心机、离心试管固体药品:碘化钾、铜屑液体药品: HCl(2mol/L、 浓)、 H2SO4(2mol/L)、 HNO3(2mol/L、 浓)、 NaOH(2mol/L、 6mol/L、 40%)、氨水(2mol/L、浓)、CuSO4(0.2mol/L)、ZnSO4(0.2mol/L)、CdSO4(0.2mol/L)、 CuCl2(0.5mol/L) 、 Hg(NO3)2(0.2mol/L) 、 SnCl2(0.2mol/L) 、 AgNO3(0.1mol/L) 、 Na2S(0.1mol/L)、KI(0.2mol/L)、KSCN(0.1mol/L)、Na2S2O3(0.5mol/L)、NaCl(0.2mol/L)、 金属汞、葡萄糖溶液(10%)材料:pH试纸、玻璃棒三、实验内容:(一)铜、银、锌、镉、汞氧化物或氢氧化物的生成和性质1、铜、锌、镉氢氧化物的生成和性质在分别装有 0.5mL0.2mol/L CuSO4、ZnSO4、CdSO4 溶液的三支试管中滴加新配制 的2mol/L NaOH溶液,观察溶液颜色及状态。
将各沉淀分成两份:分别加入2mol/L H2SO4 和2mol/L NaOH,观察现象。
CuSO4 + 2NaOH === Cu(OH)2↓(兰)+ Na2SO4ZnSO4 + 2NaOH === Zn(OH)2↓(白) + Na2SO4CdSO4 + 2NaOH === Cd(OH)2↓(白)+ Na2SO4Cu(OH)2 + H2SO4 === CuSO4 + 2H2OCu(OH)2 + 2NaOH === Na2[Cu(OH)4]Zn(OH)2 + H2SO4 === ZnSO4 + 2H2OZn(OH)2 + 2NaOH === Na2[Zn(OH)4]Cd(OH)2 + H2SO4 === CdSO4 + 2H2OCd(OH)2 酸性特别弱,不易溶于强碱中,只缓慢溶于热、浓的强碱中。
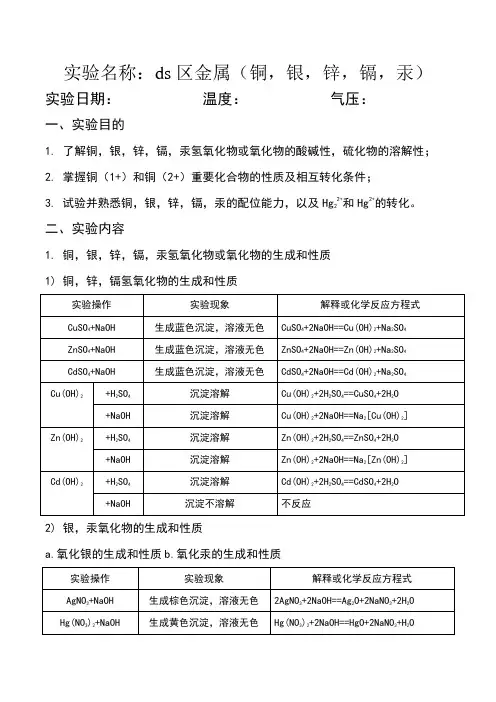
实验名称:ds区金属(铜,银,锌,镉,汞)实验日期:温度:气压:
一、实验目的
1.了解铜,银,锌,镉,汞氢氧化物或氧化物的酸碱性,硫化物的溶解性;
2.掌握铜(1+)和铜(2+)重要化合物的性质及相互转化条件;
3.试验并熟悉铜,银,锌,镉,汞的配位能力,以及Hg22+和Hg2+的转化。
二、实验内容
1.铜,银,锌,镉,汞氢氧化物或氧化物的生成和性质
1)铜,锌,镉氢氧化物的生成和性质
2)银,汞氧化物的生成和性质
a.氧化银的生成和性质
b.氧化汞的生成和性质
2.锌,镉硫化物的生成和性质
根据实验现象并查阅有关数据,填充下表,并对铜,银,锌,镉,汞硫化物的溶解情况作出结论,并写出有关反应方程式。
3.铜,银,锌,汞的配合物1)氨合物的生成
2)汞配合物的生成和性质
4.铜,银,汞的氧化还原性1)氧化亚铜的生成和性质
2)氯化亚铜的生成和性质
3)碘化亚铜的生成和性质
4)汞(2+)和汞(1+)的相互转化
a.Hg2+的氧化性+转化为Hg22+和Hg2+的歧化反解。


实验二十一ds区金属一、实验目的1、掌握铜、银、锌、镉、汞氧化物或氢氧化物的酸碱性,硫化物的溶解性;2、掌握Cu (Ⅰ)、Cu (Ⅱ)重要化合物的性质及相互转化条件;3、试验铜、银、锌、镉、汞的配位能力以及亚汞离子和汞离子的转化。
二、实验内容(一)、铜、银、锌、镉、汞氢氧化物或氧化物的生成和性质:1 、铜、锌、镉氢氧化物的生成和性质(1)Ag2O的生成和性质:Ag++OH-===AgOH↓白色→Ag2O+H2OAg2O+2HNO3===2AgNO3+H2OAg2O+2NH3.H2O==2[Ag(NH3)2]++2OH-+H2OAg2O微溶于水,溶液呈微碱性。
它的△f H m﹩很小,不稳定,加热易分解,具有氧化性。
(2)HgO的生成和性质Hg2++2OH-==Hg(OH)2==HgO↓+H2OHgO+2HNO3==Hg(NO3)2+H2OHgO+NaOH(40℅)-----不溶HgO 有黄色和红色变体,结构相同,颜色差别完全是由于其颗粒的大小不同所致,黄色HgO晶粒较细小,红色颗粒较大。
(二)、铜、银、锌、镉、汞硫化物的生成和溶解说明:1.生成的CdS中,个别学生得到的沉淀是黄色中夹有白色沉淀,有可能是CdS晶形不一样,或有可能是生成Cd(OH)2白色沉淀。
补充:CdS沉淀颜色变化与溶液的酸度及温度有很大关系。
在冷氨性、中性或弱酸性溶液中,其沉淀为淡黄;若H+浓度增大,则沉淀将加变为深黄色。
2.在Hg(NO3)2中加入Na2S,开始生成白色沉淀,再加Na2S后变黑。
对白色沉淀再加热也不会再变化。
个别学生得到白中带有黄色的沉淀。
在中性或酸性汞盐溶液中加入S2-,即首先形成一个白色的复合物(HgCl2·2HgS):3Hg2++2Cl-+2S2-====HgCl2·2HgS若再加S2-,则白色沉淀→ 黄色→ 棕色→ 黑色:2HgCl·2HgS+S2-====3HgS+2Cl-此沉淀不溶与其它,只溶于王水、Na2S。

实验11 ds区元素(铜、银、锌、镉、汞)的性质一、实验目的1、掌握铜、锌氢氧化物的酸碱性;2、掌握铜、银、锌、汞的配合物的生成和性质;6、掌握铜、银、锌、汞离子的分离与鉴定方法。
二、实验原理IB IIBCu Zn Cu(+2,+1)Zn(+2)Ag Cd Ag(+1)Cd(+2)Au Hg Au(+1,+3)Hg(+2,+1)蓝色的Cu(OH)2呈现两性,在加热时易脱水而分解为黑色的CuO。
AgOH在常温下极易脱水而转化为棕色的Ag2O。
Zn(OH)2呈两性,Cd(OH)2显碱性,Hg(I, II)的氢氧化物极易脱水而转变为黄色的HgO(II)和黑色的Hg2O(I)。
易形成配合物是这两副族的特性,Cu2+、Ag+、Zn2+、Cd2+与过量的氨水反应时分别生成[Cu(NH3)4]2+、[Ag(NH3)2]+、[Zn(NH3)4]2+、[Cd(NH3)4]2+。
但是Hg2+和Hg22+与过量氨水反应时,如果没有大量的NH4+存在,并不生成氨配离子。
如:HgCl2 +2NH3=Hg(NH2)Cl↓白+2 NH4ClHg2Cl2+2NH3=Hg(NH2)Cl↓白+Hg↓黑+NH4Cl (观察为灰色)Cu2+具有氧化性,与I-反应,产物不是CuI2,而是白色的CuI:Cu2+ +I- =2CuI↓白+I2将CuCl2溶液与铜屑混合,加入浓盐酸,加热可得黄褐色[CuCl2]-的溶液。
将溶液稀释,得白色CuCl沉淀:Cu +Cu2+ +4Cl-=2[CuCl2]-[CuCl2]-←稀释→CuCl↓白+Cl-卤化银难溶于水,但可利用形成配合物而使之溶解。
例如:AgCl +2NH3 =[Ag(NH3)2]+ +Cl-红色HgI2难溶于水,但易溶于过量KI中,形成四碘合汞(II)配离子:HgI2 +2I- =[HgI4]2-黄绿色Hg2I2与过量KI反应时,发生歧化反应,生成[HgI4]2-和Hg:Hg2I2+2I- =[HgI4]2-+Hg↓黑三、实验内容1、氧化物的生成和性质(1)Cu2O的生成和性质Cu2++2OH-=Cu(OH)2↓ 蓝色Cu(OH)2+2OH- = [Cu(OH)4]-2-蓝色2[Cu(OH)4]2-+C6H12O6 (葡萄糖) =Cu2O↓(红) +4OH-+C16H12O7+2H2O或:2Cu2+ + 5OH- +C6H12O6 = Cu2O↓+ C6H11O7- + 3H2O (须加热)分析化学上利用此反应测定醛,医学上利用此反应检查糖尿病。

铜、银、锌、镉、汞实验目的1.试验并了解ds 区元素的氢氧化物(或氧化物)的酸碱性及对热稳定性2.了解铜、银、锌、镉、汞的金属离子形成配合物的特征3.了解Cu(Ⅱ)与Cu(Ⅰ),Hg(Ⅱ)与Hg(Ⅰ)的相互转化条件4.了解铜、银、锌、镉、汞的离子鉴定实验提要ds区元素包括铜、银、锌、镉和汞。
它们的价电子层结构分别为(n-1)d10ns1和(n-1)d10ns2。
在化合物中常见的氧化值。
铜为+2 和+1,银为+1,锌和镉为+2,汞为+2 和+1。
这些元素的简单阳离子具有或接近18e的构型。
在化合物中与某些阳离子有较强的相互极化作用,成键的共价成分较大。
多数化合物较难溶于水,对热稳定性较差,易形成配位化合物,化合物常显不同的颜色。
例如,这些元素的氢氧化物均较难溶于水,且易脱水变成氧化物。
银和汞的氢氧化物极不稳定。
常温下即失水变成Ag2O(棕黑色)和HgO(黄色)。
黄色HgO加热则生成桔红色HgO变体。
Cu(OH)2、Zn(OH)2和Cd(OH)2在常温下较稳定,但受热亦会失水成氧化物。
浅蓝色Cu(OH)2在80℃失水成棕黑色CuO,白色Zn(OH)2在125℃开始失水成黄色(冷后为白色)的ZnO,白色Cd(OH)2在250℃变成棕红色的CdO。
Zn(OH)2呈典型的两性氢氧化物,Cu(OH)2呈较弱的两性(偏碱),Cd(OH) 2和Hg(OH)2(HgO)呈碱性,而AgOH为强碱性。
Cu2+、Ag+、Zn2+、Cd2+、Hg2+与Na2S溶液反应都生成难溶的硫化物,即CuS(黑色),Ag2S(黑色),ZnS(白色),CdS (黄色)和HgS(黑色)。
其中HgS可溶于过量的Na2S,与S2−生成无色的HgS22−配离子。
若在此溶液中加入盐酸又生成黑色HgS沉淀。
此反应可作为分离HgS的方法。
根据ZnS、CdS、Ag2S、CuS和HgS溶度积大小,ZnS可溶于稀酸,CdS溶于6mol•L−1HCl 溶液,Ag S和2 CuS溶于氧化性的HNO3,而HgS溶于王水。
一、实验名称铜、银、锌、镉、汞的氢氧化物或氧化物的生成和性质二、实验目的1. 掌握铜、银、锌、镉、汞的氢氧化物或氧化物的生成和性质。
2. 学会观察和分析实验现象,培养实验操作技能。
3. 了解氢氧化物或氧化物的酸碱性、溶解性和配位性。
三、实验原理1. 氢氧化物或氧化物的生成:在溶液中加入适量的碱,金属离子与氢氧根离子结合生成相应的氢氧化物或氧化物。
2. 氢氧化物或氧化物的性质:根据氢氧化物或氧化物的溶解性、酸碱性、配位性等性质,判断其组成和结构。
四、实验仪器及试剂1. 仪器:试管、试管夹、烧杯、玻璃棒、滴管、酒精灯、石棉网、天平、铁架台、加热器等。
2. 试剂:硫酸铜晶体、氢氧化钠溶液、硫酸锌溶液、硫酸镉溶液、硫酸汞溶液、硫酸钠溶液、硫酸钾溶液、硫酸铵溶液、氯化钠溶液、硝酸银溶液、氨水等。
五、实验步骤1. 铜的氢氧化物或氧化物的生成和性质(1)取一支试管,加入少量硫酸铜晶体,加入适量水溶解。
(2)加入少量氢氧化钠溶液,观察现象。
(3)加热试管,观察现象。
(4)加入氨水,观察现象。
2. 银的氢氧化物或氧化物的生成和性质(1)取一支试管,加入少量硝酸银溶液,加入适量水溶解。
(2)加入少量氢氧化钠溶液,观察现象。
(3)加热试管,观察现象。
3. 锌的氢氧化物或氧化物的生成和性质(1)取一支试管,加入少量硫酸锌溶液,加入适量水溶解。
(2)加入少量氢氧化钠溶液,观察现象。
(3)加热试管,观察现象。
4. 镉的氢氧化物或氧化物的生成和性质(1)取一支试管,加入少量硫酸镉溶液,加入适量水溶解。
(2)加入少量氢氧化钠溶液,观察现象。
(3)加热试管,观察现象。
5. 汞的氢氧化物或氧化物的生成和性质(1)取一支试管,加入少量硫酸汞溶液,加入适量水溶解。
(2)加入少量氢氧化钠溶液,观察现象。
(3)加热试管,观察现象。
六、实验结果及分析1. 铜的氢氧化物或氧化物的生成和性质:加入氢氧化钠溶液后,溶液中出现蓝色沉淀,加热后沉淀溶解,加入氨水后,溶液中出现深蓝色沉淀。
Revise-实验20-铜、银、锌、镉、汞ds区元素(铜、银、锌、镉、汞)一、实验目的与要求:1.了解铜、银、锌、镉、汞氧化物或氢氧化物的酸碱性,硫化物的溶解性。
2. 掌握Cu(Ⅰ)、Cu(Ⅱ)重要化合物的性质及相互转化条件。
3. 熟悉铜、银、锌、镉、汞的配位能力,以及Hg22+和Hg2+的转化。
二、教学重点与难点:了解铜、银、锌、镉、汞氧化物或氢氧化物的酸碱性,硫化物的溶解性,熟悉铜、银、锌、镉、汞的配位能力,以及Hg22+和Hg2+的转化;掌握Cu(Ⅰ)、Cu(Ⅱ)重要化合物的性质及相互转化条件,三、教学方法与手段:讲授法;演示法四、教学课时: 4课时五、课的类型:实验课一、铜、银、锌、镉、汞氧化物或氢氧化物的生成和性质1、铜、锌、镉氧化物的生成和性质向三支试管分别盛有0.5ml 0.2mol.L-1CuSO4、ZnSO4、CdSO4溶液的试管中滴加新配制的2mol.L-1NaOH溶液,观察溶液颜色及状态。
将沉淀分成两份, 一份加硫酸另一份加NaOH溶液,观察现象。
Cu2++2OH-===Cu(OH)2↓ (蓝色沉淀)蓝色沉淀,溶解于酸,微溶于过量的碱,得到深蓝色溶液[Cu(OH)4]2-。
Cu(OH)2两性偏碱,所以需强碱使之生成配离子。
Zn2++2OH-=== Zn(OH)2↓ (白色沉淀)白色沉淀, 溶解于酸和过量的碱,典型的两性化物。
Cd 2++2OH-===Cd(OH)2↓白色沉淀,溶于酸, 不溶于碱。
Cd(OH)2 + NaOH (6M)= 不反应(Cd(OH)碱性)22. 银、汞氧化物的生成和性质(1)、氧化银的生成和性质取0.5ml 0.1mol.L-1AgNO3溶液,滴加新配制的2mol.L-1的NaOH溶液,观察沉淀的颜色和状态。
洗涤并离心,将沉淀分成两份,一份加入HNO3,另一份加入氨水,观察现象。
Ag++OH-===AgOH↓白色沉淀2AgOH===Ag2O+H2O 黑色沉淀Ag2O+2HNO3===2AgNO3+H2OAg2O+2NH3.H2O==2[Ag(NH3)2]++2OH-+H2O氢氧化银不稳定,很容易被氧化成黑色的Ag2O,此黑色沉淀溶于硝酸得到银离子,加入氨水得到银氨络合溶液。
实验名称:ds区金属(铜,银,锌,镉,汞)实验日期:温度:气压:
一、实验目的
1.了解铜,银,锌,镉,汞氢氧化物或氧化物的酸碱性,硫化物的溶解性;
2.掌握铜(1+)和铜(2+)重要化合物的性质及相互转化条件;
3.试验并熟悉铜,银,锌,镉,汞的配位能力,以及Hg22+和Hg2+的转化。
二、实验内容
1.铜,银,锌,镉,汞氢氧化物或氧化物的生成和性质
1)铜,锌,镉氢氧化物的生成和性质
2)银,汞氧化物的生成和性质
a.氧化银的生成和性质
b.氧化汞的生成和性质
2.锌,镉硫化物的生成和性质
根据实验现象并查阅有关数据,填充下表,并对铜,银,锌,镉,汞硫化物的溶解情况作出结论,并写出有关反应方程式。
3.铜,银,锌,汞的配合物
1)氨合物的生成
2)汞配合物的生成和性质
4.铜,银,汞的氧化还原性1)氧化亚铜的生成和性质
2)氯化亚铜的生成和性质
3)碘化亚铜的生成和性质
4)汞(2+)和汞(1+)的相互转化
a.Hg2+的氧化性
b.Hg2+转化为Hg22+和Hg2+的歧化反解。
实验名称:ds区金属(铜,银,锌,镉,汞)
实验日期:温度:气压:
一、实验目的
1.了解铜,银,锌,镉,汞氢氧化物或氧化物的酸碱性,硫化物的溶解性;
2.掌握铜(1+)和铜(2+)重要化合物的性质及相互转化条件;
3.试验并熟悉铜,银,锌,镉,汞的配位能力,以及Hg22+和Hg2+的转化。
二、实验内容
1.铜,银,锌,镉,汞氢氧化物或氧化物的生成和性质
1)铜,锌,镉氢氧化物的生成和性质
2)银,汞氧化物的生成和性质
a.氧化银的生成和性质
b.氧化汞的生成和性质
2.锌,镉硫化物的生成和性质
根据实验现象并查阅有关数据,填充下表,并对铜,银,锌,镉,汞硫化物的溶解情况作出结论,并写出有关反应方程式。
3.铜,银,锌,汞的配合物
1)氨合物的生成
2)汞配合物的生成和性质
4.铜,银,汞的氧化还原性1)氧化亚铜的生成和性质
2)氯化亚铜的生成和性质
3)碘化亚铜的生成和性质
4)汞(2+)和汞(1+)的相互转化
a.Hg2+的氧化性
b.Hg2+转化为Hg22+和Hg2+的歧化反解。