国家药品审评中心审评人员公示名单2015.04
- 格式:doc
- 大小:132.50 KB
- 文档页数:6

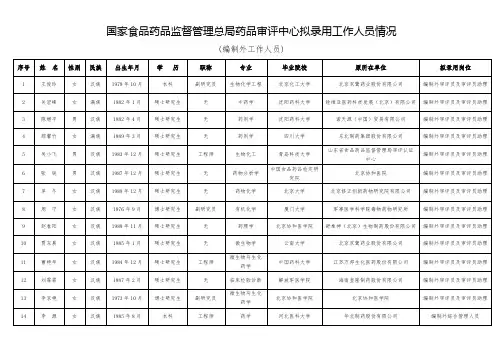

药品审评中心审评人员公示名单 (2015年4月)部门姓名 所负责工作分机中心主任许嘉齐611中心副主任尹红章602中心副主任侯仁萍603中心领导中心主任助理胡 军协助分管主任负责中药药品审评的技术管理工作604负责审评技术资料管理、审评任务分发调度及相关督查协调工作。
承担相关审评报告综合以及审评文件管理,组织开展与新药审评相关的核查、验证工作;承担主动撤回申请和超过规定时限未按要求提交补充资料等品种的相关处理工作;负责与国家食品药品监督管理局相关部门协调技术审评工作;承担业务咨询及业务信息管理工作。
负责中心文电、会务、档案等日常运转工作以及安全保密、印章管理、外部联络等工作。
承担中心交办的其他工作。
副部长温宝书303副部长王 敏172 何燕萍101张晓东102王 鹏104黄清竹105业务管理部协调员刘 璐106负责中药、民族药及天然药物临床试验申请和注册申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责中药、民族药及天然药物7~8类临床试验申请、7~9类注册申请、各类注射剂注册申请、相关补充申请以及进口再注册申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
部长胡 军604 副部长周跃华486阳长明401张永文402曲建博406金 芳407李计萍408周 刚409韩 炜412中药民族药药学部成员马秀璟413负责化学药物1~3类临床试验申请和注册申请、国际多中心临床试验申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责化学药物3类临床试验申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
副部长马玉楠577王 旸502任连杰505康建磊506王亚敏507于 红508王宏亮511马 磊512张 宁513霍秀敏514化药药学一部成员刘宗英515 负责化学药物4~5类临床试验申请、进口药注册申请、进口再注册申请、相关补充申请及其他申请的药学研究资料及生物等效性试验资料的技术审评工作,提出药学专业和相应生物等效性资料的审评意见并形成药学专业审评报告。
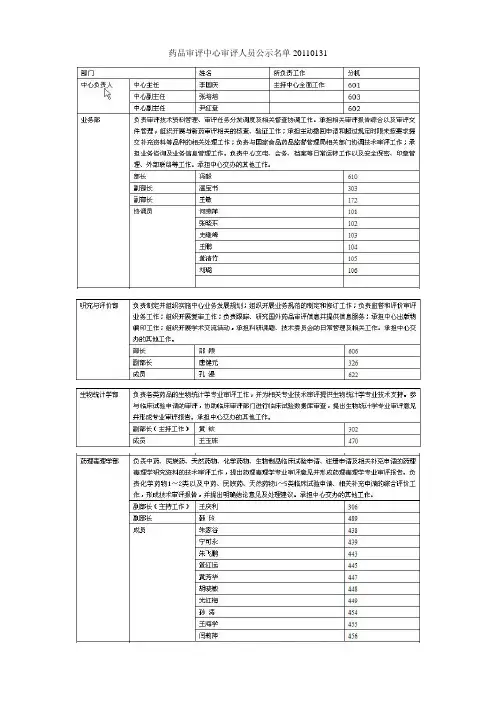
药品审评中心审评人员公示名单20110131关于国家食品药品监督管理局药品审评中心调整主要职责和内设机构的批复国食药监人函[2010]219号(一)业务管理部负责审评技术资料管理、审评任务分发调度及相关督查协调工作。
承担相关审评报告综合以及审评文件管理,组织开展与新药审评相关的核查、验证工作;承担主动撤回申请和超过规定时限未按要求提交补充资料等品种的相关处理工作;负责与国家食品药品监督管理局相关部门协调技术审评工作;承担业务咨询及业务信息管理工作。
负责中心文电、会务、档案等日常运转工作以及安全保密、印章管理、外部联络等工作。
承担中心交办的其他工作。
(二)中药民族药药学部负责中药、民族药及天然药物临床试验申请和注册申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责中药、民族药及天然药物7~8类临床试验申请、7~9类注册申请、各类注射剂注册申请、相关补充申请以及进口再注册申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(三)化药药学一部负责化学药物1~3类临床试验申请和注册申请、国际多中心临床试验申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。
负责化学药物3类临床试验申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(四)化药药学二部负责化学药物4~5类临床试验申请、进口药注册申请、进口再注册申请、相关补充申请及其他申请的药学研究资料及生物等效性试验资料的技术审评工作,提出药学专业和相应生物等效性资料的审评意见并形成药学专业审评报告。
负责化学药物4~5类临床试验申请以及5~6类注册申请、进口药临床试验申请、进口再注册申请、相关补充申请及其他申请的综合评价工作,形成技术审评报告,并提出明确结论意见及处理建议。
承担中心交办的其他工作。
(五)生物制品药学部负责生物制品临床试验申请、注册申请及相关补充申请的药学研究资料的技术审评工作,提出药学专业审评意见并形成药学专业审评报告。

关于公布第四批重新聘任的国家药品GMP检查员名单的通知
国食药监办[2010]284号
各省、自治区、直辖市食品药品监督管理局(药品监督管理局):
为加强对药品GMP检查员的管理,规范检查员队伍建设,按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家局综合考评,李卫华等123人为第四批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP检查员证》。
附件:第四批重新聘任的国家药品GMP检查员名单
国家食品药品监督管理局
二○一○年七月十九日
附件:
第四批重新聘任的国家药品GMP检查员名单。
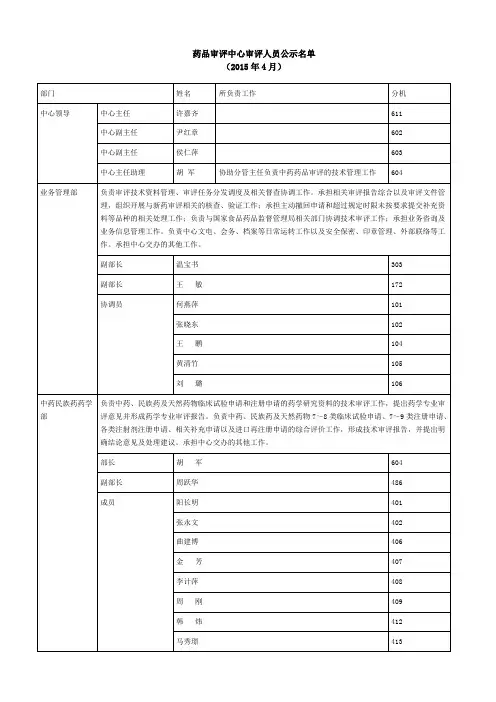

2015 年 7月CDE 药品审评报告Insight - China Pharma Data2015 年 8 月2015 年 7 月 CDE 药品审评报告——丁香园 Insight 数据库7 月热点•CFDA 发布 2 项公告,以解决药品审评问题•7 个 1.1 类新药品种申报临床•3.1 类首家抢仿集中神经系统领域•7 个进口化药首次在中国申报临床•百济神州、江苏恒瑞等收获 1.1 类新药获批临床_______________________________________________________________________________________对于药品研发和注册人员来说,7 月注定是骚动的一个月。
7 月 22 日,国家食品药品监督管理局( CFDA)发布公告,要求 1622 个受理号的申请注册人开展药物临床试验数据自查核查工作,如不能确保临床试验数据的真实性、可靠性和完整性,则需自主撤回注册申请。
7 月31 日,CFDA 再次发布公告,向社会征求解决药品注册申请积压问题的意见,欲提高仿制药审批标注,同时优化和改变生物等效性试验审评程序,并解决积压的同品种、注册申报造假行为等问题。
CFDA 连续出台政策,下定决心整改药品注册审评,但目前效果如何尚不可知。
在临床试验自查核查结果以及征求意见水落石出之前,我们一起来回顾下 7 月的药品审评情况。
根据丁香园 Insight - China Pharma Data 数据库最新统计, 2015 年 7 月 CDE 共承办新的药品注册申请有 845个(以受理号计,下同),与 6 月份(783 个)相比有所增长,增长量主要来源于化药。
以下,分别来分析化药、中药、生物制品的申报受理及审评审批情况。
一、化药申报受理情况:7 月份 CDE 共承办新的化药注册申请以受理号计 757 个。
其中各个申请类型的具体数据如下所示:Insight 系列报告1.新药(1)1.1 类新药7 个 1.1 类新药品种申报临床根据 Insight 数据库统计,7 月份 CDE 共承办化药 1.1 类新药申请以受理号计有 23 个,涉及 7 个品种,均为临床申请。

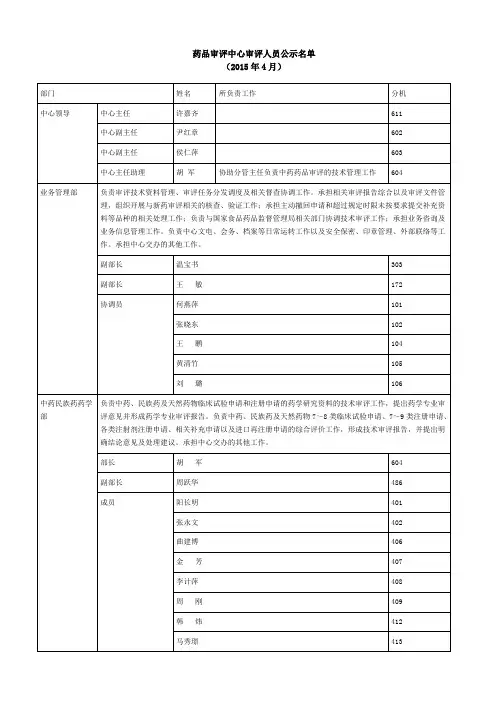
关于公布第三批重新聘任的国家药品GMP检查员名单的通知国食药监办[2009]823号各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为加强对药品GMP检查员的管理,规范检查员队伍建设,按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家局综合考评,彦玲等55人为第三批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP检查员证》。
附件:2009年第三批重新聘任的国家药品GMP检查员名单国家食品药品监督管理局二○○九年十二月八日附件:2009年第三批重新聘任的国家药品GMP检查员名单彦玲北京市药品监督管理局魏锡庚北京市药品监督管理局药品认证管理中心李利佳石家庄市食品药品监督管理局蒋灵君河北省衡水市食品药品监督管理局孙晋霞山西省食品药品监督管理局吴林彬山西省药品认证管理中心魏荣保内蒙古自治区食品药品监督管理局魏晶辽宁省食品药品监督管理局技术审评中心董英沈阳市食品药品监督管理局宋敏大连市食品药品监督管理局魏旭吉林市食品药品监督管理局姜国明吉林省食品药品认证和培训中心闻平黑龙江省食品药品稽查局杨东旭黑龙江省食品药品稽查局丁杰黑龙江省齐齐哈尔市食品药品监督管理局杨伟东上海市食品药品监督管理局朱璟刚上海市食品药品监督管理局唐媛江苏省苏州食品药品监督管理局范瑞泉江苏省南通食品药品监督管理局程颖江苏省食品药品检验所何金华浙江省食品药品监督管理局(原台州市椒江分局副局长)洪盈盈浙江省金华市食品药品监督管理局许红安徽省食品药品监督管理局江浩安徽省铜陵市食品药品监督管理局黄怀元福建省食品药品监督管理局许婉锌厦门市食品药品监督管理局王新建山东省食品药品监督管理局王玉强济南市食品药品监督管理局华丽萍青岛市食品药品监督管理局高卫胜山东省聊城市食品药品监督管理局张群江西省药品认证中心林昆江西省赣州市食品药品监督管理局张伟东郑州市食品药品监督管理局陶建伟河南省三门峡市食品药品监督管理局张国强湖北省食品药品监督管理局直属分局张跃丽湖北省宜昌市食品药品监督管理局文平兰湖南省湘潭市食品药品监督管理局陈鸿平湖南省常德市食品药品监督管理局向道斌广东省珠海市食品药品监督管理局童志华广西桂林市食品药品监督管理局陈海峰海南省食品药品监督管理局稽查总队王刚海南省食品药品监督管理局稽查总队李克健重庆市食品药品监督管理局龚士学重庆市药品检验所张刚林四川省广元食品药品监督管理局廖晓虎四川省德阳食品药品检验所高向军四川省食品药品检验所陈家彦贵州省食品药品监督管理局徐彤皓昆明市食品药品监督管理局陈文燮西藏自治区食品药品监督管理局刘燕陕西省食品药品监督管理局王成忠陕西省食品药品监督管理局钟家强陕西省安康市食品药品监督管理局李士博甘肃省药品检验所张训缨新疆维吾尔自治区食品药品监督管理局。
2015 年1 月CDE 药品审评报告INSIGHT - China Pharma Data2015 年2 月2015 年1 月CDE 药品审评报告——丁香园Insight 数据库导读∙化药1.1 类新药再添SGLT2 抑制剂∙正大天晴子公司申报克唑替尼∙深圳微芯重大专项抗癌新药西达本胺获得生产批件∙恒瑞申报生物制品1类新药注射用SHR-1210_____________________________________________________________________________________________根据丁香园Insight 数据库最新统计,2015年1月国家食品药品监督管理总局药品审评中心(CDE)共承办新的药品注册申请以受理号计有661个,与去年同期(887个)相比有所减少。
以下,分别来分析化药、中药、生物制品的申报受理及审评审批情况。
一、化药申报受理情况:1 月份CDE 共承办新的化药注册申请以受理号计有567 个,涉及256 个品种。
其中各个申请类型的详细数据如下所示:INSIGHT 系列报告1. 新药新药的申请量近乎是仿制药的两倍,有反常态在以往月份中,新药与仿制药的申请量总是大体持平,而 1 月份CDE 新承办的化药新药申请以受理号计有235 个,近乎是仿制药申请量(122 个)的两倍,有反常态。
近年来国家鼓励药物创新,引导制药企业提高创新能力、创仿结合,避免仿制药低水平过度重复,国内制药企业的研发观念也在逐步转变。
(1)1.1 类新药1 月份共有7 个化药1.1 类新药品种申报,又添SGLT2 抑制剂根据丁香园Insight 数据库显示,1 月份CDE 共承办化药 1.1 类新药申请以受理号计有22 个,涉及7 个品种。
其中北京康辰药业的抗肿瘤药物诺拉曲塞为上市申请,其余品种均为首次申报的临床申请。
具体数据,如下所示:其中,上海艾力斯医药科技有限公司申报的艾格列净是国内继江苏恒瑞的恒格列净、山东轩竹的加格列净之后的第三个SGLT2(钠-葡萄糖协同转运蛋白2)抑制剂,用于治疗 2 型糖尿病。
关于公布第五批重新聘任的国家药品GMP检查员名单的通知
国食药监安[2011]64号
各省、自治区、直辖市食品药品监督管理局(药品监督管理局):
为加强对药品GMP检查员的管理,规范检查员队伍建设,按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家局综合考评,刘明华等167人为第五批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP检查员证》。
附件:第五批重新聘任的国家药品GMP检查员名单
国家食品药品监督管理局
二○一一年二月九日
附件:
第五批重新聘任的国家药品GMP检查员名单。
关于公布第二批重新聘任的国家药品GMP检查员名单的通知国食药监办[2009]739号各省、自治区、直辖市食品药品监督管理局(药品监督管理局):按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家食品药品监督管理局综合考评,张亚东等120人为第二批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP检查员证》。
附件:第二批重新聘任的国家药品GMP检查员名单国家食品药品监督管理局二○○九年十一月三日附件:第二批重新聘任的国家药品GMP检查员名单北京市:张亚东、屈浩鹏、胡美芳、张娟天津市:牛东斌、马竹波河北省:许海鹰、赵立新、鞠捷频、杜增辉山西省:库晓娟、韩小平、李青翠、于如海内蒙古自治区:田秀芬辽宁省:龙雨飞、钟红玲、王晓黎、孙东吉林省:高笑天、于秀丽、李忠山、管恩杰、于文静黑龙江省:敖淑芬、张利平、弓起君、母凯、周声上海市:柳涛、沈建华、王乐菲江苏省:崔晓红、沈沁、赵洪运、李明先、焦灵利、范青峰浙江省:王清舟(省局安监处、原杭州市药监局安监处)、吴悦(认证中心)、吴永勤(认证中心)、李会林(省所)、叶兴福(台州市局安监注册处处长)、叶毅妮(省局安监处)、王海燕(嘉兴市局安监注册处处长)、黄泓(台州市局安监注册处)安徽省:金斌、宫文武、肖华、张永玲福建省:吴春敏、周仰青、潘碧英、庄江兴、李天杨江西省:蔡恒民、俞持师、胡晓翔、戴寿昌山东省:冉大强、刘学起、孙敏、胡德福、丁艳、周一鸿、徐政行河南省:郑霄昙、党明安、李学鑫、潘会朝湖南省:梁建宁、李再新、曾秋初、刘利军湖北省:陈俊、余健、李冰、刘爱萍广东省:李志伟、丁波、罗小萍、叶永才、陈哲、贾立平广西壮族自治区:罗远秀、韦广辉海南省:陈国彪、林芳梅重庆市:操复川、陈绩、罗萍四川省:吴锐、杨麟、张良君、白兰彬贵州省:高良美、杨蕤、冯英云南省:何道慧、欧阳楠、李哲媛、冯杰陕西省:唐小波、王四清、齐惠丽、沈四清甘肃省:朱晓红青海省:姜世贤宁夏回族自治区:张屏新疆维吾尔自治区:古丽斯坦国家局药品认证中心:孙京林、陈燕、马东光、闫兆光、岳勇、陈慧萍、吴爱军、刘爽、王元、叶笑。
关于公布第一批重新聘任的国家药品GMP检查员名单的通知国食药监办[2009]313号2009年06月12日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为进一步加强对药品GMP检查员的管理,规范检查员队伍建设,依据《药品管理法》、《药品管理法实施条例》的相关规定,国家局决定对药品GMP检查员进行重新聘任,并核发《国家药品GMP检查员证》。
经各省(区、市)食品药品监管部门推荐和国家食品药品监督管理局综合考评,姚胜林等137名药品GMP检查员为第一批重新聘任的国家药品GM P检查员,现予公布并核发《国家药品GMP检查员证》。
国家食品药品监督管理局二○○九年六月十二日附件:第一批重新聘任的国家药品GMP检查员名单北京市:姚胜林、张凤梅、张岩、孔力天津市:黎阳、王守斌、吴妍汶河北省:马琳、高志清、段春改山西省:王玉军、赵运江、朴晋华、王泽山内蒙古自治区:范曼昕、云秀玲辽宁省:刘智勇、佟宝光、朱延峰、王怡君、刘知音吉林省:武永峰、王琳、王喜民、李雪冬黑龙江省:战丹、谭宏宇、陈雷、张丁丁上海市:刘伟强、李建平、颛孙燕、刘丹华、沈晴、胡建国、张华江苏省:王敦岚、李国亮、姜莉、王立新、胡勇、王惠明、陈伟浙江省:吴相勇、胡淼、梅源、陈玉清、胡飞凤、钟钰、高素英、钱先凤安徽省:周鹏程、储德全、李涛、丁家碧、许世辉福建省:张时勇、黄荔红、肖容英、史晓燕、陈文钦、谢永军、林冬青江西省:张军平、王栋、徐群志、徐飞、张朝霞山东省:李玉基、韩莹、国明、周勇、何慧、林炳勇、曹森河南省:王智明、张伟琦、谷静芳、杨胜亚、关蕾湖南省:曾三平、刘雁鸣、李文、吴胜丹、汪灿、杨清、黄晟、唐春辉湖北省:胡少玉、涂林、姚茂斌、费路华广东省:黄坤斌、江映珠、吴生齐、肖奕阳、谢正福、李薇、林盛文、钟向红、毕军广西壮族自治区:文东旭、梁柳青、许有诚海南省:王有生、王琨、周毓惠重庆市:梁渝陵、李霞、杨成钢、邓开英四川省:孙雪奇、何晓、徐杰、黄玉兰、王伯颖、曾必勇贵州省:黄铭铸、杨永东、张谆、宋勤云南省:王彬、陈祖芬、范兵、魏伟西藏自治区:达娃仓决、刘敬奎陕西省:林毅、翁吉安、杨志信、王力甘肃省:王兰霞青海省:刘海青宁夏回族自治区:海学武、刘雪岚新疆维吾尔自治区:李金凤中国药品生物制品检定所:宁保明关于公布第二批重新聘任的国家药品GMP检查员名单的通知国食药监办[2009]739号2009年11月03日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):按照国家局开展药品GMP检查员重新聘任工作计划,经各省(区、市)食品药品监管部门推荐,国家食品药品监督管理局综合考评,张亚东等120人为第二批重新聘任的国家药品GMP检查员,现予公布并核发《国家药品GMP检查员证》。