喹诺酮类抗菌药分类、构效关系.
- 格式:doc
- 大小:378.00 KB
- 文档页数:3

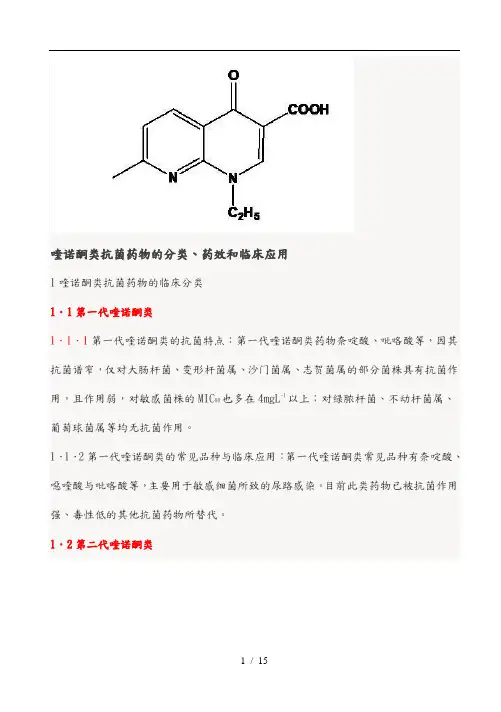
喹诺酮类抗菌药物的分类、药效和临床应用1喹诺酮类抗菌药物的临床分类1.1第一代喹诺酮类1.1.1第一代喹诺酮类的抗菌特点:第一代喹诺酮类药物奈啶酸、吡咯酸等,因其抗菌谱窄,仅对大肠杆菌、变形杆菌属、沙门菌属、志贺菌属的部分菌株具有抗菌作用,且作用弱,对敏感菌株的MIC90也多在4mgL-1以上;对绿脓杆菌、不动杆菌属、葡萄球菌属等均无抗菌作用。
1.1.2第一代喹诺酮类的常见品种与临床应用:第一代喹诺酮类常见品种有奈啶酸、噁喹酸与吡咯酸等,主要用于敏感细菌所致的尿路感染。
目前此类药物已被抗菌作用强、毒性低的其他抗菌药物所替代。
1.2第二代喹诺酮类1.2.1第二代喹诺酮类的抗菌特点:第二代喹诺酮类较第一代喹诺酮类抗菌活性强,对革兰阴性杆菌作用包括了部分绿脓杆菌,可达到有效尿药浓度,临床应用不良反应明显较第一代喹诺酮类少见。
1.2.2第二代喹诺酮类的常见品种与临床应用:第二代喹诺酮类有新噁酸、噻喹酸、噁噻喹酸、吡喹酸、吡哌酸等。
临床上主要用于肾盂肾炎、尿路感染与肠道感染的治疗。
1.2.3典型药物实例:吡哌酸(吡卜酸,Pipemidic Acid,Dolcol,Pipram,PPA)抗菌谱较广,对革兰阴性杆菌如大肠杆菌、绿脓杆菌、变形杆菌、痢疾杆菌等有较好的抗菌作用,对绿脓杆菌、变形杆菌的抗菌作用比对奈啶酸、头孢氨苄与羧苄西林强;作用机制是抑制细胞DNA的复制和转录。
吡哌酸一般采用口服给药,口服后部分吸收,成人单次口服0.5g和1.0g后,血药峰浓度为3.8mgL-1和5.4mgL-1,半衰期为3.1h;本品吸收后可分布于肾、肝等组织,胆汁中药物浓度高于血浆浓度;本品主要经肾排泄,给药后24h58%~68%的药物从尿液中排出,部分自粪便排出。
吡哌酸在临床主要用于尿路感染和肠道感染的治疗,本品与庆大霉素、卡那霉素、多黏菌素、青霉素等抗生素联用有协同作用,对绿脓杆菌、大肠杆菌、变形杆菌的作用增强。
1.3第三代喹诺酮类第三代喹诺酮类是20世纪70年代后期以后开发上市的药物,为一系列新型氟取代的4-氟喹诺酮类结构类似物。

喹诺酮类抗菌药的构效关系及不同成酸盐的原因在我们的日常工作中经常会遇到诸如盐酸左氧氟沙星、乳酸左氧氟沙星、甲磺酸左氧氟沙星等喹诺酮类药物的困惑,且在论坛上多次被大家所提及。
本人以微薄之力,短见浅识地向大家介绍为什么会出现如此让人摸不着头脑的问题。
在此首先要万分感谢广州医科大学有机化学教研室陈老师、临药网clinphar老师、丁香网药物化学讨论版天使猪及其他老师的指导,正是在他们的引导下我从自以为通天彻地地撰写了这篇文章到发现重大技术错误到现在才可以有脸出来。
本文涉及有机化学、药物化学等内容,对化学头晕乏力,心悸气促的网友们大可以直接阅读表格后的一段。
首先在了解这个问题前大家应该先了解喹诺酮类抗菌药的构效关系和有机酸的部分理化性质和结构特性。
(一)、喹诺酮类抗菌药的构效关系喹诺酮类抗菌药作用机制主要为双重抑制拓扑异构酶Ⅱ(DNA 旋转酶)和拓扑异构酶Ⅳ,从而影响DNA的正常形态与功能达到抗菌目的。
DNA是以高度螺旋卷紧的形式存在于菌体内,如果不卷紧,则其长度远远超过细胞壁,根本无法容纳在细胞壁中,也无法进行正常的DNA复制、转录、转运与重组。
DNA螺旋酶的作用就是使DNA保持高度卷紧状态。
喹诺酮类药物妨碍此种酶,造成染色体的不可逆损害,而使细菌细胞不再分裂。
拓扑异构酶Ⅳ在细胞壁的分裂中对细菌染色体的分裂起关键的作用。
喹诺酮类药物的毒性包括:1.极易与金属离子形成螯合物,所有喹诺酮类药物的一个共同特性是与金属离子特别是二价金属离子形成螯合物,不仅降低了药物的抗菌活性,同时也使体内的金属离子流失,尤其对妇女,老人和儿童能引起缺铁、缺锌、缺钙等症。
这方面内容可以翻阅《有机化学》路易斯酸碱理论及配合物等相关理论。
2.光毒性;3.药物相互反应(与P450);4. 软骨毒性。
5.有少数药物还有中枢毒性,胃肠道反应和心脏毒性。
这些毒性都与其化学结构有关。
1、A环是抗菌作用的基本结构,变化小;B环可作较大的改变,可以是苯环、吡啶环、嘧啶环等。




1 品种及作用喹诺酮类药物化学结构构效关系:1、喹诺酮母核的3位均有羧酸基,6位引入氟原子可增强抗菌作用并对金葡菌有抗菌活性。
2、7位引进哌嗪环可提高对金葡菌及绿脓杆菌的抗菌作用(如诺氟沙星),哌嗪环被甲基哌嗪环取代(如培氟沙星),则脂溶性增加,肠道吸收增强,细胞的穿透性提高,半衰期延长。
3、在8位引进第二个氟原子,可进一步提高肠道吸收,延长半衰期(如洛美沙星等)。
4、N-1修饰以环丙基团(环丙沙星)或噁嗪基团(氧氟沙星)可扩大抗菌谱,增强对衣原体、支原体及分支杆菌(结核杆菌与麻风杆菌等)的抗菌活性,噁嗪环还可提高水溶性,使药物在体内不被代谢,以原形经尿排泄。
分代及特点:第一代 萘啶酸、 吡哌酸对G -杆菌作用强,仅适用于尿路、肠道感染第二代 诺氟沙星、氧氟沙星、环丙沙星对G -菌作用强,体内较稳定,毒性降低,可用于各系统感染第三代 左氧氟沙星 、依诺沙星、氟罗沙星、洛美沙星、司帕沙星、格帕沙星在二代基础上增加了对G +球菌、衣原体、支原体、军团菌和结核杆菌的作用,安全性高,半衰期长第四代 莫西沙星、加替沙星 、克林沙星在三代基础上增加了对抗G +球菌的活性,增加了对厌氧菌的抗菌活性 抗菌作用:1、喹诺酮类药物对肠杆菌科细菌具有强大的抗菌作用,以环丙沙星为最高,左氧氟沙星和氧氟沙星次之;对不动杆菌和铜绿假单胞菌的抗菌作用较肠杆菌科细菌差;流感嗜血杆菌呈高度敏感,奈瑟氏菌属多呈敏感。
X N O OH O F R7R1R2R5R82、喹诺酮类药物对G+球菌亦具有抗菌作用,但其抗菌作用明显较肠杆菌科细菌低,以左氧氟沙星相对最高,环丙沙星和氧氟沙星略低;仅对金黄色葡萄球菌(除甲氧西林耐药外)具抗菌活性。
3、对衣原体、支原体、军团菌和结核分支杆菌及其他分支杆菌具有一定作用。
药动学特性:1、多数品种口服吸收良好,血药浓度相对较高。
2、半衰期较长,多在3-7h。
3、蛋白结合率低,大多为14%-30%。
4、体内分布广泛,组织和体内浓度常高于或等于血药浓度,可达有效治疗水平。




喹诺酮类药物结构特点与特性、作用机制、特点、分类和抗菌谱喹诺酮类药物是化学合成抗菌药,该类药物化学结构、作用机制均不同于其他抗菌药,且具有抗菌谱广、对革兰阴性菌抑制作用强于革兰阳性菌特点,是治疗各种感染性疾病高效且安全一类药物。
喹诺酮类结构特点与特性喹诺酮类是以4-喹诺酮为基本结构的合成类抗菌药,在4-喹诺酮母核N1位、C5位、C6位、C7位、C8位引入不同基团,形成各具特点喹诺酮类药物。
1.抗菌活性C6位引入氟原子同时,C7位引入哌嗪基后,药物与DNA回旋酶亲和力和抗菌活性显著提高,抗菌谱明显扩大,药动学性质显著改善。
N1位引入环丙基后,环丙沙星、司帕沙星、莫西沙星、加替沙星和加雷沙星等药物对革兰阳性菌、衣原体、支原体杀灭作用进一步增强,C6位脱去氟原子且C8位引入二氟甲基的加雷沙星对革兰阴性菌、革兰阳性菌、厌氧菌、支原体、衣原体均具有与莫西沙星类似的良好活性和药动学特征,毒性更低,诞生C6非氟氟喹诺酮类药物。
2.脂溶性C7位引入甲基哌嗪环,可增加氧氟沙星、氟罗沙星和左氧氟沙星药物脂溶性,提高口服生物利用度和对细菌的穿透力。
C8位引入氯原子或氟原子,进一步提高药物口服生物利用度,延长药物消除半衰期,提高药物脂溶性具有扩大抗菌谱和增强抗菌活性效果。
3.光敏反应C8位引入氯原子或氟原子后,在提高疗效同时,增强药物光敏反应,药物包括司帕沙星、氟罗沙星和洛美沙星。
以甲氧基取代C8位氯原子或氟原子时,在提高疗效同时还可降低光敏反应,药物包括莫西沙星和加替沙星。
4.中枢神经系统毒性C7位哌嗪环取代基团与γ-氨基丁酸受体拮抗剂结构相似,可拮抗GABA受体产生中枢神经系统症状。
喹诺酮类药物与茶碱或非甾体类抗炎药合用时易产生中枢毒性。
C6位有疏水性的氟原子使喹诺酮类药物具有一定脂溶性,易于透过血脑屏障。
去掉C6位氟原子的加雷沙星与NSAID合用不诱发惊厥反应,不影响GABA与γ-氨基丁酸A型受体结合,中枢神经系统毒性显著减低。
喹诺酮类抗菌药分类、构效关系
喹诺酮类抗菌药的基本结构为吡酮羧酸类衍生物,综合临床使用的喹诺酮类抗菌药的结构,归纳其基本结构通式如下:
12345678Y
X N 1
COOH
R 2
R 3R 4
5
O A B
该类药物的结构特点是在其基本母核结构上一般1位为取代的氮原子,3位为羧基,4位为酮羰基,5、7、8位可有不同的取代基,第三代、四代喹诺酮类抗菌药6位为氟原子。
喹诺酮类药物按其母核的结构特征可以分为以下四类: (1)萘啶羧酸类(naphthyridinic acids )
N N
2CH 3
H 3C
COOH
O
N N CH 2CH 3
N
COOH
O
F
HN
萘啶酸 依诺沙星
nalidixic acid enoxacin
(2)吡啶并嘧啶羧酸类(pyridopyrimidinic acids )
N N
N 2CH 3
COOH
O
N
N N
N 2CH 3
COOH
O
N
HN
吡咯酸 吡哌酸 piromidic acid pipemidic acid
(3)噌啉羧酸类(cinnolinic acids )
N
N O O
CH 2CH 3COOH
O
西诺沙星 cinoxacin
(4)喹啉羧酸类(quinolinic acids )
N CH 2CH 3
COOH
O
N
HN
F
N
O
F
N
HN
COOH
诺氟沙星 环丙沙星
norfloxacin ciprofloxacin
N
O
CH 3
COOH
F
N
N O
H 3C
N
O
F COOH
OCH 3
H N
N
氧氟沙星 莫西沙星
ofloxacin moxifloxacin
N
O
F
N
HN
COOH
F
3
NH 2
H 3C
N
O
F
N
HN
COOH
OCH 3
3
司帕沙星 加替沙星 sparfloxacin gatifloxacin
在这四类结构中,喹啉羧酸类药物最多,发展最快。
根据喹诺酮类抗菌药的化学结构和抗菌作用的关系,将该类药物的构效关系总结如下: 1.吡啶酮酸的A 环是抗菌作用的基本药效基团,变化较小,其中3位-COOH 和4位C=O 是抗菌活性必需基团,若被其他取代基取代则活性消失。
2.B 环可作较大改变,可以是苯环(X=CH ,Y=CH )、吡啶环(X=N ,Y=CH )、嘧啶环(X=N ,Y=N )等。
3.1位取代基为烃基或环烃基活性较佳,其中以乙基或与乙基体积相近的氟乙基或环丙基的取代活性较好。
4.5位可引入氨基,提高吸收能力或组织分布选择性。
5.6位引入氟原子可使抗菌活性增大。
引入其他不同取代基对抗菌活性贡献的大小顺序为:-F >-Cl >-CN≥-NH 2≥-H 。
6.7位引入五元或六元杂环,抗菌活性均增加,以哌嗪基最好。
7.8位以氟、甲氧基取代或与1位成环,可使活性增加。