电极过程动力学
- 格式:doc
- 大小:188.00 KB
- 文档页数:3
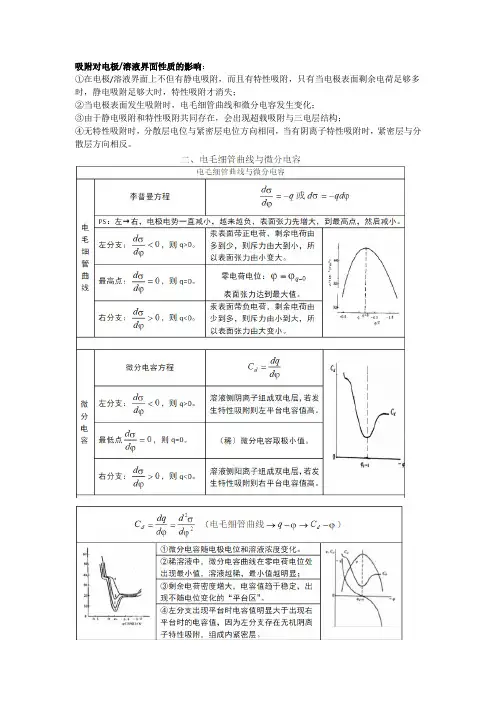
吸附对电极/溶液界面性质的影响:①在电极/溶液界面上不但有静电吸附,而且有特性吸附,只有当电极表面剩余电荷足够多时,静电吸附足够大时,特性吸附才消失;②当电极表面发生吸附时,电毛细管曲线和微分电容发生变化;③由于静电吸附和特性吸附共同存在,会出现超载吸附与三电层结构;④无特性吸附时,分散层电位与紧密层电位方向相同,当有阴离子特性吸附时,紧密层与分散层方向相反。
电极过程——电极表面附近薄液层中进行的过程与电极表面上发生的过程的总称。
电极过程单元步骤:①液相传质——反应粒子向电极表面传递;②表面转化(前置)——反应粒子在电极表面或附近液层发生某些转化;③电化学——反应粒子在电极/溶液界面得到电子或失去电子;④表面转化(后置)——反应产物在电极表面或附近液层发生某些转化;⑤a、新相生成——反应产物不溶时,反应产物生成新相;b、液相传质——反应产物可溶时,产物粒子从电极表面向溶液中或溶液电极内部迁移。
电极极化——电流通过电极时,电极电势偏离平衡电极电势的现象。
过电势——表示某一电流密度下极化电势与平衡电势之差。
①阳极过电势:②阴极过电势:控制步骤——电极过程中最慢的单元步骤。
极化曲线——电极上电势随电流密度变化的关系曲线。
传质过程(溶液):①对流——物质粒子随液体流动而移动。
A、自然对流——液体各部分之间由于存在浓度差或温度差产生的密度差或密度梯度而产生的对流;B、强制对流——通过搅拌而引起的对流。
②扩散——溶液中某一组分由于存在浓度梯度(或化学势梯度)而发生该组分向减少这种梯度的方向转移的过程。
③电迁移——带电粒子在电场梯度或电势梯度的作用下而引起的迁移过程。
扩散层——通过电流时,由于物质迁移缓慢而引起浓度发生扩散的液层。
稳态扩散——溶液中任意一点的浓度不再随时间变化的扩散过程。
(扩散速度与时间无关,反应粒子浓度分布只与空间有关,扩散层厚度一定)非稳态扩散——溶液中任意一点的浓度随时间变化的扩散过程。

电极过程动力学
电极过程动力学是一门研究电极表面的化学、物理过程的科学。
它涉及电化学反应的定义、电解池运行的机制以及电极间相互作用的步骤。
它涵盖了催化作用、阴阳极反应和过渡状态等一系列电化学过程,影响着电极表面反应活性、微结构、表面形貌和表面拓扑等,进而影响着电极表面电化学反应机制,比如电子传递机制、还原反应、氧化反应等。
此外,它还涉及电极表面涂层和金属原子的形成、失效及变质等现象。
电极过程动力学的研究在很大程度上受益于先进的检测技术,例如电化学显微镜(ECM)、原子力显微镜(AFM)以及等离子体质谱(ICP)等。
利用这些技术,可以观测电极表面形貌,检测指示电极和硫化物等微生物物质,还可以用于测定电极表面的微结构和电化学反应的机制。
电极过程动力学研究前景广阔,对于新型电极产品的研发尤其重要,它广泛应用于电池、燃料电池、水处理和电子器件的开发等领域。
此外,它还可以被应用于生物传感器的开发,以便检测病毒、细胞和基因。
比如,已有研究表明,电极过程动力学可以用于研究蛋白质和生物标记物的电化学反应特性,以有效地开发新型生物传感器。
电极过程动力学是一个复杂的概念,受多种因素影响,在实践中它不仅为电池、燃料电池、水处理和电子器件的发展奠定基础,还有助于新型生物传感器的开发,以检测细胞、病毒和基因等。
因此,电极过程动力学对研究电池、生物传感器、氧化反应机理以及珠宝等物质的耐久性具有重要的意义。
未来,电极过程动力学的研究将发展出更加先进的技术,以提高生物传感器精度,更好地满足人们的需求。




电极过程动力学基础、技术与应用电极过程动力学是电化学领域的重要基础理论,它研究了电化学反应中电荷转移和质量传递过程的速率规律。
了解电极过程动力学的基础原理和技术应用对于实现电化学分析、电化学合成和电池材料研究具有重要意义。
首先,电极过程动力学研究的基础是泊松-布尔兹曼方程。
该方程描述了电解液中离子浓度和电势之间的关系,进而揭示了电化学反应速率与电场强度、电荷转移的关系。
这为我们理解电极反应速率的控制机理奠定了基础。
其次,了解电极过程动力学的技术应用有助于优化电化学分析的方法。
通过研究反应速率与电极电位、离子浓度等参数的关系,我们可以确定最佳的测量条件,提高电化学分析的灵敏度和准确性。
例如,在电化学传感器中,我们可以通过修改电极材料和电位的控制,来实现对特定物质的高选择性检测。
此外,电极过程动力学的理论还可以指导电化学合成的优化。
通过调控反应条件和电极材料,我们可以增强所需产物的选择性和活性,提高电化学合成的效率和经济性。
这在有机合成和能源转换领域具有广阔的应用前景。
最后,电极过程动力学的研究对于电池材料的开发和性能改进也至关重要。
通过了解电极反应速率的控制机制,我们可以设计更高效的电池材料,提高其能量密度、循环寿命和安全性能。
在新能源领域,电极过程动力学的研究将有助于推动电池技术的突破和革新。
综上所述,电极过程动力学是电化学领域的基础理论,具有广泛的技术应用前景。
通过深入研究电极过程动力学的基础原理和应用技术,我们可以在电化学分析、电化学合成和电池材料研究等领域取得更加创新和突破性的进展。

电极过程动力学电极过程动力学是电化学中的一个重要分支,它着重研究电极电荷转移过程和相关的动力学机制。
电极过程动力学的研究对象包括电化学反应速率、电极化学反应的机理以及电化学反应的动态过程等。
本文将从电极反应速率、电位调控机理以及实际应用方面对电极过程动力学进行详细的介绍和分析。
一、电极反应速率1. 项里反应速率常数项里反应速率常数是衡量电极反应速率的重要参数。
它表示单位时间内反应物和产物之间的数量变化率。
在计算过程中,可以根据电荷转移过程中的动力学机制来确定项里反应速率常数。
通常情况下,项里反应速率常数与反应物和产物之间的活化能和电荷转移系数有关。
一般来说,项里反应速率常数越大,反应速率越快。
2. 泊松分布模型泊松分布模型是一种根据电子传输动力学研究电极反应速率的经典方法。
泊松分布模型假设电子从电极表面进入液相中的分布满足泊松分布。
据此,可以利用该模型计算出电极反应速率以及与之相关的电极化学反应机理。
然而,实际情况中,由于电极表面可能存在着非均匀性和多孔性等特征,泊松分布模型过于理想化,难以准确预测电极反应速率。
3. 热力学因素对电极反应速率的影响热力学因素对电极反应速率有着重要的影响。
根据热力学定律,电位差和电极之间的电势差会影响电子传输和离子转移速率。
当电极电位愈高,电位差就愈大,因此,电子和离子的传输速率就变得更快。
此外,反应物和产物之间的物理和化学吸附现象也会影响电极反应速率。
这些因素的影响程度需要结合具体的条件和反应机理来进行考虑。
二、电位调控机理1. 电位和电场电位是电子在电场作用下所具有的势能差。
由于电场力是由电荷带来的,因此,电位和电场强度是密切相关的。
在电极过程动力学中,电位的变化会影响电子传输过程,进而影响电极化学反应的速率和机理。
2. 离子选择电位离子选择电位可以影响电极的电化学反应机理和速率。
当电极表面存在多种离子时,离子选择电位会决定电极表面上离子种类的比例。
因此,在研究电极过程动力学时,需要对离子选择电位进行分析和控制。

电化学电极过程动力学复习、难点、习题传质过程(扩散极限电流)j d 影响传(电)荷过程传质过程(扩散极限电流)j d 影响传(电)荷过程电极过程动力学电极过程动力学控制电化学过程加快或减缓电化学反应速度(电流)控制电化学过程加快或减缓电化学反应速度(电流)超电势(电化学、浓差)极化现象三(二)电极体系j 0 ,η,α,B-V 方程,Tafel 公式极化曲线超电势--电流曲线jja =j= 10-3Acm-2’b =j= 10-6Acm-2’c =j= 10-9Acm-2’交换电流密度对i-η曲线的影响电荷传递系数对i-η曲线的影响Tafel曲线阳极超电势阴极超电势E=ϕa-ϕcI/A电解电池I-V曲线液相中的三种传质过程注意其所传输的物种及发生在溶液体相或在固/液界面电极界面溶液层的几部分反应物浓度体相电极溶液δ氢电极的极化曲线示意图H+ 离子的还原和析出氢气过程H3O+H3O+ H3O+adH adH2H2H3O+ + M + e M-H + H2O 迟缓放电机理Volmer反应氢超电势Hydrogen OverpotentialH 3O ++ M + e M-H + H 2O迟缓放电机理Volmer 反应(a) H 3O ++M-H+e M+H 2O+H 2Heyrovsky 反应(b) M-H + M-H 2M + H2Tafel反应4.(a) H 3O ++M-H+e M+H2O+H 2电化学脱附机理Heyrovsky 反应(b) M-H + M-H 2M + H 2Tafel 反应3. H 3O + + M + e M-H + H 2O 迟缓放电机理Volmer 反应3, 4(a), 4(b) 皆可能为速度控制步骤2H ++ 2e 2H ad (2M-H) M-H + M-H 2M + H (2][2irad Fk j Η=(忽略逆过程)][][ln '+ΗΗ−=r ad o r F RT ϕϕ][][ln '+ΗΗ−=ir ad o ir F RT ϕϕ][][ln'+ΗΗ−=ir ad o ir F RT ϕϕ⎭⎬⎫⎩⎨⎧−Η=ΗRT F c r ad ir ad ηexp ][][2][2irad Fk j Η=⎭⎬⎫⎩⎨⎧−Η=RT F Fk j c r ad η2exp ][22⎭⎬⎫⎩⎨⎧−=RT F j c η2exp 0jzFRT j zF RT c lg 303.2lg 303.20−=η注意: 没有α!21=α电化学方法的主要优点1. 通过方便调节电极电势显著地改变反应速度2. 较易控制电极反应方向3. 电极反应一般在常温常压下进行4. 反应所用氧化剂或还原剂为电子,环境污染少电化学学习重点物理化学固态电化学光电化学生物电化学量子化学统计热力学溶液电化学(电解质溶液)平衡态电化学热力学。


电极过程动力学导论
电极过程动力学是研究电极反应物的运动轨迹及其速率变化规律的学科。
电极过程动力学是电极反应的理论基础,对于阐明电极过程的机理,解释电极反应的发展趋势,估计电极反应的反应速率等方面都起着关键作用。
电极过程动力学的研究从热力学出发,从电极反应体系的热力学性质,电化学条件,电极反应物的质量比,电解液的组成等多方面来研究电极反应物的运动轨迹及其速率变化规律。
电极过程动力学要求电极反应物的运动轨迹及其速率变化规律必须与电极反应的电动势和电流密切相关,以便能够准确地描述电极过程的动力学过程。
另外,在电极反应的过程中,由于参与的物质的数量不断发生变化,因此电极反应物的运动轨迹及其反应速率也会随之发生变化,这种变化可以通过电极过程动力学来描述。
电极过程动力学也可以应用于电化学传感器,电极过程动力学能够很好地描述电极反应物的运动轨迹及其速率变化规律,从而帮助设计出能够更好检测物质浓度变化的传感器。
总之,电极过程动力学是一门研究电极反应物的运动轨迹及其速率变化规律的学科,是电极反应的理论基础,在研究电极反应的机理,解释电极反应的发展趋势,估计电极反应的反应速率,设计传感器等方面都有着重要的作用。

5.电极过程和电极过程动力学5.1电化学装置的可逆性:化学反应可逆性;热力学上可逆性5.2电极的极化5.3电极过程的控制步骤:电极反应的特点;电极反应的控制步骤5.4电荷转移动力学方程5.5交换电流密度与电极反应速度常数5.6稳态极化时的电极动力学方程5.7浓差极化及其电机动力学方程5.8化学极化分解电压E分:在可逆情况下使电解质有效组元分解的最低电压,称为理论分解电压(V e)。
理论分解电压是阳极平衡电极电位(εe(A))与阴极平衡电极电位(εe(K))之差。
Ve=εe(A)- εe(K)(10 - 5)当电流通过电解槽,电极反应以明显的速度进行时,电极反应将会明显偏离平衡状态,而成为一种不可逆状态,这时的电极电位就是不平衡电位,阳极电位偏正,阴极电位偏负。
这时,能使电解质熔体连续不断地发生电解反应所必需的最小电压叫作电解质的实际分解电压。
显然,实际分解电压比理论分解电压大,有时甚至大很多。
实际分解电压简称分解电压(V),是阳极实际析出电位(ε(A))和阴极析出电位(ε(K))之差。
V=ε(A)- ε(K)(10 - 6)当得知阴、阳极在实际电解时的偏离值(称为超电位)就可以算出某一电解质的实际分解电压。
分解电压符合能斯特方程,可以表示为如下形式:式中E i,E0分别表示实际和标准状态下组元i的分解电压;a i__组元的活度;n i __组元在熔盐中的化合价;F __ 法拉弟常数;可以看出,温度和电解质组成均会影响分解电压电极极化电解时的实际分解电压比理论分解电压要大很多,这是由于电流通过电解槽时,电极反应偏离了平衡状态。
通常将这种偏离平衡电极电位的现象称为极化现象。
电解过程实际分解电压和理论分解电压之差称为超电压。
⏹电解电极反应一般包含1:☐(1)反应离子由熔体向双电层移动并继续经双电层向电极表面靠近。
这一阶段在很大程度上靠扩散实现,扩散则是由于导电离子在熔体和双电层外界的浓度差别引起的。
☐(2)反应离子在电极表面进行电极反应前的转化过程,如表面吸附等;☐(3)在电极上的电子传递- - 电化学氧化或电化学还原反应;☐(4)反应产物在电极表面进行反应后的转化过程,例如自电极表面的脱附,反应产物的复合、分解和其它化学反应;☐(5)反应产物形成新相,或反应产物自电极表面向电解质熔体的传递。
吸附对电极/溶液界面性质的影响:①在电极/溶液界面上不但有静电吸附,而且有特性吸附,只有当电极表面剩余电荷足够多时,静电吸附足够大时,特性吸附才消失;②当电极表面发生吸附时,电毛细管曲线和微分电容发生变化;③由于静电吸附和特性吸附共同存在,会出现超载吸附与三电层结构;④无特性吸附时,分散层电位与紧密层电位方向相同,当有阴离子特性吸附时,紧密层与分散层方向相反。
电极过程——电极表面附近薄液层中进行的过程与电极表面上发生的过程的总称。
电极过程单元步骤:①液相传质——反应粒子向电极表面传递;②表面转化(前置)——反应粒子在电极表面或附近液层发生某些转化;③电化学——反应粒子在电极/溶液界面得到电子或失去电子;④表面转化(后置)——反应产物在电极表面或附近液层发生某些转化;⑤a、新相生成——反应产物不溶时,反应产物生成新相;b、液相传质——反应产物可溶时,产物粒子从电极表面向溶液中或溶液电极内部迁移。
电极极化——电流通过电极时,电极电势偏离平衡电极电势的现象。
过电势——表示某一电流密度下极化电势与平衡电势之差。
①阳极过电势:②阴极过电势:控制步骤——电极过程中最慢的单元步骤。
极化曲线——电极上电势随电流密度变化的关系曲线。
传质过程(溶液):①对流——物质粒子随液体流动而移动。
A、自然对流——液体各部分之间由于存在浓度差或温度差产生的密度差或密度梯度而产生的对流;B、强制对流——通过搅拌而引起的对流。
②扩散——溶液中某一组分由于存在浓度梯度(或化学势梯度)而发生该组分向减少这种梯度的方向转移的过程。
③电迁移——带电粒子在电场梯度或电势梯度的作用下而引起的迁移过程。
扩散层——通过电流时,由于物质迁移缓慢而引起浓度发生扩散的液层。
稳态扩散——溶液中任意一点的浓度不再随时间变化的扩散过程。
(扩散速度与时间无关,反应粒子浓度分布只与空间有关,扩散层厚度一定)非稳态扩散——溶液中任意一点的浓度随时间变化的扩散过程。
电极过程动力学
电极过程动力学是一门讨论电极反应机制的学科,旨在研究电极反应中的各种化学反应的动力学行为,并研究如何影响电极反应。
它是实验金属电化学学科的基础,它为电极反应中的反应机制提供了理论框架,以便能更好地理解和解释各种电极反应的化学机理。
电极过程动力学主要关注电极反应的快速发生,它所研究的概念包括电极反应的能量和速率,反应机理,电化学动力学,反应机理的构型变化等。
在研究电极过程动力学时,需要考虑电极容量、势能条件以及相关的反应机理。
电极容量是指电极表面上的反应物分子的会聚程度,它可以影响电极反应的动力学。
势能条件是指反应物和中间体之间的势能差,它可以决定反应物是否能发生反应。
而反应机理是指介导电极反应的反应步骤,可以帮助我们更好地理解和控制电极反应。
电极过程动力学的研究可以分为实验研究和理论计算两个部分。
实验研究是首先使用电化学实验法研究电极反应的快速发生,并根据实验结果推测反应机理。
而理论计算则是根据实验结果,使用各种方程式、数学模型或计算机模拟的方法,来计算电极反应的动力学行为和机理。
电极过程动力学的研究对无机电化学,有机电化学,可见光电极反应,腐蚀电极反应,生物电极反应等电极反应形式都具有重要意义。
电极过程动力学有助于促进电极材料的发展,并且可以应用于新型能源系统的设计。
总之,电极过程动力学的研究可以帮助理解电极反应中的反应机制,探索和解释电极反应的化学机理,推动电极材料的发展,从而有助于改善能源存储和有效利用能源。
电极过程动力学
一、实验目的
通过对铜电极的阳极极化曲线和阴极极化曲线的测定,绘制出极化曲线图,从而进一步加深对电极极化原理以及有关极公曲线理论知识的理解。
通过本实验,熟悉用恒电流法测定极化曲线。
二、实验原理
当电池中由某金属和其金属离子组成的电极处于平衡状态时,金属原子失去电子变成离子获得电子变成原子的速度是相等的,在这种情况下的电极称为平衡电极电位。
电解时,由于外电源的作用,电极上有电流通过,电极电位偏高了平衡位,反应以一定的速度进行,以铜电极Cu|Cu2+为例,它的标准平衡电极电位是+0.337V,若电位比这个数值更负一些,就会使Cu2+获得电子的速度速度增加,Cu失去电子的速度减小,平衡被破坏,电极上总的反应是Cu2+析出;
反之,若电位比这个数值更正一些,就会使Cu失去电子的速度增加,Cu2+获得电子的速度减小,电极上总的反应是Cu溶解。
这种由于电极上有电流通过而导致电极离开其平衡状态,电极电位偏离其平衡的现象称为极化,如果电位比平衡值更负,因而电极进行还原反应,这种极化称为阴极极化,反之,若电位比平衡值更正,因而电极进行氧化反应,这种极化称为阳极极化。
对于电极过程,常用电流密度来表示反应速度,电流密度愈大,反应速度愈快。
电流密度的单位常用安培/厘米2,安培/米2。
由于电极电位是影响影响电流密度的主要因素,故通常用测定极化曲线的方法来研究电极的极化与电流密度的关系。
一、实验方法及装置
本实验电解液为CuSO4溶液(溶液中CuSO4.5H2O浓度为165g/l,H2SO4 180g/l);电极用φ=0.5mm铜丝作为工作电极,铂片电极作为辅助电极。
为了测得不同电流密度下的电极电位,以一个甘汞电极与被测电极组成电池,甘汞电极通过盐桥与被测电极相通,用CHI660B电化学工作站测得不同电流密度下对应的阴极或阳极极化曲线。
装置如图所示
3 1——铜丝(工作电极Ф1.0mm);
2——铂片(辅助电极);3——甘汞电极;4——盐桥;
二、实验步骤
1、将铜电极的工作表面用0号金相砂纸磨光,用蒸馏水洗净,用滤
纸擦干,然后放入装有CuSO
溶液的电解槽中。
4
2、在装有饱和KCl溶液的电解槽中放入盐桥连通管和甘汞电极。
3、测定阴极、阳极极化曲线
1)注意将工作电极(铜丝)接绿色夹子,甘汞电极接白色夹子(参比电极),辅助电极(铂片)接红色夹子,使盐桥所用连通管尖端靠近工作电极工作面。
2)打开CHI660B电化学工作站的电源和计算机,然后在桌面上双击chi660b 图标运行CHI660B电化学工作站软件。
在Control菜单下选择Open Current Potential测试开路电位。
3)点击Setup菜单下Technique选项,在弹出的Electrochemical
Techniques窗口中选择Chronopotentiometry(计时电位法),点OK确认。
4)阴极极化曲线的测定:点击Setup菜单下Parameters选项,在弹出的
Chronopotentiometry Parameters窗口中设置参数。
Cathodic Current(A)、Anodic Current(A)均设置为0.005A;High E Limit(V)为0.5V,Low E Limit(V)
为-0.5V;Initial Polarity选Cathodic(阴极)进行阴极极化曲线的测定。
Cathodic Current(A)、Anodic Current(A)依次设置为
0.010A,0.015A,0.020A重复上面实验。
阳极极化曲线的测定:点击Setup菜单下Parameters选项,在弹出的Chronopotentiometry Parameters窗口中设置参数。
Cathodic Current(A)、Anodic Current(A)均设置为0.005A;High E Limit(V)为0.5V,Low E Limit(V) 为-0.5V;Initial Polarity选Anodic(阳极)进行阳极极化曲线的测定。
Cathodic Current(A)、Anodic Current(A)依次设置为
0.010A,0.015A,0.020A重复上面实验。
注意:阴阳极交替试验可减少电极打磨次数。
5)在Control菜单下选择Run Experiment 开始实验。
结束实验可在Control 菜单下选择Stop Run或在工具栏中直接点击▲开始,■结束。
6)点击工具栏中将曲线放大。
7)在Graphics菜单下点击Copy to Clipboard至word打印。
4、关掉电源,取出电极冲洗干净。
三、数据处理
1.根据测得的电动势计算出阳、阴极电位,以伏为单位。
φ阳(阴)=φ实测-φ甘汞
2.根据电流及面积计算出电流密度,以安培/厘米2为单位。
四、编写实验报告
1.简述实验原理,方法及流程;
2.填写实验记录、数据处理及图表;
3.实验分析;
4.建议、意见。