同时检测多巴胺,抗坏血酸和尿酸的石墨烯-贵金属纳米复合物基电化学传感器
- 格式:pdf
- 大小:402.55 KB
- 文档页数:1

石墨烯修饰金电极的制备及其同时测定多巴胺和尿酸艾永青;胡芹芹;肖虎勇;连盼盼;吕鉴泉【摘要】Graphene modified gold electrode(Gr/Au) was got by the method that fresh grapheme which was prepared based on the Hummers method was attached to the surface of gold electrode.The electrochemical properties of the graphene modified gold electrode and the electrochemical behaviors of dopamine and uric acid at Gr/AuElectrode were investigated by cyclic voltammetry.The result shows that the electrochemical oxidation and reduction of dopamine and uric acid could be electrocatalyzed.Dopamine and Uric acid could be detected simultaneously with the exist of ascorbic acid.There are linear relationships between the anoidic peak current and the concentration ofdopamine(1.0~1000 μmol/L),uric acid(30~1000 μmol/L) in diff erential pulse voltammograms,the detection limits are 0.67 μmol/L and 6.0μmol/L,respectively.%将Hummers法合成的新鲜石墨烯滴涂于金电极表面,制备了石墨烯修饰金电极(Gr/AuE)。

多巴胺电化学传感器专利技术综述多巴胺电化学传感器是一种基于电化学技术的传感器,用于检测多巴胺在生物体系中的含量。
多巴胺是一种重要的神经递质,在多种生物过程中发挥着关键的作用,因此准确测定其含量对于生命科学研究具有重要意义。
在过去的数十年中,开发了多种多巴胺电化学传感器,以满足不同研究需求。
本文将从专利技术方面对多巴胺电化学传感器的发展进行综述。
多巴胺电化学传感器采用电化学法检测多巴胺含量,其原理是将多巴胺转化为可氧化的还原剂,随后通过电化学反应将其氧化,并测量产生的电流。
多巴胺在电极表面的还原和氧化反应可以表示为以下式子:多巴胺+e- → 多巴胺•(还原反应)传感器中的电极表面通常涂覆有化学修饰剂,以促进多巴胺的吸附和电子转移。
多巴胺的浓度可以通过测量电流大小来确定,电流与多巴胺的浓度呈正比关系。
(二)多巴胺电化学传感器研究现状近年来,多巴胺电化学传感器研究得到了快速发展,吸引了越来越多的研究者的关注。
以下是目前多巴胺电化学传感器领域的一些主要研究进展:1. 传感器材料传感器材料对于传感器性能具有重要影响。
现有多巴胺电化学传感器材料主要有碳纳米管、金属有机骨架、纳米颗粒等。
这些材料在吸附效率、电子传递速率、物理稳定性等方面具有各自的优势,已被广泛应用于多巴胺电化学传感器的开发中。
2. 检测技术目前多巴胺电化学传感器的检测技术主要有常规电化学检测、光电化学检测和生物传感检测等。
其中,生物传感检测利用生物信号转换成电信号,可以提高传感器的灵敏度和特异性。
而光电化学检测则通过光激发产生的电荷将传感器灵敏度提高到亚纳摩尔级别。
3. 纳米技术纳米技术是近年来多巴胺电化学传感器研究的重要方向之一。
纳米材料具有高比表面积、尺寸可控性以及物理、化学、电学等性质的独特优势,被广泛应用于传感器的制备和改性中。
例如,通过利用纳米金粒子修饰电极表面,可以显著提高传感器的特异性和灵敏度。
1. 中国专利CN109196915A该专利涉及一种基于杂多酸-多巴胺分子印迹聚合物修饰石墨烯修饰电极的多巴胺传感器。

多巴胺电化学检测研究进展王保光;张鑫;张雪华;何声太;贺涛【摘要】对近年来电化学方法在多巴胺检测方面的应用和进展进行了综述,并对其发展前景进行了展望.【期刊名称】《应用化工》【年(卷),期】2013(042)012【总页数】4页(P2267-2270)【关键词】多巴胺;灵敏度;选择性;修饰电极;电化学检测【作者】王保光;张鑫;张雪华;何声太;贺涛【作者单位】天津工业大学材料科学与工程学院,天津300387;国家纳米科学中心,北京100190;国家纳米科学中心,北京100190;国家纳米科学中心,北京100190;天津工业大学材料科学与工程学院,天津300387;国家纳米科学中心,北京100190【正文语种】中文【中图分类】TQ035;TQ320.77+2;O646多巴胺(DA)属于儿茶酚胺类物质,是哺乳动物和人类中枢神经系统中一种非常重要的信息传递物质,缺乏DA可导致一些重要疾病如精神分裂症和帕金森氏症[1],所以对DA的研究在神经生理学、临床医学、制药学等许多学科都具有十分重要的意义。
近年来,围绕着发展高灵敏度高选择性检测DA的在线分析方法,研究者做了大量的努力,电化学、化学发光、高效液相色谱法、表面等离子体共振、表面增强拉曼以及荧光法等检测DA的方法相继涌出。
在诸多方法当中,电化学分析法具有高选择性、高灵敏度、高稳定性等优点,尤其是微型电化学探针具有良好的生物相容性,能够进行活体在线分析,这使电化学分析方法成为检测DA的理想方法。
在过去几十年的时间里,电化学检测多巴胺已经取得了很大的进展。
但是,直接电化学方法检测DA面临以下问题:①抗坏血酸和尿酸与DA共存于大脑和体液中,在裸电极上三者的氧化电位相近,易对DA检测造成干扰;②AA的浓度一般为10-7~10-3 mol/L不等,且易被氧化失去两个氢原子而转变成脱氢AA,而DA 的浓度为10-8~10-6 mol/L,AA 能够还原DA的电化学氧化产物使其再生;③DA的氧化产物会在电极表面形成一层薄膜而污染电极。


碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸李珠叶1,张 萍1,刘传银1,2(1.湖北文理学院 化工与食品学院,湖北 襄阳 441053;2.低维光电材料与器件湖北省重点实验室,湖北 襄阳 441053) [摘 要]采用滴涂法和循环伏安法(CV)将碳纳米管和Co修饰到玻碳电极表面,得到碳纳米管-电沉积Co修饰电极,研究了多巴胺(DA)、尿酸(UA)在碳纳米管-电沉积Co修饰电极上的电化学响应.结果表明,在0.1mol/L磷酸缓冲液(pH=6)中,DA、UA在该电极上均显示出良好的电化学响应,碳纳米管-电沉积Co修饰的玻碳电极能够将DA和UA的氧化峰电位明显分开,两者峰电位差为124mV,并且可以在抗坏血酸(AA)存在下同时测定DA和UA.该修饰电极选择性好、稳定性高,可以实现AA存在下DA和UA共存时两种物质的定量检测. [关键词]多巴胺;尿酸;抗坏血酸;碳纳米管-电沉积钴修饰电极 [doi]10.3969/j.issn.1008-6072.2016.06.005 [中图分类号]O657.1 [文献标识码]A [文章编号]1008—6072(2016)06—0027—071 引言 多巴胺(DA)是广泛分布在哺乳动物大脑中枢神经系统中的神经递质,在中枢神经系统、肾脏和心脑血管中发挥重要作用.体内DA水平低下会导致神经紊乱,易患精神分裂症、帕金森综合症等[1].尿酸(UA)和其它羟基嘌呤一样是人体嘌呤代谢的产物,体液中UA含量过高是许多疾病的征兆,如痛风症、高血尿、心血管疾病等[2].因此,尿酸和多巴胺的检测和分析对临床诊断、了解病情进展具有重要意义.由于DA、UA具有电化学活性,而电化学分析方法以其灵敏度高,选择性好,和分析费用低廉等特点而得到了广泛的关注.但是利用电化学方法测定UA的一个主要问题是体液中共存的抗坏血酸(AA)的干扰.因此,建立在大量抗坏血酸(AA)存在下准确测定DA、UA的方法,更具有实际意义. 本文采用电沉积钴于碳纳米管修饰电极之上,研究了DA、UA在此电极上的电化学行为,优化了测定条件,探讨了DA、UA在此电极上的氧化机理,采用电化学方法测定多巴胺和尿酸.该电极在活化后能有效降低抗坏血酸对DA、AA测定的影响,实现了大量抗坏血酸存在下多巴胺、尿酸的选择性检测.该方法具有稳定性好、重现性好和准确度高的特点,对实际样品的测定结果满意.2 实验部分2.1 仪器与试剂 电化学实验均在CHI660a电化学工作站(上海辰华仪器有限公司)上完成,配备三电极体系,以玻碳电极或修饰玻碳电极为工作电极,饱和甘汞电极(SCE)为参比电极,Pt丝对电极;碳纳米管(CNTs)购自华中师范大学纳米研究院,并经酸化处理;多巴胺(DA)、尿酸(UA)、抗坏血酸2016年12月郧阳师范高等专科学校学报Dec.2016第36卷第6期Journal of Yunyang Teachers College Vol.36No.6[收稿日期]2016-09-20[基金项目]2016年度大学生创新创业项目、湖北省低维光电材料与器件重点实验室开放基金资助[作者简介]李珠叶(1994-),女,湖北襄阳人,湖北文理学院化学工程与工艺专业学生,主要从事分析化学研究. 论文联系人:刘传银(1970-),男,教授,博士.通讯联系人E-mail:liucyin2002@sina.com.YYSZXB27(AA)购自Sigma-Aldrich.其他所有试剂均为分析纯,购自上海国药集团.实验用水为超纯水.2.2 电化学实验 将裸玻碳电极为工作电极,三电极体系进行电化学实验,电沉积是在含有5%CoSO4的溶液中进行,采用循环伏安法进行电沉积;电极的表征采用交流阻抗法,在含有0.001mol/L Fe(CN)63-/4-的KCl溶液中进行,式量电位为0.22V,扫描频率为0.01-105 Hz范围内进行.3 结果与讨论3.1 电极的修饰与活化 玻碳电极(3mm)经氧化铝悬糊抛光成镜面后,将CNTs壳聚糖溶液10μL加到电极表面,红外灯下烤干,即得CNTs/GCE电极;然后将该电极插入5%CoSO4溶液中以100mV/s的扫速在-0.2到1.0V范围内循环伏安电沉积40圈,取出洗净,即得Co-CNTs/GCE修饰电极.将新修饰的Co-CNTs/GCE电极在0.1mol/L NaOH溶液中电化学活化.结果表明,随着扫描的进行,其峰电流逐渐增大,并稳定地出现一对循环伏安峰.这对峰对应着Co(III)/Co(II)在电极上的氧化还原[3-4].图1碳纳米管修饰电极的电沉积及其活化的循环伏安图Fig.1. CVs of Co electrochemical deposition on CNTs/GCE and its activation3.2 不同修饰电极的电化学表征 电极经过修饰和电沉积后,总会改变电极的面积和表面形貌,故常用循环伏安和交流阻抗法对电极进行表征.如图2(A)所示,在含有0.001mol/L Fe(CN)63-/4-的KCl溶液中,裸电极呈现一对良好的循环伏安峰,其峰电位差约95mV;然而在修饰了碳纳米管后,其峰电位差增大到175mV,但是峰电流却大大增大.这是因为碳纳米管具有较大的表面积,从而使铁氰化钾在电极上参与反应的量增大,进而使峰电流增大,然而由于壳聚糖是一种电子传递阻体,故其峰电位差会增大;而电沉积Co后,其峰电流达到最大,表明电沉积Co进一步增大了电极面积,但是当经NaOH活化后,其峰电位差和峰电流均降低,这种现象可能的原因是经活化后,其表面的氧化物转化为氢氧化物,从而降低了表面内阻,但是氢氧化物之间电子传递的能力又较强于氧化物,所以呈现出上述的现象.为了进一步表征电极的表面状态,交流阻抗法也是一种良好表征表面状况的电化学方法.图2(B)是不同电极的交流阻抗图.如图所示,裸电极呈现一条近乎450的直线,表明其表面无物质阻碍电子传递;同样其他几种修饰电极由于修饰了导电性的CNTs,并电沉积Co后,其表面均不阻碍电荷的传递,呈现为不同角度的近乎直线的交流阻抗图.交流阻抗结果与循环伏安结果相符.李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸YYSZXB28图2不同电极在0.001mol/L Fe(CN)63-/4-中的循环伏安图和交流阻抗图Fig.2. CVs and Nyquist plots of various electrodes in 0.001mol/L Fe(CN)63-/4-3.3 DA、UA在不同电极上的电化学响应 图3显示了不同电极分别在含有DA(10-4mol/L)、UA(10-4 mol/L)的磷酸缓冲溶液(pH=6)中的循环伏安图.由图3(A)可见,DA在裸GCE电极上的电流很小,修饰碳纳米管后峰电流也有上升,并且峰电位差也降低到61mV,电沉积Co后峰电位差变化不大,但峰电流增大,然而在电极经NaOH活化后,峰电位差进一步降低到51mV,峰电流进一步增大.这是由于碳纳米管有较大的比表面积,且钴的氢氧化物传递电子能力强,有利于DA在电极上的电子传递[4].而且DA在该活化后的修饰电极上的响应特别稳定,表明DA能够较快地在电极上发生氧化还原反应.由图3(B)可见,UA在4种电极上均只出现氧化峰,说明UA在电极上为完全不可逆氧化过程.UA在裸GCE(曲线a)上有一个小氧化峰,在CNTs/GCE(曲线b)氧化峰电流有所增加,但峰形差,电沉积Co后峰电位变化不大,但峰电流增大,然而电极经NaOH活化后,氧化峰电流进一步增大.这同样表明钴的氧化物虽然有催化氧化的作用,但传递电子的能力没有钴的氢氧化物强.此外,该复合膜具有高的选择性和强的抗干扰能力,使其在大量抗坏血酸存在下,能与DA、UA很好地分离,实现DA、UA的准确测定.图3不同电极下DA、UA在磷酸缓冲液(pH=6)中的循环伏安图Fig.3 CVs of DA and UA at different electrodes in pH 6PBS3.4 pH的影响 不图pH的缓冲溶液对DA、UA的测定有很大的影响,故用循环伏安法在pH 5~9范围内研究了DA、UA共存时pH对两者峰电流和峰电位的影响(如图4).DA氧化峰电流随着pH先增大后减小,当pH为6时氧化峰电流最大,故选用pH为6的磷酸缓冲溶液作为支持电解质.实验结果表明,DA,UA的氧化峰与pH呈良好的线李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸YYSZXB29YYSZXB30性关系,对于DA的氧化峰电位,线性方程为:E(V)=0.636-0.063pH,R=0.9966;对于UA的氧化峰电位,线性方程为E(V)=0.774-0.062pH,R=0.9944.从以上结果表明,DA与UA的电氧化都伴随着质子的转移,由峰电位与pH的线性关系的斜率可以推断出DA和UA的电氧化伴随着两电子两质子的过程,此结果也与以前的研究报道相符[5].图4DA,UA在不同pH下的CV图,内插图为Ep-pH关系曲线Fig.4 CVs of DA and UA in various pH PBS,inset plot is the relationship of Epversus pH3.5 不同扫速的影响 图5为DA(10-4 mol/L),UA(10-4 mol/L)在不同扫速下的循环伏安曲线.由图5(a),(b)可以看出随着扫描速度由10mV/s增加至300mV/s,它们的峰电位不断增大,峰电流也不断增大,氧化峰电位正移.将它们的峰电流分别与扫速及扫速的平方根作图,发现峰电流与扫速平方根的线性关系均比峰电流与扫速的线性关系好,故两者峰电流都与扫速平方根呈现良好的线性关系)所示,DA的回归方程为Ipa=0.383-21.960 v,r=0.9973,Ipc=-3.575+41.540 v,r=0.9972;UA回归方程为Ipa=-1.826-4.453 v,r=0.9925.表明DA,UA在该修饰电极表面是一个扩散控制过程[6].实验还发现,随着扫速的增大,峰电位与扫速的对数之间在v>80mV/s时将呈现良好的线性关系,对DA来说,Epa=0.3013+0.0209lnv,r=0.9821,Epc=0.1079-0.0399lnv,r=-0.9980.根据Laviron方程[7]:Epa=Eo/+RT(1-α)nFln(1-α)nFRTks+RT(1-α)nFlnvEpc=Eo/-RTαnFlnαnFRTks-RTαnFlnv根据线性关系的斜率和截距,可以计算出:nα=0.64,n(1-a)=1.23;ks=0.74cm/s图5 (a)DA不同扫速下的循环伏安图(b)UA不同扫速下的循环伏安图Fig.5 CVs of DA(a)and UA(b)at various scan rates李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸3.6 DA、UA在actived Co-CNTs/GCE电极上的电化学响应 图6(A)和(B)为actived Co-CNTs/GCE修饰的玻碳电极对DA和UA同时存在时固定一种物质含量改变另外一种物质含量时的循环伏安曲线.从图中可以看出DA和UA同时存在时,DA和UA的氧化峰能够明显分开.图(A)为同时含有UA(100.0μmol/L)+DA(10.0μmol/L,30.0μmol/L,50.0μmol/L,70.0μmol/L,100.0μmol/L)的PBS(0.1mol/L,pH=6.0)的溶液中的循环伏安曲线,从图中可以看出保持UA的浓度不变,改变DA的浓度,UA的氧化峰电位与峰电流几乎没有变化.图(B)为同时含有DA(100μmol/L)+UA(50μmol/L,70μmol/L,100μmol/L)的PBS(0.1mol/L,pH=6.0)溶液中的循环伏安曲线,从图中可以看出保持DA的浓度不变,改变UA的浓度,DA的氧化峰电位几乎不变,峰电流变化很小(<5%).表明actived Co-CNTs/GCE修饰的玻碳电极有可能实现DA、UA的同时检测.(A) (B)图6不同浓度的DA(A)、UA(B)共存时activated Co-CNTs/GCE电极的循环伏安曲线扫描速率;100mV/s,pH=6.0PBSFig.6 CVs of DA and UA mixture with controlled concentration of UA(A)and DA(B)at activated Co-CNTs/GCE in pH 6PBS 图7为同时含有DA+UA(10.0μmol/L,30.0μmol/L,50.0μmol/L,70.0μmol/L,100.0μmol/L)的PBS(0.1mol/L,pH=6.0)的溶液中的循环伏安曲线,由图可以看出两者在浓度相同时相互之间几乎没有干扰.为了提高分析的灵敏度利用微分脉冲伏安法(DPV),以DA,UA的氧化峰电流对其线性范围与检出限进行测定如图7所示,由图6内插图可以看出DA的峰电流与其浓度在0.50-120μmol/L范围内符合线性关系,通过线性拟合处理的直线方程为:Ip(μA)=-5.858-0.153 c(μmol/L),线性相关系数为0.9922,由线性回归方程得出DA的检出限为0.24μmol/L.实验结果还发现,本线性关系与DA单独存在时的线性响应基本一致,据此得出一定量UA的存在并不影响DA的线性检测.同样可得UA的峰电流与其浓度在2.4-160μmol/L范围内符合线性关系,线性拟合得到的直线方程为:Ip(μA)=-1.277-0.088 c(μmol/L),线性相关系数为0.9919,由线性回归方程得出UA的检出限为1.0μmol/L.同样实验也表明,该线性范围与UA单独存在时并无明显差异,据此也可得出一定量DA的存在并不影响UA的线性检测.进一步证明了图7activated Co-CNTs/GCE修饰的玻碳电极能同时测定DA,UA的可能性.李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸YYSZXB31图7 相同浓度DA,UA共存时activated Co-CNTs/GCE电极的循环伏安曲线和DPV曲线Fig.7 CVs and DPV of DA and UA with equal concentration at activated Co-CNTs/GCE3.7 AA存在下DA,UA的同时测定 图8(A)为在AA存在下,同样浓度的DA,UA在activated Co-CNTs/GCE电极上的循环伏安曲线,从图可以看出AA的存在对DA,UA的检测几乎没有影响,与没有AA存在下的图7相似,由此可以得出DA,UA的测定几乎不受AA存在的影响.该电极能够很好的在AA存在下同时测定DA和UA.为了验证上述结论的正确性,采用微分脉冲伏安法(DPV)来测定,如图8(B)所示的曲线看出110倍的AA存在使得UA的氧化峰电流有所降低(RSD=5.4%),DA的氧化峰电流变化不大(与图7相比),但两者仍能很好的测定出来,由此可得出上述结论几乎是正确的,且由图8(B)内插图依然可以看出DA,UA的峰电流与其各自的浓度均符合线性关系.图8 (A)AA存在下DA,UA同时测定activated Co-CNTs/GCE电极的CV和DPV曲线Fig.8 CVs and DPV of DA and UA in the presence of AA3.8 干扰实验 在最佳测定条件下,研究其它干扰物对DA、UA测定的影响.实验结果表明,100倍的Cl-、K+、NO3-、Mg2+、Zn2+、Na+、对混合物的测定不干扰,100倍的双氧水、抗坏血酸、1000倍的葡萄糖均无干扰,由此可以看出该修饰电极抗干扰能力强,选择性好,可以用于DA、UA的同时测定.3.9 稳定性和重现性 在优化条件下,考察activated Co-CNTs/GCE的重现性和稳定性.将DA,UA,在同一支Co-CNTs/GCE上平行测定5次,其相对标准偏差(RSD)分别为2.6%,1.8%.这说明制备的电极具有较好的稳定性.用同样的方法分别制备了6支Co-CNTs/GCE,分别测定含有40μmol/L的DA,UA的混合溶液,RSD为3.7%,4.3%.这表明所制备的电极以及制备方法具有较好的重现性,能用于实际样品的测定.3.10 回收率和实际样品分析 为了验证该电极对样品测定的准确度和应用性,分别采用加标回收的方法对模拟样品和实际尿液进行了测定.实验结果表明,DA的回收率在96.6-102.4%之间,而UA的加标回收李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸YYSZXB32率在95.5-104.2%之间,表明该方法具有良好的准确性,能用于实际样品的测定.4 结论 采用电沉积钴于CNTs修饰电极后活化制备了activated Co-CNTs/GCE修饰电极,研究了该电极对DA,UA的电化学响应并能在同时测定时不相互干扰,研究表明该电极对DA,UA的氧化具有良好的催化作用,并能够有效消除抗坏血酸存在的干扰,线性范围宽、检出限低.在AA存在下的DA,UA共存体系中,该修饰电极能不受AA的干扰,同时测定出DA,UA.该电极抗干扰能力强、稳定性好,有望用于实际样品的测定.[参考文献][1]Finchce,Cohen D M.Aging,Metabolism and Alzheimer dis-ease:review and hypotheses[J].Exp Neurol,1997,143(1):82-102.[2]A.Niaz,J.Fischer,J.Barek,B.Yosypchuk,Sirajuddin,M.I.Bhanger,Voltammetric Determination of 4-NitrophenolUsing a Novel Type of Silver Amalgam Paste Electrode[J].Elec-troanalysis 2009,21:1786-1791.[3]W.Huang,C.Yang,S.Zhang,Simultaneous determinationof 2-nitrophenol and 4-nitrophenol based on themulti-wallcarbon nanotubes Nafion-modified electrode[J].Anal.Bioanal.Chem.2003,375:703-707.[4]Liu CY,Liu ZY,Peng R,Zhong ZC,Quasireversible Processof Dopamine on Copper-Nickel Hydroxide Composite/NitrogenDoped Graphene/Nafion Modified GCE and Its Electrochemical Ap-plication[J].J Anal Methods in Chemistry,2014,724538.[5]CY Liu,JM Hu,Electrocatalytic Oxidation of Dopamineat a Nanocuprous Oxide-Methylene Blue Composite Glassy Car-bon Electrode[J].Electroanalysis,2006,3:478-484[6]A.J.Bard,L.R.Faulkner,Electrochemical Methods,Fun-damentals and Applications[M].Wiley,New York,USA,2001,222.[7]Laviron,E.,General expression of the linear potential sweepvoltammogram in the case of diffusionless electrochemical systems[J].J.Electroanal.Chem.1979,101:19-28.【编校:胡军福】Simultaneous Determination of Dopamine and Uric Acid at Electrodeposited CobaltOxide-carbon Nanotubes Modified Electrode in the Presence of Ascorbic AcidLI Zhu-ye1,ZHANG-Ping1,LIU Chuan-yin1,2(1.College of Chemical Engineering and Food Science,Hubei University of Arts and Science,Xiangyang 441053;China;2.Hubei Key Laboratory of Low Dimensional Materials and Devices,Xiangyang 441053,China)Abstract:Cobalt oxide was modified onto the surface of carbon nanotubes modified GCE by cyclic voltammetricalmethod and the electrochemical response of DA and UA were investigated on the proposed electrode.It indicates that DAand UA shows favorable electrochemical response in pH 6PBS respectively,and the electro-separation of peak for the e-lectro-oxidation of DA and UA with peak separation of 124mV,which can be used to simultaneous determination of DAand UA.The results also show that the simultaneous determination of DA and UA can also be processed in the presenceof ascorbic acid with favorable reproduction and accuracy and has been used to determinate DA and UA in simulated andreal samples with satisfactory results.Key words:dopamine;uric acid;ascorbic acid;electro-deposited Co-CNTs modified electrode李珠叶,张 萍,刘传银:碳纳米管-电沉积Co修饰电极在抗坏血酸存在下同时测定多巴胺和尿酸YYSZXB33。


电化学传感器在尿酸检测中的应用电化学传感器在尿酸检测中的应用尿酸被认为是衡量血清尿酸水平的最佳指标,有助于预防和控制痛风。
由于尿酸检测技术的进步,尿酸检测在健康管理和病理诊断中变得越来越重要。
电化学传感器不仅具有分析速度快,简便,成本低廉,能够在现场测量和监控的优点,而且具有非常敏感的测量性能,在医疗诊断和环境监测领域被广泛使用。
本文重点介绍电化学传感器用于尿酸检测的原理和应用,以及未来的发展前景。
一、电化学传感器在尿酸检测中的原理电化学传感器应用于尿酸检测的原理是,在电极表面沉积脂肪酸与尿酸的还原活性形成稳定的电极反应物,当尿酸和脂肪酸混合时,尿酸在电极表面还原,并且会产生电子,这会导致电极电位的变化,持续时间与尿酸含量成正比,以此来测量尿酸含量。
二、电化学传感器在尿酸检测中的应用由于电化学传感器的良好的可行性和易于操作,也是迅速,方便,稳定,准确,以及可以实现连续测量服务,因此,它已经被广泛应用于尿酸检测。
1. 尿酸快速测量快速检测尿酸是非常重要的,可以帮助人们及时发现疾病,减少病情恶化,改善患者的健康情况。
由于电化学传感器的敏感性,速度快,可以快速准确地检测尿酸,不需要额外的装置,便于现场测量和监控,大大缩短了尿酸检测的时间,满足了患者对快速检测结果的需求。
2. 尿酸连续监测由于尿酸检测的一次性,常规的检测方式只能检测出一次性尿酸浓度,而不能监测血清尿酸的变化趋势。
电化学传感器可以通过连续检测技术实现对尿酸的连续监测,能够有效地监测血清尿酸浓度的变化,从而及时发现尿酸水平异常的变化趋势,有效预防和控制痛风的发病。
三、电化学传感器用于尿酸检测的未来发展电化学传感器在即刻尿酸检测中取得了成功,但仍有一些挑战需要克服。
例如,提高传感器精度和稳定性,开发新型传感器技术,建立更高效的分析方法,开发小型化,低成本的传感器系统等。
未来,电化学传感器将在尿酸检测中发挥更大的作用,从而改善人们的健康情况。
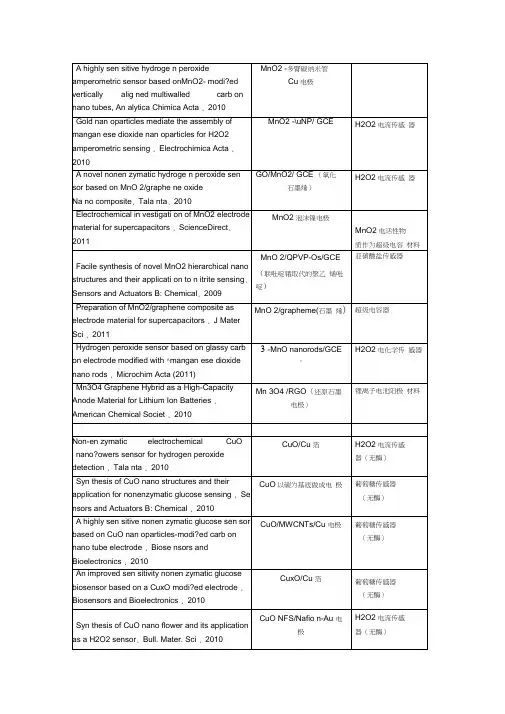
f-MWCNTs /GCESWCNH/GCE (单臂碳纳米管) graphe ne /GCEGR -CS/GCE,(石墨烯-壳聚糖)chitosan-graphene-GCE (壳聚糖-石墨烯) nano-Cu/PPy/GCE (聚吡咯) CPB/chitosan/GCE 溴化十六烷基吡啶 Chitosa n-CTAB /GCE亚硝酸盐MnO2/QPVP-Os/GCE (联吡啶锇取代的 聚乙烯吡啶) nano-Au/Ch/GCE (氯化胆碱)CR-GO/GCE (还原型氧化石墨烯) Nano-AI2O3 /GCEDAB /GCE (双十二烷基溴化铵) 对乙酰氨基酚 f-MWCNTs /GCE MWNT or SWNT/EPPGMWCNTs:graphite/GCE 多臂碳纳米管和石墨混合 Carbon nano tubes paste electrodes 碳纳米管糊电极 graphene /GCE (石墨烯)PAMAMPAMAM/Fe3O4 /GCE PAMAM/CoTe /GCE纳米AI2O3,对有机磷分子有较好的氧化还原活性。
其氮原子上一对孤对电子易于从溶液中结合一个氢质子•。
人们充分利用生物高分子壳聚糖的生物相容性、低 不断开发它的应用领域。
在分析化学上,己用于分离富Kazunori 等用壳聚糖修饰电极测定 北京大学叶宪曾研究组曾用壳聚糖修饰玻Au (lll ),Ag (l ),Pt (ll )和 Pd (ll )。
尿酸和乙酰氨基酚对葡萄糖检测的干扰。
多巴胺花状 ZnO/GCE多巴胺传感器同时检测多巴胺和对乙酰氨基酚 同时检测尿酸、多巴胺和抗坏血酸 抗坏血酸存在下检测多巴胺 抗坏血酸存在下检测多巴胺 同时检测抗坏血酸、多巴胺、尿酸 同时测定多巴胺和尿酸 同时检测多巴胺和抗坏血酸 同时检测多巴胺和抗坏血酸亚硝酸盐传感器 亚硝酸盐传感器亚硝酸盐传感器 对亚硝酸盐的检测检测水样中的亚硝酸盐同时检测多巴胺和对乙酰氨基酚 测定对乙酰基氨基酚 对乙酰氨基酚(扑热息痛) 对乙酰氨基酚对乙酰氨基酚的检测,不受多巴 胺和抗坏血酸的干扰测定牛奶中的双酚 A 测定水中的双酚A壳聚糖分子链上有许多游离的氨基, 而使壳聚糖成为带正电荷的聚电解质 毒性、生物可降解性以及可食用性, 集痕量Ni (ll ) , Cu (ll ) , Cd (ll )。

金属纳米团簇在电化学领域的应用研究进展高小惠;陈卫【摘要】尺寸小于2 nm的金属纳米团簇是由几个到几百个原子组成的纳米结构材料.对于金属纳米团簇,由于其大部分甚至所有金属原子可能暴露于表面而具有高的表面原子比例,该独特的原子堆积结构使其具有高的表面活性,因此其在催化反应中具有重要应用价值.同时,其明确的原子排列和堆积结构使其可作为模型催化剂,用于研究纳米结构-性能之间的关系.笔者简要总结了近年来金属纳米团簇的研究进展和现状,重点总结了其在电化学领域的应用,包括电催化和电化学传感,最后对其未来在电催化和电分析领域的应用前景进行了展望.%Metal nanoclusters with core size less than 2 nm are a kind of nanostructured materials consisting of several to a few hundred of atoms.For metal nanoclusters,due to the high surface-to-volume ratio resulting from the exposure of most of or even all metal atoms, they usually show excellent catalytic activities and therefore have promising applications in catalysis fields.Meanwhile, because of the clear atomic arrangement structure, metal nanoclusters can be used as model catalysts to study the relationship between structure and property of nanostructure.In this review article,the authors highlight the development of metal nanoclusters in recent years and mainly focus on their applications in electrochemical fields including the electrocatalysis and electrochemical sensors.Finally,the authors give an outlook on the application of metal nanoclusters in electrocatalysis and electroanalysis.【期刊名称】《安徽大学学报(自然科学版)》【年(卷),期】2017(041)006【总页数】8页(P30-37)【关键词】金属纳米团簇;纳米粒子;电催化;电化学;电化学传感【作者】高小惠;陈卫【作者单位】中国科学院长春应用化学研究所电分析化学国家重点实验室,吉林长春 130022;中国科学院大学化学与化工学院,北京 100049;中国科学院长春应用化学研究所电分析化学国家重点实验室,吉林长春 130022【正文语种】中文【中图分类】O646;O614.12金属纳米团簇由于具有高的尺寸单分散性、明确的组成和结构及大量暴露的活性位点,不仅为深入理解催化活性和结构的关系提供了理想的催化剂模型,同时也作为一种高经济效益的催化材料而具有实际应用价值.二十世纪七十年代,研究者发现极细金属雏晶的价带结构可能不同于本体金属和较大金属纳米粒子,以致金属粒子表面热动力学发生变化,从而产生不同的催化活性和物理性质[1].随后,Brust等[2-3]提出了合成单层硫醇配体保护金纳米粒子的两相和单相法(即BrustSchiffrin 方法),为金属纳米团簇提供了一种简便有效的尺寸可控制备方法,大大促进了其后续的发展.通过对该方法进行改进,Jin课题组[4]合成、表征和研究了多种原子尺度上结构精确的金纳米团簇,并完成了一些特定尺寸的金属纳米团簇的单晶结构解析,如Au20,Au25, Au38,Au144.与此同时,国内外的其他实验小组也相继报道了各类过渡金属纳米簇的合成和性能研究,包括铂、钯、银、铜和合金等[5]. 伴随合成和表征取得的重大进步,金属纳米团簇的应用开始受到广泛关注.利用其分立能级产生的荧光,该纳米材料被广泛应用于金属离子和生物分子的高灵敏和高选择性传感、检测,如强荧光金、银纳米团簇对氰根离子的响应,蛋白质包裹金纳米簇对汞离子的快速检测和低聚核苷酸保护银纳米团簇与DNA高选择性配对等[5].若将金属纳米团簇的荧光性质与其良好的生物兼容性、低毒性相结合,金属纳米簇还可用于生物标记、成像、诊断、治疗和药物传递等[6].除了荧光性能,人们发现基于其特有的可调控的表面结构和电子结构,金属纳米簇在催化反应中具有不同寻常的高活性和高选择性.例如,相对于较大金纳米粒子所要求的100 ℃高温催化条件,反相胶束包覆的金纳米簇可在室温下完成炔烃加氢催化[7].而在4-硝基苯甲醛加氢转化成4-硝基苯甲醇反应中,不同尺寸金纳米簇表现出了不同的催化活性和选择性,其中Au38获得了最高转化率[8].对于二氧化钛负载金纳米簇催化一氧化碳氧化反应,密度泛函理论和实验都证明了该反应只在界面金属位点上发生[9-10].电化学催化作为催化领域的一个重要研究体系,金属纳米团簇的电化学性能及其在电化学,特别是电催化领域中的潜在应用已引起人们的极大兴趣.笔者将对近年来金属纳米团簇在电化学领域(包括电催化和电化学传感)的研究进展进行简要综述.众所周知,为了满足实际应用的需求,燃料电池的阴极氧还原和阳极燃料分子氧化反应需要有效的催化剂才能达到特定的电流密度和输出电压.与铂族金属高的电催化活性相比,本体金由于较差的催化性能而在电催化领域很少受到关注.然而,当金催化剂尺寸下降到纳米量级时,其不同的能级结构和表面活性使其催化性能发生了显著改变.2009年,Chen等[11]研究了一系列尺寸不同的金纳米团簇在碱性溶液中对氧还原反应的催化性能,并评价了氧还原反应中金纳米团簇的尺寸效应(Au11, Au25, Au55, Au140).如图1所示,在0.1 M KOH中,不同尺寸的金纳米团簇在氧还原反应中给出了不同的线性扫描曲线和极化曲线[11].其尺寸相关效应表现在以下两个方面:1) 整体极限电流密度和表观动力学极限电流密度随着尺寸的增加而降低,即Au11 > Au25 ≈ Au55 > Au140; 2) 氧还原起始电位随着纳米簇尺寸的增加而负移,Au11(-0.10 V)> Au25 (-0.16 V)≈Au55 (-0.20 V)> Au140(-0.25 V).另外,根据KouteckyLevich方程的线性回归结果,除了较大尺寸的Au140外,其他较小的金纳米簇在实验条件下都给出了4电子的氧还原动力学参数,如表1所示[11].该研究结果表明,与本体金不同,纳米尺度的金团簇对氧还原具有较高的电催化活性,可作为一种有效的燃料电池阴极催化剂.在另一项工作中,Phani课题组[12]利用溴化十六烷基三甲基铵辅助电沉积方法制备了金原子簇,并研究了其在酸性溶液中对氧还原的电催化活性.线性扫描伏安曲线表明金纳米团簇产生的氧还原电流密度是本体金电极的两倍,表明金纳米簇对氧还原具有直接的4电子反应路径.结合其相对于标准氢电极0.025 V的半波电位,该研究显示合成的金纳米团簇具有高的氧还原电催化活性.而在2014年,陈卫课题组[13]报道了Au25纳米团簇带电状态对其氧还原催化活性的影响.该研究结果发现带负电荷的纳米团簇表现出最正的氧还原起始电位和最大的电流密度.根据其两电子氧还原过程,负电荷金纳米团簇修饰电极上的最高过氧化氢产率高达86%,可作为氧还原制过氧化氢的高效电催化剂.近年来,基于金纳米团簇构建的复合材料在电催化领域也取得了一定的研究进展.例如,Uosaki课题组[14]的相关研究表明,在酸性溶液中,不同于本体金电极,金纳米簇沉积的硼掺杂金刚石(GNC/BDD)电极给出了4电子的电催化氧气还原过程.而在没有表面保护剂和还原剂的条件下,唐智勇教授等[15]研究了金纳米簇与石墨烯复合材料对氧还原的催化性能.结果表明,相对于商业铂/碳催化剂、石墨烯片、较大金纳米粒子/石墨烯复合材料和单独硫醇保护的金纳米簇,无表面活性剂保护的金纳米簇/石墨烯复合材料对氧还原反应表现出更正的起始还原电位(-0.10 V),更大的极限电流密度(4.11 mA·cm-2)和高的抗甲醇毒化能力.这些优异的氧还原电催化性能可归结于金纳米簇极小的尺寸、表面活性剂的缺失,以及金纳米簇与石墨烯之间的协同效应.随后,其他课题组也相继报道了不同金纳米簇与石墨烯复合材料在催化氧还原反应中的应用[16-18].除了作为电催化剂外,人们发现金纳米簇可与商业铂/碳催化剂复合,从而提高铂/碳催化剂在催化氧还原反应中的稳定性[19].如图2所示,与单独商业铂/碳不同,沉积金纳米簇的商业铂/碳在研究的电势范围内进行30 000圈的循环伏安耐受性测试之后,其活性和表面积并没有发生明显的变化[19].这表明修饰的金纳米簇对铂纳米粒子能够起到很好的稳定作用,从而避免其在长时间工作中的溶解和活性下降.同时,原位X射线吸收近边光谱和电化学循环伏安机制研究进一步解释了金纳米团簇通过提高铂的氧化电势来增加复合材料的电化学稳定性.图2B中氢吸脱附区没有明显变化,表明铂的活性面积不变;图2D中阴影部分给出了氢吸脱附区的变化,表明铂的活性面积降低.随着对金纳米团簇研究的深入,研究者们希望把金属纳米团簇的研究扩展到其他过渡金属.众所周知,铂族纳米材料具有优异的电催化性能,因此,对铂族金属纳米团簇的制备和催化性能研究具有重要价值.Jin课题组[20]报道,硫醇保护的钯纳米簇在碱性溶液中对氧还原反应的起始电位仅为 -0.09 V,同时,其在空气中表现出了良好的稳定性.进一步研究表明,如果除去钯纳米簇的表面配体,表面洁净的钯纳米簇的氧还原起始电位将进一步提高,可正移至-0.02 V,且具有比商业铂/碳更高的质量活性.该研究结果表明,无配体保护的钯纳米簇可暴露更多的表面催化活性位点,从而大大提高其在催化反应中的电子传递和物质传输速率.在另外一项研究中,中科院长春应化所廖伍平和陈卫团队[21]利用三棱柱有机金属配位笼限域合成了超细的铂纳米簇,其可作为氢析出反应的高效电催化剂.研究结果显示,所合成的金属配位笼限域铂纳米簇的氢析出起始还原电位与铂/碳催化剂相当,但是在-0.40、-0.48、-0.53和-0.60 V电位下的氢析出电流密度分别为商业铂/碳的1.1、1.38、1.6和2倍.该研究表明,限域铂纳米簇具有比商业铂/碳更高的电催化性能.另外,据文献报道[22-23],镍基材料是一种具有应用前景的氧溢出催化剂.据此,研究者将原子级别结构精确的镍纳米团簇负载于炭黑上,并应用于氧溢出催化反应,发现其性能超越NiO和铂,并与铱金属相当[24].密度泛函理论表明,在反应过程中,吸附物种成键构象的微小变化可能会改变反应的决速步骤.该工作的重要性在于为实验和理论研究提供了直接的桥梁.作为金的同族金属,银纳米团簇的电化学应用近年来也受到了关注.笔者利用2,3二巯基丁二酸作为配体,合成了尺寸约为0.7 nm 的Ag7纳米团簇.电化学氧还原实验结果表明,该银纳米簇相对于较大的银纳米粒子,对氧还原反应具有更正的起始还原电位(正移150 mV)和更大的极限电流密度.该实验结果表明,银纳米簇与金纳米簇具有类似的尺寸相关电催化效应[25].随后,笔者课题组研究了无表面活性剂保护的银纳米簇与碳量子点复合物对氧还原反应的电催化活性.研究结果显示,该复合物具有与铂/碳催化剂相当的氧还原电催化活性,但具有比铂/碳更好的抗甲醇毒化能力,进一步表明银簇可能成为一种潜在的非铂电催化剂[26].在另外一项研究中,利用石墨烯作为载体,Jin等[27]报道了银纳米簇不仅具有良好的催化活性和抗毒化能力,同时在氧气饱和0.1 M KOH中给出了优异的电化学稳定性.除了金、银纳米团簇外,铜纳米簇在氧还原反应中也给出-0.07 V的较正的起始还原电位,与前面报道的Au11以及某些铂基催化剂相当[28].同样,类似于金、银纳米簇的尺寸效应,已有研究发现较小尺寸铜纳米团簇具有较高的氧还原催化性能.但是,值得注意的是,目前报道的铜纳米团簇电催化氧还原主要是通过两电子反应进行,有利于过氧化氢的产生[29].对环境和生物体系中金属离子和小分子的分析检测对于人类的生存和发展至关重要.在众多分析技术中,电化学技术由于具有操作简单,检测灵敏度和选择性高,易于现场、实时和原位检测而受到人们的青睐.近年来,由于金属纳米团簇具有高的电化学活性而被用作电化学传感材料.下面将从生物小分子和金属离子检测两个方面总结金属纳米簇在构建电化学传感器方面的研究进展.通过将谷胱甘肽保护的Au25纳米簇固定在溶胶凝胶内,Lee课题组[30]报道了一种检测抗坏血酸和多巴胺的双功能电流传感器.如图3所示[30],在0.1 M KCl中,随着待测物浓度的增加,循环伏安曲线的峰电流密度明显增加,并且在0.71~44.4 μM的浓度范围内给出了线性回归曲线.对于抗坏血酸和多巴胺,检测下限分别为0.31和0.35 μM.值得一提的是,在该传感器中,对抗坏血酸的催化氧化是不可逆的,而多巴胺的氧化反应却是可逆的.进一步研究认为,在溶胶凝胶膜中,Au25以负电荷的形式存在.当在电化学体系中经过正向电位扫描后,Au25被氧化,从而具有中性电荷.形成的中性电荷Au25可以氧化溶液中的待测组分,而Au25本身被还原回原有的负电荷形式.该反应过程产生的还原电流与待测组分浓度之间具有线性关系.同样,利用Au25纳米簇,朱俊杰教授课题组[31]发现在存在下,修饰在ITO上用蛋白质保护的金纳米簇的电化学发光能够对多巴胺产生高灵敏和高选择性的快速响应,从而实现对多巴胺的电化学发光分析.另外,采用多酶标记碳空心纳米链作为信号放大剂,聚多巴胺保护的金纳米簇功能化电化学免疫传感器可用于检测溴化火焰阻燃剂[32].同时,利用核酸外切酶进行放大,石墨烯稳定的金纳米簇则提供了一个超灵敏的传感平台,可用于HIV基因检测,其检测限为30 aM[33].由于不同配体保护的金属纳米簇以及不同尺寸的金属纳米簇具有不同的物理化学性质,笔者课题组利用铜纳米簇构建了针对不同分析物的传感平台.首先,利用水溶性谷胱甘肽作为配体,负载在二氧化钛上的Cu6(SG)3成功地用于葡萄糖电化学传感.由实验得到葡萄糖浓度(c)与响应电流(J)之间的线性校准方程在4.07 μM~20 mM浓度范围内可以表达为:J = 0.015 1× c + 0.014 5[34].随后,采用可溶于有机和水相的对巯基苯甲酸作为配体,合成了Cu7为主的纳米簇,该团簇可用于对肼进行高敏感和高选择性的电化学检测.其响应电位和检测限分别为0.25 V和1.04 μM,检测性能优于文献中报道的银、铂、钯贵金属材料[35].最近,笔者用苯并恶唑作为有机配体,合成了Cu6(C7H4NOS)6纳米团簇[34].如图4所示[34],该铜纳米团簇修饰的玻碳电极在0.1 M磷酸缓冲液中不仅表现了对过氧化氢的良好传感性能,且对葡萄糖、多巴胺、维生素C、尿酸和NaCl等潜在物质具有明显的抗干扰性.根据i-t曲线,在1.8×10-6 ~15×10-6 M范围内浓度电流具有线性关系,检测下限为1.8 ×10-6 M.金属纳米簇的电化学发光可用于金属离子的电化学检测.例如,利用三乙胺作为共反应试剂,Fang等[36]报道了蛋白质保护的Au25的电化学发光,并证实其在半胱氨酸的掩蔽下可用于Pb2+检测.电化学发光响应信号与金属离子浓度之间呈对数关系.进一步研究表明其发光机制主要是基于胺的氧化,而不是荧光物种.根据上述总结,由于具有高的表面活性,金属纳米簇在电化学催化和传感领域具有巨大应用潜力.但是,就电催化而言,目前对金属纳米簇的研究主要集中于阴极氧还原反应,而对其他阴极反应或者阳极反应,如甲醇、甲酸氧化,二氧化碳还原等报道较少.因此,金属纳米簇在电化学领域的应用仍有很大的开拓空间.另外,由于金属纳米簇具有极小的尺寸,因此在电化学体系中容易被氧化,或者聚集和坍塌而导致活性降低,故其电化学稳定性需要进一步提高,这也是金属纳米簇应用于电化学领域的一大挑战.显而易见,对于电化学传感而言,目前所能检测的物质仅仅局限于某些特定物种,特别是对金属离子的报道较少.因此,通过调控金属纳米团簇结构和性能,如改变尺寸或者表面配体,进一步扩展金属纳米簇可检测对象范围、提高检测灵敏度和选择性、降低检测限等将大大促进金属纳米团簇在电化学传感领域的应用和金属纳米簇的进一步发展.【相关文献】[1] ROSS P N, KINOSHITA K, STONEHART P.The valence band structure of highly dispersed platinum[J].J Catal, 1974, 32 (1): 163-165.[2] BRUST M, WALKER M, BETHELL D, et al.Synthesis of thiol-derivatised gold nanoparticles in a two-phase Liquid-Liquid system[J].J Chem Soc, Chem Commun, 1994 (7): 801-802.[3] BRUST M, FINK J, BETHELL D, et al.Synthesis and reactions of functionalized gold nanoparticles[J].J Chem Soc, Chem Commun, 1995 (16): 1655-1656.[4] JIN R C.Atomically precise metal nanoclusters: stable sizes and opticalproperties[J].Nanoscale, 2015, 7 (5): 1549-1565.[5] LU Y Z, CHEN W.Sub-nanometre sized metal clusters: from synthetic challenges to the unique property discoveries[J].Chem Soc Rev, 2012, 41 (9): 3594-3623.[6] SONG X R, GOSWAMI N, YANG H H, et al.Functionalization of metal nanoclusters for biomedical applications[J].Analyst, 2016, 141 (11): 3126-3140.[7] LEE L C, ZHAO Y.Room temperature hydroamination of alkynes catalyzed by gold clusters in interfacially cross-linked reverse micelles[J].ACS Catal, 2014, 4 (2): 688-691. [8] LI G, JIANG D E, KUMAR S, et al.Size dependence of atomically precise gold nanoclusters in chemoselective hydrogenation and active site structure[J].ACS Catal, 2014, 4 (8): 2463-2469.[9] VILHELMSEN L B, HAMMER B.Identification of the catalytic site at the interface perimeter of Au clusters on rutile TiO2(110)[J].ACS Catal, 2014, 4 (6): 1626-1631.[10] NIE X T, QIAN H F, GE Q J, et al.CO oxidation catalyzed by oxide-supportedAu25(SR)18 nanoclusters and identification of perimeter sites as active centers[J].ACS Nano, 2012, 6 (7): 6014-6022.[11] CHEN W, CHEN S W.Oxygen electroreduction catalyzed by gold nanoclusters: strong core size effects[J].Angew Chem Int Edit, 2009, 48 (24): 4386-4389.[12] JEYABHARATHI C, KUMAR S S, KIRUTHIKA G V M, et al.Aqueous CTAB-assisted electrodeposition of gold atomic clusters and their oxygen reduction electrocatalytic activity in acid solutions[J].Angew Chem Int Edit, 2010, 49 (16): 2925-2928.[13] LU Y Z, JIANG Y Y, GAO X H, et al.Charge state-dependent catalytic activity of[Au25(SC12H25)18] nanoclusters for the two-electron reduction of dioxygen to hydrogen peroxide[J].Chem Commun, 2014, 50 (62): 8464-8467.[14] YAGI I, ISHIDA T, UOSAKI K.Electrocatalytic reduction of oxygen to water at Au nanoclusters vacuum-evaporated on boron-doped diamond in acidicsolution[J].Electrochem Commun, 2004, 6 (8): 773-779.[15] YIN H J, TANG H J, WANG D, et al.Facile synthesis of surfactant-free Aucluster/graphene hybrids for high-performance oxygen reduction reaction[J].ACS Nano, 2012, 6 (9): 8288-8297.[16] XU S J, WU P Y.Facile and green synthesis of a surfactant-free Au clusters/reduced graphene oxide composite as an efficient electrocatalyst for the oxygen reductionreaction[J].J Mater Chem A, 2014, 2 (33): 13682-13690.[17] WANG Q A, WANG L K, TANG Z H, et al.Oxygen reduction catalyzed by gold nanoclusters supported on carbon nanosheets[J].Nanoscale, 2016, 8 (12): 6629-6635. [18] KWAK K, AZAD U P, CHOI W, et al.Efficient oxygen reduction electrocatalysts based on gold nanocluster-graphene composites[J].Chemelectrochem, 2016, 3 (8): 1253-1260. [19] ZHANG J, SASAKI K, SUTTER E, et al.Stabilization of platinum oxygen-reduction electrocatalysts using gold clusters[J].Science, 2007, 315 (5809): 220-222.[20] ZHAO S, ZHANG H, HOUSE S D, et al.Ultrasmall palladium nanoclusters as effective catalyst for oxygen reduction reaction[J].Chemelectrochem, 2016, 3 (8): 1225-1229. [21] WANG S T, GAO X H, HANG X X, et al.Ultrafine Pt nanoclusters confined in a calixarene-based {Ni24} coordination cage for highefficient hydrogen evolutionreaction[J].J Am Chem Soc, 2016, 138 (50): 16236-16239.[22] FAZLE KIBRIA A K M, TARAFDAR S A.Electrochemical studies of a nickel-copper electrode for the oxygen evolution reaction (OER)[J].International Journal of Hydrogen Energy, 2002, 27(9): 879-884.[23] ZHAO Z, WU H, HE H, et al.Self-standing non-noble metal (Ni-Fe) oxide nanotube array anode catalysts with synergistic reactivity for high-performance water oxidation[J].J Mater Chem A, 2015 (3):7179-7186.[24] KAUFFMAN D R, ALFONSO D, TAFEN D, et al.Electrocatalytic oxygen evolution with an atomically precise nickel catalyst[J].ACS Catal, 2016, 6 (2): 1225-1234.[25] LU Y Z, CHEN W.Size effect of silver nanoclusters on their catalytic activity for oxygen electro-reduction[J].J Power Sources, 2012, 197: 107-110.[26] LIU M M, CHEN W.Green synthesis of silver nanoclusters supported on carbon nanodots: enhanced photoluminescence and high catalytic activity for oxygen reduction reaction[J].Nanoscale, 2013, 5 (24): 12558-12564.[27] JIN S, CHEN M, DONG H F, et al.Stable silver nanoclusters electrochemically deposited on nitrogen-doped graphene as efficient electrocatalyst for oxygen reduction reaction[J].J Power Sources, 2015, 274: 1173-1179.[28] WEI W T, LU Y Z, CHEN W, et al.One-pot synthesis, photoluminescence, and electrocatalytic properties of subnanometer-sized copper clusters[J].J Am Chem Soc, 2011, 133 (7): 2060-2063.[29] WEI W, CHEN W.Size-dependent catalytic activity of copper nanoclusters for oxygen electroreduction in alkaline solution[J].International Journal of Smart and Nano Materials, 2013, 4 (1): 62-71.[30] KUMAR S S, KWAK K, LEE D.Amperometric sensing based on glutathione protected Au-25 nanoparticles and their pH dependent electrocatalytic activity[J].Electroanal, 2011, 23 (9): 2116-2124.[31] LI L L, LIU H Y, SHEN Y Y, et al.Electrogenerated chemiluminescence of Au nanoclusters for the detection of dopamine[J].Anal Chem, 2011, 83 (3): 661-665. [32] LIN M H, LIU Y J, CHEN X F, et al.Poly(dopamine) coated gold nanocluster functionalized electrochemical immunosensor for brominated flame retardants using multienzyme-labeling carbon hollow nanochains as signal amplifiers[J].Biosens Bioelectron, 2013, 45 (15): 82-88.[33] WANG Y J, BAI X N, WEN W, et al.Ultrasensitive electrochemical biosensor for HIV gene detection based on graphene stabilized gold nanoclusters with exonuclease amplification[J].ACS Appl Mater Inter, 2015, 7 (33): 18872-18879.[34] GAO X H, LU Y Z, LIU M M, et al.Sub-nanometer sized Cu6(GSH)3 clusters: one-step synthesis and electrochemical detection of glucose[J].J Mater Chem C, 2015, 3 (16): 4050-4056.[35] GAO X, DU C, ZHANG C, et al.Copper nanoclusters on carbon supports for the electrochemical oxidation and detection of hydrazine[J].ChemElectroChem, 2016, 3 (8): 1266-1272.[36] FANG Y M, SONG J, LI J A, et al.Electrogenerated chemiluminescence from Au nanoclusters[J].Chem Commun, 2011, 47 (8): 2369-2371.。
![同时探测水溶液中抗坏血酸、多巴胺和尿酸的电化学传感器及其制备方法和电化学方法[发明专利]](https://uimg.taocdn.com/5dfe80e588eb172ded630b1c59eef8c75fbf95a6.webp)
专利名称:同时探测水溶液中抗坏血酸、多巴胺和尿酸的电化学传感器及其制备方法和电化学方法
专利类型:发明专利
发明人:陈喆,郭启闻,姚蕾,王戈明,邓泉荣,林志东,付萍
申请号:CN202111387123.1
申请日:20211122
公开号:CN114235915A
公开日:
20220325
专利内容由知识产权出版社提供
摘要:本发明属于电化学传感器技术领域,具体涉及一种同时探测水溶液中抗坏血酸、多巴胺和尿酸的电化学传感器及其制备方法和电化学方法。
电化学传感器的制备包括以下步骤:1)电极修饰液的制备:以β环糊精(CD)的用量就计,将0.9‑1.1gβ环糊精均匀分散于15ml0.4‑0.55mg·ml‑1的氧化石墨烯(GO)水溶液中,超声分散10‑15小时,得到氧化石墨烯与β环糊精的电极修饰液;2)修饰玻碳电极的制备:将18‑22μL的氧化石墨烯与β环糊精的电极修饰液滴涂至玻碳电极表面,红外线加热烤干,得到修饰玻碳电极。
以本发明得到的修饰玻碳电极作为工作电极,可以在低浓度的情况,识别水溶液中抗坏血酸、多巴胺和尿酸,检测限,灵敏度高。
申请人:武汉工程大学
地址:430000 湖北省武汉市东湖新技术开发区光谷一路206号
国籍:CN
代理机构:北京轻创知识产权代理有限公司
代理人:陈熙
更多信息请下载全文后查看。

电化学传感器用碳材料的制备及应用综述摘要:近年来电化学传感器由于对痕量物质检测敏感,被广泛应用于环境保护监测及医学检测等相关领域,由于碳材料具有成本低廉、检测灵敏度高、操作简单等优势,使其在电化学传器的制备过程脱颖而出。
本文综述了新型碳纳米材料、改性碳材料的制备及其修饰电极用作电化学传感器在痕量检测方面的作用。
关键词:传感器、改性、氮良好的导电、导热性,比表面积大是新型碳纳米材料具有的显著特征,使其能满足电化学传感器的性能需求,为了提高进一步碳纳米材料的电催化活性、稳定性、检测灵敏度等高性能电化学传感器需求,研究者采用不同类型的原子、分子等对碳材料进行掺杂,发现改性后的碳材料性能有明显的提升。
相比于传统化学的测定方法,成本低,操作简单,灵敏度高等优势成为改性碳材料修饰电极的一大特点。
目前关于改性碳材料的研究很多,普遍应用于一些环境或人体体液中微量物质含量的测定。
本文对新型碳纳米材料(碳纳米管、石墨烯和多孔碳)的制备方法,单独氮掺杂碳材料和复合材料掺杂碳材料的制备及其修饰电极作为电化学传感器在微量物质含量测定方面的应用进行详细的介绍。
1、改性碳材料在电化学传器的制备过程的应用应用于电化学传感器中的碳材料能够促进电子的移动和降低电化学氧化还原中的过电位作用[1]。
由于通过物理化学的方法对原型碳材料(新型碳纳米材料如碳纳米管、石墨烯、多孔碳等)进行改性掺杂其他类型的原子、分子等,使之提高电化学传感器的性能。
1.1碳纳米管碳纳米管具有高比表面积,良好的导电和机械性能,在电化学领域前景广阔。
碳纳米管的制备有两种方法:一是电弧放电、激光烧蚀法等热处理法,二是化学气相沉积法[2]。
电弧放电、激光烧蚀法是利用电弧放电或激光烧蚀将石墨加热到3000-4000℃,使碳原子挥发,从而生成碳纳米管[2]。
但热处理的方法制得的碳纳米管副产物较多,为了解决这个问题,在使用电弧法的过程中,Ebbesen[3]等人发现采用在空气中加热的方法可以除去副产物,制得纯的多壁碳纳米管。
流量传感测试方法综述摘要流量是工业控制与生产中的一个重要参数。
随着现代工业的飞速发展,流量测量的准确性要求越来越高,从而越来越多的测量方法和测量仪器涌现出来。
但是测量对象的复杂多样性,使得测量方法也带有了一定的针对性,并且仍有许多流量测量问题难以解决。
本文主要对现有的流量测量方法进行综述,同时对基于石墨烯材料的传感器在不同领域中发挥的作用进行综述,最后设想不同的组装器件将石墨烯材料用于流量传感中。
,关键词:1;流量2;流量计3;石墨烯4;传感器5;网状石墨烯6;丝状石墨烯-聚合物1引言:1.1流量计的意义计量是工业生产的眼睛。
流量计量是计量科学技术的组成部分之一,它与国民经济、国防建设、科学研究有密切的关系。
做好这一工作,对保证产品质量、提高生产效率、促进科学技术的发展都具有重要的作用,特别是在能源危机、工业生产自动化程度愈来愈高的当今时代,流量计在国民经济中的地位与作用更加明显。
在各种流体计量中,水量计量与我们的生活密切相关。
水资源是人类生产生活的最关键资源。
中国是一个干旱缺水严重的国家。
淡水资源总量为28000亿立方米,占全球水资源的6%,居世界第四位,但人均只有2200立方米,仅为世界平均水平的1/4,是全球13个人均水资源最贫乏的国家之一。
所以只有准确的计量水流量,才能更加快捷、准确、合理的调配水资源。
水表是测量水流量的仪器,但现在现有水表中,存在许多问题。
例如涡轮流量计的涡轮会因为水垢而变得不灵敏;多数流量计经长时间使用后,灵敏度急剧下降,造成水资源浪费等等。
尤其在北方,水质普遍比较差,水表易生垢。
所以制作以新型材料为基础的流量计成为了解决问题的关键方法。
石墨烯作为一种新兴材料,其优异的物理性质有潜力成为这种传感器的核心部件。
石墨烯在室温下有极高的电子迁移率;超强的力学性能;超大的比表面积等等。
它已经在很多领域展示了其优秀的传感特性,所以我们也有理由相信在流量传感领域还有我们还未探索到的价值。
第49卷第7期2021年4月广州化工Guangzhou Chemical IndustryVol.49No.7Apr.2021LiFeP()4改性电极同时测定抗坏血酸、多巴胺和尿酸*梁亚鸣,袁红雁(四川大学化学工程学院,四川成都610065)摘要:将磷酸铁锂(LiFePO4>LFP)与石墨(G)混合后用于改性普通玻碳电极(GCE),制备出一种新型电化学传感器(LFP-G/GCE),利用锂离子的脱嵌加速电子转移,实现同时检测抗坏血酸(AA)、多巴胺(DA)和尿酸(UA)O通过循环伏安法(CV)和差分脉冲伏安法(DPV)研究了LFP-G/GCE对AA、DA和UA的电化学行为。
此外,LFP-G/GCE可用于检测人血清中的UA,计算出人血清中UA的初始浓度为375|xM o AA和DA的回收率也令人满意。
因此LFP材料的应用可以扩展到电化学传感领域。
关键词:磷酸铁锂;电化学传感器;抗坏血酸;多巴胺;尿酸中图分类号:TP212.2文献标志码:A文章编号:1001-9677(2021)07-0088-07LiFePO4Modified Electrode for Simultaneous Determination ofAscorbic Acid,Dopamineand Uric Acid*LIANG Ya-ming,YUAN Hong-yan(College of Chemical Engineering of Sichuan University,Sichuan Chengdu610065,China)Abstract:A new electrochemical sensor(LFP-G/GCE)was prepared by mixing lithium iron phosphate(LiFePO4, LFP)with graphite(G)to modify glassy carbon electrode(GCE),and utilizing intercalation and deintercalation of Li-ion of LFP accelerated the electron transfer,the LFP-G/GCE determination of ascorbic acid(AA),dopamine(DA)and uric acid(UA)simultaneously.The electrochemical behaviors of LFP-G/GCE toward AA,DA and UA were investigated by the methods of cyclic voltammetry(CV)and differential pulse voltammetry(DPV).Furthermore,LFP-G/GCE can be used to detect UA in human serum,the original concentration of UA in human serum was calculated as375|jl M.The recoveries of AA and DA in serum samples were also satisfactory.The application of the battery material LFP can be extended to the field of electrochemical sensing.Key words:lithium iron phosphate;electrochemical sensor;ascorbic acid;dopamine;uric acidLiFePO4(LFP)作为一种正极材料,具有低毒、低成本、循环能力强、安全性高等优势,自1997年报道以来被广泛研究并实现工业化生产⑴。
工程技术理论前沿2017年3月第29卷·307·
同时检测多巴胺,抗坏血酸和尿酸的石墨烯/贵金属纳米复合物基电化学传感器
徐小萌任俊鹏陆婉婷王成鑫王欢(指导老师)
吉林建筑大学材料科学与工程学院,吉林长春 130118
摘要:抗坏血酸(AA),多巴胺(DA)和尿酸(UA)是人类代谢过程中的重要化合物,是目前生物学和化学的研究热点之一。
AA,DA和UA含量的变化与人体的健康密切相关,当浓度偏离正常水平时导致一些疾病的发生,如帕金森症、精神分裂症、癫痫、亨廷顿氏舞蹈症、抑郁症、通风等。
最近,电化学传感器由于其良好的敏感性、选择性、分析周期短等特点,已经被广泛地应用到检测AA、DA和UA的含量当中。
但是空白电极上AA、DA和UA的氧化峰重叠导致三者的区分困难,而无法检测。
[1]。
关键词:石墨烯;抗坏血酸;贵金属纳米复合物
中图分类号:TP212 文献标识码:A 文章编号:1671-5586(2017)29-0307-01
迄今为止,大量的纳米催化材料用于修饰电极制备同时检测AA、DA和UA的电化学传感器,主要包括金属纳米材料、碳基材料、聚合物等[2]。
贵金属纳米传感器表现出优异的催化活性、稳定性好,但目前面临的问题是纳米尺寸的贵金属粒子在表面活性剂修饰时在化学势的作用下,会发生团聚,电化学活性的表面积会降低,传感器的灵敏度也会下降。
近年来,一些科研工作者将铂、金、钯等金属纳米粒子组装到碳基纳米材料上特别是石墨烯材料,不仅防止了金属纳米粒子之间的聚集,而且极大地增加了复合材料电活性的比表面积、降低了成本,且两者之间的协同作用和电子的转移,使得石墨烯/贵金属纳米复合物用于各种传感器中并取得不错的结果。
1 石墨烯/Au纳米粒子复合物传感器
迄今为止,很多的Au纳米粒子复合物广泛作为电极材料,用于同时检测AA,DA和UA,主要有石墨烯/ Au纳米复合材料、石墨烯/Fe3O4 @ Au复合材料、碳纳米管/ Au纳米复合材料和Au @ MoS2 核壳材料。
其中石墨烯/Au纳米复合材料,由于其独特的电子和催化性能,比单体材料更大的表面和更好的协同作用,得到了极大的关注。
Yan等人[3]利用简单的液相还原法制备了三维石墨烯凝胶/金纳米复合材料,并制作了同时检测AA、DA和UA的电化学传感器。
在最佳条件下,3DGH/AuNPs/GCE对AA,DA和UA的线性响应分别为1.0-700,0.2-30,1-60 µM,计算检测限为28 nM(AA),2.6 nM(DA)和5nM(UA),并且一些通常共存的物质(如赖氨酸,甘氨酸,葡萄糖,柠檬酸等)对传感器的干扰几乎可以忽略不计,选择性较好。
2 石墨烯/Pt纳米粒子复合物传感器
Pt基纳米催化剂的成本较高,且纳米尺寸下催化剂易聚集,基于此制备石墨烯/Pt纳米复合催化剂用于电催化是一种不错的选择。
Li等人[4]利用一步反应制备了石墨烯/Pt复合物,研究了石墨烯/Pt纳米粒子复合物传感器对抗坏血酸和多巴胺的电化学响应和催化行为,结果发现AA和DA氧化的两个峰值电位之间的差异超过200 mV,可以将AA和DA 完全区分开。
同时利用传感器对含有AA和DA的尿液进行了检测,结果表明,石墨烯/Pt纳米粒子复合材料将可能应用于临床使用中的AA和DA的常规分析。
3 石墨烯/Pd纳米粒子复合物传感器
商业上催化电极材料一般是贵金属Pt基材料,但是由于其成本问题,制约了传感器的商业发展。
一种方法是采用成本较低并且能替代Pt的金属,如Pd。
然而,与铂相比,钯具有低得多的活性,需要研究一种改进的Pd基催化剂的设计。
众多科学家为此做出了很多努力,一般通过改变Pd的形貌、纳米结构、或者使用载体等手段提高催化剂的催化性能。
例如,通过纳米Pd与石墨烯结合形成石墨烯/Pd催化剂,具有较高的电催化活性和稳定性。
Wang等人[5]基于石墨烯/立方体Pd纳米复合材料修饰玻璃碳电极制作了DA和UA电化学传感器,利用循环伏安法和差分脉冲伏安法研究了电化学行为,发现新型石墨烯/立方体Pd纳米复合物传感器表现出良好的灵敏度,优异的选择性和出色的稳定性。
石墨烯/双金属纳米粒子复合物传感器。
4 石墨烯/双金属纳米复合物传感器
与单金属纳米颗粒相比,双金属纳米粒子可以保留各组分的功能特性,并通过相互协同效应,增加表面积,增强电催化能力,促进电子转移和提高生物相容性。
基于不同的合成策略,研究者制备了各种形貌结构如中空,异质,核壳,合金和孔隙的双金属纳米晶体。
近年来报道了石墨烯/双金属纳米粒子复合材料,在电分析和电催化中表现出良好的电化学性能。
Yan等人[6]通过一步还原乙二醇溶液合成石墨烯/Pd-Pt纳米复合材料,制备了电化学传感器,同时测定AA,DA和UA,并应用于人尿和血清样品中AA,DA和UA的检测,表现出比单一组分更高的催化活性。
5 结语
石墨烯/贵金属纳米复合物电化学传感器展现出较大的比表面积、较高的催化活性、较好的稳定性,并解决了催化剂成本偏高问题,在同时检测AA、DA和UA领域具有巨大的应用前景。
参考文献
[1]Ramesh P,Suresh G S,J.Electroanal.Chem,561,2004:173-180.
[2]Bao Y,Song J,Mao Y,et al.Electroanalysis,2011,23(4):878-884.
[3]Zhu Q,Bao J,Huo D,et al.Sensors and Actuators B,2017,238:1316-1323.
[4]Li F,Chai J,Yang H,et al.Talanta,2010,81(3):1063-1068.
[5]Wang J,Yang B,Zhong J,et al.Journal of Colloid and Interface Science,2017,497:172-180.
[6]Yan J,Liu S,Zhang Z,et al.Colloids and Surfaces B:Biointerfaces,2013,111(1):392- 397.
吉林省大学生创新创业项目(201610191016)资助
指导教师:王欢,吉林建筑大学材料科学与工程学院,讲师。