化学晶胞计算
- 格式:ppt
- 大小:1.77 MB
- 文档页数:32

1.“均摊法”确定晶体的化学式
(1)原则:晶胞任意位置上的一个粒子如果是被n个晶胞所共有,那么每个晶胞对这个粒子分得的份额就是1/n
①长方体(包括立方体)晶胞中不同位置的粒子数的计算
顶点:为8个晶胞共有,1/8属于该晶胞。
棱:为4个晶胞共有,1/4属于该晶胞。
面心:为2个晶胞共有,1/2属于该晶胞
体心:处于晶胞内部,全部属于该晶胞
②非长方体晶胞中粒子视具体情况而定。
如石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三个六边形共有,每个六边形占1/3;当晶胞为六棱柱时,其顶点上的粒子被6个晶胞共用,每个粒子属于该晶胞的部分为1/6,而不是1/8。
注意:审题时一定要注意是“分子结构”还是“晶体结构”,若是分子结构,其化学式由图中所有实际存在的原子个数决定,且原子个数可以不互质(即原子个数比可以不约简)。
2.晶体密度、晶胞体积和晶胞参数(晶胞边长)的求算
对于立方晶胞,可建立如下求算途径:。

晶胞摩尔体积计算公式晶胞摩尔体积计算公式是一个用来计算晶体原子数密度和晶体容积的公式。
许多科学家和工程师都熟悉这个公式,但它也有一些令人混淆的方面。
本文旨在介绍这种公式,以深入了解它的基本原理和应用。
晶胞摩尔体积的概念是由P.W. Anderson在1937年提出的,它是一种在晶体中表示原子数密度的方法,可以用于预测晶体容积。
它通过描述晶体中固定晶胞的体积来计算晶体的原子数密度。
具体来说,它的公式为:V=(N/4π) * (a/h)^3其中,V表示晶胞体积,N表示晶体中原子的数量,a表示晶体中原子半径,h表示晶体中晶胞间距。
在计算晶胞摩尔体积时,最重要的一点就是准确估算晶体原子的数量。
为了确定此值,最常用的方法是从晶体样品中提取一枚样本,然后使用X射线衍射原理来确定原子数。
计算晶胞摩尔体积时还需要正确确定晶体原子的半径。
关于这一值,能够提供有效的估算值的有效工具是无结构X射线衍射(USAXS)仪器。
另外,X射线吸收光谱(XAS)也可以用来推断晶体原子半径。
最后,晶胞摩尔体积的计算还需要正确确定晶体的晶胞间距。
在这一步中,X射线衍射也起到了相当重要的作用。
X射线衍射可以用来确定晶胞间距,以及晶体的物相。
综上所述,可以看出,晶胞摩尔体积计算公式是一个重要的工具,它可以用来正确估算晶体容积和原子数密度。
它所用的各种技术也可以应用于原子结构的研究,如确定原子半径和晶体的物相,从而更深入地了解晶体结构。
此外,晶胞摩尔体积计算公式可以用于实际工程中,例如在石油、化学和建筑领域中,它可以帮助研究人员更准确地计算物质的容积和重量以及晶体原子数密度,从而更好地控制生产活动。
综上所述,晶胞摩尔体积计算公式是一种重要的工具,它可以准确估算晶体容积和原子数密度。
它的使用需要对晶体原子的数量、半径和晶胞间距有一个准确的估计。
在实际工程中,这种公式有助于计算物质的容积和重量,从而更好地控制生产活动。
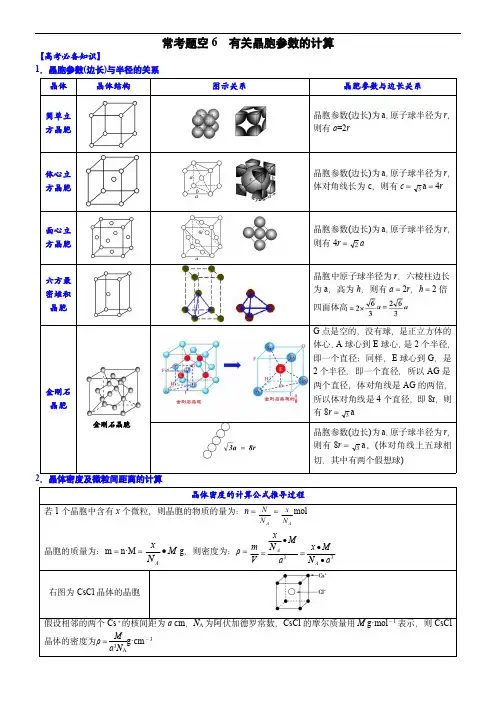
常考题空6有关晶胞参数的计算【高考必备知识】1.晶胞参数(边长)与半径的关系晶体晶体结构图示关系晶胞参数与边长关系简单立方晶胞晶胞参数(边长)为a ,原子球半径为r ,则有a =2r体心立方晶胞晶胞参数(边长)为a ,原子球半径为r ,体对角线长为c ,则有c =3a =4r面心立方晶胞晶胞参数(边长)为a ,原子球半径为r ,则有4r =2a六方最密堆积晶胞晶胞中原子球半径为r ,六棱柱边长为a ,高为h ,则有a =2r ,h =2倍四面体高金刚石晶胞金刚石晶胞G 点是空的,没有球,是正立方体的体心,A 球心到E 球心,是2个半径,即一个直径;同样,E 球心到G ,是2个半径,即一个直径,所以AG 是两个直径,体对角线是AG 的两倍,所以体对角线是4个直径,即8r ,则有8r =3a晶胞参数(边长)为a ,原子球半径为r ,则有8r =3a 。
(体对角线上五球相切,其中有两个假想球)2.晶体密度及微粒间距离的计算晶体密度的计算公式推导过程若1个晶胞中含有x 个微粒,则晶胞的物质的量为:n =AN N =AN x mol晶胞的质量为:m =n·M =M N x A g ,则密度为:ρ=33aN M x a MN xV m A A 右图为CsCl 晶体的晶胞假设相邻的两个Cs +的核间距为a cm ,N A 为阿伏加德罗常数,CsCl 的摩尔质量用M g·mol -1表示,则CsCl 晶体的密度为ρ=Ma 3N Ag·cm -33.金属晶体空间利用率的计算方法(1)空间利用率的定义及计算步骤①空间利用率(η):指构成晶体的原子、离子或分子总体积在整个晶体空间中所占有的体积百分比②%1003433a r V V 球数空间利用率晶胞球类型晶体结构示意图图示关系简单立方堆积原子的半径为r ,立方体的棱长为2r ,则V 球=43πr 3,V 晶胞=(2r )3=8r 3,空间利用率=V 球V 晶胞×100%=43πr 38r 3×100%=6 ≈52%体心立方晶胞原子的半径为r ,体对角线c 为4r ,面对角线b 为2a ,由(4r )2=a 2+b 2得a =43r 。

晶胞的计算一、晶胞在高考中的地位分析:2008、2009年新课标,未对晶胞的计算进行考查;2010年新课标:37(4),一空,化学式的计算;2011年新课标:37(5),三空,晶胞中原子个数及密度的计算;2012年新课标:37(6),两空,晶胞密度、离子距离的计算。
二、常见的晶胞计算题:第一类:金属堆积方式的简单计算(空间利用率和密度)[选三P76] 晶胞密度 =m(晶胞)/V(晶胞)空间利用率=[V(球总体积)/V(晶胞体积)]×100%【注】1m=10dm=102 cm=103 mm=106 um=109 nm=1012 pm①简单立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:②体心立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:③面心立方最密堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:再假设该金属的摩尔质量为Mg/mol,N A为阿伏伽德罗常数的数值,试计算该晶胞的密度:【总结】必须掌握的常见晶胞及晶体结构分子晶体:干冰、冰晶胞图形、晶胞组成特点;原子晶体:金刚石(晶体硅)、二氧化硅晶胞组成特点、边长(体积、密度、原子最近距离)的计算方式;金属晶体:四种堆积方式的名称、图形、代表金属、边长(体积、密度、原子最近距离)的计算方式;离子晶体:NaCl、CsCl、CaF2晶胞图形、晶胞组成、边长(体积、密度、原子最近距离)的计算方式。
【练习】中学化学教材中展示了NaCl晶体结构,它向三维空间延伸得到完美晶体。
NiO(氧化镍)晶体的结构与NaCl 相同,Ni2+与最临近O2-的核间距离为 a cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7 g/mol)。
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。
其结果为晶体仍呈电中性,但化合物中Ni 和O的比值却发生了变化。

晶胞的计算一、晶胞在高考中的地位分析:2008、2009年新课标,未对晶胞的计算进行考查;2010年新课标:37(4),一空,化学式的计算;2011年新课标:37(5),三空,晶胞中原子个数及密度的计算;2012年新课标:37(6),两空,晶胞密度、离子距离的计算。
二、常见的晶胞计算题:第一类:金属堆积方式的简单计算(空间利用率和密度)[选三P76]晶胞密度 =m(晶胞)/V(晶胞)空间利用率=[V(球总体积)/V(晶胞体积)]×100%【注】1m=10dm=102 cm=103 mm=106 um=109 nm=1012 pm①简单立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:②体心立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:③面心立方最密堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:再假设该金属的摩尔质量为Mg/mol,N A为阿伏伽德罗常数的数值,试计算该晶胞的密度:【总结】必须掌握的常见晶胞及晶体结构分子晶体:干冰、冰晶胞图形、晶胞组成特点;原子晶体:金刚石(晶体硅)、二氧化硅晶胞组成特点、边长(体积、密度、原子最近距离)的计算方式;金属晶体:四种堆积方式的名称、图形、代表金属、边长(体积、密度、原子最近距离)的计算方式;离子晶体:NaCl、CsCl、CaF2晶胞图形、晶胞组成、边长(体积、密度、原子最近距离)的计算方式。
【练习】中学化学教材中展示了NaCl晶体结构,它向三维空间延伸得到完美晶体。
NiO(氧化镍)晶体的结构与NaCl 相同,Ni2+与最临近O2-的核间距离为a cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7 g/mol)。
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。
其结果为晶体仍呈电中性,但化合物中Ni 和O的比值却发生了变化。


pm、nm、μm、mm、cm等之间的换算及读法现在重点记(化学晶胞计算用):1毫米(m m)=10丝米(dmm)1丝米(dmm)=10忽米(cmm)1忽米(cmm)=10微米(μm)1微米(μm)=1000纳米(nm)1纳米(n m)=1000皮米(pm)规律自上而下丝忽微纳皮3个10 两个千(1000)...以后记1:1毫米(m m)=10丝米(dmm)1丝米(dmm)=10忽米(cmm)1忽米(cmm)=10微米(μm)1微米(um)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(f m)=1000阿米(am)复习记1米(m)=10分米(dm)1分米(dm)=10厘米(cm)1厘米(cm)=10毫米(mm)1毫米(m m)=10丝米(dmm)1丝米(dmm)=10忽米(cmm)1忽米(cmm)=10微米(μm)1微米(um)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(f m)=1000阿米(am)1米(m)=10分米(dm)1分米(dm)=10厘米(cm)1厘米(cm)=10毫米(mm)1毫米(mm)=1000微米(μm)1微米(um)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(fm)=1000阿米(am)简记2 ........1厘米(cm)=10毫米(mm)1毫米(mm)=1000微米(um)1微米((μm)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(fm)=1000阿米(am)再说(下条较全).......1米(m)=10分米(dm)1分米(dm)=10厘米(cm)1厘米(cm)=10毫米(mm)1毫米(mm)=10丝米(dmm)1丝米(dmm)=10忽米(cmm)1忽米(cmm)=10微米(μm)1微米(μm)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(fm)=1000阿米(am)其他回答1米(m)=10分米(dm)=10^2厘米(cm)=10^3毫米(mm)=10^6微米(um)= 10^9纳米(nm)=10^10埃米(A)=10^12皮米(pm)傻蛋二35 |发布于2014-06-20 22:52举报|评论最佳答案1(m)=10(dm)=10^2(cm)=10^3(mm)=10^6(um)=10^9(nm)=10^10(A)=10^12(pm)举报|评论怎么倒换算xibeizi122 |浏览2349 次发布于2011-10-21 08:50最佳答案m,dm,=10^-1mcm,=10^-2mμm,=10^-6mnm,=10^-9mpm,=10^-12m埃=10^-10m=0.1纳米满意请采纳O(∩_∩)O~本回答由提问者推荐评论180氯金酸采纳率:84% 来自团队:数学百分百擅长:教育/科学化学理工学科其他回答1厘米(cm)=10毫米(mm)1毫米(mm)=1000微米(um)1微米((μm)=1000纳米(nm)1纳米(nm)=1000皮米(pm)1皮米(pm)=1000飞米(fm)1飞米(fm)=1000阿米(am)长度是国际单位制(SI)中的七个基本物理量的量纲之一,符号L。



晶胞的计算
化学晶胞计算公式:M=Na×N。
构成晶体的最基本的几何单元称为晶胞(Unit Cell),其形状、大小与空间格子的平行六面体单位相同,保留了整个晶格的所有特征。
晶胞是能完整反映晶体内部原子或离子在三维空间分布之化学-结构特征的平行六面体最小单元。
分子是由组成的原子按照一定的键合顺序和空间排列而结合在一起的整体,这种键合顺序和空间排列关系称为分子结构。
由于分子内原子间的相互作用,分子的物理和化学性质不仅取决于组成原子的种类和数目,更取决于分子的结构。
