晶胞结构及计算
- 格式:docx
- 大小:622.39 KB
- 文档页数:5

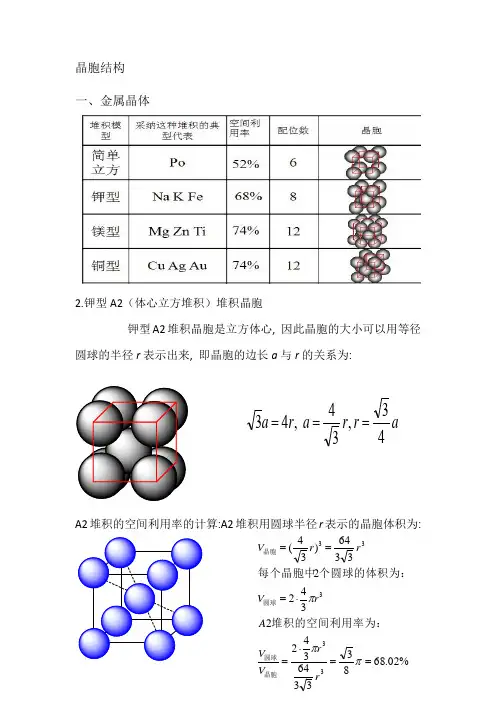
晶胞结构一、金属晶体2.钾型A2(体心立方堆积)堆积晶胞钾型A2堆积晶胞是立方体心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A2堆积的空间利用率的计算:A2堆积用圆球半径r 表示的晶胞体积为:ar r a r a 43,34 ,43===%02.68833364342234223364)34(33333==⋅=⋅===πππr r V V A rV rr V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中3.六方最密堆积(4)A1(面心立方最密堆积)A1是ABCABCABC······型式的堆积,从这种堆积中可以抽出一个立方面心点阵,因此这种堆积型式的最小单位是一个立方面心晶胞。
A1堆积晶胞是立方面心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A1堆积空间利用率的计算:A1堆积用圆球半径r 表示的晶胞体积为:(5)A4堆积形成晶胞A4堆积晶胞是立方面心点阵结构, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A4堆积的空间利用率的计算:A4堆积用圆球半径r 表示的晶胞体积为: ra r a 22 ,42==%05.742312163441344 4216)22(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中ar r a r r a 83,38 ,8243===⨯=%01.34163335123484348 833512)38(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中二、原子晶体1.金刚石立体网状结构,每个碳原子形成4个共价键,任意抽出2个共价键,每两个单键归两个六元环所有,而不是只归一个六元环所有(如图所示,红色的两个碳碳单键,可以构成蓝色和紫红色的两个六元环)。


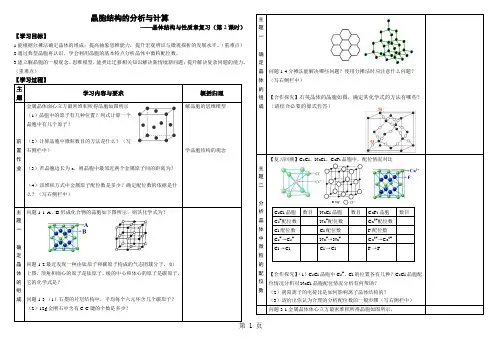
晶胞结构的分析与计算——晶体结构与性质章复习(第2课时)【学习目标】1.能根据分摊法确定晶体的组成;提高抽象思维能力,提升宏观辨识与微观探析的发展水平。
(重难点)2.通过典型晶胞再认识,学会利用晶胞的基本特点分析晶体中微粒配位数。
3.建立解晶胞的一般观念、思维模型,能类比迁移相关知识解决新情境新问题;提升解决复杂问题的能力。
(重难点),则晶胞中最邻近两个金属原子间的距离为?最近发现一种由钛原子和碳原子构成的气态团簇分子,如顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是?分摊法能解决哪些问题?使用分摊法时应注意什么问题?石英晶体的晶胞如图,确定其化学式的方法有哪些?晶胞中,配位情况对比CsCl晶胞数目NaCl晶胞数目CaF2晶胞数目+Ca2+配位数1.有下列某晶体的空间结构示意图。
图中●和化学式中M分别代表阳离子,图中○和化学式中N分别代表阴离子,则化学式为MN2的晶体结构为()A B C D2.下列说法正确的是()(N A表示阿伏加德罗常数)A.1mol冰中含有氢键的个数为2 N AB.12g石墨中含有C-C键的个数为3N AC.二氧化硅晶体中存在四面体网状结构,O处于中心,Si处于4个顶点D.密置层在三维空间堆积可得体心立方堆积和面心立方最密堆积3.氮化碳结构如下图所示,其硬度超过金刚石,下列有关氮化碳的说法不正确的是()A.氮化碳属于原子晶体B.氮化碳中碳显-4价,氮显+3价C.氮化碳的化学式为C3N4D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连4.ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。
立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm.密度为(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为pm(列示表示)5.晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。

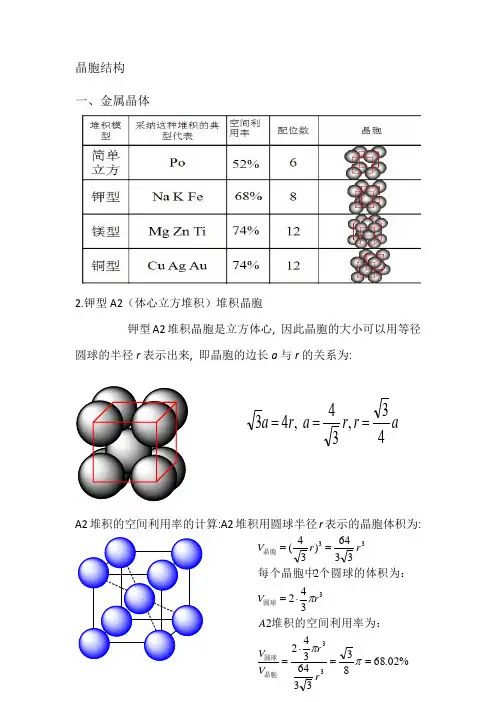
晶胞结构一、金属晶体2.钾型A2(体心立方堆积)堆积晶胞钾型A2堆积晶胞是立方体心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A2堆积的空间利用率的计算:A2堆积用圆球半径r 表示的晶胞体积为:ar r a r a 43,34 ,43===%02.68833364342234223364)34(33333==⋅=⋅===πππr r V V A rV rr V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中3.六方最密堆积(4)A1(面心立方最密堆积)A1是ABCABCABC······型式的堆积,从这种堆积中可以抽出一个立方面心点阵,因此这种堆积型式的最小单位是一个立方面心晶胞。
A1堆积晶胞是立方面心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A1堆积空间利用率的计算:A1堆积用圆球半径r 表示的晶胞体积为:(5)A4堆积形成晶胞A4堆积晶胞是立方面心点阵结构, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A4堆积的空间利用率的计算:A4堆积用圆球半径r 表示的晶胞体积为: ra r a 22 ,42==%05.742312163441344 4216)22(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中ar r a r r a 83,38 ,8243===⨯=%01.34163335123484348 833512)38(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中二、原子晶体1.金刚石立体网状结构,每个碳原子形成4个共价键,任意抽出2个共价键,每两个单键归两个六元环所有,而不是只归一个六元环所有(如图所示,红色的两个碳碳单键,可以构成蓝色和紫红色的两个六元环)。

晶胞参数计算公式晶胞参数是材料表征的重要参数,因而晶胞参数的计算十分重要。
本文针对晶胞参数的计算,详细介绍了晶胞参数计算公式中的一些重要概念及计算方法。
首先,晶胞参数是描述物质电学性质的概念,包括晶胞体积、晶胞定律、晶格常数和晶体结构等。
其中晶胞体积指:物质经过特定初始条件下晶胞构型变化后占用的总空间,是两个基本晶胞参数。
晶胞定律指:晶胞的长、宽、高之间的关系,是一种结构参数的表示。
晶格常数指:两个原子之间的距离,是一种晶胞结构参数的表示。
晶体结构是指:物质中原子构成的定向三维晶体结构。
晶胞参数计算公式包括晶胞参数计算公式和晶格常数计算公式。
晶胞参数计算公式用于计算晶胞体积,晶胞定律及晶体结构,主要有两种计算方法:一种是基于原子坐标的公式,如Bravais(1848)公式、Voronoi(1908)公式和Ginzburg-Landau(1950)公式;另一种是基于晶胞参数的公式,如Hilbert(1912)公式、Madelung(1925)公式和Ladd(1977)公式。
晶格常数计算公式用于计算晶格参数,主要有两种计算方法:一种是基本元素计算法,如Weaire(1892)公式和Morse(1931)公式;另一种是分子力学计算法,如Lennard-Jones(1938)公式和Stillinger-Weber(1985)公式。
现代晶体学通过实验测量元素晶体中原子间距离,利用晶胞参数和晶格常数计算公式,可以准确地确定晶体结构,进而研究物质的物理性质,为应用物理学的发展作出贡献。
在电子结构的计算中,也使用晶胞参数和晶格常数计算公式,分析不同晶体结构的能带结构和电子电荷密度等。
因此,晶胞参数计算公式和晶格常数计算公式是材料表征的重要工具,它们是物理化学所不可缺少的技术手段,极大地提高了研究物质性质的精度。
无论是在材料物理研究中,还是在电子结构计算中,晶胞参数计算公式和晶格常数计算公式都是物理学家必备的技术工具,必将对物理研究和应用物理学的发展产生重要作用。
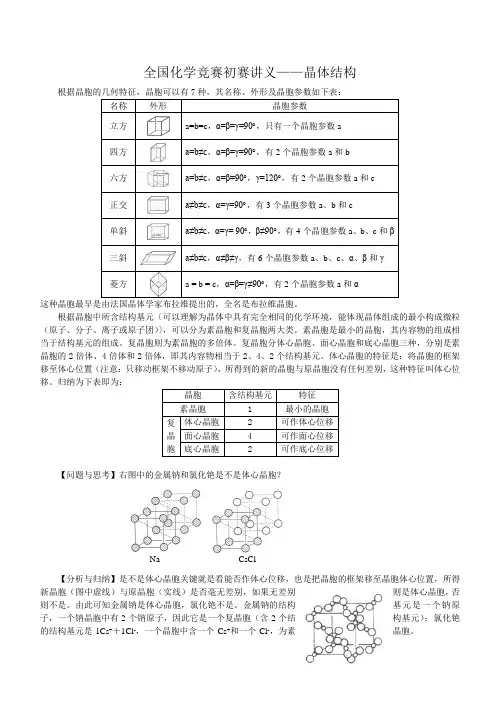
全国化学竞赛初赛讲义——晶体结构 根据晶胞的几何特征,晶胞可以有7种,其名称、外形及晶胞参数如下表:名称外形 晶胞参数 立方a=b=c ,α=β=γ=90︒,只有一个晶胞参数a 四方a=b≠c ,α=β=γ=90︒,有2个晶胞参数a 和b 六方a=b≠c ,α=β=90︒,γ=120︒,有2个晶胞参数a 和c 正交a≠b≠c ,α=γ=90︒,有3个晶胞参数a 、b 和c 单斜a≠b≠c ,α=γ= 90︒,β≠90︒,有4个晶胞参数a 、b 、c 和β 三斜a≠b≠c ,α≠β≠γ,有6个晶胞参数a 、b 、c 、α、β和γ 菱方a =b =c ,α=β=γ≠90︒,有2个晶胞参数a 和α这种晶胞最早是由法国晶体学家布拉维提出的,全名是布拉维晶胞。
根据晶胞中所含结构基元〔可以理解为晶体中具有完全相同的化学环境,能体现晶体组成的最小构成微粒(原子、分子、离子或原子团)〕,可以分为素晶胞和复晶胞两大类。
素晶胞是最小的晶胞,其内容物的组成相当于结构基元的组成。
复晶胞则为素晶胞的多倍体。
复晶胞分体心晶胞、面心晶胞和底心晶胞三种,分别是素晶胞的2倍体、4倍体和2倍体,即其内容物相当于2、4、2个结构基元。
体心晶胞的特征是:将晶胞的框架移至体心位置(注意:只移动框架不移动原子),所得到的新的晶胞与原晶胞没有任何差别,这种特征叫体心位移。
归纳为下表即为:晶胞含结构基元 特征 素晶胞1 最小的晶胞 复晶胞 体心晶胞2 可作体心位移 面心晶胞4 可作面心位移 底心晶胞 2 可作底心位移【问题与思考】右图中的金属钠和氯化铯是不是体心晶胞?【分析与归纳】是不是体心晶胞关键就是看能否作体心位移,也是把晶胞的框架移至晶胞体心位置,所得新晶胞(图中虚线)与原晶胞(实线)是否毫无差别,如果无差别则是体心晶胞,否则不是。
由此可知金属钠是体心晶胞,氯化铯不是。
金属钠的结构基元是一个钠原子,一个钠晶胞中有2个钠原子,因此它是一个复晶胞(含2个结构基元);氯化铯的结构基元是1Cs ++1Cl -,一个晶胞中含一个Cs +和一个Cl -,为素晶胞。

典型晶体结构认识及相关计算一、试验目的①加深对几种典型晶体结构的认识,熟悉三种典型晶体结构的画法,②学会找三种典型晶体结构的四面体间隙和八面体间隙和计算各种间隙半径③熟悉各种晶面指数和晶向指数的求法④加深对各种典型晶体结构的各晶面的原子分布图的认识,数量掌握各种晶体结构的致密度、面密度,线密度的计算二、几种典型的晶体结构1、面心立方面心立方晶胞的立方体的八个顶角各有一个原子,在六个面的中心还存在一个原子,其结构图如下图1所示:2、体心立方体心立方晶胞是立方体的八个顶角各有一个原子,在体内中心还有一个原子,其结构图如图2所示:3、密排六方密排六方晶胞是在正六方体的十二个顶角各有一个原子,上下两底面中心各有一个原子,在两底面之间还有三个原子。
其结构图如图3所示:3、线密度:某个晶向上原子所占的线长度与晶向长度的比值。
eg.bcc晶体的[111]晶向,其原子排列情况如图5所示:4、晶面指数求法:(略)注意事项:求晶面指数时,坐标系原点不能位于所要求的晶面上。
5、 晶向指数求法:(略)6、 晶面间距晶面(hkl )的晶面间距的求法为:⎪⎪⎪⎪⎪⎩⎪⎪⎪⎪⎪⎨⎧+++=++=++=2222222222)(3)(41)()()(1c l a l hk h d l k h a d c lb k a h d hkl hklhkl四、验报告主要内容1、计算体心立方、面心立方的致密度,假设密排六方的2=ac ,求这种密排六方晶胞的致密度。
2、画出面心立方晶胞的(100)、(110)、(111)晶面和体心立方的(100)、(110)、(111)的晶面以及密排六方的(001)晶面的截面图,计算它们的面密度,同时求出各种晶面的晶面间距d 。
3、画出面心立方晶胞[110]、[100]、[111]和体心立方晶胞的[111]、[100]、[110]晶向上的原子分布图,并计算它们的线密度。
4、综合2、3的相关计算,根据派纳力公式)1(212υπυτ---=b ap e G ,找出面心立方和体心立方中最密排面(面密度最大)和最密排方向的组合,其组合即为滑移系。

晶胞结构及计算范文晶胞结构是晶体中原子的排列方式,是研究晶体性质和行为的基础。
晶体中原子的排列具有三维周期性,这种周期性与晶胞结构有着密切的关系。
计算晶胞结构可以通过实验方法或者理论模拟方法来实现。
晶胞结构包括晶体的晶胞参数和晶体的点阵类型。
晶体的晶胞参数包括晶胞的边长和晶胞的夹角。
晶体的点阵类型包括立方晶系、单斜晶系、正交晶系、三斜晶系、六方晶系和四方晶系等几种类型。
实验方法可以通过透射电子显微镜(TEM)、X射线衍射(XRD)、中子衍射等技术来确定晶胞结构。
其中,X射线衍射是最常用的一种方法。
它利用X射线束照射到晶体上,通过观察和测量射线的衍射图样来确定晶体的晶胞结构。
这一方法可以得到非常精确的结果,但是需要实验设备和技术的支持。
理论模拟方法可以通过计算机模拟来计算晶胞结构。
其中最常用的方法是密度泛函理论(DFT)和分子动力学模拟(MD)。
DFT是一种基于电子结构理论的方法,可以计算晶体中电子的分布和能级结构,并通过这些信息来确定晶胞结构。
MD模拟是一种基于牛顿力学运动方程的方法,可以模拟晶体中原子的位置和运动轨迹,并通过这些信息来确定晶胞结构。
在DFT计算中,晶体的结构可以通过优化晶胞参数和原子位置来确定。
首先,需要选择一个适当的晶胞类型和初始参数,然后通过调节晶胞参数和原子位置,使得晶体的总能量达到最小值。
通过多次迭代计算,可以逐步优化晶胞的参数和原子的位置,直到得到满意的结果。
在MD模拟中,晶胞结构的计算通常是在已知的晶体结构基础上进行的。
首先,需要选择一个合适的原子间相互作用势能模型,然后通过计算每个原子的受力和加速度,来模拟晶体中原子的运动。
通过经过一段时间的模拟,可以得到晶体中原子的位置和运动轨迹。
通过分析和处理这些数据,可以确定晶体的晶胞结构。
总的来说,晶胞结构和计算是研究晶体性质和行为的重要方面。
通过实验方法和理论模拟方法,我们可以获得晶体的晶胞参数和点阵类型,进而研究晶体的物理性质和化学行为。
必刷题晶胞结构分析与计算建议完成时间:60分钟选择题:精选20题实际完成时间:分钟非选择题:精选0题1(2023·广东广州·统考三模)研究者利用冷冻透射电子显微镜,在石墨烯膜上直接观察到了自然环境下生成的二维晶体,其结构如图所示。
下列说法正确的是A.石墨烯属于烯烃,可发生加成反应B.石墨烯中碳原子的杂化轨道类型为sp2C.二维晶体的化学式为CaCl2D.二维晶体中Ca和Cl的配位数均为6【答案】B【详解】A.石墨烯属于碳单质,不含有H元素,不属于烯烃,不能发生加成反应,故A错误;B.石墨烯为平面结构,C的价层电子对数为3,故碳原子的杂化轨道类型为sp2,故B正确;C.每个Ca周围距离最近的Cl有3个,每个Cl周围距离最近的Ca有3个,故二维晶体的化学式为CaCl,故C错误;D.由C分析知,二维晶体中Ca和Cl的配位数均为3,故D错误;故选B。
2(2023·重庆沙坪坝·校考模拟预测)X为一种由汞(Hg)、锗(Ge)、锑(Sb)形成的可作潜在拓扑绝缘体材料的新物质,其晶胞如图所示(底面为正方形)。
下列说法错误的是A.X的化学式为GeHgSb2B.与Hg 距离最近的Sb 的数目为4C.若晶胞中原子1的坐标为(0,0,0),则原子2的坐标为34,34,34D.设X 的最简式的分子量为M r ,则X 晶体的密度为4M r ×1021N A a 2c g ⋅cm -3【答案】C【详解】A .X 中含Hg 个数为4×14+6×12=4,Ge 个数为8×18+4×12+1=4,Sb 个数为8,则X 的化学式为GeHgSb 2,故A 正确;B .以右侧面的Hg 分析,与Hg 距离最近的Sb 的数目为4,故B 正确;C .若晶胞中原子1的坐标为(0,0,0),则原子2在上面那个立方体的体对角线的四分之一处,其z 坐标为12+12×14=58,则其坐标为34,34,58 ,故C 错误;D .设X 的最简式的分子量为M r ,则X 晶体的密度为M r g ⋅mol -1N A mol -1×4(a ×10-7cm )2×c ×10-7cm =4M r ×1021N A a 2c g ⋅cm -3,故D 正确。
晶胞结构及计算
一、键数与配位数的判断
1.下列说法中正确的是()
A.金刚石晶体中的最小碳原子环由6个碳原子构成
B.晶体中只要有阳离子,就有阴离子
C.1 mol SiO2晶体中含2 mol Si—O键
D.金刚石化学性质稳定,即使在高温下也不会和O2反应
2.下列叙述正确的是()
A.分子晶体中的每个分子内一定含有共价键
B.原子晶体中的相邻原子间只存在非极性共价键
C.离子晶体中可能含有共价键
D.金属晶体的熔点和沸点都很高
3.(2015·湖北黄石9月调研)晶体硼的结构如右图所示。
已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。
下列有关说法不正确的是()
A.每个硼分子含有12个硼原子
B.晶体硼是空间网状结构
C.晶体硼中键角是60°
D.每个硼分子含有30个硼硼单键
4.冰晶石(Na3AlF6)是离子化合物,由两种微粒构成,冰晶石晶胞结构如图所示,“”位于大立方体顶点和面心,“”位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处“”所代表的微粒是________(填具体的微粒符号)。
5.某离子晶体的晶胞结构如图所示。
试回答下列问题:
(1)晶体中每一个Y同时吸引着________个X,每个X同时吸引着________个Y,该晶体的化学式是________________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有________个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为__________。
二、晶胞中的综合计算
6.(2017·成都七中高三上10月阶段测试)已知单质钒的晶胞为,则V 原子的配位数是__________,假设晶胞的边长为d cm,密度为ρg·cm-3,则钒的相对原子质量为______________。
7.(2017·临汾一中高三上学期期中)K2S的晶胞结构如图所示。
其中K+的配位数为________,S2-的配位数为________;若晶胞中距离最近的两个S2-核间距为a cm,则K2S晶体的密度为________ g·cm-3(列出计算式,不必计算出结果)。
8.(2016·华中师大附中高三5月月考)NaH的晶胞如图,则NaH晶体中阳离子的配位数是
________;设晶胞中阴、阳离子为刚性球体且恰好相切,求阴、阳离子的半径比r(-) r(+)=
________。
答案精析
1.A [金属晶体中只有阳离子,没有阴离子;因每个Si 与相邻4个O 以共价键相结合,故1 mol SiO 2中含有4 mol Si —O 键;金刚石在一定条件下可以与O 2反应生成CO 2。
] 2.C 3.B 4.Na +
解析 黑球的个数是8×18+6×12=4,白球的个数为12×1
4+8=11,而Na 3AlF 6中钠离子与
AlF 3-
6的个数比是3∶1,所以钠离子应是12个,所以图中▽应代表Na +。
5.(1)4 8 XY 2或(Y 2X) (2)12 (3)109°28′
解析 (1)此结构虽不符合晶胞“无隙并置”,但仍可用此立方结构单元计算晶体组成。
每个最小立方单元中只有1个Y ,且每个Y 同时吸引4个X ,而X 处于顶点上为8个立方单元所共有,即每个X 同时吸引8个Y 。
在每个该立方单元中含X :18×4=1
2(个),含Y 1个,则化
学式为XY 2或Y 2X 。
(2)在一个立方单元中,每个X 与它的距离最接近的X 有3个,则每个X 周围有3×8
2=12(个)(每个面为两个立方单元共有)。
(3)在此立方单元中,Y 与4个X 形成
正四面体结构,故键角为109°28′。
6.8 1
2
ρd 3N A
解析 根据晶胞图可知,每个矾原子周围距离最近的有8个矾原子,所以矾的配位数为8,每个晶胞中含有的矾原子数为1+8×18=2,晶胞的体积为d 3cm 3,根据ρ=2M
N A V ,可知,钒的
相对原子质量M =12ρVN A =1
2ρd 3N A 。
7.4 8
4×110N A ·(2a )3[或4×1106.02×1023·(2a )3
]
解析 K 2S 的晶胞中,每个K +
周围等距最近的S 2-
有4个,所以K +
的配位数为4,每个S 2
-
周围等距最近的K +
有8个,所以S 2-
的配位数为8。
晶胞中距离最近的两个S 2-
核间距为a cm ,为每个面对角线距离的一半,则晶胞的边长为2a cm ,故K 2S 晶体的密度为ρ=m V =
4×110N A (2a )3[或4×110
6.02×1023·(2a )3]。
8.6 0.414(或2-1)
解析 NaH 的晶胞与氯化钠的相似,则NaH 晶体中阳离子的配位数是6;NaH 晶体中阴阳离
子的半径和为晶胞边长a (如图
)的一半即a
2
,钠离子的半径为对角
线的14,即为24a ,氢负离子的半径为12a -24a ,所以H -半径与Na +
半径之比为r (-)r (+)=
12a -24a
2
4a =0.414。