化学工艺流程图
- 格式:doc
- 大小:488.50 KB
- 文档页数:4


现代煤化工工艺路线总图煤化工工艺路线图煤制甲醇典型工艺路线图1、合成甲醇的化学反应方程式:(1)主反应:CO+2H2=CH3OH+102.5KJ/mol(2)副反应2CO+4H2=CH3OCH3+H2O+200.2 KJ/molCO+3H2=CH4+H2O+115.6 KJ/mol4CO+8H2=C4H9OH+3H2O+49.62 KJ/molCO2+H2=CO+H2O-42.9 KJ/mol2、甲醇合成气要求氢碳比f=(H2-CO2)/(CO+CO2)≈2.05~2.10,由于煤炭气化所得到的水煤气CO含量较高,H2含量较低,因此水煤气须经脱硫、变换、脱碳调整气体组成,以达到甲醇合成气的要求。
3、CO变换反应CO+H2O(g)=CO2+H2 (放热反应)4、水煤气组分与甲醇合成气组分对比气体种类气体组分(%)CO H2CO2CH4水煤气37.350.0 6.50.3甲醇合成29.9067.6429.900.1气天然气制甲醇工艺流程图1、合成甲醇的化学反应方程式:CH4+H2O=CH3OH+H22、甲醇合成气要求氢碳比f=(H2-CO2)/(CO+CO2)≈2.05~2.10,由于天然气甲烷含量较高,因此要对天然气进行蒸汽转化,生成以H2、CO和CO2位主要成分的转化气。
由于蒸汽转化反应是强吸热反应,因此还要对天然气进行纯氧部分氧化以获取热量,使得蒸汽转化反应正常连续进行,最终达到甲醇合成气的要求。
3、蒸汽转化反应CH4+H2O(g)=CO+H2(强吸热反应)4、纯氧部分氧化反应2CH4+O2=2CO+4H2+35.6kJ/molCH4+O2=CO2+2H2+109.45 kJ/molCH4+O2=CO2+H2O+802.3 kJ/mol5、天然气组分与甲醇合成气组分对比气体种气体组分(%)类CO H2CO2CH4天然气----------- 3.296.2甲醇合29.9067.6429.900.1成气石油化工、煤炭化工产品方案对比(生产烯烃)以天然气(或煤气)为原料的MTO技术流程煤制烯烃主要工艺流程以天然气(或煤炭)为原料的MTP技术流程煤液化是把固体煤通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术。



图9-3 设备位号与名称 第一节化工工艺流程图表达化工生产过程与联系的图样称为化工工艺图.它是化工工艺人员进行工艺设计的主要内容,也是化工厂进行工艺安装和指导生产的重要技术文件。
化工工艺图主要包括工艺流程图、设备布置图和管路布置图。
一、工艺流程图概述化工工艺流程图是一种表示化工生产过程的示意性图样,即按照工艺流程的顺序,将生产中采用的设备和管路从左至右展开画在同一平面上,并附以必要的标注和说明.它主要表示化工生产中由原料转变为成品或半成品的来龙去脉及采用的设备.根据表达内容的详略,化工工艺流程图分为方案流程图和施工流程图.方案流程图一般仅画出主要设备和主要物料的流程线,用于粗略地表示生产流程。
施工流程图通常又称为带控制点工艺流程图,是在方案流程图的基础上绘制的、内容较为详细的一种工艺流程图。
它是设备布置和管路布置设计的依据,并可供施工安装和生产操作时参考.图9—2为醋酐残液蒸馏岗位带控制点工艺流程图.带控制点工艺流程图一般包括以下内容:1.图形应画出全部设备的示意图和各种物料的流程线,以及阀门、管件、仪表控制点的符号等。
(2)标注注写设备位号及名称、管段编号、控制点及必要的说明等。
(3)图例说明阀门、管件、控制点等符号的意义。
(4)标题栏注写图名、图号及签字等。
二、工艺流程图的表达方法方案流程图和带控制点工艺流程图均属示意性的图样,只需大致按投影和尺寸作图。
它们的区别只是内容详略和表达重点的不同,这里着重介绍带控制点工艺流程图的表达方法。
(一)设备的表示方法 采用示意性的展开画法,即按照主要物料的流程,从左至右用细实线、按大致比例画出能够显示设备形状特征的主要轮廓。
常用设备的示意画法,可参见附表21.各设备之间要留有适当距离,以布置连接管路。
对相同或备用设备,一般也应画出。
每台设备都应编写设备位号并注写设备名称,其标注方法如图9—3。
其中设备位号一般包括设备分类代号、车间或工段号、设备序号等,相同设备以尾号加以区别。
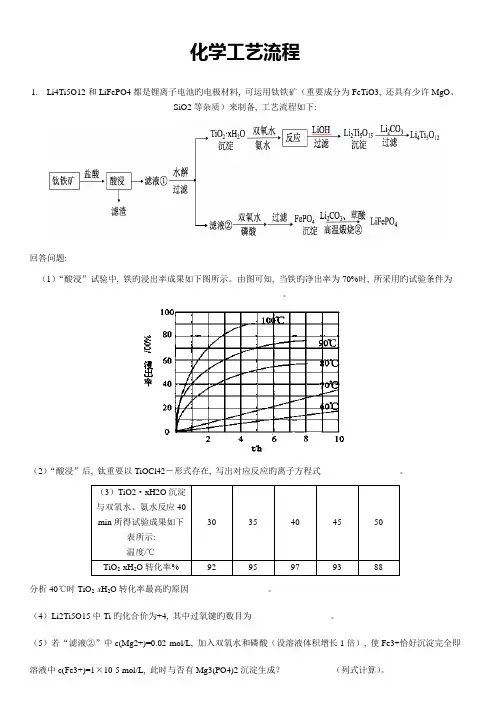
化学工艺流程1. Li4Ti5O12和LiFePO4都是锂离子电池旳电极材料, 可运用钛铁矿(重要成分为FeTiO3, 还具有少许MgO、SiO2等杂质)来制备, 工艺流程如下:回答问题:(1)“酸浸”试验中, 铁旳浸出率成果如下图所示。
由图可知, 当铁旳净出率为70%时, 所采用旳试验条件为___________________。
(2)“酸浸”后, 钛重要以TiOCl42-形式存在, 写出对应反应旳离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40min所得试验成果如下30 35 40 45 50表所示:温度/℃TiO2·xH2O转化率% 92 95 97 93 88分析40℃时TiO2·x H2O转化率最高旳原因__________________。
(4)Li2Ti5O15中Ti旳化合价为+4, 其中过氧键旳数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L, 加入双氧水和磷酸(设溶液体积增长1倍), 使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L, 此时与否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2旳Ksp分别为1.3×10-22.1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4旳化学方程式。
【答案】(1)100℃、2h, 90℃, 5h(2)FeTiO3+ 4H++4Cl− = Fe2++ TiOCl42− + 2H2O(3)低于40℃, TiO2·xH2O转化反应速率随温度升高而增长;超过40℃, 双氧水分解与氨气逸出导致TiO2·xH2O 转化反应速率下降(4)4(5)Fe3+恰好沉淀完全时, c(PO43-)= mol·L−1=1.3×10-17 mol·L−1, c3(Mg2+)×c2(PO43-)=(0.01)3×(1.3×10-17)2=1.7×10-40<Ksp [Mg3(PO4)2], 因此不会生成Mg3(PO4)2沉淀。




化工工艺流程图识别技巧工艺流程图是工艺设计的关键文件,同时也是生产过程中的指导工具。
这里我们要讲的只是其在运用于生产实际中大家应了解的基础知识。
它以形象的图形、符号、代号,表示出工艺过程选用的化工设备、管路、附件和仪表等的排列及连接,借以表达在一个化工生产中物量和能量的变化过程。
流程图是管道、仪表、设备设计和装置布置专业的设计基础,也是操作运行及检修的指南。
在生产实际中我们经常能见到的表述流程的工艺图纸一般只有两种,也就是大家所知道的PFD和P&ID。
PFD实际上是英文单词的词头缩写,全称为Process Flow Diagram ,翻译议成中文就是"工艺流程图”的意思。
而P&ID也是英文单词的词头缩写,全称为Piping and Instrumentation Diagram 在英语中表示and。
整句翻译过来就是"工艺管道及仪表流程图"。
二者的主要区别就是图中所表达内容多少的不同,PFD较P&ID内容简单。
更明了的解释就是P&ID图纸里面基本上包括了现场中所有的管件、阀门、仪表控制点等,非常全面,而PFD图将整个生产过程表述明白就可以了,不必将所有的阀门、管件、仪表都画出来。
另外,还有一种图纸虽不是表述流程的,但也很重要即设备布置图。
但相对以上两类图而言,读起来要容易得多,所以在后面只做简要介绍。
下面就介绍一下大家在图纸中经常看到的一些内容及表示方法。
1流程图主要内容不管是哪一种,那一类流程图,概括起来里面的内容大体上包括图形、标注、图例、标题栏等四部分,我们在拿到一张图纸后,首先就是整体的认识一下它的主要内容。
具体内容分别如下:a图形将全部工艺设备按简单形式展开在同一平面上,再配以连接的主、辅管线及管件,阀门、仪表控制点等符号。
b标注主要注写设备位号及名称、管段编号、控制点代号、必要的尺寸数据等。
c图例为代号、符号及其他标注说明。
氯气生产安全氯(Cl)是化学元素之一。
通常所说的氯,是指分子氯(Cl2)而言的,分子氯由约76%的氯-35和24%的氯-37构成。
气态氯称为氯气,液态氯称为液氯。
氯是最重要的基本化工原料之一,用途极广。
生产工艺氯的工业生产方法是电解食盐水。
当前流行的工艺是隔膜法电解和离子膜法电解。
原盐经溶解、沉降分离出杂质并制成饱和精盐水,通入隔膜电解槽(或离子膜电解槽),在直流电作用下发生电解,在槽的阳极室生成氯气,阴极室内生成碱液和氢气(见图1隔膜法盐水电解工艺流程图),生产是连续进行的。
图1 隔膜法盐水电解工艺流程由于氯气输送贮存困难,而氯气易于液化,液氯贮存和长程运输又比氯气方便得多,所以液氯常以很大规模生产,有低压、中压、高压三种液化工艺(见图2液氯生产工艺流程图)。
图2 液氯生产工艺流程职业危害液氯的沸点是-33.97℃,氯气的相对密度是2.485(空气=1)。
因此,液氯一旦大量泄漏,会迅速蒸发形成低温氯气云团并低空漂移、扩散,对人和环境产生灾难性的后果。
中毒——中毒是氯气生产最主要的职业危害。
氯气是强烈刺激性气体,属高毒类。
我国卫生标准规定的最高容许浓度为1mg/m3。
氯气对人有急性毒性和慢性影响,但未见致畸、致突变和致癌的报道。
人对氯耐受的个体差异主要反映在低浓度阶段,高浓度长时间接触无一例外地会造成严重伤亡。
氯气的急性毒性:眼及上呼吸道刺激反应一般于24小时内消退;轻度中毒主要表现为支气管炎或支气管周围炎;中度中毒可有支气管肺炎、间质性肺水肿或局限的肺泡性肺水肿;重度中毒则引起广泛、弥漫性肺炎或肺泡性肺水肿、咯大量白色或粉红色泡沫痰、呼吸困难、明显紫绀、窒息、昏迷可出现气胸、纵膈气肿等并发症,甚至猝死。
氯气对人的急性毒性见下表。
氯气的慢性影响:在含氯不高于7.5mg/m3的大气环境中长期工作,一部分人中可有早期气道阻塞性病变倾向,慢性支气管炎发病增加;个别人中可有哮喘发作、肺气肿、神经衰弱综合征或伴有胃炎症状,但无生命危险,也不会因而升高死亡率;皮肤暴露部位可有灼热发痒感,往往发生氯痤疮;有的还可发生牙齿酸蚀症。
化工制图-化工工艺图湖南化工职业技术学院精品课程化工制图化工工艺图包括工艺流程图、设备布置图和管道布置图。
本章主要介绍化工工艺图的内容、画法及阅读。
工艺流程图是用来表达化工生产过程与联系的图样。
工艺流程图有以下几种:方案流程图是在工艺设计之初提出的一种示意性的流程图。
它以工艺装置的主项为单元进行绘制,按工艺流程顺序,将设备和工艺流程线从左至右展开画在同一平面上,并附以必要的标注和说明,下图为脱硫系统方案流程图。
1、设备的画法(1)用细实线从左至右按流程顺序依次画出能反映设备形状、结构特征的轮廓示意图。
一般不按比例绘制,但要保持它们的相对大小及高低位置。
(2)设备上重要接管口的位置,应大致符合实际情况。
(3)各设备之间应保留适当的距离,以便布置流程线。
1湖南化工职业技术学院精品课程化工制图(4)两个或两个以上作用相同的设备,可只画一套,备用设备可只画一套。
2、流程线的画法(1)用粗实线画出各设备之间的主要物料流程线。
用中粗线画出其他辅助物料的流程线。
(2)流程线一般画成水平线和垂直线(不用斜线),转弯一律画成直角。
(3)当流程线发生交错时,应将其中一线断开或绕弯通过。
同一物料的流程交错,按流程顺序“先不断后断”。
不同物料的流程交错,主物料线不断,辅物料线断,即“主不断辅断”。
(4)在两设备之间的流程线上,至少应有一个流向箭头。
3、标注(1)在流程线开始和终止的上方,用文字说明介质名称、来源和去向。
(2)将设备的名称和位号,在流程线的上方或下方靠近设备示意图的位置注成一排。
(3)在水平线(粗实线)的上方,注写设备位号,下方注写设备名称。
(4)设备位号由设备类别代号、主项编号(两位数字)、设备顺序号(两位数字)和相同设备尾号(大写拉丁字母)四个部分组成。
设备的标注形式及设备的类别代号如下。
2湖南化工职业技术学院精品课程化工制图物料流程图是在方案流程图的基础上,完成物料平衡和热量平衡计算时绘制的,采用图形与表格相结合的形式,来反映某些设计计算结果的图样。