舒马曲坦相关杂质
- 格式:doc
- 大小:526.35 KB
- 文档页数:2

琥珀酸舒马曲坦的合成工艺改进
丁磊;富强;沈晗;唐锋
【期刊名称】《药学进展》
【年(卷),期】2007(31)4
【摘要】目的:改进琥珀酸舒马曲坦的合成工艺. 方法:以4-肼基-N-甲基-苄基磺酰胺盐酸盐与4,4-二甲氧基-N,N-二甲基-丁胺为起始原料,改用多聚磷酸和磷酸二氢钠作为催化剂,后处理采用异丙醚和丙酮作为重结晶溶剂,经缩合、重排、环合、成盐的4步反应合成琥珀酸舒马曲坦. 结果:获得纯度和收率均较满意的目标产物,总收率由文献报道的8.5%提高到12.7%. 结论:此改进后的合成工艺成本低,操作简便易行,适于工业化生产.
【总页数】3页(P171-173)
【作者】丁磊;富强;沈晗;唐锋
【作者单位】江苏先声药物研究有限公司药物合成研究室,江苏,南京,210042;江苏先声药物研究有限公司药物合成研究室,江苏,南京,210042;江苏先声药物研究有限公司药物合成研究室,江苏,南京,210042;江苏先声药物研究有限公司药物合成研究室,江苏,南京,210042
【正文语种】中文
【中图分类】R971;TQ460.31
【相关文献】
1.琥珀酸舒马曲坦固体分散体颗粒溶出度的测定 [J], 徐俊;闫启东;石雷
2.微渗析技术研究琥珀酸舒马曲坦在大鼠脑和血中的药代动力学 [J], 张雄;唐星;
3.琥珀酸舒马曲坦的工艺研究 [J], 管宜河; 于小红; 谢帆; 张少林; 王俊华
4.琥珀酸舒马曲坦的工艺研究 [J], 管宜河; 于小红; 谢帆; 张少林; 王俊华
5.琥珀酸舒马曲坦的剂型研究 [J], 郑文秀; 管宜河
因版权原因,仅展示原文概要,查看原文内容请购买。

琥珀酸舒马普坦残留溶剂方法确认报告文件编号:RSH6019-1起草人:日期:审核人:日期:日期:批准人:日期:目录一、概述二、验证目的三、验证范围四、验证人员五、验证依据六、验证内容七、验证结论八、附色谱图九、批准一、概述药物中的残留溶剂系指在原料药或辅料的生产中以及制剂的制备过程中使用的,但在工艺过程中未能完全除去的有机溶剂,我司在琥珀酸舒马普坦生产过程中使用了有机溶剂甲醇、乙醇、乙酸乙酯,因残留溶剂会影响产品的安全性,故需对琥珀酸舒马普坦的残留溶剂方法进行确认。
二、验证目的通过对琥珀酸舒马普坦残留溶剂的分析方法的专属性、精密度进行确认,确保方法的可行性,以便为有效控制琥珀酸舒马普坦的质量提供依据。
三、验证范围针对琥珀酸舒马普坦残留溶剂测定方法的可靠性及可行性。
四、验证人员张玲、黄翠、张茜、向波五、验证依据5.1 ICH Q2A、ICH Q2B、 ICH Q3C5.2 中国药典2010版二部附录VIII P 残留溶剂测定法5.3中国药典2010版二部附录XIX A药品质量标准分析方法验证指导原则六、验证内容6.1、验证用仪器、试剂、对照品6.2、验证方法6.2.1色谱条件:仪器:Agilent 7890A 检测器:FID色谱柱:DB-624 30m*0.53mm*3.0um 进样口温度:200℃检测器温度:200℃柱温:起温度始60℃,维持5分钟,以每分钟30℃的速度升温到150℃,维持6分钟。
流速:3.0ml/min 分流比:10:1 进样量:1ul载气:氮气空气:400ml/min 氢气:30ml/min6.2.1.1溶液的配制6.2.1.1.1供试品溶液:精密称取琥珀酸舒马普坦0.2g至10ml量瓶中,加N,N-二甲基甲酰胺溶解并稀释至刻度,摇匀,作为供试品溶液。
6.2.1.1.2储备溶液:精密称取甲醇150mg于100mL量瓶中,加N,N-二甲基甲酰胺溶解并稀释至刻度,摇匀,作为甲醇储备溶液;精密称取乙醇250mg于100mL量瓶中,加N,N-二甲基甲酰胺溶解并稀释至刻度,摇匀,作为乙醇贮备溶液;精密称取乙酸乙酯250mg于100mL量瓶中,加N,N-二甲基甲酰胺溶解并稀释至刻度,摇匀,作为乙酸乙酯贮备溶液;。

FDA批准新的琥珀酸舒马普坦注射剂
佚名
【期刊名称】《世界临床药物》
【年(卷),期】2006(27)5
【摘要】美国FDA批准新的琥珀酸舒马普坦4mg注射剂(Imitrex Injection),用于紧急治疗有或无先兆的偏头痛。
本品采用Imitrex STATdose系统。
患者仅启动按钮就可方便地获得4mg剂量的药物。
【总页数】1页(P257-257)
【关键词】琥珀酸舒马普坦;FDA批准;注射剂;紧急治疗;偏头痛;e系统
【正文语种】中文
【中图分类】R944;R97
【相关文献】
1.舒马曲坦鼻吸粉获FDA批准用于治疗偏头痛 [J], 黄世杰
2.顶空毛细管气相色谱法测定琥珀酸舒马普坦中7种有机溶剂的残留量 [J], 李娟;蔡蓝洁;艾朝辉;孔杜林
3.琥珀酸舒马普坦固体脂质纳米粒的制备及处方优化 [J], 屈晓梅;张芳
4.对舒马普坦治疗反应的预测:舒马普坦和那拉曲坦集合患者数据库 [J], Christoph-Diener H.;Ferrari M.;Mansbach H.;高方
5.国家食品药品监督管理局修订琥珀酸舒马普坦口服制剂说明书 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。

舒马曲坦胶囊的制备与质量控制张敬如;赵凯;黄复生;王昆【摘要】Objective To prepare sumatriptan capsules and establish the quality standard for them. Methods HPLC was used to determine the content of sumatriptan. Results Sumatriptan showed a good linear relationship in the range of 50-1 600 ng/mL( r = 0. 999 9) and the average recovery was up to (105. 73 ±4. 58)% , RSD was 4. 33%. The mean intra-day RSD and inter - day RSD were 2.20% and 2. 59%. Conclusion This standard is precise and can be used for the quality control of sumatriptan capsules.%目的制备舒马曲坦胶囊并建立其质量控制方法.方法采用高效液相色谱(HPLC)法测定制剂中舒马曲坦.结果舒马曲坦质量浓度在50~1600 ng/mL范围内与峰面积线性关系良好(r=0.9999),平均回收率为(105.73±4.58)%,RSD为4.33%(n=6),日内、日间精密度平均RSD为2.20%和2.59%.结论质量控制方法稳定可靠,可用于舒马曲坦胶囊的质量控制.【期刊名称】《中国药业》【年(卷),期】2012(021)021【总页数】3页(P32-34)【关键词】舒马曲坦胶囊;质量控制;高效液相色谱法【作者】张敬如;赵凯;黄复生;王昆【作者单位】中国人民解放军第三军医大学基础部病原生物学教研室,重庆400038;中国人民解放军第三军医大学基础部病原生物学教研室,重庆 400038;中国人民解放军第三军医大学基础部病原生物学教研室,重庆 400038;中国人民解放军第三军医大学基础部病原生物学教研室,重庆 400038【正文语种】中文【中图分类】R927.2;R971偏头痛是一种慢性神经血管紊乱性疾病,全球发病率约为10%~15%,随着生活节奏的加快和工作压力的加大,发病率呈上升趋势。
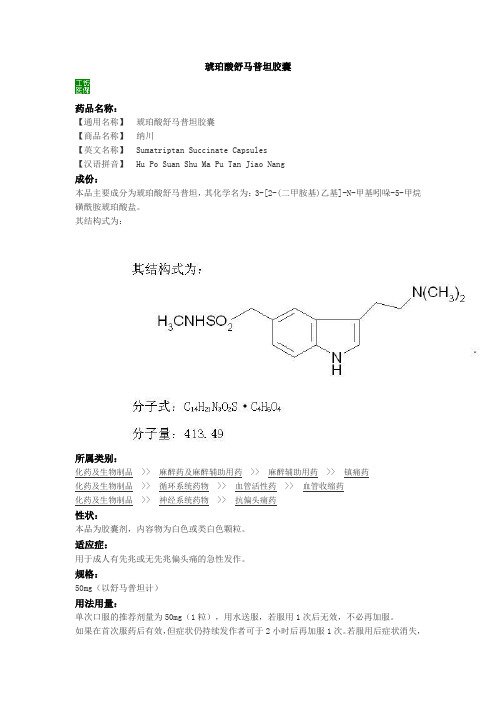
琥珀酸舒马普坦胶囊药品名称:【通用名称】琥珀酸舒马普坦胶囊【商品名称】纳川【英文名称】 Sumatriptan Succinate Capsules【汉语拼音】 Hu Po Suan Shu Ma Pu Tan Jiao Nang成份:本品主要成分为琥珀酸舒马普坦,其化学名为:3-[2-(二甲胺基)乙基]-N-甲基吲哚-5-甲烷磺酰胺琥珀酸盐。
其结构式为:所属类别:化药及生物制品>> 麻醉药及麻醉辅助用药>> 麻醉辅助用药>> 镇痛药化药及生物制品>> 循环系统药物>> 血管活性药>> 血管收缩药化药及生物制品>> 神经系统药物>> 抗偏头痛药性状:本品为胶囊剂,内容物为白色或类白色颗粒。
适应症:用于成人有先兆或无先兆偏头痛的急性发作。
规格:50mg(以舒马普坦计)用法用量:单次口服的推荐剂量为50mg(1粒),用水送服,若服用1次后无效,不必再加服。
如果在首次服药后有效,但症状仍持续发作者可于2小时后再加服1次。
若服用后症状消失,但之后又复发者,应待前次给药24小时后方可再次用药。
单次口服的最大推荐剂量为100mg (2粒)。
24小时内的总剂量不得超过200mg(4粒)。
不良反应:据国外文献报道:一、主要不良反应1、心脏的不良反应:急性心肌梗塞,致命性心律失常(如:心动过速,室颤,心跳骤停),甚至于有报道病人使用舒马普坦后数小时内死亡,但上述事件的发生率微乎其微。
舒马普坦还可导致冠脉痉挛,6348例临床试验中,有两例病人在服用舒马普坦后即刻出现冠脉痉挛的不良反应,但这些不良反应并未出现严重的临床后果。
2、脑血管的不良反应:脑出血,蛛网膜下腔出血,脑梗塞和其它事件,有些还出现致命的结果,但舒马普坦与这些事件的关联并不确定,相当一部分病例中,看起来更象是本来就存在脑血管病变,而将相关症状误认为系偏头痛(其实不是)所致,进而采用舒马普坦治疗。
抗偏头痛药丁二酸舒马坦(Sumatriptan Succinate)
周斌
【期刊名称】《国外医药:合成药.生化药.制剂分册》
【年(卷),期】1993(14)4
【摘要】异名 ImIGran,GR43175C 化学名 3-[2-(二甲胺基)乙基]-N-甲基-1 H-吲哚-5-甲胺基磺酰基丁二酸药效分类抗偏头痛药开发单位 (英国)Glaxo LaboratoriesLtd 上市厂商 1991年在荷兰首次上市偏头痛是一种单侧型头痛,常伴有恶心和呕吐。
在西方国家有10%以上的人患有此病,且大多数患者为女性。
其病因学机制尚待阐明,但已知偏头痛与颅血管显著而持续的扩张有关。
偏头痛一直是用麦角胺来治疗的,该药对颈动脉吻合具有血管收缩作用,
【总页数】3页(P241-243)
【关键词】抗偏头痛药;丁二酸舒马坦;新药
【作者】周斌
【作者单位】
【正文语种】中文
【中图分类】R971.1
【相关文献】
1.抗偏头痛药——Sumatriptan(舒马坦) [J], 郭丽仪
2.抗偏头痛药舒马曲坦的合成进展 [J], 张雪峰;王兴涌;杨志林;侯永春;沈春红
3.抗偏头痛药——舒马普坦 [J], 王佑宏;孙铁民
4.国外上市新药:抗偏头痛药丁二酸舒马坦 [J], 周斌
5.治抗偏头痛药舒马坦(Sumatriptan) [J], Bate.,DN;李春元
因版权原因,仅展示原文概要,查看原文内容请购买。
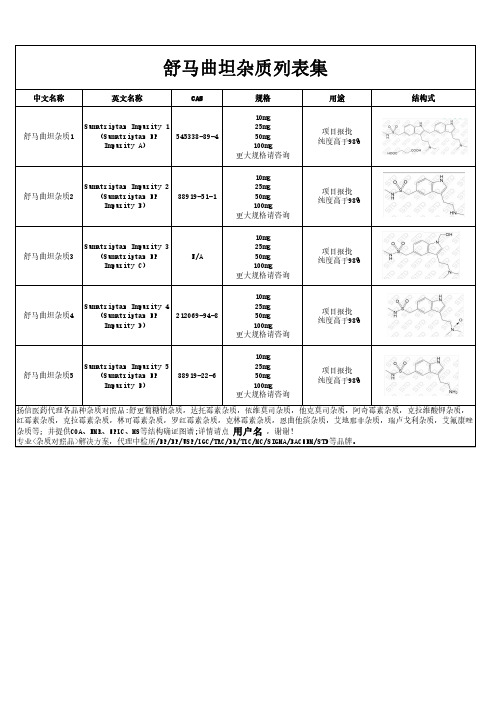
相关杂质整理列表
中文名英文名CAS号规格纯度结构式
舒马曲坦杂质1(舒马曲坦EP杂
质A)Sumatriptan
Impurity 1
(Sumatripta
n EP Impurity
A)
545338-89-
4
10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质2(舒马曲坦EP杂
质B)Sumatriptan
Impurity 2
(Sumatripta
n EP Impurity
B)
88919-51-1 10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质3(舒马曲坦EP杂
质C)Sumatriptan
Impurity 3
(Sumatripta
n EP Impurity
C)
N/A 10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质4(舒马曲坦EP杂
质D)Sumatriptan
Impurity 4
(Sumatripta
n EP Impurity
D)
212069-94-
8
10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质5(舒马曲坦EP杂
质E)Sumatriptan
Impurity 5
(Sumatripta
n EP Impurity
E)
88919-22-6 10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质6(舒马曲坦EP杂
质F)Sumatriptan
Impurity 6
(Sumatripta
n EP Impurity
F)
N/A 10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质7(舒马曲坦EP杂
质G)Sumatriptan
Impurity 7
(Sumatripta
n EP Impurity
G)
N/A 10mg-25mg-50mg-100mg ≥99%
舒马曲坦杂质8(舒马曲坦EP杂
质H)Sumatriptan
Impurity 8
(Sumatripta
n EP Impurity
H)
1391052-5
9-7
10mg-25mg-50mg-100mg ≥99%
湖北扬信医药科技有限公司经营上万种杂质对照品(优势供应硫酸羟氯喹杂质、硝苯地平杂质、沙丁胺醇杂质、达格列净杂质、厄贝沙坦杂质、阿莫西林克拉维酸钾杂质、利伐沙班杂质、阿托伐他汀钙杂质、西格列汀杂质、利格列汀杂质等),并代理销售中检所、STD、LGC、TLC、EP、USP、TRC等多个品牌产品,提供上万种标准品
对照品,真诚为您服务。