双液系沸点组成图的绘制
- 格式:doc
- 大小:120.50 KB
- 文档页数:6
双液系沸点-成分图的绘制一、实验目的1、用冷凝回流法测定不同浓度的环己烷-乙醇体系的沸点;2、正确使用阿贝折射仪;3、绘制沸点-成分图,确定体系的最低恒沸点和相应的组成。
二、实验原理1、沸点-成分图在恒压下,完全互溶双液体系的沸点与成分关系有三种情况(如图1-1、1-2、1-3):(1)溶液沸点介于二纯组分之间,如甲苯与苯;(2)溶液有最高恒沸点,如卤化氢和水,丙酮和氯仿等;(3)溶液有最低恒沸点,如环己烷和乙醇,水和乙醇等。
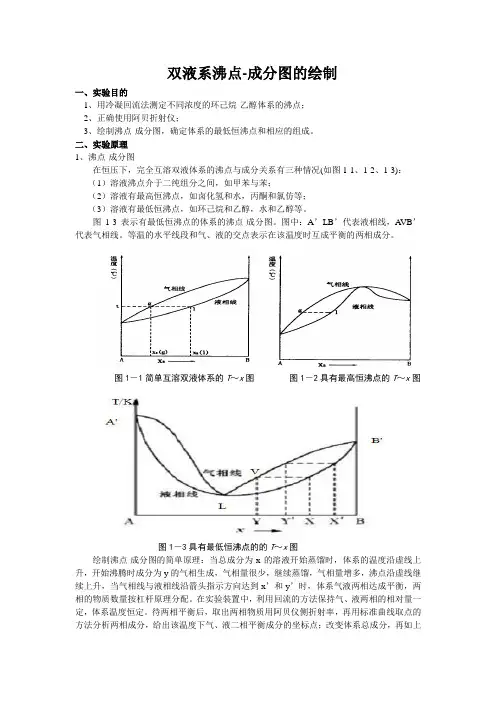
图1-3表示有最低恒沸点的体系的沸点-成分图。
图中:A’LB’代表液相线,A VB’代表气相线。
等温的水平线段和气、液的交点表示在该温度时互成平衡的两相成分。
图1-1简单互溶双液体系的T~x图图1-2具有最高恒沸点的T~x图图1-3具有最低恒沸点的的T~x图绘制沸点-成分图的简单原理:当总成分为x的溶液开始蒸馏时,体系的温度沿虚线上升,开始沸腾时成分为y的气相生成,气相量很少,继续蒸馏,气相量增多,沸点沿虚线继续上升,当气相线与液相线沿箭头指示方向达到x’和y’时,体系气液两相达成平衡,两相的物质数量按杠杆原理分配。
在实验装置中,利用回流的方法保持气、液两相的相对量一定,体系温度恒定。
待两相平衡后,取出两相物质用阿贝仪侧折射率,再用标准曲线取点的方法分析两相成分,给出该温度下气、液二相平衡成分的坐标点;改变体系总成分,再如上法找出另一对坐标点。
将所有气相点和液相点连成气相线和液相线,即得T-x平衡图。
2、阿贝仪的使用阿贝仪利用了折射和全反射全反射原理设计而成。
将样品滴在棱镜上,旋转棱镜使目镜能看到半明半暗现象。
旋转补偿棱镜消除色散,在转动棱镜使明暗界线正好与目镜中的十字线交点重合,从标尺上直接读取折射率。
三、实验仪器及药品1、仪器恒沸点仪阿贝尔折射仪(WZS-I 940168)蒸馏瓶电阻丝变压器水银温度计(50~100℃,分度值0.1℃)恒温水浴装置5mL、20mL移液管滴瓶万分之一天平2、药品乙醇环己烷图1-4 恒沸点仪四、实验内容1、沸点和两相成分的测定1)洗净、烘干蒸馏瓶,加20mL乙醇使温度升高并沸腾,每隔30s记一次数据;2)待温度稳定3min后,记最终温度及大气压;3)断电,用两只滴管取支管口处气相冷凝液及蒸馏瓶中液体,用阿贝折射仪测折射率,气相冷凝液测1次,液相测2次;4)蒸馏瓶中依次加2mL、2mL、3mL、4mL、5mL环己烷,按上述方法测沸点及气液两相折射率;5)回收母液,少量环己烷洗蒸馏瓶3~4次,注入20mL环己烷,测纯沸点及气液两相折射率;6)再向蒸馏瓶中依次加0.5mL、0.5mL、0.5mL、2mL、5mL、5mL乙醇,分别测沸点及气、液两相折射率。

实验报告姓名学号专业化学(师范)年级、班级课程名称物理化学实验实验项目实验类型 验证 设计 综合实验时间实验指导老师马国正实验评分一、实验目的(1)用回流冷凝法测定沸点时气相与液相的组成,绘制双液系相图。
并找出恒沸点混合物的组成及恒沸点的温度。
(2)掌握测定双组分液体的沸点及正常沸点的测定方法。
(3)了解阿贝折光仪的构造原理,熟悉掌握阿贝折光仪的使用方法。
二、实验原理(1)沸点的定义沸点是液体饱和蒸汽压和外压相等时的温度,双液系的沸点不仅于外压有关,而且还与两种液体的相对含量有关。
(2)理想二组分系统的拉乌尔定律理想的二组分体系在全部浓度范围内符合Raoult定律。
结构相似、性质相似的组分间可以形成近似的理想体系,这样可以形成简单的T-x(y)图。
大多数情况下,曲线将出现或正或负的偏差。
当这一偏差足够大时,在T-x(y)曲线上将出现极大点(负偏差)或极小点(正片差)。
这种最高和最低沸点称为恒沸点,所对应的溶液称为恒沸混合物。
(3)平衡时气相、液相的组成确定回流冷凝法保持气液相对量不变,测定双液系沸点,通过阿贝折射仪测定其液相折射率确定气液相平衡时的组成,通过双液系气液平衡时的组成对校正后的沸点作图,得到在1个大气压下乙醇-乙酸乙酯气液平衡相图。
三、仪器与试剂沸点仪(1套)小试管(5mL带软木塞)(若干)阿贝折射仪(1台)烧杯(2个)1/10温度计(50~100℃)(1支)吸管(2支)擦镜纸乙酸乙酯(A.R.)无水乙醇(A.R.)不同比例的乙醇-乙酸乙酯混合液丙酮(C.P.)无水乙醇(A.R.)四、实验步骤(1)折射率-体积分数工作曲线取几滴纯乙醇、纯乙酸乙酯分别测定其折射率,两点作n D26−φ工作曲线(n-V)。
(2)折射率-摩尔分数工作曲线在n D26−φ线上取8个点,利用乙醇、乙酸乙酯密度合量比(%)等条件将以上点对应的体积分数换算成摩尔分数,按对应的折射率重新绘n D26−x点,再将点连成平滑曲线,即为n D26−x工作曲线(n-x)(3)溶液的沸点与平衡气-液相组成测定a)样品I-VI分别为乙醇体积分数为5%、15%、22%、38%、50%、90%的乙醇-乙酸乙酯混合液。


异丙醇—环己烷双液系相图一、实验目的:1.掌握回流冷凝法测定溶液沸点的方法。
2.绘制异丙醇—环己烷双液系的沸点—组成图,确定其恒沸组成及恒沸温度。
3.了解阿贝折射仪的构造原理,掌握阿贝折射计的原理及使用方法。
二.基本原理:根据相律:f + φ = c + 2 ,对二组分体系:f = 4 - φ,f max = 3 (T,P,x)。
对于二组分体系,常常保持一个变量为常量,而得到立体图形的平面截面图。
这种平面图可以有三种:p-x图,T-x图,T-p图。
常用的是前两种。
在平面图上,f*=3-φ,f*max=2,同时共存的相数φmax=3。
单组分的液体在一定外压下,它的沸点是一定值,把两种完全互溶的挥发性液体(组分A 和B)互相混合后,在某一定温度下,平衡共存的气液两相的组成,通常并不相同,因此如果在恒压下将溶液蒸馏,测定馏出物(气相)和蒸馏液(液相)的折射率,就能找出平衡时气液两相的成分,并绘出沸点—组成(T—x)图线,在常温下,两种液态物质以任意比例相互溶解所组成的体系称之为完全互溶双液系。
完全互溶双液系在恒定压力下的沸点—组成图可分为三类:(1)溶液沸点介于两纯组分沸点之间(如图1),(2)溶液存在最低沸点(图2)和(3)溶液存在最高沸点(图3)。
(2)、(3)被称为具有恒沸点的双液系,即体系处于恒沸点时气、液两相的组成相同,其相应的溶液称为恒沸点混合物。
此时对恒沸点混合物进行蒸馏,所得气相与液相组成相同,因此我们不能用普通蒸馏方法获得任一纯组分。
异丙醇—环己烷双液系属于具有最低恒沸点一类的体系。
T—x图在进行蒸馏或分馏时是必不可少的,而分馏在提纯溶剂和石油工业中也得到广泛应用,所以这种图是具有很大的实用价值的。
本实验的目的就是要绘制异丙醇—环己烷的T—x图并找出恒沸点混合物的组成。
1.沸点—组成图的绘制为了绘制沸点—组成图,可采取不同的方法。
在本实验中,我们采用的是一种物理方法—通过折射率的测定,来间接的获取溶液组成,它具有简捷、准确的特点。



大学生化学实验技能竞赛笔试试题一、单项选择题(共35小题,每小题2分,共70分)1、用阿贝折光仪测量液体折射率时,操作中不正确是()_。
A、应将样品缓慢而均匀地滴在棱镜镜面上B、折光仪的零点事先应当用标准液进行校正C、应调节补偿镜使视场内呈现清晰的明暗界线D、折光仪应与超级恒温槽串接以保证恒温测量2、双液系沸点-组成图绘制实验中根据哪一个物理量确定溶液组成:()。
A、旋光度B、吸光度C、折光率三氯甲烷-醋酸-水三液系相图的绘制D、电导率3、重量分析中沉淀的溶解损失所属误差的是()CA、过失误差B、操作误差C、系统误差D、随机误差4、量取25.00ml盐酸溶液,该选用实验室中常用哪种仪器()A、25mL量筒B、移液管(25.00mL)C、100mL量筒D、50ml烧杯5、对于用Gouy磁天平法测量物质磁化率实验,说法中不正确是()。
A、选用合适的标准物标定磁场强度B、实验中应缓慢加大励磁电流C、称量时,样品管应正好处于两个磁极之间,且其底部正好与磁极中心线齐平其它D、实验前在样品管中填充颗粒状的样品6、分光光度计检测器直接测定的是()A、散射光强度B、透过光强度C、吸收光强度D、折射光强度7、对沉降分析最大干扰有()。
A、粒子的聚结B、液体的对流C、包括A和BD、粒子颗粒大小不均8、在配位滴定中,用返滴法测定Al3+时,在pH=5~6,下列金属离子标准溶液中适用于返滴定过量EDTA的为()_________。
A、Mg2+B、Zn2+C、Bi3+D、Ag+9、由二氧化锰制锰酸钾,应选择的试剂是()CA、Cl2+KClB、王水+KClC、KOH+KClO3D、浓H2SO4+KClO310、以下试剂不能作为基准物质的是()A、优级纯金属锌B、100-110℃干燥Na2CO3C、优级纯Na2B4O7•5H2OD、100-110℃干燥K2Cr2O711、热重分析作出谱图不能()。
A、从质量变化的化学计量关系推测物质发生脱水、分解或氧化反应的产物B、定量说明物质的热稳定性C、确定物质发生相变、异构化反应等过程的温度D、确定物质发生脱水、分解或氧化反应的温度12、实验中正确配制0.2mol∙L-1Na2CO3溶液方法的是()A、用托盘天平称取5.72gNa2CO3∙10H2O于100mL烧杯中,加100mL蒸馏水、搅拌溶解。

双液体系气—液平衡相图的绘制一、实验目的1. 绘制环己烷—异丙醇双液体系的沸点组成图,确定其恒沸组成和恒沸温度。
2. 掌握回流冷凝管法测定溶液沸点的方法。
3.掌握阿贝折射仪的使用方法。
二、实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不 同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
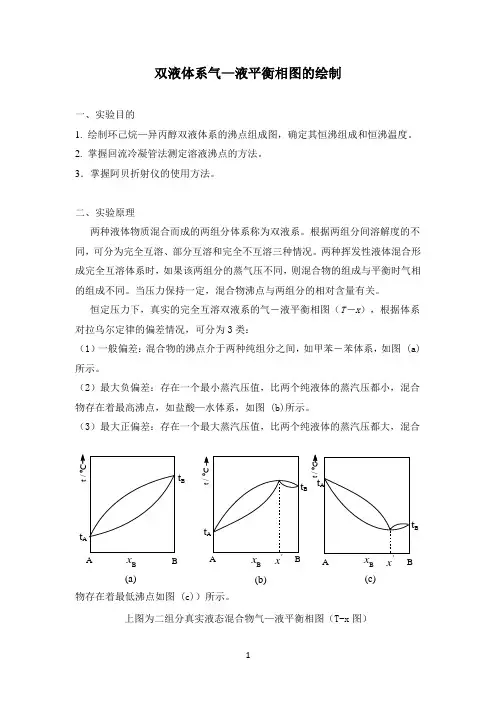
恒定压力下,真实的完全互溶双液系的气-液平衡相图(T -x ),根据体系对拉乌尔定律的偏差情况,可分为3类:(1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图 (a)所示。
(2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸—水体系,如图 (b)所示。
(3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合物存在着最低沸点如图 (c))所示。
上图为二组分真实液态混合物气—液平衡相图(T-x 图)t At AtAt Bt B t Bt / o Ct / o t / o x Bx Bx BABAABB(a)(b)(c)x 'x '后两种情况为具有恒沸点的双液系相图。
它们在最低或最高恒沸点时的气相和液相组成相同,因而不能象第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离出一种纯物质和另一种恒沸混合物。
为了测定双液系的T-x相图,需在气-液平衡后,同时测定双液系的沸点和液相、气相的平衡组成。
本实验以环己烷-异丙醇为体系,该体系属于上述第三种类型,在沸点仪中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T-x相图。
本实验中两相的成分分析均采用折光率法测定。
三、仪器与试剂1、仪器:沸点仪1台;调压变压器1台;阿贝折射仪1台;温度计(0-100℃) 1支;长滴管1个;短滴管2支;2、试剂:环己烷(分析纯);异丙醇(分析纯)异丙醇—环己烷标准溶液(异丙醇分别为0.20,0.40,0.50,0.60,0.80,0.90)四、主要实验步骤1. 测定环己烷、异丙醇及标准溶液的折射率调节阿贝折射仪,用一支干燥的短滴管吸取环己烷数滴,注入折射仪的加液孔内,测定其折射率n,读数两次,取其平均值。

实验六完全互溶双液体系沸点~组成图的绘制一、实验目的1.了解溶液的沸点与气液二相组成的关系;2.绘制环己烷-异丙醇溶液的沸点~组成图;3.进一步理解分馏原理;4.掌握阿贝折光仪的正确使用方法。
二、基本原理液体的沸点是液体的饱和蒸气压与外压相等时的温度。
在一定的外压下,单一组分的液体有确定的沸点值,对于一个完全互溶的双液体系,沸点不仅与外压有关,还和液体的组成有关。
在常温下,具有挥发性的A和B两种液体以任意比例相互溶解所组成的物系,在恒定压力下表示该溶液沸点与组成关系的相图称之为沸点~组成图,即T ~x图。
完全互溶双液体系在恒压下的沸点~组成图大致可分为以下三类。
图6-1简单互溶双液体系的T~x图图6-2具有最高恒沸点的T~x图图6-3具有最低恒沸点的的T~x图第Ⅰ类:溶液沸点介于两纯组分沸点之间,如苯与甲苯的混合体系,其沸点~组成图如图6-1所示。
此类溶液在恒压下蒸馏时,其气相组成和液相组成并不相同,具有较低蒸气压的液体(B)在气相中的组成X B(g)总是小于在液相中的组成X B(l),因此可以通过反复蒸馏——精馏,使互溶的二组分完全分离。
第Ⅱ类:溶液具有最高恒沸点,如卤化氢和水、丙酮与氯仿等,其沸点~组成图如图6-2所示。
第Ⅲ类:溶液具有最低恒沸点,如苯与乙醇、乙醇与水、环己烷与异丙醇、环己烷与乙醇、乙醇与1,2-二氯乙烷等,其沸点~组成图如图6-3所示。
在第Ⅱ、Ⅲ类的T ~x图中,出现极值点(极大值或极小值),在极值点处加热蒸发时,只能使气相的总量增加,气液相组成及沸点均保持不变,此点的温度称为恒沸点。
在恒沸点时,气相的组成与液相的组成相同,称为恒沸组成。
而具有此组成的混合物称为恒沸混合物。
对于Ⅱ、Ⅲ两类溶液,简单的反复蒸馏只能获得某一纯组分和恒沸混合物,而不能同时得到两种纯组分。
恒沸点和恒沸混合物的组成与外压有关,改变外压可使恒沸点和恒沸混合物的组成发生变化。
本实验环己烷与异丙醇的混合物属于第Ⅲ类溶液,具有最低恒沸点。

双液系沸点-组成图测绘实验报告实验时间:2015年4月15日学号:1120132970 一、目的要求1.测定相应组成时的沸点并制作常压下环已烷—无水乙醇双液系的平衡相图。
2.从沸点组成图了解分馏原理。
3.了解沸点的测定技术,掌握两组分液体沸点的测定方法。
4.掌握折光率与组成的关系及阿贝折光仪的测量原理和使用方法。
二.实验原理1、由液态物质混合而成的二组分系统称为双液系统。
若两液体能以任意比例互溶,称其为完全互溶双液系,若两液体只能部分互溶,称其为部分互溶双液系。
一个完全互溶的二元体系,两个纯液体组分在所有组成范围内完全互溶。
在定压下,完全互溶的二元体系的沸点—组成图可分为三类,如图C7.1所示。
a.溶液的沸点介于两纯组分沸点之间,如苯一甲苯体系;b.溶液有最低恒沸点,如环己烷-乙醇体系;c.溶液有最高恒沸点,如丙酮—氯仿体系。
下面以a为例,简单说明绘制沸点-组成图的原理。
加热总组成为x1的溶液,体系的温度上升,达液相线上1点时溶液开始沸腾,组成为x2的气相开始生成,但气相量很少,趋于0,x1、x2二点代表达到平衡时液、气两相组成。
继续加热,气相量逐渐增多,沸点继续上升,气、液二相组成分别在气相线和液相线上变化,当达某温度(如2点)并维持温度不变时,则x3、x4为该温度下液、气两相组成,气相、液相的量之比按杠杆规则确定。
从相律f = c - p +2可知:当外压恒定时,在气、液两相共存区域自由度等于1;当温度一定时,则气、液两相的组成也就确定,总组成一定,由杠杆规则可知两相的量之比也已确定。
因此,在一定的实验装置中,全回流的加热溶液,在总组成、总量不变时,当气相的量与液相的量之比也不变时(达气-液平衡),则体系的温度也就恒定。
分别取出气、液两相的样品,分析其组成,得到该温度下气、液两相平衡时各相的组成。
改变溶液总组成,得到另一温度下气、液两相平衡时各相的组成。
测得溶液若干总组成下的气液平衡温度及气、液相组成,分别将气相点用线连接即为气相线,将液相点用线连接即为液相线,得到沸点-组成图。
实验名称:二组分溶液沸点——组成图的绘制班级:09级应化一班 学号:0120 报告人:裴哲民同组人:匡江梅,李琪瑶,潘齐常,陈斌,梁细莲 实验时间:2011年9月16日 辅导老师:李传华 一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
二. 基本原理在一定的外压下,纯液体的沸点是恒定的,但对于完全互溶双液系,沸点不仅与外压有关,而且还与其组成有关,并且在沸点时,平衡的气-液两相组成往往不同。
根据相律:F=C-P+2,一个气液共存的二组分体系,其自由度为2,只需再任意确定一个变量,其自由度就减为1,整个体系的存在状态就可以用二维图来描述。
本实验中采用在一定压力下,作出体系的温度T 和组分x 的关系图,即T-x 图。
完全互溶体系的T-x 图可分为三类:①液体与Raoult 定律的偏差不大,在T-x 图上,溶液的沸点介于两种纯液体的沸点之间(图),如苯-甲苯系统;②由于两组分的相互作用,溶液与Raoult 定律有较大的负偏差,在T-x 图上存在最高沸点(图),如卤化氢-水系统;③ 溶液与Raoult 定律有较大的正偏差,在T-x 图上存在最低沸点(图),如乙醇-水系统。
②和③类溶液,在最高或最低沸点时的气-液两相组成相同,这些点称为恒沸点,此浓度的溶液称为恒沸点混合物,相应的温度称为恒沸温度,相应的组成称为恒沸组成。
本实验所要测绘的环己烷-乙醇体系即属于第二类溶液。
对于一个组成恒定的封闭系t/t/t/AAABBBx B (a ) x B (b ) 气气气液液液x B (c )统,当系统达到气液平衡温度时,气液两相的组成和温度恒定不变,以此便能得到该温度下的平衡气-液两相组成的一对坐标。
依次改变系统的组成就能得到一系列的平衡气-液两相组成坐标点,用光滑曲线连接即成相图。
实验所用的沸点仪结构如图2,冷凝管底部的小球用以收集冷凝下来的气相样品。
董 超 编 写实验六 双液系沸点-组成图的绘制【重要提示】环己烷-异丙醇溶液的浓度调整为:序号1 2 3 4 5 6%V 异丙醇10% 20% 35%50% 70% 85%一、实验原理部分书写要点1.二组分气-液平衡相图的概况及其特征(简单概括....); 2.本实验所涉及双液系的特点; 3.本实验绘制相图所使用的实验方法。
【注】:实验原理部分如果较长,可附页书写;物理化学实验教材另需预习内容:(1) Excel 常用函数 ④ round P 13(2) 金属电阻温度计P 131物理化学理论课相关内容:① §6.1 相律P 228 ② §6.4 二组分真实液态混合物的气-液平衡相图2.温度-组成图P 244二、实验原始数据记录室温:______________ 大气压:______________气相折光率gD n 及其测定温度T ∕℃液相折光率lD n 及其测定温度T ∕℃1 2 3 1 2 3 溶液序号T b ∕℃ gDn T g D nT g Dn T l Dn T l Dn T l D nT 1 2... ... ... ... ... ... ... ... ... ... ... ... ... (6)董 超三、实验数据处理要求1.计算气、液相折光率测定值的平均值,并根据环己烷-异丙醇双液系的温度系数41410Ddn dt−−=−×℃进行温度校正; 2.用Excel 软件对教材P 48的环己烷-异丙醇双液系的D x n −异丙醇数据进行二次多项式拟合,建立()D x f n =异丙醇的拟合方程;3.由()D x f n =异丙醇的拟合方程根据经过温度校正的折光率计算气、液相的平衡组成; 4.绘制环己烷-异丙醇双液系的沸点组成图; 5.根据相图确定恒沸点的相关数据:,b T 恒、x 异丙醇,恒,并作误差分析。
四、实验数据处理部分书写参考格式1.环己烷-异丙醇双液系的()D x f n =异丙醇拟合方程为:______(填入拟合方程表达式)_____2.折光率温度校正及气、液相平衡组成计算环己烷-异丙醇双液系的温度系数41410Ddn dt−−=−×℃编 写3.环己烷-异丙醇双液系沸点-组成图相图示例,b T 恒(实验)﹦_______,,b T 恒(文献)﹦_______ x 异丙醇,恒(实验)﹦_______,x 异丙醇,恒(文献)﹦_______恒沸点相对误差:,b T 恒68.6568.65−℃×100%=_________恒沸物组成相对误差:,0.410.41x −异丙醇恒×100%=_________【注】:环己烷-异丙醇双液系的D x n −异丙醇数据二次多项式拟合方法、相图的计算机绘制方法均见相应教程。
完全互溶双液系气液平衡相图的绘制一•实验目的1 •测定常压下环己烷—乙醇二元系统的气液平衡数据,绘制沸点—组成相图。
2•掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。
3•掌握阿贝折射仪的使用方法。
二.实验原理两种液体物质混合而成的两组分体系称为双液系。
根据两组分间溶解度的不同,可分为完全互溶、部分互溶和完全不互溶三种情况。
两种挥发性液体混合形成完全互溶体系时,如果该两组分的蒸气压不同,则 混合物的组成与平衡时气相的组成不同。
当压力保持一定,混合物沸点与两组分的相对含量有关。
恒定压力下,真实的完全互溶双液系的气一液平衡相图( T — X ),根据体系对拉乌尔定律的偏差情况,可分为3类:(1) 一般偏差:混合物的沸点介于两种纯组分之间,如甲苯一苯体系,如图2.7(a)所示。
(2 )最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸 —水体系,如图2.7(b)所示。
(3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合物存在着最低沸点如图 2.7(c))所示。
后两种情况为具有恒沸点的双液系相图。
它们在最低或最高恒沸点时的气相和液相组成相同,因而不 能象第一类那样通过反复蒸馏的方法而使双液系的两个组分相互分离,而只能采取精馏等方法分离岀一种 纯物质和另一种恒沸混合物。
为了测定双液系的 T —X 相图,需在气一液平衡后,同时测定双液系的沸 点和液相、气相的平衡组成。
本实验以环己烷一乙醇为体系,该体系属于上述第三种类型,在沸点仪(如 图2.8 )中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成, 即可作出T —X 相图。
本实验中两相的成分分析均采用折光率法测定。
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量 物质的折光率时要求温度恒定。
溶液的浓度不同、组成不同,折光率也不同。
因此可先配制一系列已知组成的溶液,在恒定温度下测其折光率,作岀折光 率一组成工作曲线,便可通过测折光率的大小在工作曲线上找岀未知溶液的 组成。