卫生部颁药品标准(新药转正标准中药第40册)
- 格式:doc
- 大小:260.50 KB
- 文档页数:38

新药转正标准
新药转正标准是指新药上市后,需要满足的一些标准,以确保新药的
安全、有效性和性价比。
新药转正标准涵盖了新药研究、开发、生产、质
量控制、文献分析、临床试验、安全性合规性、市场政策、价格策略等多
个方面。
1、新药研究和开发:要求新药的研究和开发过程具有严格的科学性、系统性和合理性,对化学药物的合成和生物药物的研制进行充分研究,确
定该药物的有效成分、活性指标和药效性等相关参数,确保新药的质量和
功能。
2、新药生产和质量控制:要求新药生产环节要求严格执行规范工艺,采用国家认可的先进技术和设备,确保新药生产过程的质量安全、有效性
和可靠性。
3、文献分析:要求新药的开发过程中要进行充分的文献分析,采用
最新研究成果,不断完善新药的开发技术,确保新药的可靠性。
4、临床试验:要求新药的临床试验缜密审慎,要符合GMP的质量管
理要求,要确保安全性和有效性,有效预防和控制新药对患者带来的风险。
5、安全性合规性:要求在新药上市前,要严格遵守国家关于药品安
全和合规性的法律法规,确保新药的安全性符合国家标准。

国家药品标准《新药转正标准》第77册至88册国家药典编委会主编规格:全12册大16开总定价:1920元优惠价:1180元国家药品标准《新药转正标准》第77册至88册新药转正标准77-88现货低价关于国家药品标准《新药转正标准》第77册至88册征订的通知本次汇编的转正标准共计587个品种(中药545个品种,化药42个品种),共分12册(77册至88册),并定于2011年9月5日前出版发行。
望从事药品科研、生产、检验单位及流通企业关注并认购。
该汇编定价为160元/册。
总定价:1920元国家药品标准《新药转正标准》第77册至88册国家药典编委会主编规格:全12册大16开总定价:1920元优惠价:1180元国家药品标准《新药转正标准》第77册至88册新药转正标准77-88现货低价关于国家药品标准《新药转正标准》第77册至88册征订的通知本次汇编的转正标准共计587个品种(中药545个品种,化药42个品种),共分12册(77册至88册),并定于2011年9月5日前出版发行。
望从事药品科研、生产、检验单位及流通企业关注并认购。
该汇编定价为160元/册。
总定价:1920元国家药品标准《新药转正标准》第77册至88册国家药典编委会主编规格:全12册大16开总定价:1920元优惠价:1180元国家药品标准《新药转正标准》第77册至88册新药转正标准77-88现货低价关于国家药品标准《新药转正标准》第77册至88册征订的通知本次汇编的转正标准共计587个品种(中药545个品种,化药42个品种),共分12册(77册至88册),并定于2011年9月5日前出版发行。
望从事药品科研、生产、检验单位及流通企业关注并认购。
该汇编定价为160元/册。
总定价:1920元国家药品标准《新药转正标准》第77册至88册国家药典编委会主编规格:全12册大16开总定价:1920元优惠价:1180元国家药品标准《新药转正标准》第77册至88册新药转正标准77-88现货低价关于国家药品标准《新药转正标准》第77册至88册征订的通知本次汇编的转正标准共计587个品种(中药545个品种,化药42个品种),共分12册(77册至88册),并定于2011年9月5日前出版发行。

新药转正中药标准卫生部颁药品标准(新药转正标准中药第一册)(15种)雌性柞蚕蛾拼音名:Cixingzuocane英文名:书页号:X1-27 标准编号:WS3-125(Z-31)-92(Z)批准文号:(90)卫药准字Z-19号本品为天蚕蛾科昆虫柞蚕Antheraea Pernyi Guerin-Meneville的未交配的雌性蚕蛾,经排尿、去翅、去足的干燥体。
【性状】本品由头、胸、腹三部分组成。
全身披覆深浅不同的黄褐色短毛。
体长约4cm,头部小,复眼一双,呈深褐色,口器退化,胸部由前胸、中胸、后胸三部组成腹部肥硕,末端较圆,可认出七个环节。
【鉴别】取本品4g,研细,加无水乙醇40ml,振摇5分钟,滤过,取滤液,加无水乙醇稀释至50ml,摇匀,吸取1ml置10ml量瓶中,加无水乙醇稀释至刻度,摇匀后照分光光度法(中国药典1990年版一部附录52页)测定,在269nm波长处有最大吸收。
【检查】水分取本品15g,照水分测定法(中国药典1990年版一部附录30页烘干法)测定。
不得过8%。
【炮制】除去杂质,粉碎成细粉。
【性味与归经】咸、温,归肝、肾经。
【功能与主治】补肾益肾,温脾助胃,宁心安神,调气活血。
用于调整内分泌紊乱。
【用法与用量】2~3g,入丸、散用。
【贮藏】置0~-10℃保存。
蛾苓丸拼音名:Eling Wan英文名:书页号:X1-29 标准编号:WS3-125(Z-31)-92(Z)批准文号:(90)卫药准字Z-19号本品为雌性柞蚕蛾等经加工制成的水丸。
【制法】以上药味,粉碎成细粉,混匀,用水泛丸,制成1000粒,烘干,用煅赭石粉挂衣,硅腊粉打光,即得。
【性状】本品为暗红色的水泛丸,除去外衣,显灰黄色或棕黄色;味甘。
【鉴别】(1) 取本品,置显微镜下观察:不规则分枝状团块无色,遇水合氯醛液溶化,菌丝无色或淡棕色,直径4~6μm,细长,稍弯曲有分枝。
(2) 取本品15粒,研细,加无水乙醇30ml,振摇提取5分钟,滤过,取滤液置50ml量瓶中,加乙醇稀释至刻度,摇匀,精密吸取1.0ml,置10ml量瓶中,加乙醇稀释至刻度,摇匀后照分光光度法(中国药典1990年版一部附录52页)测定,在269nm波长处有最大吸收。


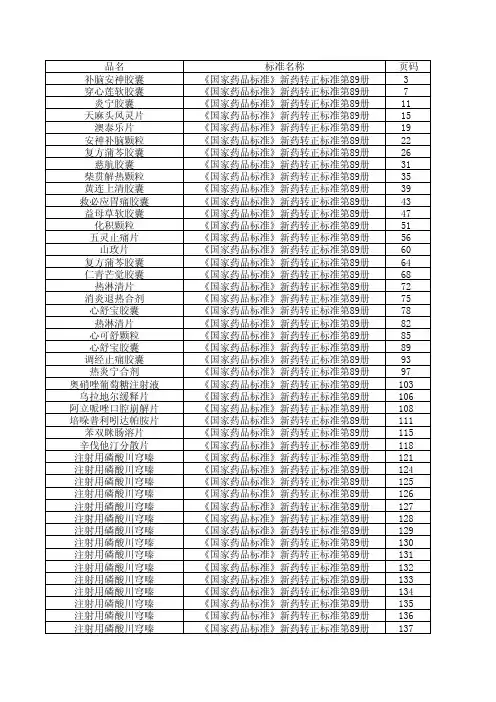
新药转正中药标准卫生部颁药品标准(新药转正标准中药第四十三册)(24种)保心宁胶囊拼音名:Baoxinning Jiaonang英文名:书页号:X43-45 标准编号:WS3-109(Z-99)-2003(Z)【处方】丹参干浸膏枳壳干浸膏当归干浸膏三七【性状】本品为胶囊剂,内容物为棕褐色的粉末?味苦、微涩。
【鉴别】取[含量测定]项下的供试品溶液相对照品溶液分别作为供试品溶液和对照品溶液。
另取丹参、枳壳、当归对照药材各1g,分别加乙醚40ml,置水浴上加热回流提取1小时,提取液挥干溶剂,残渣加乙醇1ml使溶解,分别制成丹参、枳壳、当归对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取上述五种溶液各2μl,分别点于同一硅胶G薄层板上,以甲苯-丙酮(95:5)为展开剂,展开,取出,晾干。
置日光下检视,供试品色谱中,在与对照品丹参酮ⅡA色谱相应的位置上,显相同的粉红色斑点。
在与丹参对照药材色谱相应的位置上,显相同的粉红色斑点。
置紫外光灯(365nm)下检视,供试品色谱中,在与对照品丹参酮ⅡA色谱相应的位置上,显相同的暗红色荧光斑点,在与丹参对照药材色谱相应的位置上,显相同的暗红色荧光斑点。
在与对照药材枳壳色谱相应的位置上,显相同的亮紫色荧光斑点。
在与对照药材当归色谱相应的位置上,显相同的亮蓝绿色荧光斑点。
【检查】应符合胶囊剂项下有关的各项规定(中国药典2000年版一部附录ⅠL)。
【含量测定】取本品4g,精密称定,置索氏提取器中,加乙醚40ml,在水浴上加热回流提取3小时,提取液回收乙醚致干,残渣加乙醇溶液至5ml量瓶中,并加乙醇稀释至刻度,作为供试品溶液。
另取丹参酮ⅡA对照品,精密用乙醇制成每1ml中约含1mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,精密吸取上述两种溶液各2μl,分别点于同一硅胶G薄层板上,以甲苯-丙酮(95:5)为展开剂,展开,取出,晾干。

卫生部颁药品标准新药转正西药标准卫生部颁药品标准(新药转正标准西药第八册)(15种)复方氯化钾颗粒拼音名:Fufang Lü huajia Keli英文名:Compound Potassium Chloride Granules书页号:X8-50 标准编号:WS1-(X-107)-96Z批准文号:(91)卫药准字X-158号本品含钾(K+)总量,按干燥品计,应为标示量的90.0~110.0%。
【处方】氯化钾 898g碳酸氢钾 137gL-赖氨酸盐酸盐 250g辅形剂适量矫味剂适量─────────────────────全量1600g【性状】本品为类白色或微黄色颗粒,加水溶解即有气泡产生。
【鉴别】(1)取本品约50mg,加水5ml使溶解,加茚三酮约5ml,加热即产生蓝紫色。
(2)取本品约1g,加水适量使溶解,加稀硫酸即泡沸,发生二氧化碳气;此气通入氢氧化钙试液中,即发生白色沉淀。
(3)本品的水溶液显钾盐与氯化物(中国药典1995年版二部附录Ⅲ)的鉴别反应。
【检查】总氯量取本品约0.3g,精密称定,加水50ml使溶解,再加糊精溶液(1→50)5ml与荧光黄指示液8滴,用硝酸银滴定液(0.1mol/L)滴定至溶液由黄绿色变为微红色。
每1ml的硝酸银滴定液(0.1mol/L)相当于3.545mg的Cl。
本品含氯量应为26.7~32.7%。
干燥失重取本品,在60℃减压干燥至恒重,减失重量不得过4.0%(中国药典1995年版二部附录ⅧL)。
其他应符合颗粒剂项下有关的各项规定(中国药典1995年版二部附录ⅠN)。
【含量测定】对照溶液的制备精密称取105℃干燥至恒重的氯化钾0.2g,置500ml量瓶中,加水适量使溶解,并稀释至刻度,摇匀,精密量取上述溶液25ml,置100ml量瓶中,加水至刻度,摇匀,精密量取0.2、0.4、0.6、0.8、1.0ml,分别置25ml量瓶中,加水至刻度,摇匀。
供试品溶液的制备取本品10包,精密称定,研细,精密称取适量(约相当于钾1g)置1000ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取10ml,置100ml量瓶中,加水稀释至刻度,摇匀。

第一章绪论习题一、选择题【A型题】1.以中医药理论为指导,运用现代科学技术,研究中药药剂的配制理论、生产技术、质量控制与合理应用的综合性应用技术科学,称为A.中成药学 B.中药制剂学 C.中药调剂学 D.中药药剂学 E.工业药剂学2.研究中药方剂调配技术、理论和应用的科学,称为A.中成药学 B.中药制剂学 C.中药调剂学D.中药药剂学 E.中药方剂学3.《药品生产质量管理规范》的简称是A.GMP B.GSP C.GAP D.GLP E.GCP4.非处方药的简称是A.WTO B.OTC C.GAP D.GLP E.GCP5.《中华人民共和国药典》第一版是A.1949年版 B.1950年版 C.1951年版 D.1952年版 E.1953年版6.中国现行药典是A.1977年版 B.1990年版 C.1995年版 D.2000年版E.2005年版7.《中华人民共和国药典》是A.国家组织编纂的药品集B.国家组织编纂的药品规格标准的法典C.国家食品药品监督管理局编纂的药品集D.国家食品药品监督管理局编纂的药品规格标准的法典E.国家药典委员会编纂的药品集8.世界上第一部药典是A.《佛洛伦斯药典》 B.《纽伦堡药典》 C.《新修本草》D.《太平惠民和剂局方》 E.《神农本草经》9.药品生产、供应、检验及使用的主要依据是A.药品管理法 B.药典 C.药品生产质量管理规范D.药品经营质量管理规范 E.调剂和制剂知识10.药材在进行提取或用于直接入药前所进行的挑选、洗涤、蒸、炒、焖、煅、炙、烘干和粉碎等过程,称为A.中药制剂 B.中药制药 C.中药净化 D.中药纯化 E.中药前处理11.我国最早的制药技术专著《汤液经》的作者是A.后汉张仲景 B.晋代葛洪 C.商代伊尹 D.金代李杲 E.明代李时珍12.我国第一部由政府颁布的中药成方配本是A.《神农本草经》 B.《五十二病方》 C.《太平惠民和剂局方》 D.《经史证类备急本草》E.本草纲目13.将液体药剂分为溶液、胶体溶液、混悬液和乳浊液,属于A.按照分散系统分类 B.按照给药途径分类C.按照制备方法分类 D.按照物态分类 E.按照性状分类14.根据《局颁药品标准》将原料药加工制成的制品,称为A.调剂 B.药剂 C.制剂 D.方剂 E.剂型15.中药材经过加工制成具有一定形态的成品,称为A.成药 B.中成药 C.制剂 D.药品 E.剂型16.根据疗效确切、应用广泛的处方大量生产的药品称为A.成药 B.中成药 C.制剂 D.药品 E.药物17.对我国药品生产具有法律约束力的是A.《美国药典》 B.《英国药典》 C.《日本药局方》D.《中国药典》 E.《国际药典》18.《中华人民共和国药典》一部收载的内容为A.中草药 B.化学药品 C.生化药品 D.生物制品E.中药19.下列叙述中不属于中药药剂学任务的是A.吸收现代药剂学及相关学科中的有关理论、技术、方法B.完善中药药剂学基本理论C.研制中药新剂型、新制剂D.寻找中药药剂的新辅料E.合成新的药品20.最早实施GMP的国家是A.法国,1965年 B.美国,1963年 C.英国,1964年D.加拿大,1961年 E.德国,1960年【B型题】[21~24]A.1988年3月 B.659年 C.1820年 D.1498年E.1985年7月1日21.中华人民共和国卫生部正式颁布中国的第一部GMP是在22.第一部《中华人民共和国药品管理法》开始施行的时间是23.《美国药典》第一版颁布于24.世界上第一部全国性药典-—《新修本草》在中国颁布施行的年代是[25~28]A.处方 B.新药 C.药物 D.中成药 E.制剂25.用于治疗、预防和诊断疾病的物质称为26.根据《中国药典》、《国家食品药品监督管理局药品标准》或其他规定处方,将原料药加工制成的药品称为27.未曾在中国境内上市销售的药品称为28.医疗和药剂配制的书面文件称[29~32]A.《美国药典》 B.《英国药典》 C.《日本药局方》D.《国际药典》 E.《中国药典》29.B.P.是30.J.P.是31.U.S。

新药转正中药标准卫生部颁药品标准(新药转正标准中药第四册)(17种)大黄通便冲剂拼音名:Dahuang Tongbian Chongji英文名:书页号:X4-37 标准编号:WS3-049(Z-15)-93(Z)批准文号:(91)卫药准字Z-72号本品为大黄流浸膏经加工制成的冲剂。
【性状】本品为黄棕色颗粒;气清香,味甜、微苦涩。
【鉴别】取本品24g,加甲醇适量,置水浴上加热回流1小时,滤过,滤液浓缩至5ml。
照下述方法试验:(1) 取提取物约0.5g,加1%氢氧化钠溶液10ml,煮沸,放冷,滤过。
取滤液2ml,加稀盐酸数滴使呈酸性,加乙醚10ml,振摇,乙醚层显黄色,分取乙醚层,加氨试液5ml,振摇,乙醚层仍显黄色,氨液层显持久的樱红色。
(2) 取提取物约0.5g,置瓷坩锅中,坩锅上覆以载玻片,置石棉网上直火徐徐加热,至载玻片上呈现升华物后,取下载玻片,放冷,置显微镜下观察,有菱形针状、羽状和不规则状结晶,滴加氢氧化钠试液,结晶溶解,溶液显紫红色。
(3) 取提取物约0.5g,置水浴上蒸干,加水20ml使溶解,滤过,滤液加盐酸2ml,置水浴上加热30分钟,立即冷却,用乙醚20ml分2次提取,合并乙醚液,蒸干,残渣加氯仿1ml使溶解,作为供试品溶液。
另取大黄对照药材0.1g,加乙醇20ml,浸渍1小时,滤过,取滤液5ml,蒸干,残渣加水10ml、盐酸1ml,自“置水浴上加热30分钟”起同上制成对照药材溶液。
再取大黄酸对照品,加甲醇制成每1ml含1mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典1990年版一部附录57页)试验,吸取供试品溶液2μl、对照药材溶液和对照品溶液各4μl,分别点于同一含羧甲基纤维素纳为粘合剂的硅胶H薄层板上,以石油醚(30~60℃)-甲酸乙酯-甲酸(15:5:1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同的五个橙色荧光斑点;在与对照品色谱相应的位置上,显相同的橙色荧光斑点,氨熏后斑点变为红色。
卫生部关于颁布第三批中成药部颁标准的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 卫生部关于颁布第三批中成药部颁标准的通知(卫药发[91]第28号)各省、自治区、直辖市、计划单列市卫生厅(局):“《中华人民共和国卫生部药品标准》(中药成方制剂第三册)”已由卫生部药典委员会审计完毕,现予颁布,并于1992年2月l日起正式执行。
有关重新登记注册等问题,请按我部卫药字[89]第28号“关于颁布第一批‘乙肝扶正胶囊’等一百七十种中成药卫生部药品标准的通知”执行。
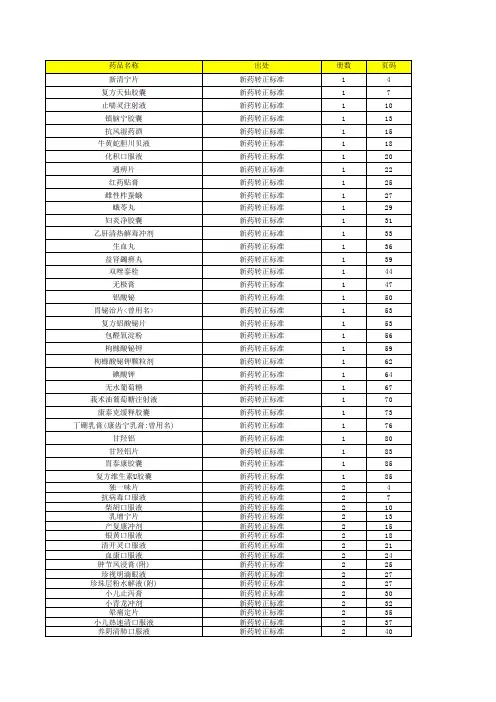
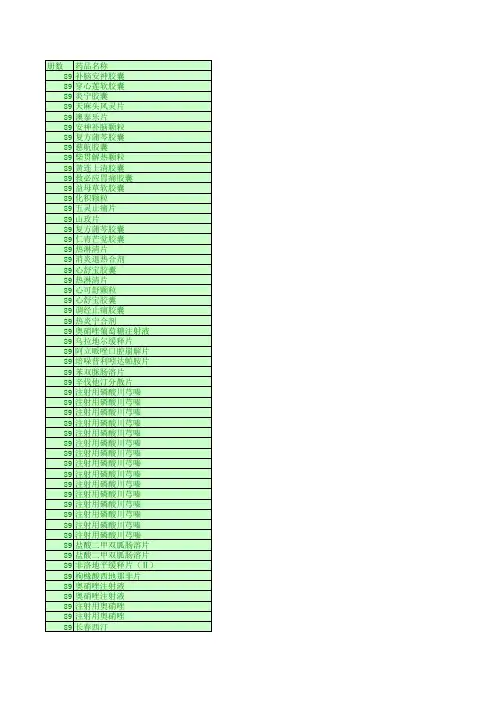
附件:中成药部颁品种批准文号卫生部统一编号卫生部一九九一年七月十八日附件:中成药部颁品种批准文号卫生部统一编号十全大补膏 ZZ-2457十香暖脐膏 ZZ-2458十滴水 ZZ-2459七制香附丸 ZZ-246O八宝玉枢丸 ZZ-2461八宝镇惊丸 ZZ-2462人参天麻药酒 ZZ-2464 九制香附丸 ZZ-2465九宝丸 ZZ-2466三七活血丸 ZZ-2467三宝胶囊 ZZ-2468三蛇胆川贝糖浆 ZZ-2469 下锭 ZZ-2470大枫子油 ZZ-2471山楂化滞丸 ZZ-2472山楂降压丸 ZZ-2473山楂调中丸 ZZ-2474川贝止嗽合剂 ZZ-2475 广羚散 ZZ-2476小儿四症丸 ZZ-2477小儿肝炎冲剂 ZZ-2478 小地抽风散 ZZ-2479小儿肺炎散 ZZ-2480小儿健脾散 ZZ-2481小儿清肺止咳片 ZZ-2482 五子衍宗片 ZZ-2491五更太平丸 ZZ-2492五香丸 ZZ-2493止血定痛片 ZZ-2494止咳定喘丸 ZZ-2495止痫散 ZZ-2496中满分消丸 ZZ-2497牛黄至宝丸 ZZ-2498牛黄消炎丸 ZZ-2499风火眼药 ZZ-2500风湿关节炎丸 ZZ-2502 风湿关节炎片 ZZ-2503 风湿灵片 ZZ-2504风湿药酒料 ZZ-2505 风湿镇痛丸 ZZ-2506 心安胶囊 ZZ-2507引阳索 ZZ-2508可利肝冲剂 ZZ-2509 龙脑安神丸 ZZ-2510 四红丹 ZZ-2511仙灵脾酒 ZZ-2512冬凌草片 ZZ-2513生乳汁 ZZ-2514白花蛇膏 ZZ-2515宁神定志丸 ZZ-2516 卫生散 ZZ-2483飞龙夺命丸 ZZ-2484 马钱子散 ZZ-2485天麻胶囊 ZZ-2486开光复明丸 ZZ-2487 开胃山楂丸 ZZ-2488 木香分气丸 ZZ-2489 长春红药片 ZZ-2490 倪疖膏 ZZ-2525伤科跌打丸 ZZ-2526 血宁片 ZZ-2527血宁胶囊 ZZ-2528舟车丸 ZZ-2529安阳虎骨药酒 ZZ-2530安阳精制膏 ZZ-2531安神补脑液 ZZ-2532关节止痛膏 ZZ-2533羊痫疯丸 ZZ-2534妇科乌金丸 ZZ-2535苁蓉补肾丸 ZZ-2536苓连片 ZZ-2537杏仁止咳冲剂 ZZ-2538抑亢丸 ZZ-2539抗栓再造丸 ZZ-2540抗痨胶囊 ZZ-2541肝舒片 ZZ-2542龟鹿滋肾片 ZZ-2543补血催生丸 ZZ-2544加味左金丸 ZZ-2517加味西黄丸 ZZ-2518耳炎药膏 ZZ-2519百咳宁片 ZZ-2520百梅止咳冲剂 ZZ-2521当归丸 ZZ-2522当归苦参丸 ZZ-2523壮腰健肾丸 ZZ-2524参桂鹿茸丸 ZZ-2563贴积膏 ZZ-2564复方五仁醇胶囊 ZZ-2565复方贝母散 ZZ-2566复方半夏片 ZZ-2567复方百部止咳冲剂 ZZ-2568 复方罗汉果止咳冲剂 ZZ-2569 复方虎杖片 ZZ-2570种子三达丸 ZZ-2572保幼化风丹 ZZ-2573保婴夺命散 ZZ-2574追风活络酒 ZZ-2575洋参保肺丸 ZZ-2576养血祛风丸 ZZ-2577宫糜膏 ZZ-2578祛暑片 ZZ-2579屏风生脉胶囊 ZZ-2580 降压平片 ZZ-2581珠珀保婴散 ZZ-2582补肾斑龙片 ZZ-2545阿胶益寿晶 ZZ-2546鸡骨草肝炎冲剂 ZZ-2547 武红灵散 ZZ-2548青果止嗽丸 ZZ-2549板蓝根片 ZZ-2550拔毒膏 ZZ-2551罗黄降压片 ZZ-2552固本延龄丸 ZZ-2553和中理脾丸 ZZ-2554乳疮丸 ZZ-2555河车补丸 ZZ-2556泻痢固肠片 ZZ-2557宝咳宁冲剂 ZZ-2558定喘膏 ZZ-2559参苓健脾丸 ZZ-2560参茸天麻酒 ZZ-2561参茸蛤蚧保肾丸 ZZ-2562通幽润燥丸 ZZ-2602梅苏丸 ZZ-2603菊明降压丸 ZZ-2604乾元丸 ZZ-2605接骨七厘片 ZZ-2606眼药锭 ZZ-2607婴儿安片 ZZ-2608得生片 ZZ-2609麻杏止咳糖丸 ZZ-2610 蚕茧眼药 ZZ-2583唇齿清胃丸 ZZ-2584柴黄片 ZZ-2585哮喘丸 ZZ-2586透表回春丸 ZZ-2587健儿疳积散 ZZ-2588健儿全鹿丸 ZZ-2589健胃片 ZZ-2590健康补脾丸 ZZ-2591健脾康儿片 ZZ-2592消瘿气瘰丸 ZZ-2593润肺化痰丸 ZZ-2594海龙胶 ZZ-2595海马万应膏 ZZ-2596益肝冲剂 ZZ-2597拳参片 ZZ-2598宽胸舒气化滞丸 ZZ-2599 调经活血片 ZZ-2600溃疡宁片 ZZ-2629寒喘丸 ZZ-2630强肾镇痛丸 ZZ-2632 蓝花药 ZZ-2633蒲公英片 ZZ-2634蒲地蓝消炎片 ZZ-2635 感冒止咳糖浆 ZZ-2636 感冒药片 ZZ-2637感冒咳嗽冲剂 ZZ-2638 痔疮外洗药 ZZ-2611 清肝片 ZZ-2612清胃和中丸 ZZ-613清暑益气丸 ZZ-2614 琥珀还晴丸 ZZ-2615 搜风顺气丸 ZZ-2616 搜风理肺丸 ZZ-2617 蛤蚧养肺丸 ZZ-2618 跌打止痛片 ZZ-2619 跌打风湿酒 ZZ-2620 遗尿散 ZZ-2621喘舒片 ZZ-2622舒郁九宝丸 ZZ-2623 舒络养肝丸 ZZ-2624 痢必灵片 ZZ-2625温脾止泻丸 ZZ-2626 温脾固肠散 ZZ-2627 清平宁冲剂 ZZ-2628 照山白浸膏片 ZZ-2639 愈风丹 ZZ-2640腮腺炎片 ZZ-2641缠喉散 ZZ-2642慢惊丸 ZZ-2644膏药咀 ZZ-2645精制银翘解毒片 ZZ-2646赛金化毒散 ZZ-2647增力再生丸 ZZ-2648醋制香附丸 ZZ-2649鹤草芽栓 ZZ-2650镇咳宁糖浆 ZZ-2651橘红梨膏 ZZ-2652磨积散 ZZ-2653藏青果冲剂 ZZ-2654顾狂马宝散 ZZ-2655囊虫丸 ZZ-2656——结束——。
新药转正标准
新药转正标准是指新药从临床试验阶段成功转化为市场上销售的标准。
新药的研发和上市是一个复杂而又严格的过程,其中新药转正标准是至关重要的一环。
本文将从药物临床试验、药物质量标准、药物生产工艺等几个方面来探讨新药转正标准的相关内容。
首先,药物临床试验是新药转正的重要环节。
临床试验是指在人体上进行的药物试验,其目的是评价药物的安全性和有效性。
在临床试验阶段,药物需要经历临床前研究、临床试验设计、临床试验执行和临床试验报告等多个环节。
只有经过严格的临床试验,并获得相关部门的批准,药物才能进入下一阶段的生产制造。
其次,药物质量标准也是新药转正的重要考量因素。
药物质量标准是指药物在生产过程中应符合的一系列标准和规定,包括药物的纯度、稳定性、溶解度等多个方面。
只有符合相关的药物质量标准,药物才能保证在生产和使用过程中的质量和安全。
此外,药物生产工艺也是新药转正的关键环节之一。
药物生产工艺是指药物从原料到成品的整个生产过程,包括原料的采购、生产工艺的设计、生产设备的选择等多个方面。
在药物生产工艺中,需要严格按照相关的法规和标准进行操作,确保药物的生产过程符合规范,从而保证药物的质量和安全。
综上所述,新药转正标准涉及到药物临床试验、药物质量标准、药物生产工艺等多个方面,是一个综合性的考量。
只有在这些方面都符合相关的标准和规定,新药才能成功转正并投放市场。
因此,对于新药的研发和上市,需要严格遵循相关的法规和标准,确保新药的质量和安全,为人们的健康提供保障。
根据药智网药品标准在线查询数据库整理1.中国药典中国药典2010年版一部中国药典2010年版二部中国药典2010年版三部中国药典2010年版一部勘误表中国药典2010年版二部勘误表中国药典2010年版三部勘误表中国药典2005年版一部中国药典2005年版二部中国药典2005年版三部中国药典2005版勘误一部中国药典2005版勘误二部2005药典增补本(2006)二部2005年药典增补(2009)中国药典2000年版一部中国药典2000年版二部2000年版2002年增补本2000年版2004年增补本2.国监局单页标准国监局单页标准(2000年前)国监局单页标准(2000)国监局单页标准(2001)国监局单页标准(2002)国监局单页标准(2003)国监局单页标准(2004)国监局单页标准(2005)国监局单页标准(2006)国监局单页标准(2007)国监局单页标准(2008)国监局单页标准(2009)国监局单页标准(2010)药典委员会勘误国家药品标准修订件药品检验补充检验方法和项目化学药品地标升国标16册化学药品地标升国标16册(修订)国药典综发(2006)3.中成药标准汇编 (地标升国标)内科肾系分册内科心系分册内科肺系分册骨伤科分册口腔肿瘤儿科分册内科肝胆分册内科脾胃分册内科气血津液分册脑系经络肢体分册外科妇科分册眼科耳鼻喉科皮肤科分册4.进口药品标准进口药复核标准汇编(2003)进口药品复核标准汇编2001年进口药品复核标准汇编2000年进口药品复核标准汇编2002年进口药品单页标准(2003)进口药品单页标准(2004)进口药品单页标准(2005)进口药品单页标准(2006)进口药品单页标准(2007)5.卫生部药品标准卫生部药品标准(二部)第一册卫生部药品标准(二部)第二册卫生部药品标准(二部)第三册卫生部药品标准(二部)第四册卫生部药品标准(二部)第五册卫生部药品标准(二部)第六册生化药品89年版第一册抗生素药品第一册<八九年>化学药品及制剂第一册藏药第一册蒙药分册维吾尔药分册6.中药成方制剂第一册第二册第三册第四册第五册第六册第七册第八册第九册第十册第十一册第十二册第十三册第十四册第十五册第十六册第十七册第十八册第十九册第二十册第二十一册(中药保护) 7.新药转正标准新药转正标准1新药转正标准2新药转正标准3新药转正标准4新药转正标准5新药转正标准6新药转正标准7新药转正标准8新药转正标准9新药转正标准10新药转正标准11新药转正标准12新药转正标准13新药转正标准14新药转正标准15新药转正标准16新药转正标准17新药转正标准18新药转正标准19新药转正标准20新药转正标准21新药转正标准22新药转正标准23新药转正标准24新药转正标准25新药转正标准26新药转正标准27新药转正标准28新药转正标准29新药转正标准30新药转正标准31新药转正标准32新药转正标准33新药转正标准34新药转正标准35新药转正标准36新药转正标准37新药转正标准38新药转正标准39新药转正标准40新药转正标准41新药转正标准42新药转正标准43新药转正标准44新药转正标准45新药转正标准46新药转正标准47新药转正标准48新药转正标准49新药转正标准50新药转正标准51新药转正标准52新药转正标准53新药转正标准54新药转正标准55新药转正标准56新药转正标准57新药转正标准58新药转正标准59新药转正标准60新药转正标准61新药转正标准62新药转正标准63新药转正标准64新药转正标准65新药转正标准66新药转正标准67新药转正标准68新药转正标准69新药转正标准70新药转正标准71新药转正标准72新药转正标准73新药转正标准74新药转正标准75新药转正标准768.化药地标升国标化学药品地标升国标1册化学药品地标升国标2册化学药品地标升国标3册化学药品地标升国标4册化学药品地标升国标5册化学药品地标升国标6册化学药品地标升国标7册化学药品地标升国标8册化学药品地标升国标9册化学药品地标升国标10册化学药品地标升国标11册化学药品地标升国标12册化学药品地标升国标13册化学药品地标升国标14册化学药品地标升国标15册化学药品地标升国标16册。
卫生部颁西药标准卫生部颁药品标准(二部第四册)(103种)阿司匹林栓拼音名:A※sipilin Shuan英文名:SUPPOSITORIA ASPIRINI书页号:E4-51 标准编号:本品含阿司匹林(C9H8O4)应为标示量的90.0~110.0%。
【性状】本品为乳白色或微黄色的栓剂。
【鉴别】取本品适量(约相当于阿司匹林0.6g),加乙醇20ml,微温溶解,置冰浴中冷却5分钟,并不断搅拌,滤过,滤液置水浴上蒸干,残渣照乙酰水杨酸项下的鉴别(中国药典1990年版二部4页)试验,显相同的反应。
【检查】游离水杨酸除检测波长改用300nm外,照含量测定项下的方法,取水杨酸对照品,用乙醇制成每1ml中含10μg的溶液,精密量取10μl,注入液相色谱仪,调节检测灵敏度,使水杨酸峰高在满量程的20%以上,精密量取含量测定项下供试品续滤液10μl,注入液相色谱仪,所得水杨酸相应保留时间的峰面积,不得大于对照品的峰面积,以阿司匹林计,含游离水杨酸不得过1.0%。
其他应符合栓剂项下有关的各项规定(中国药典1990年版二部附录7 页)。
【含量测定】照高效液相色谱法(中国药典1990年版二部附录34页)测定。
系统适用性试验用十八烷基硅烷健合硅胶为填充剂,甲醇-0.1%二乙胺水溶液-冰醋酸(40:60:4)为流动相,检测波长为280nm,理论板数按阿司匹林峰计算应不低于2000,阿司匹林峰、水杨酸峰和内标物质峰的分离度应符合要求。
校正因子测定取阿司匹林对照品约150mg,精密称定,置50ml量瓶中,精密加入内标溶液5ml(每1ml含咖啡因4mg的乙醇溶液),用乙醇溶解并稀释至刻度,摇匀。
精密量取2ml,置50ml量瓶中,用乙醇稀释至刻度,摇匀。
量取10μl注入液相色谱仪,计算校正因子。
供试品溶液的制备与测定取本品5粒,精密称定,置小烧杯中,在40~50℃水浴上微温熔融,在不断搅拌下冷却至室温,精密称出适量(约相当于阿司匹林150mg),置50ml量瓶中,精密加入内标溶液5ml和乙醇适量,在40~50℃水浴中充分振摇使供试品溶解,用乙醇稀释至刻度,置冰浴中冷却1小时,取出迅速滤过,精密量取续滤液2ml,置50ml量瓶中,用乙醇稀释至刻度,摇匀。
新药转正中药标准卫生部颁药品标准(新药转正标准中药第四十册)(25种)百艾洗液拼音名:Baiai Xiye英文名:书页号:X40-32 标准编号:WS3-213(Z-30)-2002(Z)【处方】苦参百部黄柏地肤子艾叶蛇床子枯矾冰片薄荷油【性状】本品为棕黄色的混悬液体,静置后有细微沉淀;气芳香,涂于皮肤上有清凉感。
【鉴别】(1)取本品40ml,用醋酸乙酯振摇提取3次,每次20ml,合并醋酸乙酯液,置水浴上蒸干,残渣加醋酸乙酯0.5ml使溶解,作为供试品溶液。
另取蛇床子素对照品,加无水乙醇制成每1ml含1mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取供试品溶液5μl、对照品溶液2μl,分别点于同一硅胶G薄层板上,以正己烷-醋酸乙酯(4:1)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。
(2)取本品4ml,置水浴上浓缩至约1ml,置离心管中,加无水乙醇1ml,摇匀,离心,取上清液作为供试品溶液。
另取黄柏对照药材0.1g,加无水乙醇5ml,置水浴上回流15分钟,滤过,滤液作为对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取上述两种溶液各2μl,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(7:1:2)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。
(3)取本品20ml,用石油醚(60~90℃)振摇提取3次,每次20ml,合并石油醚液,浓缩至约2ml,作为供试品溶液。
另取薄荷油对照品,加石油醚(60~90℃)制成每1ml含50μl的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以甲苯-醋酸乙酯(19:1)为展开剂,展开,取出,晾干,喷以2%香草醛硫酸溶液-乙醇(1:4)的混合溶液,在105℃加热至斑点显色清晰。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
(4)取本品10ml,加乙醚振摇提取2次,每次20ml,合并乙醚液,挥干,残渣加无水乙醇2ml使溶解,作为供试品溶液。
另取冰片对照品,加无水乙醇制成每1ml含2mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取供试品溶液4μl、对照品溶液2μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-苯-醋酸乙酯(9:2:1)为展开剂,展至约7cm,取出,晾干,再以石油醚(60~90℃)-苯-醋酸乙酯(6:1:1)为展开剂,展至约16cm,取出,晾干,喷以磷钼酸试液,置105℃加热至斑点显色清晰。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
【检查】相对密度应不低于1.01(中国药典2000年版一部附录ⅦA)。
pH值应为4.0~5.5(中国药典2000年版一部附录ⅦG)。
装量照最低装量检查法(中国药典2000年版一部附录ⅫC)检查,应符合规定。
微生物限度应符合阴道用制剂的规定(中国药典2000年版2002年增补本微生物限度检查法)。
【含量测定】照高效液相色谱法(中国药典2000年版一部附录ⅥD)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;乙腈-0.1%三氟醋酸溶液(7.5:92.5)为流动相;检测波长为204nm。
理论板数按苦参碱峰计算应不低于1500。
对照品溶液的制备精密称取苦参碱对照品适量,加上述流动相制成每1ml含70μg的溶液,即得。
供试品溶液的制备精密量取本品10ml,置100ml量瓶中,加水至刻度,摇匀,精密量取10ml,置具塞锥形瓶中,精密加氯仿30ml、浓氨试液1ml,密塞,称定重量,时时振摇,放置24小时后,再称定重量,用氯仿补足减失的重量,摇匀,分取氯仿层,精密量取15ml,置蒸发皿中,蒸干,残渣加上述流动相使溶解,转移至10ml量瓶中,并加流动相至刻度,摇匀,即得。
测定法分别精密吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。
本品每1ml含苦参以苦参碱(C15H24N2O)计,不得少于0.60mg。
【功能与主治】清热解毒,燥湿杀虫,祛风止痒。
用于湿热下注所致的阴痒,带下量多,尿频、急、数、痛,小便黄赤等,以及霉菌性阴道炎、滴虫性阴道炎、非特异性阴道炎、瘙痒等见上述证候者。
【用法与用量】外用,取本品20ml,加温开水稀释至200ml,制成洗液,用冲洗器冲洗或局部浸洗、坐浴,一日2次。
7天为一疗程,或遵医嘱。
【规格】每瓶装(1)100ml (2)200ml【贮藏】密封。
【有效期】3年参贝北瓜颗粒拼音名:Shenbei Beigua Keli英文名:书页号:X40-36 标准编号:WS3-388(Z-080)-2002(Z)【外方】北瓜清膏党参干姜浙贝母南沙参【性状】本品为黄棕色至深棕色的颗粒;气香,味甜、微辛。
【鉴别】(1)取[含量测定]项下的供试品溶液作为供试品溶液。
另取浙贝母对照药材2g,加浓氨溶液2ml和氯仿20ml,振摇,放置过夜,滤过,滤液蒸干,残渣加氯仿1ml使溶解,作为对照药材溶液。
再取贝母素甲、贝母素乙对照品,分别加氯仿制成每1ml含1mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取供试品溶液与对照药材溶液各8μl,对照品溶液各2μl,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以正己烷-醋酸乙酯-二乙胺(6: 4:1)为展开剂,两次展开,第一次展距7cm,第二次展距13cm,取出,晾干,喷以稀碘化铋钾试液。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,显相同颜色的斑点。
(2)取本品15g,加乙醚100ml,置水浴上加热回流1小时,滤过,弃去乙醚液,残渣置水浴上挥尽乙醚,加甲醇100ml,加热回流1小时,滤过,滤液蒸干,残渣加水30ml使溶解,用水饱和的正丁醇振摇提取3次(20、15、15ml),合并正丁醇提取液,用水洗涤3次(30、20、20ml),弃去水洗液,正丁醇液蒸干,残渣加无水乙醇1ml使溶解,作为供试品溶液。
另取干姜对照药材3g,加水60ml,加热回流1小时,滤过,滤液用水饱和的正丁醇振摇提取3次(20、15、15ml),合并正丁醇提取液,蒸干,残渣加无水乙醇1ml使溶解,作为对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取供试品溶液5μl、对照药材溶液2μl,分别点于同一硅胶G薄层板上,以苯-甲酸乙酯-甲醇(14:3: 0.5)为展开剂,展开,取出,晾干,喷10%硫酸乙醇溶液,加热至斑点显色后立即分别置紫外光灯(365nm)和日光下检视。
供试品色谱中,在与对照药材色谱相应的位置上,紫外光下显相同颜色的荧光主斑点,日光下显相同颜色的主斑点。
【检查】应符合颗粒剂项下有关的各项规定(中国药典2000年版一部附录ⅠC)。
【正丁醇提取物】取本品约2g,称定重量,置100ml锥形瓶中,精密加入水饱和的正丁醇50ml,密塞,称定重量,静置1小时,超声处理20分钟,放冷,再称定重量,用水饱和的正丁醇补足减失的重量,摇匀,滤过,精密量取续滤液25ml,置已干燥至恒重的蒸发皿中,水浴蒸干,在105℃干燥3小时,移至干燥器中,冷却30分钟,迅速精密称定重量,计算,即得。
本品以干燥品计算,含正丁醇提取物不得少于8.5%。
【含量测定】取本品装量差异项下的内容物,研细,取25g,精密称定,置100ml烧杯中,用水60ml溶解,用浓氨溶液调节pH值至10~12,转移至分液漏斗中,烧杯用少量水分次洗涤,水洗液并入分液漏斗中,用氯仿振摇提取5次(40、40、30、30、20ml),合并氯仿提取液,用少量水洗涤2次,弃去水洗液,氯仿液置水浴上蒸干,残渣用少量氯仿溶解,加在碱性氧化铝柱(100~200目,2g,内径15mm)上,用氯仿-甲醇(50:1)的混合液80ml洗脱,收集洗脱液,蒸干,残渣用氯仿溶解使成1ml,作为供试品溶液。
精密称取在五氧化二磷干燥器中真空干燥24小时后的贝母素乙对照品,加氯仿制成每1ml含1mg的溶液,作为对照品溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,精密吸取供试品溶液6μl、对照品溶液1μl与3μl,分别交叉点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以正己烷-醋酸乙酯-二乙胺(8:4:1)为展开剂,两次展开,每次展距8cm,取出,晾干,在110℃烘约1小时,驱尽二乙胺,以稀碘化铋钾试液为显色剂浸板显色,取出,冷风吹干,在薄层板上覆盖同样大小的玻璃板,周围用胶布固定,照薄层色谱法(中国药典2000年版一部附录ⅥB 薄层扫描法) 进行扫描,波长:λ<[S]>=503nm,λ<[R]>=620nm,测量供试品吸收度积分值与对照品吸收度积分值,计算,即得。
本品每袋含浙贝母以贝母素乙(C27H43NO3)计,不得少于48μg。
【功能与主治】补脾益肺,止咳化痰。
用于肺脾气虚之咳嗽、痰多、气短、乏力等。
【用法与用量】开水冲服,一次8g,一日3次。
【规格】每袋装8g【贮藏】密封。
【有效期】2年儿感清口服液拼音名:Erganqing Koufuye英文名:书页号:X40-24 标准编号:WS3-602(Z-122)-2002(Z)【处方】荆芥穗薄荷化橘红黄芩紫苏叶法半夏桔梗甘草【性状】本品为棕黄色的澄清液体;气芳香,味微苦。
【鉴别】(1)取本品20ml,加石油醚(30~60℃)提取2次,轻轻振摇,每次25ml,合并石油醚液,挥散至1ml,作为供试品溶液。
另取化橘红对照药材1g,加70%乙醇25ml,超声处理15分钟,滤过,滤液蒸干,残渣加水10ml使溶解,加石油醚(30~60℃)25ml,同法制成对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以正己烷-醋酸乙酯(17:4)为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。
(2)取荆芥穗、薄荷各1.5g,混匀,照挥发油测定法(中国药典2000年版一部附录ⅩD),加入石油醚(60~90℃)1ml,缓缓加热至沸,并保持微沸2小时,放冷,取石油醚液作为对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录ⅥB)试验,吸取[鉴别](1)项下的供试品溶液与上述对照药材溶液各10μl,分别点于同一硅胶G薄层板上,以正己烷-醋酸乙酯(17:3)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,在105℃加热至斑点显色清晰。