原电池电动势与电极电位
- 格式:ppt
- 大小:771.50 KB
- 文档页数:47

原电池电动势的测定一、 实验目的1、测定Cu —Zn 电池的电动势和Cu 、Zn 电极的电极电位。
2、了解可逆电池,可逆电极,盐桥等概念。
3、学会一些电极的制备和处理方法。
二、 实验原理电池由正、负两极组成。
电池在放电过程中,正极起还原反应,负极起氧化反应,电池内部还可以发生其它反应,电池反应是电池中所有反应的总和。
电池除可用来提供电能外,还可用它来研究构成此电池的化学反应的热力学性质。
从化学热力学知道,在恒温、恒压、可逆条件下,电池反应有以下关系:G nFE ∆=- (1)式中G ∆是电池反应的吉布斯自由能增量;n 为电极反应中得失电子的数目;F 为法拉第常数(其数值为965001C mol -⋅);E 为电池的电动势。
所以测出该电池的电动势E 后,进而又可求出其它热力学函数。
但必须注意,测定电池电动势时,首先要求电池反应本身是可逆的,可逆电池应满足如下条件:(1)电池反应可逆,亦即电池电极反应可逆;(2)电池中不允许存在任何不可逆的液接界;(3)电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电位。
在进行电池电动势测量时,为了使电池反应在接近热力学可逆条件下进行,采用电位计测量。
原电池电动势主要是两个电极的电极电势的代数和,如能测定出两个电极的电势,就可计算得到由它们组成的电池的电动势。
由(1)式可推导出电池的电动势以及电极电势的表达式。
下面以铜-锌电池为例进行分析。
电池表示式为:4142()()()()Zn s ZnSO m CuSO m Cu s ||||符号“|”代表固相(Zn 或Cu )和液相(4ZnSO 或4CuSO )两相界面;“‖”代表连通两个液相的“盐桥”;1m 和2m 分别为4ZnSO 和4CuSO 的质量摩尔浓度。
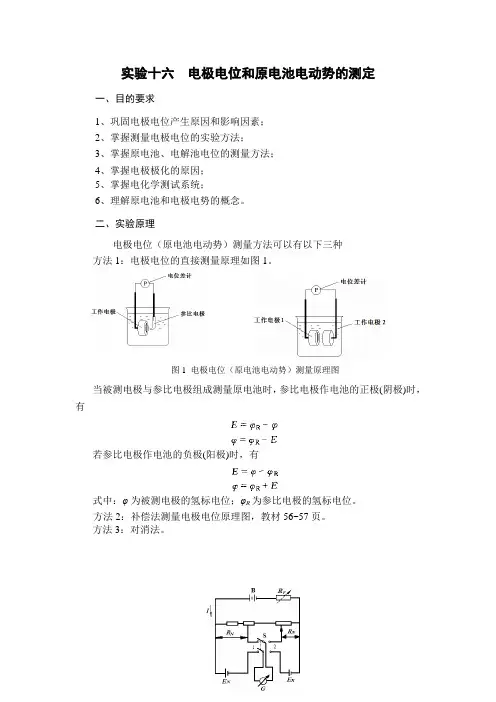
图1 电极电位(原电池电动势)测量原理图实验十六 电极电位和原电池电动势的测定一、目的要求1、巩固电极电位产生原因和影响因素;2、掌握测量电极电位的实验方法;3、掌握原电池、电解池电位的测量方法;4、掌握电极极化的原因;5、掌握电化学测试系统;6、理解原电池和电极电势的概念。
二、实验原理电极电位(原电池电动势)测量方法可以有以下三种方法1:电极电位的直接测量原理如图1。
当被测电极与参比电极组成测量原电池时,参比电极作电池的正极(阴极)时,有若参比电极作电池的负极(阳极)时,有式中:φ为被测电极的氢标电位;φR 为参比电极的氢标电位。
方法2:补偿法测量电极电位原理图,教材56~57页。
方法3:对消法。
图2 补偿法测量电极电位测量原理图对消法测定电动势就是在所研究的电极(电池)的外电路上加一个方向相反的电压。
当两者相等时,电路的电流为零(通过检流计指示)。
此时,所研究的电池的电动势就可以从外电路的电压数值读出。
原电池是由两个“半电池”组成,每个半电池中有一个电极和相应的溶液。
由不同的半电池可以组成各式各样的原电池,电池中的正极起还原作用,负极起氧化作用,电池的电动势等于两个电极电位的差值:左右ϕϕϕϕ-=-=-+E++++=a nF RT ln 0ϕϕ ---+=a nFRT ln 0ϕϕ 例如Cu-Zn 电池 Zn|ZnSO 4(a 1)||CuSO 4(a 2)|CuZn 的电极电位22201ln 2Zn Zn Zn Zn Zn RT F a ϕϕ+++=- Cu 的电极电位22201ln 2Cu Cu Cu Cu Cu RT F a ϕϕ+++=- Cu-Zn 电池的电动势为: ++++--=2222Cu n /Zn Zn 0Cu 0ln 2)(ααϕϕZ Cu /F RT E 三、仪器与药品 电化学测试系统 1套 饱和甘汞电极 1只盐桥 1个 电解池 1套Cu 电极片 1个 Fe 电极片 1个容量瓶 1个 量筒 1个广口瓶 3个 饱和KCl 溶液CuSO4(0.1mol.L-1)溶液 CuSO4(0.01mol.L-1)溶液NaCl (0.1mol.L-1)溶液四、实验步骤图4 工作电极的结构示意图 1、电极制备工作电极表面要平整,不能出现尖角或台阶,这些结构将会影响电极电位的分布。

第9章电分析化学法导论【9-1】解释下列名词。
原电池,电解池,电池电动势,电极电位,液接电位,标准电位,条件电位,平衡电位,浓差极化,电化学极化,超电位,指示电极,参比电极,工作电极。
答:原电池:将化学能编为电能的装置。
电解池:将电能变为化学能的装置。
电池电动势:流过电池的电流为零或接近于零时两电极间的电位差,以E池表示。
电极电位:任何电极与标准氢电极构成原电池所测得的电动势作为该电极的电极电位。
液接电位:在两个组成不同或浓度不同的电解质溶液互相接触的液-液界面间所存在的一个微小的电位差,称为液体接界电位,简称液接电位。
标准电位:298.15K时,以水为溶剂,当氧化态和还原态活度等于1时的电极电位。
条件电位:由于电极电位受溶液离子强度、配位效应、酸效应等因素的影响,因此使用标准电极电位ϕ0有其局限性。
对于一个实际体系在某一特定条件下,该电对的氧化型总浓度和还原型总浓度均为1mol·.L-1时的实际电位的实际电位。
平衡电位:在一个可逆电极中,金属成为阳离子进入溶液以及溶液中的金属离子沉积到金属表面的速度相等时,反应达到动态平衡,亦即正逆过程的物质迁移和电荷运送速度都相同,此时该电极上的电位值称为平衡电极电位。
浓差极化:发生电极反应时,电极表面附近溶液浓度与主体溶液浓度不同所产生的现象称为浓差极化。
电化学极化:由于电极反应的速率较慢而引起的电极电位对平衡电位值的偏离现象。
超电位:由于极化,使实际电位和可逆电位之间存在差异,此差异即为超电位η。
指示电极:用于无电极反应发生的平衡体系或在测量过程中溶液浓度不发生可觉察变化体系的电极。
参比电极:在测量过程中其电极电位几乎不发生变化的电极。
工作电极:有电极反应发生电极表面溶液浓度随电极反应发生显著变化体系的电极的电极。
【9-2】盐桥的作用是什么?对盐桥中的电解质溶液应有什么要求?答:盐桥的作用是尽可能降低液接电位。
盐桥电解质的要求是:(1)正、负离子的迁移速率大致相等(如KCl,KNO3, NH4NO3等),且可达到较高浓度;(2)与半电池中溶液不发生化学反应。


化学反应中的电极电势与电池电动势化学反应是一种涉及原子和分子之间重组的过程,而电池则是利用化学反应产生电能的装置。
电极电势和电池电动势是描述电化学反应中电子转移能力的重要参数。
本文将介绍电极电势和电池电动势的概念、影响因素以及它们之间的关系。
一、电极电势的概念与测量电极电势是指电极与溶液或气体之间的电势差。
在电化学反应中,电极上电子的转移产生电势差,进而影响反应的进行。
电极电势能够反映电子在电极上的活动程度,是判断电极是氧化还是还原的参数。
电极电势通常用标准电极电势(E°)来表示,单位为伏特(V)。
测量电极电势的方法有很多种,其中最常用的方法是通过比较电池。
比较电池由两个半电池组成,可以产生一个已知电势差的电池。
通过将待测电极与比较电池相连,测量它们之间的电势差,从而确定待测电极的电势差。
二、电极电势的影响因素1. 温度:电极电势随温度的变化而变化。
温度升高会导致电极电势升高或降低,具体取决于反应的热力学性质。
2. 浓度:电极电势与参与反应的物质浓度有关。
当参与反应的物质浓度发生改变时,电极电势也会发生变化。
3. 压力:对于气体电极,电极电势随气体的分压变化而变化。
增大气体分压会导致电极电势升高。
4. pH 值:对于溶液电极,电极电势会受到 pH 值的影响。
改变溶液pH 值能够改变电极电势。
三、电池电动势的概念与计算电池电动势是指电池两个电极之间的电势差,表征了电化学反应产生的电能。
电池电动势通常用电池电动势(Ecell)来表示,单位为伏特(V)。
计算电池电动势的方法是通过测量两个电极的电极电势,并利用Nernst 方程进行计算。
Nernst 方程是描述电极电势与反应物浓度之间关系的数学方程。
Ecell = E°cell - (RT/nF)ln(Q)其中,E°cell 是标准电动势,R 是气体常数,T 是温度,n 是电子转移的摩尔数,F 是法拉第常数,Q 是反应物的活度积。


电解池原电池电动势电势计算电解池是一种将化学能转化为电能的装置。
在电解池中,通过电解反应使电流产生,从而把化学能转化为电能,是化学电池中最常用的一种。
电解池的原电池电动势就是在标准状态下,由电解反应引起的电动势,是电解池中化学能转变为电能的能力。
下面是电解池原电池电动势的电势计算方法。
一. 原电池电动势的定义原电池电动势E0是指在标准活化状态下,以纯物质作氧化剂和还原剂,产生1mol电子时,电池中的电势差。
二. 标准电极电势的测定标准电极电势是指在标准条件下,电化学电池中氧化反应和还原反应中电子的转移系数都是1时所测定的电极电势,它是用标准电极强度计测定的。
三. 标准电动势计算公式标准电池电动势的计算公式是:E0cell = E0cathode - E0anode其中,E0cell是标准电池电动势,E0cathode是还原电极的标准电极电势,E0anode是氧化电极的标准电极电势。
对于化学方程式2H+ + 2e− → H2,它的标准电极电势为0V。
对于化学方程式Cu2+ + 2e− → Cu,它的标准电极电势为+0.34V。
因此,铜/铜离子电池的标准电池电动势为:E0cell = E0cathode - E0anode = 0V - (+0.34V) = -0.34V四. 温度影响对于每个化学电池来说,它的电动势都会随着温度的变化而变化。
五. 氧化还原电位氧化还原电位是一种描述氧化还原反应趋势的物理量。
在实际应用中,氧化还原电位的计算、测定与预测是很关键的。
六. 应用范围电解池原电池电动势的电势计算是电化学基础知识之一,它在工业、生物、医学、环保等领域都有着广泛的应用。
对于电解池中的原电池电动势,它的电势计算是非常重要的,只有通过电势计算才能确定电池的电势差,从而实现化学能和电能之间的转化。

原电池电动势的测定及应用实验报告实验目的1、学会Cu、Zn电极的制备和简单处理方法。
2、测定Cu-Zn原电池的电动势和Cu、Zn电极的电极电势。
3、掌握电位差计(包括数字式电子电位差计)的测量原理和正确使用方法。
实验原理电池电动势E的测定必须是在热力学可逆的条件下进行。
因此在测定时,首先要求被测电池反应本身是可逆的,即要求电池的电极反应是可逆的,并且不存在不可逆的液体接界,同时要求电池在放电或充电过程都必须在平衡态或无限接近平衡态下进行,即要求通过电池的电流无限小。
当一个可逆的化学反应是在无限缓慢的情况下进行时,就可以认为该电池的反应是在接近热力学可逆的条件下进行的。
而一个电池反应的快慢是以通过该电池电流的大小反映的,当通过电池的电流无限小时,则该可逆电池的反应就是在接近热力学可逆的情况下进行的。
为了使可逆电池在接近热力学可逆条件下进行,通常采用根据补偿法或称对消法(在外电路上加一个方向相反而电动势几乎相等的电池)设计的电位差计来测量电池的电动势。
液体接界电势的存在会破坏电池的可逆性,所设计的电池要尽量避免出现液接界,在精确度要求不高的测量中,常用“盐桥”来减小液接界电势。
电位差计(示意图如下),是利用补偿法测量直流电动势(或电压)的精密仪器,其工作原理如图所示:工作电源E,限流电阻R p,滑线电阻R AB构成辅助回路,待测电源E x(或标准电池E n),检流计G和R AC构成补偿回路。
按图中规定电源极性接入E、E x,双向开关K打向2,调节C点,使流过G中的电流为零。
(称达到平衡。
若E<E x或E、E x极性接反,则无法达到平衡),则E x=V AC=I R AC 即E x被电位差I R AC所补偿。
I为流过滑线电阻R AB的电流,称辅助回路的工作电流。
若已知I和R AC就可求出E x。
实际的电位差计,滑线电阻由一系列标准电阻串联而成,工作电流总是标定为一固定数值I0,使电位差计总是在统一的I0下达到平衡,从而将待测电动势的数值直接标度在各段电阻上(即标在仪器面板上),直接读取电压值,这称为电位差计的校准。

原电池电动势实验三 原电池电动势的测定和应用一、实验目的1、掌握用电化学工作站测定原电池电动势的原理和方法。
2、了解电动势测定的应用。
二、实验原理可设计成原电池的化学反应,发生失去电子进行氧化反应的部分可作为阳极,发生获得电子进行还原反应的部分可作为阴极,两个半电池组成一个原电池。
电池的书写习惯是左方为负极,即阳极,右方为正极,即阴极。
符号“|”表示两相界面,液相与液相之间一般加上盐桥,以符号“¦¦”表示,。
如电池反应是自发的,则其电动势为正,等于阴极电极电势+E 与阳极电极电势-E 之差,即 -+-=E E E以铜-锌电池为例。
铜-锌电池又称丹尼尔电池(Daniell cell ),是一种典型的原电池。
此电池可用图示表示如下:)1(114-⋅=-kg mol a ZnSO Zn +⋅=-Cu kg mol a CuSO )1(124左边为阳极,起氧化反应Zn e a Zn 2)(12++其电极电势为)()(ln 22+---==Zn a Zn a F RT E E E θ阳 右边为阴极,起还原反应e a Cu 2)(22++ Cu其电极电势)()(ln 22+++-==Cu a Cu a F RT E E E θ阴 总的电池反应)(22a Cu Zn ++ Cu a Zn ++)(12原电池电动势)()(ln 2)(22++-+--=Cu a Zn a F RT E E E θθ=)()(ln 222++-Cu a Zn a F RT E θ θ-E 、θ+E 分别为锌电极和铜电极的标准还原电极电势,)(2+Zn a 和)(2+Cu a 分别为 +2Zn 和+2Cu 的离子活度。
本实验所测定的三个电池为:1、原电池 饱和)()()(22K C l s Cl Hg l Hg - +⋅-)()01.0(33s Ag dm mol AgNO 阳极电极电势 )25/(106.72410.0//4/)(22-⨯-==--℃t V E V E H g s Cl H g阴极电极电势 )(ln //+++==++Ag a FRT E E E Ag Ag Ag Ag θ )25/(00097.0799.0//-⨯-=+℃t V E AgAg θ 原电池电动势 Hg s Cl Hg Ag Ag E Ag a FRT E E E E /)(/22)(ln -+=-=+-++θ2、原电池 )1.0()(3-⋅-dm mol KCl s AgCl Ag +⋅-Ag dm mol AgNO )01.0(33 阳极电极电势 )(ln /)(---=Cl a FRT E E Ag S AgCl θ )25/(000645.02221.0//)(-⨯-=℃t V E Ag S AgCl θ阴极电极电势 )(ln //+++==++Ag a FRT E E E Ag Ag Ag Ag θ 原电池电动势 [])()(ln /)(/+--++-=-=+Ag a Cl a F RT E E E E E Ag S AgCl Ag Ag θθ 其中 90.001.031=⋅±-γ的AgNO kg mol77.01.01=⋅±-γ的KCl kg mol稀水溶液中3-⋅dm mol 浓度可近似取1-⋅kg mol 浓度的数值。

第一章绪论1, 电化学:研究两类导体的界面现象以及上面发生的化学变化的一门科学2, 电化学反应:在两类导体界面间进行的有电子参加的化学反应.(电极反应)3 第一类导体:凡是依靠物体内部自由电子的定向运动而导电的物体,即载流子为自由电子(或空穴)的导体,叫做电子导体,也称第一类导体。
第二类导体:凡是依靠物体内的离子运动而导电的导体叫做离子导体,也称第二类导体。
4 电解质的分类:(1)弱电解质与强电解质—根据电离程度(2)缔合式与非缔合式—根据离子在溶液中存在的形态(3)可能电解质与真实电解质—根据键合类型5 法拉第定律: 电极上通过的电量与电极反应中反应物的消耗量或产物的产量成正比.法拉第定律成立的前提是:电子导体中不包含离子导电的成分,而离子导体中也不包含电子导电的成分。
电化当量:电极上通过单位电量所形成产物的质量.电流效率=当一定电量通过时,在电极上实际获得的产物质量/同一电量通过时根据法拉第定律应获得的产物质量第二章电解质溶液6离子水化:由于离子在水中出现而引起结构上的总变化。
离子水化影响双电层呵极化,离子水化影响电解质的扩散系数和活度系数,7水化热(焓):一定温度下,1mol自由气态离子由真空进入大量水中形成无限稀溶液时的热效应称为离子的水化热8水化膜:离子与水分子相互作用改变了定向取向的水分子性质,受这种相互作用的水分子层称为水化膜。
水化膜可分为原水化膜与二级水化膜。
9 水化数:水化膜中包含的水分子数。
主要指原水化膜(原水化数),但由于原水化膜与二级膜之间无严格界限,所以是近似值;是定性概念,不能计算与测量只有离子停留的时间大于水分子取向的时间才能形成原水化膜,离子电荷越多,半径越小,离子水化数越大。
物质粒子在溶液中的传质方式有三种:即电迁移,扩散和对流.10 离子在化学势梯度作用下的运动——扩散(稳态和非稳态)离子在电场作用下的运动——电迁移11离子间相互作用的离子氛理论离子氛的概念:由于中心离子的电场是球形的,故这一层电荷的分布也是球形对称的,我们将中心离子周围的这层电荷所构成的球体称为离子氛。

图1 电极电位(原电池电动势)测量原理图实验十六 电极电位和原电池电动势的测定一、目的要求1、巩固电极电位产生原因和影响因素;2、掌握测量电极电位的实验方法;3、掌握原电池、电解池电位的测量方法;4、掌握电极极化的原因;5、掌握电化学测试系统;6、理解原电池和电极电势的概念。
二、实验原理电极电位(原电池电动势)测量方法可以有以下三种 方法1:电极电位的直接测量原理如图1。
当被测电极与参比电极组成测量原电池时,参比电极作电池的正极(阴极)时,有若参比电极作电池的负极(阳极)时,有式中:φ为被测电极的氢标电位;φR 为参比电极的氢标电位。
方法2:补偿法测量电极电位原理图,教材56~57页。
方法3:对消法。
图2 补偿法测量电极电位测量原理图对消法测定电动势就是在所研究的电极(电池)的外电路上加一个方向相反的电压。
当两者相等时,电路的电流为零(通过检流计指示)。
此时,所研究的电池的电动势就可以从外电路的电压数值读出。
原电池是由两个“半电池”组成,每个半电池中有一个电极和相应的溶液。
由不同的半电池可以组成各式各样的原电池,电池中的正极起还原作用,负极起氧化作用,电池的电动势等于两个电极电位的差值:左右ϕϕϕϕ-=-=-+E++++=a nFRT ln 0ϕϕ---+=a nFRT ln 0ϕϕ例如Cu-Zn 电池 Zn|ZnSO 4(a 1)||CuSO 4(a 2)|Cu Zn 的电极电位22201ln2Zn Zn ZnZnZn RT Fa ϕϕ+++=-Cu 的电极电位22201ln2C u C u C uC uC u R T Fa ϕϕ+++=-Cu-Zn 电池的电动势为:++++--=2222Cun /ZnZnCu0ln2)(ααϕϕZ Cu/FRT E三、仪器与药品电化学测试系统 1套 饱和甘汞电极 1只 盐桥 1个 电解池 1套 Cu 电极片 1个 Fe 电极片 1个容量瓶 1个 量筒 1个 广口瓶 3个 饱和KCl 溶液CuSO4(0.1mol.L-1)溶液 CuSO4(0.01mol.L-1)溶液 NaCl (0.1mol.L-1)溶液 四、实验步骤图4 工作电极的结构示意图1、电极制备工作电极表面要平整,不能出现尖角或台阶,这些结构将会影响电极电位的分布。
原电池电动势的测定实验目的1.测定Cu—Zn电池的电动势和Cu、Zn电极的电极电位。
2.了解可逆电池、可逆电极、盐桥的概念。
3.学会一些电极的制备和处理方法。
4.掌握电位差计的测量原理和使用方法。
5.掌握简易电位差计的组装和使用。
实验原理Daniell电池 Zn|ZnSO4(C1)||CuSO4(C2)|Cu负极反应 Zn→Zn2+(αZn2+)+2e-正极反应 Cu2+(αZn2+)+2e-→Cu总电池反应 Zn + Cu2+(αCu 2+)→Zn2+(αZn2+)+ Cu反应的Δr Gm为ΔrGm=ΔrGΘm+RTln(αZn2+/αCu2+)Δr G m=-nFEΘ E=EΘ-RT/2Fln(αZn2+/αCu2+)E=φ+-φ-φ+=φΘCu2+-RT/2Fln(1/αCu2+)φ-=φΘZn2+-RT/2Fln(1/αZn2+)仪器与药品晶体管直流稳压电源1台,电阻箱(9999.9Ω)3个,指针检流计(10A)1台,双刀双掷开关1个,单刀双掷开关(带保护电阻)1个,标准电池1个,甘汞电极1个,铜电极2支,锌电极1支,电极管4支,50ml烧杯4只,饱和KCl溶液,0.1000mol*L-1 CuSO4溶液,0.0100mol*L-1 CuSO4溶液,0.1000mol*L-1 ZnSO4溶液,待测半电池若干个。
实验步骤1.按图接好线路,将R4调在1018.6Ω,R3调在581.4Ω,使R3+R4=1600Ω,接通直流稳压电源,双刀双掷开关掷向标准电池一边调节R2至检流计不偏转为止。
2.接上待测电池,双刀双掷开关掷向待测电池一边,R2保持不变,调整R3及R4。
直到检流计指针不偏转为止,记下读数。
注意:在调整R3及R4时。
应使R3+R4应使等于1600Ω。
将双刀双掷开关掷向待测电池一边,再次复查检流计是否偏转,若不偏转上述测定值可以使用,若有偏转须重调R2使之不偏转,然后掷向待测电池一边重复测定。
原电池电动势的测定及其应用I 、目的要求1、 测定Cu — Zn 电池的电动势和Cu Zn 电极的电极电位2、 了解可逆电池,可逆电极,盐桥等概念。
3、 学会一些电极的制备和处理方法。
U 、仪器与试剂NDM-1精密数字直流电压测定仪、标准电池(惠斯登电池)、铜棒电极,锌棒 电极、玻璃电极管2个、饱和甘汞电极(SCE 、洗耳球、小烧杯、细砂纸 、ZnSO4(0.100moldn -3),CuSO4(0.100 moldm -3) , KCI(O.1OO moldm -3),饱和 KCI 溶 液,稀硫酸、稀硝酸。
川、实验原理凡是能使化学能转变为电能的装置都称之为电池 的可逆电池而言:(△ r G m ) T , p = -Nfe,M[dT)p式中,F 为法拉弟(Farady)常数;n 为电极反应式中电子的计量系数;E 为电 池的电动势。
可逆电池应满足如下条件:(1) 电池反应可逆,亦即电池电极反应可逆。
(2) 电池中不允许存在任何不可逆的液接界。
(3) 电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦 即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度 不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电 位。
用电位差计测量电动势也可满足通过电池电流为无限小的条件。
可逆电池的电动势可看作正、负两个电极的电势之差。
设正极电势为 © +, 负极电势为©-,贝U: E=© +- © —电极电势的绝对值无法测定,手册上所列的电极电势均为相对电极电势, 即 以标准氢电极作为标准(标准氢电极是氢气压力为101325Pa,溶液中I 「为1), 其电极电势规定为零。
将标准氢电极与待测电极组成一电池, 所测电池电动势就 是待测电极的电极电势。
由于氢电极使用不便,常用另外一些易制备、电极电势 稳定的电极作为参比电极。