×100%
例: 25 0C时,0.1mol/L的CH3COOH 溶液中,C(H+)=1.0×10-3mol/L,求 该温度下CH3COOH的电离度?
影响电离度大小的因素: (1)内因:弱电解质本身的性质 (2)外因:
a.温度:
b.浓度:
[注意]讲一种弱电解质的电离度时,应 指出该电解质溶液的浓度和温度,如 不注明温度通常指25℃。
方法
醋盐 酸酸
对实验现象的解释
备注
比较浓度均为1mol/L的盐酸和醋酸的导电性 盐酸 溶液的pH 大 小 盐酸中氢离子浓度大 和醋 酸都 为等
与镁条反应 慢 快 盐酸中氢离子浓度大 浓度 的一 元酸
溶液的导电性 弱 强 盐酸中离子浓度大
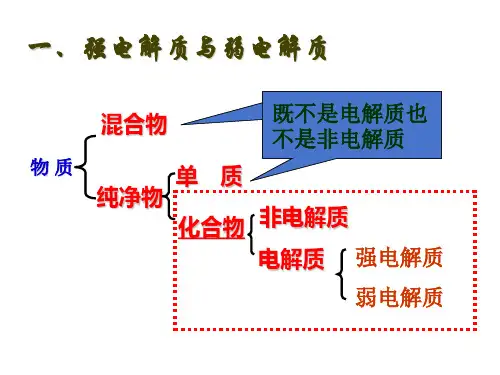
2.强电解质和弱电解质
强电解质
弱电解质
定义 溶于水后能够全部电 溶于水后只有部
强弱电解质的区分依据不是看该物质水溶性的大 小,也不是看其水溶液导电能力的强弱,而是看电 离的是否完全.
思考并讨论 1.难溶物一定是弱电解质吗?
2.强电解质溶液的导电能力一定强吗?
3.强电解质溶液的导电能力一定强于弱电解质吗? 4.强酸的酸性一定比弱酸强吗?
结论:电解质的强弱与 Ⅰ物质的溶解性无关, Ⅱ与导电能力无关
下列物质能导电的是_a_._c_.e_._,属
于强电解质的是_d_._h_.l_.o_,属于弱 电解质的是__i._j_.k_.m__._,属于非电
解质的是__f_.g_.___.
a.铜丝 b.金刚石 c.石墨 d.NaCl e.盐酸 f.蔗糖 g.CO2 h.Na2O i.硬脂酸 j.醋 酸 k.碳酸 l.碳酸氢铵 m.氢 氧化铝 n.氯气 o. BaSO4
电离程度 完全电离