核外电子排布和元素周期律
- 格式:ppt
- 大小:296.50 KB
- 文档页数:37

原子核外电子排布与元素周期律一、核外电子的排布规律⑴核外电子运动的特征:质量小,运动空间小,运动速度快,没有确定的轨道。
(2)电子云:电子在核外空间作高速运动,没有确定的轨迹,好象带负电荷的云雾笼罩在原子核的周围,人们形象地称之为电子云。
(3)电子层:根据电子的能量差别和通常运动区域离核的远近不同,核外电子处于不同的电子层。
(4)电子层排布倾向能量最低:核外电子总是尽先排布在能量最低的电子层里,然后由里往外,依次排布在能量逐步升高的电子层里。
(5)各电子层容纳的电子数:各电子层最多容纳的电子数是2n 2个,最外层电子数不超过8个(K 层不超过2个),次外层电子数不超过18个,倒数第三层不超过32个。
(6)电子层排布的表示方法:原子结构示意图1、排布规律⑴核外电子排布与能量关系电子离核距离: 近 → 远 电子能量: 低 → 高 ⑵核外电子的分层排布 ① 核外电子层能量不同 电子层离核距离: 近 → 远 电子能量: 低 → 高电子层数(n ): 1 (K) 2(L) 3 (M) 4 (N) 5 (O)② 电子排布规律Ⅰ 能量最低原理:先排满低能量电子层,再依次排布在能量较高的电子层中。
Ⅱ 各电子层最多容纳的电子数:2n 2 Ⅲ 最外层电子数≤8 Ⅳ 次外层电子数≤18 Ⅴ 倒数第三层电子数≤32注意:以上三条规律不是孤立的,而是相互制约,必须同时满足。
2、常见元素微粒结构特点稀有气体元素原子的电子层结构与同周期的非金属元素的阴离子的电子层结构相同,与下一周期的金属元素形成的阳离子的电子层结构相同。
如:(1)核外有2个电子微粒(与He 原子电子层结构相同的离子):H -、Li +、Be 2+ (2)核外有10个电子微粒(与Ne 原子电子层结构相同的微粒):阳离子:+Na 、+2Mg 、+3Al 、+4NH 、+O H 3;阴离子:N -3、O -2、F -、OH -、NH -2;分子:Ne 、HF 、H 2O 、NH 3、CH 4(3)核外有18个电子微粒(与Ar 原子电子层结构相同的微粒):离子:Cl -、S 2-、P 3-、K +、Ca 2+ 分子:Ar 、HCl 、H 2S 、SiH 4、H 2O 2、PH 3、C 2H 6 (4)前18号元素的原子构的特殊性○111 H ○2最外层有1个电子的元素:H 、Li 、Na ○3最外层有2个电子的元素:Be 、Mg 、He ○4最外层电子数等于次外层电子数的元素:Be 、Al 。

原子核外电子排布与元素周期律一、原子结构(Z 个)原子核注意:(N 个) 质量数(A)=质子数(Z)+中子数(N)1.X 原子序数= = =核外电子(Z 个)2.原子核外电子的排布规律:①电子总是尽先排布在能量 的电子层里;②各电子层最多容纳的电子数是 ;③最外层电子数不超过 个(K 层为最外层不超过 个),次外层不超过 个,倒数第三层电子数不超过 个。
电子层: 一(能量最低) 二 三 四 五 六 七 对应表示符号: 3.元素、核素、同位素元素: 。
核素: 。
同位素: 。
(对于原子来说) 二、元素周期表 1.编排原则:①按 递增的顺序从左到右排列 ②将 相同..的各元素从左到右排成一横行..。
(周期序数=原子的电子层数) ③把 相同..的元素按电子层数递增的顺序从上到下排成一纵行..。
=原子最外层电子数 2.结构特点:核外电子层数 元素种类第一周期 种元素短周期 第二周期 种元素周期 第三周期 种元素元 (7个横行) 第四周期 种元素 素 (7个周期) 第五周期 种元素 周 长周期 第六周期 种元素 期 第七周期 未填满(已有 种元素) 表 主族:ⅠA ~ⅦA 共7个主族族 副族:ⅢB ~ⅦB 、ⅠB ~ⅡB ,共7个副族 (18个纵行) 第Ⅷ族: 纵行,位于 之间 (16个族) 零族: ① 主族(A ):由 和 元素共同组成的族(除第18纵列)列序与主族序数的关系② 副族(B ):完全由 元素组成的族(第8、9、10纵列除外)③ Ⅷ族:包括 三个纵列。
④ 0族:第 纵列,该族元素又称为 元素。
三、元素周期律1.元素周期律: 。
元素性质的周期性变化实质是... 。
族碱金属元素: ( 是金属性最强的元素,位于周期表 ) 第ⅦA 族卤族元素: ( 是非金属性最强的元素,位于周期表 ) ★判断元素金属性和非金属性强弱的方法:(1)金属性强(弱)——① ;② ;③ 。
(2)非金属性强(弱)——① ;② ;③ 。
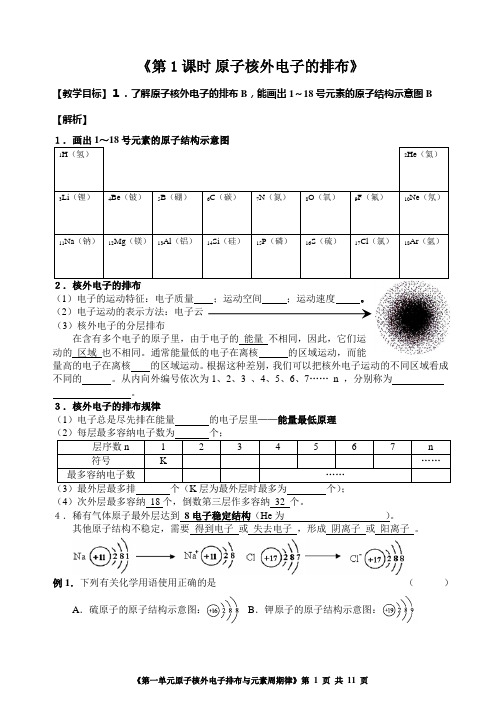
《第1课时原子核外电子的排布》【教学目标】1.了解原子核外电子的排布B,能画出1~18号元素的原子结构示意图B 【解析】(1)电子的运动特征:电子质量;运动空间;运动速度。
(2)电子运动的表示方法:电子云(3)核外电子的分层排布在含有多个电子的原子里,由于电子的能量不相同,因此,它们运动的区域也不相同。
通常能量低的电子在离核的区域运动,而能量高的电子在离核的区域运动。
根据这种差别,我们可以把核外电子运动的不同区域看成不同的。
从内向外编号依次为1、2、3 、4、5、6、7……n ,分别称为。
3.核外电子的排布规律(1)电子总是尽先排在能量的电子层里——能量最低原理)最外层最多排个(层为最外层时最多为个)(4)次外层最多容纳18个,倒数第三层作多容纳32 个。
4.稀有气体原子最外层达到8电子稳定结构(He为)。
其他原子结构不稳定,需要得到电子或失去电子,形成阴离子或阳离子。
例1.下列有关化学用语使用正确的是()A.硫原子的原子结构示意图:B.钾原子的原子结构示意图:C.氯离子的离子结构示意图:D.原子核内有10个中子的氧原子:《第1课时 原子核外电子的排布》练习1.下列有关Si 4214的说法不正确的是()A .Si 4214原子核内含有14个质子B .Si 4214的原子序数为14C .Si 4214的核外电子数为14D .Si 4214原子核内含有42个中子2.某微粒的核外电子的数目分别为:K 层2个,L 层8个,M 层8个,该微粒是( )A .氩原子B .钾离子C .氯离子D .无法确定3.某元素的原子核外有三个电子层,其最外层电子数是次外层电子数的一半,则此元素是( )A .SB .C C .SiD .Cl 4.下列表示式书写正确的是 ( )A .Cl -的结构示意图B .铝原子的结构示意图C .S 2-的结构示意图D .镁原子的结构示意图5.与Ne 的核外电子排布相同的离子是 ( )A .ClB .Na +C .K +D .S 2-6.某元素的原子最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为( )A .3B .7C .8 .D .107.元素A 的原子获得2个电子或元素B 的原子失去3个电子后,它们的电子排布均与氖原 子的电子排布相同。



原子核外电子排布和元素周期律原子是由原子核和围绕核运动的电子组成的。
原子核由质子和中子组成,而质子的数量决定了原子的元素。
原子核外的电子以不同的方式排布,这种排布决定了元素的化学性质。
元素周期律描述了元素的周期性变化规律,是化学中最重要的概念之一原子核外电子排布是描述电子在原子中的位置和能量分布的方式。
根据量子力学理论,电子存在于不同的能级上,每个能级可以容纳一定数量的电子。
根据波尔模型,原子的外层电子称为价电子,也是化学反应中参与原子间相互作用的电子。
原子核外电子排布可以通过倒易电子构型的方式来表示。
倒易电子构型表示了一个元素最外层电子的分布情况。
在倒易电子构型中,外层电子被表示为和最接近核心的壳层相同的能级。
例如,石墨的原子核是由6个质子和6个中子组成的,其倒易电子构型为1s²2s²2p²。
这意味着石墨的最外层电子是在2p轨道上的。
在倒易电子构型中,电子的分布遵循普遍原则、泡利不相容原理和阜居规则。
普遍原则指出,电子首先填充能量最低的轨道。
泡利不相容原理指出,一个轨道上最多只能容纳两个电子,并且这两个电子的自旋方向必须相反。
阜居规则指出,当填充轨道时,电子会尽量选择不同的轨道来填充,以最小化库伦排斥力。
元素周期律是根据元素的原子核中质子的数量和原子核外电子的排布,将元素按照一定规律排列的表格。
最早的元素周期表是由门捷列夫于1869年提出的。
现代元素周期表按照亨利·莫西里夫在1913年提出的核电荷排列。
元素周期表按照原子序数的增加顺序列出了所有已知元素。
原子序数是指原子核中质子的数量,也是元素周期表中元素的核电荷。
元素周期表的每一行称为一个周期,原子序数在周期内逐渐增加。
元素周期表的每一列称为一个组,元素周期表中的元素按照相似的性质分布在同一组中。
元素周期表按照一定的规律排列,这些规律反映了元素的原子结构和化学性质的周期性变化。
最著名的周期性性质是元素的物理性质和化学性质的周期性变化。
原子核外电子排布和元素周期律首先,我们来了解一下原子的结构。
原子是由质子、中子和电子组成的。
质子和中子位于原子核中心,质子的电荷为正,中子的电荷为中性。
电子则围绕原子核的轨道上运动,电子的电荷为负。
原子核外电子排布描述了电子如何分布在原子的不同能级(轨道)上。
根据能级理论,电子可以处于不同的能级和亚能级上。
其中,第一能级最靠近原子核,能级数越高,离原子核越远。
每个能级最多容纳2n^2个电子,其中n为能级数。
例如,第一能级最多容纳2个电子,第二能级最多容纳8个电子。
根据电子能级的规律,我们可以了解到元素周期表的排布方式。
元素周期表是将化学元素按照原子序数的增序排列的表格。
元素周期表可以分为周期和族两个方向。
元素周期表的周期是指元素周期性质的变化规律。
周期表中的每一个周期代表着一个能级。
在同一个周期中,元素的最外层电子壳的能级相同,受到的核吸引力相近,因此具有类似的化学性质。
元素周期表的周期依次为K、L、M、N、O等,对应着原子的能级。
元素周期表的族是指元素的主族和次族。
主族元素是指位于周期表左边的元素,它们具有相似的化学性质。
主族元素的最外层电子壳填满的电子数都相同。
例如,第一族(碱金属)的元素最外层电子壳只填满了一个电子,第二族(碱土金属)的元素最外层电子壳填满了两个电子。
次族元素是指位于周期表右边的元素,它们具有相似的化学性质。
次族元素的最外层电子壳填满的电子数也相同。
例如,第十六族(卤族)的元素最外层电子壳填满了六个电子。
元素周期表的排列方式和周期性质的变化规律可以总结为以下几点:1.周期性:在元素周期表中,各周期的化学性质有规律地变化。
例如,金属元素通常位于周期表左侧,具有良好的导电性和热导性,而非金属元素通常位于周期表右侧,具有较差的导电性。
2.原子半径:随着周期数的增加,原子半径逐渐增大。
这是因为随着电子层数的增加,电子对原子核的屏蔽作用增强,电子云的尺寸增大。
3.电离能:随着周期数的增加,元素的电离能逐渐增大。