溶解度及溶解度曲线图
- 格式:ppt
- 大小:1.37 MB
- 文档页数:13


知识总结:溶解度曲线
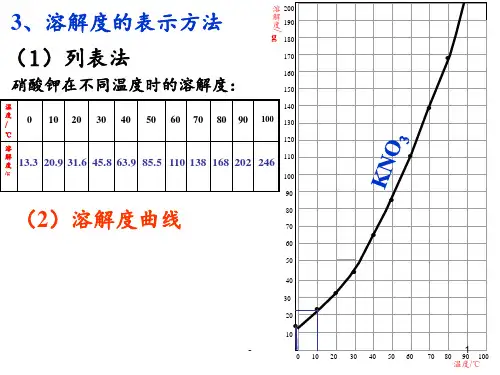
溶解度曲线知识归纳
一、点的意义
1.溶解度曲线上的点表示物质在该点所示湿度下的溶解度,溶液所处的状态是饱
和溶液。
2.溶解度曲线下面的面积上的点,表示溶液所处的状态是不饱和状态,依其数据
配制的溶液为对应湿度时的不饱和溶液。
3.溶解度曲线上面的面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,
且该溶质有剩余。
4.两条溶解度曲线的交点,表示在该点所示的湿度下,两种物质的溶解度相等。
二、变化规律
1.大多数固体物质的溶解度随湿度升高而增大,曲线为"陡升型,如硝酸钾。
2.少数固体物质的溶解度受湿度的影响很小,曲线为”缓升型,如氯化钠。
3.极少数固体物质的溶解度随湿度的升高而减小,曲线为"下降型,如氢氧化钙。
4.气体物质的溶解度均随湿度的升高而减小(纵坐标表示体积),曲线也为”下
降型,如氧气。
三、应用
1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性。
2.比较相同湿度时(或一定湿度范围内)不同物质溶解度的大小。
3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分
离提纯的方法。
4.确定溶液的状态(饱和与不饱和).。


溶解度与溶解度曲线实验溶解度是指在一定温度下,溶质在溶剂中单位体积的最大溶解量。
而溶解度曲线是溶解度与温度之间的关系曲线。
了解溶解度及溶解度曲线对于理解物质之间的相互作用、溶解过程以及溶液的性质都具有重要意义。
本文将介绍溶解度与溶解度曲线的实验方法及实验过程。
实验材料:1. 温度计2. 100毫升量筒3. 静态密闭容器4. 各种溶质和溶剂实验步骤:1. 准备工作:a. 清洗容器和仪器,确保无杂质。
b. 确定所需溶质和溶剂的种类。
c. 按照所需温度范围,准备相应的温度计。
2. 实验前的计划:根据选定的溶质和溶剂,制定一系列不同温度的实验条件,以获得溶解度与温度之间的关系。
3. 实验操作:a. 在容器中加入一定量的溶剂,使用温度计测量溶剂的初始温度。
b. 向容器中加入少量溶质,并搅拌溶液直到溶质彻底溶解。
c. 逐步增加溶质的质量,继续搅拌溶液,直到出现溶质无法完全溶解的情况。
d. 记录此时溶质的质量以及温度,并重新测量溶液的温度。
e. 重复以上步骤,直至达到所有实验温度。
4. 实验数据处理:将实验中记录的溶质的质量和温度数据整理为表格或图表。
根据此数据,可以绘制溶解度曲线,从而了解溶解度与温度之间的关系。
注意事项:1. 溶剂和容器需要事先清洗,防止杂质对实验结果的影响。
2. 溶质的质量需要逐步增加,以确定溶解度的极限。
3. 实验时需保持溶液的搅拌,以促进溶质与溶剂的混合和溶质的溶解过程。
4. 实验过程中需要及时记录溶质的质量和温度,以保证数据的准确性。
通过溶解度与溶解度曲线实验,我们可以获得溶解度与温度之间的关系。
这在实际应用中具有广泛的意义,例如在药物制剂中,了解药物在不同温度下的溶解度可以指导其制备工艺;在环境科学领域,了解气体在水中的溶解度曲线有助于研究水体中的气体交换过程。
因此,溶解度与溶解度曲线实验对于科学研究和工程应用都具有重要意义。
总结起来,通过溶解度与溶解度曲线实验,我们可以了解溶解度与温度之间的关系。
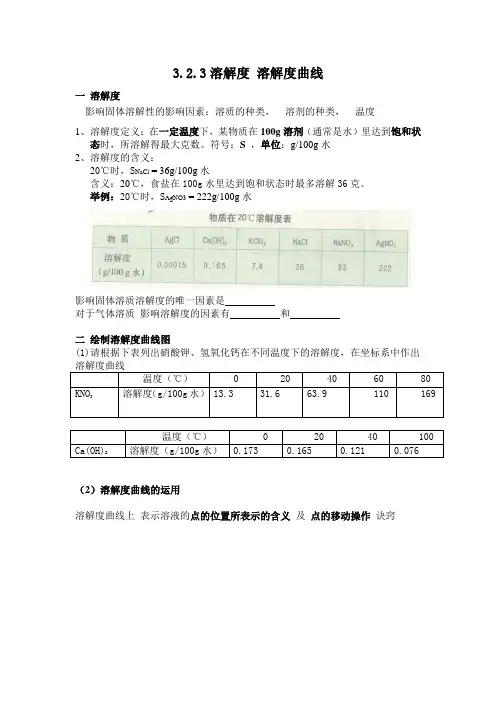
3.2.3溶解度溶解度曲线一溶解度影响固体溶解性的影响因素:溶质的种类,溶剂的种类,温度1、溶解度定义:在一定温度下,某物质在100g溶剂(通常是水)里达到饱和状态时,所溶解得最大克数。
符号:S,单位:g/100g水2、溶解度的含义:20℃时,S NaCl = 36g/100g水含义:20℃,食盐在100g水里达到饱和状态时最多溶解36克。
举例:20℃时,S AgNO3 = 222g/100g水影响固体溶质溶解度的唯一因素是对于气体溶质影响溶解度的因素有和二绘制溶解度曲线图(1)请根据下表列出硝酸钾、氢氧化钙在不同温度下的溶解度,在坐标系中作出温度(℃)0 20 40 60 80 溶解度(g/100g水)13.3 31.6 63.9 110 169 KNO3温度(℃)0 20 40 100 溶解度(g/100g水)0.173 0.165 0.121 0.076Ca(OH)2(2)溶解度曲线的运用溶解度曲线上表示溶液的点的位置所表示的含义及点的移动操作诀窍例1:右图是A、B、C三种物质的溶解度曲线,看图回答:(1)60℃时,B物质的溶解度是。
(2)10℃时,B物质的溶解度(填<、=或>)A物质的溶解度。
(3)℃时,A、B两物质的溶解度相同。
例2:.右图是X、Y、Z三种物质的溶解度曲线(1)A点所表示的意义(2)若X、Y、Z三种物质中,有一种是气态物质,该物是。
判断的依据是。
(3)20℃时,N处物质X的溶液呈(填饱和或不饱和)状态、要使该溶液从N状态变为M状态.应采取的措施有或三有关溶解度的计算公式:S 100 =m(溶质)m(溶剂)SS+100=((+(mm m溶质)溶质)溶剂)=m(m溶质)(溶液)例1、在T℃时,向80克水中加入硝酸钾固体20克,恰好达到饱和,求该温度下的溶解度例2、在20℃时,氯化钠的溶解度是36g/100g水,则在此温度下,30克水中最多能溶解氯化钠多少克?T℃,硝酸钾饱和溶液200克,蒸发20克水后析出晶体12克,则该温度时,硝酸钾的溶解度为_____________当堂训练1.下列说法正确与否,为什么?(1)20℃时,把10克食盐溶解在100克水里,所以20℃时食盐的溶解度是10 (2)20℃时,100克食盐饱和溶液里含有26.4克食盐,所以20℃时食盐的溶解度是26.4克/100克水(3)20℃时,食盐的溶解度是36克/100克水。

溶解度曲线与图像分析一、溶解度曲线【三变量: 、 、 】1.注意温度变量①a 物质溶解度大于c 物质溶解度。
( ) ②b 物质为易溶性物质。
( ) ③c 是氢氧化钙的溶解度曲线。
( ) ④a 、c 饱和溶液溶质质量分数相等。
( )⑤t 1-t 2℃之间a 饱和溶液浓度大于c 饱和溶液浓度。
( )2.注意饱和变量①t 1℃时,100ga 、c 两物质的溶液中,含a 、c 的质量相等。
( ) ②t 2℃时,b 溶液溶质质量分数大于c 溶液溶质质量分数。
( ) ③t 2℃时a 溶液的溶质质量分数比t 1℃时大。
( ) ④t 1℃时可以得到质量分数为16%的c 溶液。
( ) ⑤t 2℃时M 点所对应三种溶液的溶质质量分数:a >b >c 。
( )⑥t 2℃时将等质量的a 、b 两种物质的溶液分别降温至t ℃,析出晶体的质量a 一定大于b 。
3.注意等质量①t ℃时a 、b 饱和溶液中含有的a 、b 质量相等。
( )②t 2℃时,将a 、b 两物质的饱和溶液分别降温至t ℃析出晶体的质量a 大于b 。
( ) ③t 1℃,将a 、c 两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量a=c 。
( ) ④a 、b 两物质的饱和溶液,温度从t 1℃升高到t 2℃时,所得溶液的溶质质量分数a >b 。
4.计算①t 1℃时将20g c 物质加入50g 水中能形成60g 溶液。
( ) ②t 1℃时a 物质的饱和溶液溶质质量分数为20%。
( )③t 2℃时75g a 的饱和溶液加入一定量的水,降温到t 1℃可得到125g16%的a 饱和溶液。
④t 2℃时,将60g a 物质放入100g 水中,所得溶液中溶质与溶液质量之比为1:3。
( ) ⑤将100g 溶质质量分数为10%的a 溶液从t 2℃降温到t 1℃其质量分数仍为10%。
( ) 5.其他①t 1℃时a 、c 物质的溶解度都为20。
( ) ②降温可以使C 的不饱和溶液变为饱和。

溶解度与溶解度曲线的解读溶解度是指单位质量的溶剂在一定温度和压力下最多能溶解的溶质质量,通常以克/100克溶剂(g/100g)或克/升溶液(g/L)表示。
溶解度是化学反应中的一个重要参数,对于溶解过程的理解以及反应速率的研究具有重要意义。
溶解度受到多个因素的影响,其中包括温度、压力和溶质与溶剂之间的相互作用力。
温度对溶解度的影响是其中最显著的因素之一。
通常情况下,随着温度的升高,溶解度会增加,呈现出正相关的趋势。
这是因为在高温下,分子的平均动能增大,导致溶质分子更容易克服吸引力和相互作用力,从而更容易融入溶剂中。
另一方面,在低温下,溶剂分子的平均动能降低,相互作用力增强,溶质的溶解度相对较低。
与温度相比,压力对溶解度的影响通常较小,尤其是对于固体溶质和液体溶剂的溶解过程。
但是,对于气体溶质和液体溶剂的情况下,压力的增大可以显著提高溶解度。
这是因为根据亨利定律,气体在液体中的溶解度与其压力成正比。
增加压力可以增加溶质分子通过液体表面进入溶液的机会,从而提高溶解度。
溶质与溶剂之间的相互作用力也是影响溶解度的重要因素。
当溶质与溶剂之间的相互作用力较大时,溶解度通常较高。
相反,当溶质与溶剂之间的相互作用力较小时,溶解度则相对较低。
这是因为相互作用力较强可以促使溶质分子在溶剂中更好地分散,并与溶剂分子形成较为稳定的溶液结构。
为了更直观地了解溶解度的变化规律,可以利用溶解度曲线进行解读。
溶解度曲线是描述在一定温度下溶质溶解度随溶剂质量或摩尔分数变化的曲线。
溶解度曲线的形态可以根据溶剂的类型和条件的不同而有所不同。
常见的溶解度曲线包括饱和溶解度曲线、过饱和溶解度曲线和不饱和溶解度曲线。
饱和溶解度曲线描述了在给定温度下溶质溶解度随溶剂质量的增加而变化的情况。
在曲线上各点的坐标表示了溶剂中存在的溶质的最大可能质量。
曲线的形状通常呈正向斜率,即溶质溶解度随溶剂质量增加而增加,直到达到饱和状态。
此时,溶液中的溶质质量无法再进一步增加。

溶解度与溶解度曲线溶解度是指在特定条件下,单位溶剂中可以溶解的最大溶质的量。
溶解度通常用溶质在单位溶剂中的摩尔或质量浓度来表示,单位常用mol/L或g/L。
溶解度受多个因素的影响,包括温度、压力和溶质与溶剂之间的相互作用力等。
其中,温度是溶解度影响最为显著的因素之一。
随着温度的升高,大部分固体溶质在溶剂中的溶解度会增加,而气体溶质的溶解度则会减小。
这是由于高温会增加溶质与溶剂之间的分子热运动,从而有利于克服溶剂与溶质之间的相互作用力,使溶质更容易溶解。
相反,低温下,热运动减弱,溶剂与溶质分子之间的相互作用力增强,导致溶质溶解度减小。
除了温度,压力也会对溶解度产生影响。
对于气体溶质,在一定温度下,随着压力的增加,气体溶质的溶解度也会增加。
这是由于增加压力会使气体溶质分子更加密集,更容易与溶剂分子发生相互作用,从而增加溶解度。
而固体或液体溶质的溶解度对压力影响较小,通常可以忽略不计。
溶剂选择也会对溶解度产生重要影响。
不同的溶剂有着不同的溶解度能力,这主要与溶剂与溶质之间的化学性质和极性相关。
相似的化学性质或极性的溶质和溶剂更容易彼此相互作用,从而溶解度较高。
此外,溶剂的溶解度也会受到温度和压力的影响,但影响程度可能与溶质的影响程度不完全相同。
溶解度曲线是描述溶解度随温度变化的曲线图。
根据溶解度与温度的关系,可以得到溶解度曲线的形状。
溶解度曲线通常可以分为两种类型:显热型和隐热型。
显热型溶解度曲线表示随着温度的升高,溶解度逐渐增加,形成一个正斜率的曲线。
这是由于溶解过程是放热的,温度升高会增加溶质与溶剂分子之间的热运动,从而有利于溶质溶解。
隐热型溶解度曲线表示随着温度的升高,溶解度逐渐减小,形成一个负斜率的曲线。
这是由于溶解过程是吸热的,温度升高会增加溶质与溶剂分子之间的热运动,导致溶质分子逃逸出溶液,从而减小溶解度。
根据溶解度曲线的形状,我们可以推断溶解过程中是否有热效应。
根据溶解度曲线的斜率,我们还可以判断溶解度对温度的敏感程度。

中考化学:溶解度曲线近年来,全国各地中考中,“溶解度”以海水中的物质、侯氏制碱法、氨碱法制纯碱等初中课本中的工业流程作为背景,考察同学们对溶解度曲线上升下降、交点等特征的了解,分值通常在3-5分。
什么是溶解度曲线?溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行各物质溶解度的比较、混合物的分离与提纯、以及进行物质结晶或溶解的计算。
从溶解度曲线中能获得哪些信息?1、点① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a表示A物质在t1℃时溶解度为m1g。
② 曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。
如:图中b表示在t1℃时,A的饱和溶液中有(m2-m1)g未溶解的溶质。
③ 曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中c表示在t1℃时,A的不饱和溶液中,还需要加入(m1-m3)g A物质才达到饱和。
④ 曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d表示在t2℃,A、B两物质的溶解度都为m4g。
2、线溶解度曲线大致可以分为下面三类:①如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”。
如KNO3等大多数固体物质;②图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCl等少数固体物质;③图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
溶解度曲线怎么考?1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2.可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。

溶解度曲线及溶解度表1. 引言溶解度是指单位温度和压力下,溶质在溶剂中达到平衡时的最大溶解量。
溶解度曲线及溶解度表是描述物质在不同温度和压力下的溶解性的重要工具。
通过研究物质的溶解度曲线和制作相应的溶解度表,可以了解物质在不同条件下的溶解特性,为实际应用提供依据。
2. 溶解度曲线2.1 溶解度与温度关系物质的溶解度通常随着温度的升高而增大。
这是因为温度升高会增加分子热运动的速率和能量,使得分子间距离增大,从而有利于固体分子逃离晶格并进入溶液中。
以氯化钠(NaCl)为例,其在水中的溶解度随着温度升高而增大。
以下是氯化钠在不同温度下的溶解度数据:温度(℃)溶解度(g/100g水)0 35.710 38.220 40.730 43.340 45.82.2 溶解度与压力关系对于大部分固体物质来说,压力对其溶解度的影响并不显著。
但是对于气体溶解在液体中的情况,溶解度与压力成正比关系,即亨利定律。
亨利定律可以用来描述气体在液体中的溶解度。
以二氧化碳(CO2)在水中的溶解度为例,以下是二氧化碳在不同压力下的溶解度数据:压力(atm)溶解度(g/100g水)1 0.0392 0.0793 0.1184 0.1575 0.1973. 溶解度表溶解度表是一种将物质在不同温度和压力下的溶解度数据整理并呈现的表格。
通过查阅溶解度表,可以了解某种物质在特定条件下的最大溶解量。
以下是一份简单的氯化钠在不同温度下的溶解度表:温度(℃)溶解度(g/100g水)0 35.710 38.220 40.730 43.340 45.8通过这个溶解度表,我们可以看出在不同温度下氯化钠的溶解度变化情况。
例如,在0℃下,氯化钠的溶解度为35.7g/100g水,而在40℃下,氯化钠的溶解度增加到了45.8g/100g水。
4. 应用4.1 溶解过程控制通过研究物质的溶解度曲线和溶解度表,可以控制物质的溶解过程。
根据所需的溶液浓度和温度条件,可以确定需要加入的物质量,并且通过调整温度来控制物质的最终溶解量。