常见阳离子的分离与鉴定第II组阳离子
- 格式:ppt
- 大小:973.00 KB
- 文档页数:43



常见阳离子的分离与鉴定二实验报告一、实验目的1、了解常见阳离子的溶解特性;2、熟悉常见阳离子的分离与鉴定的方法;3、巩固常见阳离子的溶解特性,以便于进行实验中的鉴别、分离及分析;二、实验原理阳离子是指带有正电荷的离子,如钠离子(Na+)、钾离子(K+)、氯离子(Cl-)、铵离子(NH4+)等。
阳离子有着不同的电荷,溶解度和溶质的类型不同,因此,可以根据不同的溶解特性将其分离、鉴定出来。
本实验利用沉淀反应、氯化物气体滴定以及媒质对组成离子的影响,结合实验室常见阳离子的特性,在模拟实验中进行阳离子的分离与鉴定。
三、实验材料1、2.0 mol/L的NaCl溶液、KCl溶液、NH4Cl溶液、(NH4)2SO4溶液;2、2.0mol/L溴代乙酸溶液;3、分光光度计;4、蒸馏水;5、吸管、放大器、烧杯及烧瓶等实验用具;四、实验步骤1、将2.0mol/L NaCl溶液、KCl溶液、NH4Cl溶液、(NH4)2SO4溶液分别放入4个烧杯中;2、将2.0mol/L溴代乙酸溶液分别加入到4个烧杯中,观察气体的产生及沉淀反应;3、将沉淀反应结束后的物质加入蒸馏水中,然后充分搅拌;4、用分光光度计测定各烧杯中溶液的溶氧量;5、根据溶氧量的结果,鉴定出阳离子的种类;六、实验结果1、烧杯1中,溶质沉淀出白色晶体,添加溴代乙酸溶液可产生白色气体,同时溶氧量为0.4mg/L,可判定该溶液为等比例混合溶液,溶质为NaCl;2、烧杯2中,溶质沉淀出暗黄色晶体,添加溴代乙酸溶液可产生黄色气体,同时溶氧量为0.5mg/L,可判定该溶液为等比例混合溶液,溶质为KCl;3、烧杯3中,溶质沉淀出淡粉色晶体,添加溴代乙酸溶液可产生白色气体,同时溶氧量为0.7mg/L,可判定该溶液为等比例混合溶液,溶质为NH4Cl;4、烧杯4中,溶质沉淀出白色晶体,添加溴代乙酸溶液可产生淡黄色气体,同时溶氧量为3.5mg/L,可判定该溶液为等比例混合溶液,溶质为(NH4)2SO4。

实验常见阳离子的分离与鉴定-V1实验常见阳离子的分离与鉴定阳离子是指带正电荷的离子,常见的有盐酸中的K+、Na+、Mg2+、Ca2+等。
在实验室中对这些阳离子的分离和鉴定是一项比较常见的实验操作,下面将对此进行重新整理。
一、分离NH4+和Fe3+实验操作步骤:1.将NH4+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,并加入HCl,沉淀消失;3.将所得溶液加入HgCl2,出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的氨盐等。
二、分离Ba2+和Fe3+实验操作步骤:1.将Ba2+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,得到沉淀和过滤液;3.将所得沉淀加入Na2CO3,在锅炉中加热,轻轻搅拌,直到溶解;4.将溶液冷却,加入硫酸钠,出现白色沉淀。
实验操作目的:该实验可用于检测水中钙、铁的含量。
三、分离Mg2+和Fe2+实验操作步骤:1.将Mg2+和Fe2+混合,加入氨水,pH值达到9.5~10.2;2.将所得溶液加入EDTA,出现蓝色沉淀。
实验操作目的:该实验可用于检测水或者土壤中的镁和铁的含量。
四、分离Ca2+和Ba2+实验操作步骤:1.将Ca2+和Ba2+混合,加入Na2SO4;2.出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的钙盐。
五、分离Na+和K+实验操作步骤:1.将Na+和K+混合,并加入Na2CO3;2.加热,溶解后冷却,加入二甲基黄。
3.观察产生的沉淀,小型重沉。
实验操作目的:该实验可用于检测水中钠、钾的含量。


常见阳离子的鉴定二实验报告常见阳离子的鉴定实验报告一、实验目的通过实验,了解常见阳离子的实验鉴定方法,掌握其色谱分离技术,并做出实验报告。
二、实验原理阳离子的色谱分离是利用样品中各成分的不同性质,现将样品加入有机溶剂溶解,然后加入适当的色谱剂,要求色谱剂有适当的吸附性和亲水性。
通过不同阳离子在色谱剂上的吸附性、物理、化学性质等的不同,使各成分的分离效果不同。
在某个温度、某个水浴中,这种不同的物理和化学特性使各成分的活化度不同,从而使它们分离出来,从而得到初步的阳离子分离。
三、实验材料(1) 常用阳离子溶液:Na+, K+, Ca2+, Mg2+;(2) 石墨烯色谱剂:用于色谱分离。
四、实验步骤(1) 将所有常见的阳离子溶液各取出10 ml,加入有机溶剂中,混合均匀;(2) 将上述混合液加入色谱柱中,以室温热源煮沸15分钟;(3) 将热源关闭,冷却柱体至室温;(4) 通过色谱仪分析实验中四种阳离子,并打印出检测结果;(5) 根据实验结果,制作实验报告。
五、实验结果及报告色谱实验结果如下:Na+:浓度为1.5 mg/LK+:浓度为2.3 mg/LCa2+:浓度为3.2 mg/LMg2+:浓度为1.8 mg/L根据上述实验结果,可以看出Na+, K+, Ca2+, Mg2+四种常见的阳离子在色谱柱中分离后,浓度分别是1.5 mg/L、2.3 mg/L、3.2 mg/L、1.8 mg/L,即分离效果良好。
经过色谱实验,通过四种常见阳离子的分离测定,验证了样品中四种阳离子的存在,并且对阳离子的分析效果较好。
六、结论本次实验通过对四种常见阳离子的分离测定,证实了样品中Na+, K+, Ca2+, Mg2+四种阳离子的存在,并且分析效果较好。


无机化学常见阳离子分离与鉴定.doc一、分离1、氢氧根离子(OH^-)氢氧根离子与金属离子形成的沉淀可以通过NaOH沉淀法分离出来。
在水溶液中,氢氧根离子与金属离子结合形成相应的金属氢氧化物,这些氢氧化物可以形成沉淀,实现分离。
一些阳离子的氢氧化物沉淀的颜色也是它们鉴定的基础之一。
2、氟化物(F^-)氟化物结合度和其他类似的离子相比较小,因此可以和其他阴离子分离。
使用鸟巢法可以分离出氟化物,该方法使用的络合剂是季铵盐鸟巢环(NH4)3 [FeF6]。
3、碳酸盐(CO32-)在水中,CO32-可以形成与Ca2+、Ba2+、Pb2+、Ag+等阳离子结合的沉淀。
因此,通过观察生成的沉淀的颜色可以确定阳离子的存在。
氰化物形成的配合物稳定性很高,一些盐可以沉淀分离氰化物。
通过加入相应的酸可以分解盐的氰化物,若遇到硝酸银时,则可以生成白色的沉淀。
硫酸盐与Barium离子结合可以形成硫酸钡的沉淀。
可以用BaCl2试剂发生反应,观察生成的白色沉淀可以确认硫酸盐的存在。
氯化物可以通过加入AgNO3实现分离,生成白色的AgCl沉淀。
AgCl颜色淡黄色并且易溶于NH3溶液中。
二、鉴定1、铁离子(Fe3+)Fe3+可以通过与硝酸铵一起存在,在加热时生成棕黄色的Fe(OH)3沉淀。
此外,还可以借助Ti(III)还原Fe3+为Fe2+,并使用Fenton试剂检测Fe2+的产生。
2、铜离子(Cu2+)Cu2+可以通过和N,N-二乙基-1,6-二亚胺染料组成的溶液反应而呈现出深蓝色,且颜色随着浓度的增加而增加。
Zn2+可以通过向含有鞣酸的溶液中加入氢氧化钠而产生白色沉淀进行鉴定。
Mn2+可以通过加入氢氧化钠和汞齐试剂而鉴定。
试剂与汞齐反应,生成黑色沉淀,同时文中的Mn(OH)2也被沉淀。
Mg2+可以通过向可溶性的Phenolphthalein-indicator(溶于环己酮)溶液中添加MgCl2所生成的红色沉淀进行鉴定。
Al3+可通过加入含有增效剂的Eriochrome Black T试剂检测出来,试剂经络合反应后转变为紫红色,而Al3+呈现出浅紫色。

【精品】无机化学常见阳离子分离与鉴定
无机化学中,阳离子分离与鉴定是非常重要的步骤, divide the steps into several parts on the basis of their functions,浏览以下:
- 预处理:预处理是分离各种有机和无机杂质和有效物质阳离子的第一步,可以使用加草酸、高氯酸、稀硫酸等剂量分离有机杂质和无机阳离子。
- 共析:用于分离有关的化合物的有机溶剂,在共析实验中,重要的是选择适当的溶剂,可以实现离子弱共析和离子强共析。
- 根据溶解度和萃取受体的选择:根据溶解度的不同,主要分为水溶和有机溶,而有机溶非水溶即萃取受体,常见萃取受体有醚、氯仿、氨和甲醇等。
- 重结晶和提取:溶剂提取技术非常重要,原料中的阳离子萃取到某种溶剂后,应收集溶解液,用新的溶剂萃取,以尽量的减少萃取回收的溶剂的数量。
- 结晶干燥:使用适当的溶剂对结晶结果进行结晶干燥。
在结晶过程中,有一些溶剂和添加剂被带出去,而结晶干燥可以有效地去除残留的溶剂。
- 多重梯度洗脱:多重梯度洗脱可以得到更纯的产品,常用的洗脱技术有多相洗脱、多极性洗脱、溶解度变洗脱、聚丙烯酰胺凝胶层析等。
- 鉴定技术:鉴定阳离子的技术常采用X波发射(EDX)、原子荧光光谱(AES)、原子质谱(MS)等技术,分析阳离子的精确性很重要,也可以利用热分析技术,如热重分析(TGA)、热分散光元仪(DSC)来确定其组成和特性。
以上是无机化学中阳离子分离与鉴定的步骤,然而,实际操作过程根据实际情况还可能需要中和、萃取、逆流色谱、粒子分离以及晶格弛豫技术等多项技术进行支持。
在操作分离与鉴定步骤时,需要掌握相关基础知识,并仔细审查操作过程,以确保工作效果。

1. 与HCl反应Ag+ HCl AgCl ↓白色,溶于氨水Hg22+ → Hg2Cl2↓白色,溶于浓HNO3及H2SO4Pb2+ PbCl2 ↓白色,溶于热水,NH4Ac、NaOH2. 与H2SO4反应Ba2+ BaSO4↓白色,难溶于酸Sr2+ H2SO4 SrSO4↓白色,溶于煮沸的酸Ca2+ CaSO4↓白色,溶解度较大,当Ca2+浓度很大时,才析出沉淀Pb2+ PbSO4↓白色,溶于NaOH、NH4Ac、热HCl、浓H2SO4,不溶于稀H2SO4 Ag+ Ag2SO4↓白色,在浓溶液中产生沉淀,溶于热水3. 与NaOH反应Al3+ AlO2-或[Al(OH)4]- 浓NaOHZn2+ 过量NaOH ZnO2-或[Zn(OH)4]2- Cu2+ Cu(OH)42- Pb2+ PbO2-或[Pb(OH)4]2- ΔSb3+ SbO2-或[Sb(OH)4]-Sn2+ SnO22-或[Sn(OH)4]2-4. 与NH3反应Ag+ Ag(NH3)2+Cu2+ 过量NH3 Cu(NH3)42+ 深蓝Cd2+ Cd(NH3)42+Zn2+ Zn(NH3)42+6. 与H2S或(NH4)2S反应Ag+ Ag2S↓黑色Pb2+ PbS↓黑色Cu2+ Cu S↓黑色Cd2+ CdS↓黄色Bi3+ 0.3mol·L-1HCl Bi2S3↓黑色Hg22+ HgS↓+Hg↓黑色溶于王水,Na2SHg2+ H2S HgS↓黑色Sb5+ Sb2S5↓橙色Sb3+ Sb2S3↓橙色溶于浓HCl,NaOH,Na2SSn4+ SnS2↓黄色Sn2+ SnS↓褐色溶于浓HCl,(NH4)2Sx,不溶于NaOH,Zn2+ NH4Cl ZnS↓白色,溶于稀HCl溶液,不溶于HAc溶液Al3+ NH3·H2O,H2S Al(OH)3↓白色,溶于强碱及稀HCl溶液1 实验:常见阳离子的分离与鉴定(一)。
常见阳离子的分离与鉴定【实验目的】1. 巩固和进一步掌握一些金属元素及其化合物的化学性质。
2. 了解常见阳离子混合液的分离和检出的方法以及巩固检出离子的操作。
【预习作业】1. 查阅文献,找出镁试剂与铝试剂的结构式及鉴定镁离子、铝离子的方程式。
2. 以流程图方式表示,应包含试剂浓度,用量,分离手段,详细现象,最终结果。
对应的方程式在流程图上注上号码,另处写出化学反应方程式。
3. 试设计一分析流程图,分离和检出Ag+、Zn2+和Cu2+混合溶液。
【实验原理】离子的分离和鉴定是以各离子对试剂的不同反应为依据的。
这种反应常伴随着特殊的现象,如沉淀的生成或溶解,特殊颜色的出现,气体的产生等等。
各离子对试剂的作用的相似性和差异性都是构成离子分离与鉴定的基础。
也就是说,离子的基本性质是进行分离检出的基础。
因而要想掌握分离检出的方法就要熟悉离子的基本性质。
离子的分离和检出是在一定条件下进行。
所谓一定的条件主要是指溶液的酸度、反应物的浓度、反应温度、促进或妨碍反应的物质是否存在等。
为使反应向期望的方向进行,就必须选择适当的反应条件。
离子混合液中诸组分若对鉴定反应不产生干扰,便可以利用特效反应直接鉴定某种离子。
若共存的其他组分彼此干扰,就要选择适当方法消除干扰。
通常采用掩蔽剂消除干扰,通常采用遮掩剂消除干扰,这是一种比较简单、有效的方法。
但在很多情况下没有合适的遮掩剂,就需要将彼此干扰的组分分离。
沉淀分离是最经典的分离方法。
这种方法是向混合溶液中加入沉淀剂,利用形成的化合物溶解度的差异,使被分离组分与干扰组分分离。
常用的沉淀剂有HCl 、H2SO4、NaOH、NH3H2O、(NH4)2CO3及(NH4)2S。
由于元素周期表中的位置使相邻元素在化学性质上表现出相似性,因此一种沉淀剂往往可以使具有相似的元素同时产生沉淀。
这种沉淀剂称为产生沉淀的元素的组试剂。
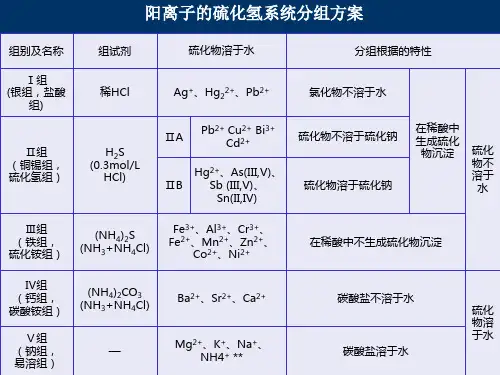
组试剂将元素划分为不同的组,逐渐达到分离的目的(见图一)。
图一常见阳离子的分离及鉴定【仪器设备和试剂】仪器:试管、烧杯、离心机、离心试管、电热炉、点滴板、试管架液体药品:Ag+、Hg2+、Pb2+、Cu2+、Fe3+、Al3+、Ba2+混合溶液(七种离子均为硝酸盐,其浓度都为10 ng・mL-1)、HCl (2 mol ・L-1、6 mol ・L-1、浓)、H2SO4-1 -1 -1 -1 -1(2 mol - L、6 mol - L-1)、HNO3 (6 mol - L )、HAc (2 mol - L、6 mol - L-1)、-1 -1 -1 -1NaOH (2 mol - L、6 mol - L-1)、KOH (2 mol - L )、NH3 -出0 (6 mol - L )、-1 -1 -1 -1 NaCl (1 mol - L )、KCl (1 mol - L )、KI (1 mol - L )、MgCl2 (0.5 mol - L )、-1 -1 -1 -1 CaCl2(0.5 mol -L 1)、BaCb(0.5 mol •L1)> AlCl 3(0.5 mol -L1)、SnCb(0.5 mol • L )、-1 -1 -1Pb(NO3)2(O.5 mol - L )、HgCb(0.2 mol - L )、CuCb (0.5 mol - L )、CuSO4 (0.2-1 -1 -1 -1 mol - L )、AgNO3 (0.1 mol - L 1)、ZnSO4(O.2 mol - L 1)、Al(NO 3)3 (0.5 mol - L 1)>-1 -1 -1 -1 NaNO3 (0.5 mol - L )、Ba(NO3)2 (0.5 mol - L )、Na2S (0.5 mol - L、1 mol - L )、-1 -1 H2S (饱和)、KSb(OH)6 (饱和)、NaHC4H4O6 (饱和)、NaAc (0.2 mol -L-、1 mol -L-)、-1 -1K2CrO4 (1 mol • L-、2 mol - L-)、Na2CO3 (12%、饱和)、NH4CI (饱和)、NH4Ac (2 mol - L-1)、(NH4)2C2O4 (饱和)、K4 [Fe(CN)6] (0.25 mol - L-1、0.5 mol - L-1)、硫代乙酰胺(5%)、对氨基苯磺酸、镁试剂、0.1%铝试剂、罗丹明B、苯、2.5%硫脲、(NH4) 2[H g(SCN)4] 试剂固体药品:亚硝酸钠、亚硫酸钠、锌粉、碳酸钠材料:pH 试纸、玻璃棒、镍丝【实验步骤】一、碱金属和碱土金属离子的鉴定1. Na+的鉴定-1在盛有0.5 mL 1 mol •_ NaCI溶液的试管中,加入0.5 mL饱和六羟基锑(v)酸钾溶液,即有白色沉淀生成。