(完整版)常见阳离子的分离及鉴定
- 格式:ppt
- 大小:563.51 KB
- 文档页数:19


实验二十四 常见阳离子的分离与鉴定(一)一、主要教学目标(一)巩固和进一步掌握一些金属元素及其化合物的性质(二)了解常见阳离子的分离和检出方法,以及巩固检出离子的操作 二、教学的方法及教学手段:讲解法,学生实验法,巡回指导法 三、教学重点:常见阳离子的分离和检出方法,以及巩固检出离子的操作 四、教学难点:常见阳离子的分离和检出方法,以及巩固检出离子的操作 五、实验设备:离心机 六、实验内容(一)碱金属,碱士金属离子的鉴定1、Na +的鉴定①用饱和六羟基锑(V )酸钾KSb(OH)6溶液↓=+66)()(OH NaSb OH KSb NaCl假若没有沉淀,可以摩擦试管内壁②用醋酸铀酰锌与Na+在醋酸缓冲溶液中生成淡黄色结晶状醋酸铀酰锋钠沉淀↓•••=++++-+++O H Ac UO Ac Zn NaAc O H Ac UOZnNa 222222229)(3)(9932、K +的鉴定:①用饱和洒石酸氢钠NaHC 4H 4O 6NaCl O H KHC O H NaHC KCl +↓+644644—3、Mg 2+的鉴定 用镁试剂:蓝色沉淀滴镁试剂加入白滴入1)()(22↓OH Mg NaOH MgCl Mg 2+与镁试剂工在碱性溶液中生成蓝色螯合物沉淀 4、Ca 2+的鉴定(用草酸铵)Cl NH O CaC O C NH CaCl 442422422)()(+↓=+白5、Ba 2+的鉴定:用K 2CrO 4溶液在HAc 和NaAc 缓冲液中+↓=+24422Ba BaCrO CrO K BaCl 示有(二)P 区和ds 区部分金属离子的鉴定 1、Al 3+的鉴定,用HAC 酸化的铝试剂红色絮状沉淀滴氨水再加水浴加热搅拌滴铝试剂→2~1,2%1.03AlCl2、Sn 2+的鉴定+↓22222)(nS Cl Hg HgCl SnCl 示有变黑变灰白透量的 3、Pb 2+的鉴定NaOHPbCrO CrOPbNaOH PbCrO CrO LK mol NO Pb 可溶于黄沉淀溶解溶液黄)()(/1)(424244223↓=+↓-+4、Sb 3+的鉴定++353,2,)(3Sb BSb SbCl 示有苯层显紫色滴罗丹罗明加加数滴苯并释放出气体变为数粒亚销酸钠滴浓盐酸溶液5、Bi 3+的鉴定 用硫脲鲜黄色配合物硫脲→+33)(NO Bi6、Cu 2+的鉴定沉淀])([])([62264CN Fe Cu CuCl CN Fe K =+7、Ag +的鉴定↓•↓AgCl HNO Cl NH Ag O H NH AgCl HCl AgNO 323233)()(白 8、Zn 2+的鉴定42444244)()(])([])([)(SO NH SCN Hg Zn SCN Hg NH ZnSO +↓→+白9、Cd 2+的鉴定:32232)()(NaNO CdS S Na NO Cd +↓=+黄 10、)(2:222示有灰色白的鉴定++Hg SnCl HgCl Hg (三)部分混合离子的分离和鉴定。


实验常见阳离子的分离与鉴定-V1实验常见阳离子的分离与鉴定阳离子是指带正电荷的离子,常见的有盐酸中的K+、Na+、Mg2+、Ca2+等。
在实验室中对这些阳离子的分离和鉴定是一项比较常见的实验操作,下面将对此进行重新整理。
一、分离NH4+和Fe3+实验操作步骤:1.将NH4+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,并加入HCl,沉淀消失;3.将所得溶液加入HgCl2,出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的氨盐等。
二、分离Ba2+和Fe3+实验操作步骤:1.将Ba2+和Fe3+混合,并加入NaOH,出现棕色沉淀;2.将沉淀过滤,得到沉淀和过滤液;3.将所得沉淀加入Na2CO3,在锅炉中加热,轻轻搅拌,直到溶解;4.将溶液冷却,加入硫酸钠,出现白色沉淀。
实验操作目的:该实验可用于检测水中钙、铁的含量。
三、分离Mg2+和Fe2+实验操作步骤:1.将Mg2+和Fe2+混合,加入氨水,pH值达到9.5~10.2;2.将所得溶液加入EDTA,出现蓝色沉淀。
实验操作目的:该实验可用于检测水或者土壤中的镁和铁的含量。
四、分离Ca2+和Ba2+实验操作步骤:1.将Ca2+和Ba2+混合,加入Na2SO4;2.出现白色沉淀。
实验操作目的:该实验可用于检测食品和饲料中的钙盐。
五、分离Na+和K+实验操作步骤:1.将Na+和K+混合,并加入Na2CO3;2.加热,溶解后冷却,加入二甲基黄。
3.观察产生的沉淀,小型重沉。
实验操作目的:该实验可用于检测水中钠、钾的含量。

常见阳、阴离子的分离和鉴定一、实验目的1.掌握常见阳离子、阴离子的基本性质; 2.了解常见阳离子、阴离子的分离方法; 3.了解常见阳离子、阴离子的鉴定方法。
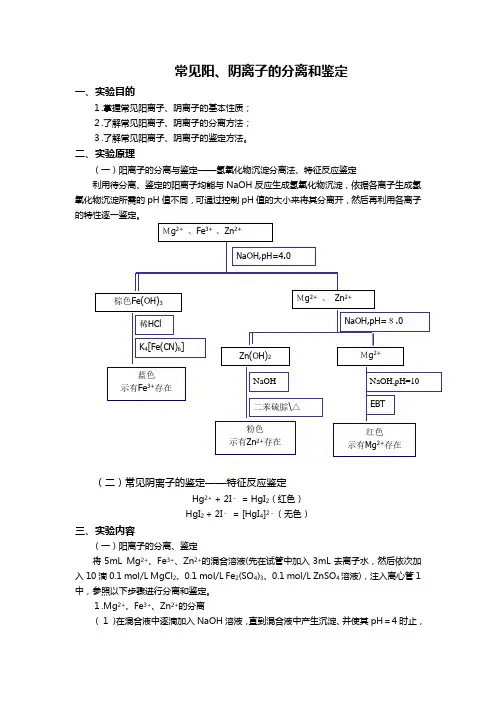
二、实验原理(一)阳离子的分离与鉴定——氢氧化物沉淀分离法、特征反应鉴定利用待分离、鉴定的阳离子均能与NaOH 反应生成氢氧化物沉淀,依据各离子生成氢氧化物沉淀所需的pH 值不同,可通过控制pH 值的大小来将其分离开,然后再利用各离子的特性逐一鉴定。
(二)常见阴离子的鉴定——特征反应鉴定Hg 2+ + 2I - = HgI 2(红色) HgI 2 + 2I - = [HgI 4]2-(无色)三、实验内容(一)阳离子的分离、鉴定将5mL Mg 2+、Fe 3+、Zn 2+的混合溶液(先在试管中加入3mL 去离子水,然后依次加入10滴0.1 mol/L MgCl 2、0.1 mol/L Fe 2(SO 4)3、0.1 mol/L ZnSO 4溶液),注入离心管1中,参照以下步骤进行分离和鉴定。
1.Mg 2+、Fe 3+、Zn 2+的分离(1)在混合液中逐滴加入NaOH 溶液,直到混合液中产生沉淀、并使其pH =4时止,Mg 2+ 、Fe 3+ 、Zn 2+Mg 2+ 、 Zn 2+棕色Fe(OH)3稀HCl NaOH,pH=4.0蓝色 示有Fe 3+存在K 4[Fe(CN)6] NaOH,pH=8.0 Zn(OH)2Mg 2+NaOH 粉色示有Zn 2+存在二苯硫腙\△ NaOH,pH=10 红色示有Mg 2+存在EBT然后离心分离。
把上清液移到另一离心管2中;沉淀用去离子水洗涤二遍后,记为沉淀1,留待下面分析。
(2)往离心管2的上层清液中继续逐滴加入NaOH溶液,直到溶液中产生沉淀、并使其pH=8时止,把上清液移到另一离心管3中;沉淀用去离子水洗涤二遍后,记为沉淀2,留待下面分析。
2.Mg2+、Fe3+、Zn2+的鉴定(1)Fe3+的鉴定取沉淀1加入去离子水及几滴盐酸,振荡试管使沉淀溶解。



实验27 常见阳离子的分离、鉴定一、实验目的1.了解常见阳离子的基本性质和重要反应。
2.掌握常见阳离子的分离原理及鉴定方法。
3.进一步练习分离、鉴定的基本操作。
二、实验原理离子的分离和鉴定是以各离子对试剂的不同反应为依据的,这种反应常伴随有特殊的现象,如沉淀的生成或溶解,特殊颜色的出现,气体的产生等等。
各离子对试剂作用的相似性和差异性都是构成离子分离与检出方法的基础,也就是说,离子的基本性质是进行分离鉴定的基础。
因而要想掌握阳离子的分离鉴定的方法,就要熟悉阳离子的基本性质。
离子的分离和鉴定只有在一定条件下才能进行。
所谓一定的条件主要指溶液的酸度、反应物的浓度、反应温度、促进或妨碍此反应的物质是否存在等。
为使反应向期望的方向进行,就必须选择适当的反应条件。
因此,除了要熟悉离子的有关性质外,还要学会运用离子平衡(酸碱、沉淀、氧化还原、配位等平衡)的规律控制反应条件,这对于我们进一步掌握离子分离条件和鉴定方法的选择将有很大帮助。
对于常见阳离子分离的性质是指常见阳离子与常用试剂的反应及其差异,重点在于应用这些差异性将离子分开。
常见阳离子与常用试剂的反应:1. 与HCl 溶液反应AgCl ↓ 白色,溶于氨水Hg 2Cl 2↓ 白色,溶于浓HNO 3及H 2SO 4 PbCl 2 ↓ 白色,溶于热水,NH 4A c 、NaOH Ba SrCa Ca 2+浓度很大时,才析出沉淀 Pb NaOH 、NH 4Ac(饱和)、热HCl 溶液、浓H 2SO 4,不溶于稀H 2SO 4 Ag3. 与NaOH 反应Al 2-或[Al(OH)4]-Zn ZnO 22-或[Zn(OH)4]2-Pb PbO 22-或[Pb(OH)4]2-Sb SbO 2-Sn 22-或[Sn(OH)4]2-Cu 2+ Cu(OH)42-4. 与NH 3反应Ag + [Ag(NH 3)2]+Cu 2+ 3)4]2+ (深蓝) Cd 2+ 3)4]2+浓NaOH △Zn[Zn(NH 3)4]2+Ni 2+3)4]2+ (蓝紫色)Co[Co(NH 3)6]4+ (土黄色) [Co(NH 3)6]3+(棕红色)5. 与(NH 4)2CO 3反应Cu Cu 2(OH)2CO 3 ↓ 浅蓝3)4]2+ 深蓝 Ag Ag 2CO 3 (Ag 2O)↓白色3)2]+ 无色 ZnZn 2(OH)2CO 3↓ 白色3)4]2+ 无色Cd Cd 2(OH)2CO 3↓ 白色[Cd(NH 3)4]2+ 无色 Hg Hg 2(OH) 2CO 3↓ 白色Hg 2 Hg 2CO 3(白)↓ → HgO ↓(黄) + Hg ↓(黑) +CO 2 ↑ Mg Mg 2(OH)2CO 3 ↓ 白色 Pb 2+Pb 2(OH)2CO 3 ↓ 白色 Bi (BiO)2CO 3 ↓ 白色 Ca 3 ↓ 白色 Sr SrCO 3 ↓ 白色 Ba 3 ↓ 白色 Al 3 ↓ 白色 Sn Sn(OH)2 ↓ 白色 Sn Sn(OH)4 ↓ 白色 Sb Sb(OH)3 ↓ 白色 6. 与H 2S 或(NH 4)2S 反应应当掌握各种阳离子生成硫化物沉淀的条件及其硫化物溶解度的差别,并用于阳离子分离。

阳离子的分离与鉴定(P44-52)1、组试剂:凡能使一组阳离子在适当的反应条件下生成沉淀而与其他组阳离子分离的试剂。
(两酸三碱:HCl、H2SO4、NaOH、NH3·H2O、(NH4)2S)PS:因为实验中需要使用的H2S、(NH4)2S都具有臭味和毒性,其中的S离子不稳定,所以我们实验时用的硫代乙酰胺(CH3CSNH2,即TAA)。
2、阳离子的系统分析:利用不同的组试剂把阳离子逐组分离再进行检出的方法。
(常见的为硫化氢系统分组分析法和两酸三碱系统分组分析法)3、为不受干扰,实验的总体思路是把阳离子先分离后鉴定,离子的分离方法有:沉淀分离法(根据离子的溶解度不同)、萃取法、离子交换法。
4、实验中阳离子未知液包括:Ag+、Pb2+、Cr3+、Mn2+、Fe3+、Co2+、Ni2+、Cu2+、Cd2+、Mg2+、Al3+等11种离子,用两酸三碱组试剂分组得以下分组情况——第一组:盐酸组Ag+,Pb2+第二组:硫酸组Pb2+第三组:氨合物组Cu2+,Cd2+,Co2+,Ni2+第四组:易溶组Mg2+第五组:两性组Al3+,Cr3+第六组:氢氧化物组Fe2+,Fe3+,Mn2+5、11种离子的特征反应+部分反应方程式AgCl + 2NH3 = [Ag(NH3)+] + Cl-Ag(NH3)+] + Cl- + 2H+ = AgCl ↓+ 2NH4+PbSO4+Ac- =[PbAc]+[PbAc]++CrO42- = PbCrO4PS:1、检验Mg 时,要注意去铵根。
2、 用H2SO4沉淀Pd 离子时,由于其沉淀速度较慢,需用玻璃杯摩擦管壁,搅拌并加乙醇。
3、 检验亚Co 离子时,加亚Sn 离子,是为了将Co 离子还原为亚Co 离子;加硫氰根是为了屏蔽Cu 离子的干扰。
2334225147557Mn NaBiO H MnO Na Bi H O ++-++++=+++336()Fe KSCN K Fe SCN ++−−→。
【精品】无机化学常见阳离子分离与鉴定
无机化学中,阳离子分离与鉴定是非常重要的步骤, divide the steps into several parts on the basis of their functions,浏览以下:
- 预处理:预处理是分离各种有机和无机杂质和有效物质阳离子的第一步,可以使用加草酸、高氯酸、稀硫酸等剂量分离有机杂质和无机阳离子。
- 共析:用于分离有关的化合物的有机溶剂,在共析实验中,重要的是选择适当的溶剂,可以实现离子弱共析和离子强共析。
- 根据溶解度和萃取受体的选择:根据溶解度的不同,主要分为水溶和有机溶,而有机溶非水溶即萃取受体,常见萃取受体有醚、氯仿、氨和甲醇等。
- 重结晶和提取:溶剂提取技术非常重要,原料中的阳离子萃取到某种溶剂后,应收集溶解液,用新的溶剂萃取,以尽量的减少萃取回收的溶剂的数量。
- 结晶干燥:使用适当的溶剂对结晶结果进行结晶干燥。
在结晶过程中,有一些溶剂和添加剂被带出去,而结晶干燥可以有效地去除残留的溶剂。
- 多重梯度洗脱:多重梯度洗脱可以得到更纯的产品,常用的洗脱技术有多相洗脱、多极性洗脱、溶解度变洗脱、聚丙烯酰胺凝胶层析等。
- 鉴定技术:鉴定阳离子的技术常采用X波发射(EDX)、原子荧光光谱(AES)、原子质谱(MS)等技术,分析阳离子的精确性很重要,也可以利用热分析技术,如热重分析(TGA)、热分散光元仪(DSC)来确定其组成和特性。
以上是无机化学中阳离子分离与鉴定的步骤,然而,实际操作过程根据实际情况还可能需要中和、萃取、逆流色谱、粒子分离以及晶格弛豫技术等多项技术进行支持。
在操作分离与鉴定步骤时,需要掌握相关基础知识,并仔细审查操作过程,以确保工作效果。
无机化学常见阳离子分离与鉴定.doc一、分离1、氢氧根离子(OH^-)氢氧根离子与金属离子形成的沉淀可以通过NaOH沉淀法分离出来。
在水溶液中,氢氧根离子与金属离子结合形成相应的金属氢氧化物,这些氢氧化物可以形成沉淀,实现分离。
一些阳离子的氢氧化物沉淀的颜色也是它们鉴定的基础之一。
2、氟化物(F^-)氟化物结合度和其他类似的离子相比较小,因此可以和其他阴离子分离。
使用鸟巢法可以分离出氟化物,该方法使用的络合剂是季铵盐鸟巢环(NH4)3 [FeF6]。
3、碳酸盐(CO32-)在水中,CO32-可以形成与Ca2+、Ba2+、Pb2+、Ag+等阳离子结合的沉淀。
因此,通过观察生成的沉淀的颜色可以确定阳离子的存在。
氰化物形成的配合物稳定性很高,一些盐可以沉淀分离氰化物。
通过加入相应的酸可以分解盐的氰化物,若遇到硝酸银时,则可以生成白色的沉淀。
硫酸盐与Barium离子结合可以形成硫酸钡的沉淀。
可以用BaCl2试剂发生反应,观察生成的白色沉淀可以确认硫酸盐的存在。
氯化物可以通过加入AgNO3实现分离,生成白色的AgCl沉淀。
AgCl颜色淡黄色并且易溶于NH3溶液中。
二、鉴定1、铁离子(Fe3+)Fe3+可以通过与硝酸铵一起存在,在加热时生成棕黄色的Fe(OH)3沉淀。
此外,还可以借助Ti(III)还原Fe3+为Fe2+,并使用Fenton试剂检测Fe2+的产生。
2、铜离子(Cu2+)Cu2+可以通过和N,N-二乙基-1,6-二亚胺染料组成的溶液反应而呈现出深蓝色,且颜色随着浓度的增加而增加。
Zn2+可以通过向含有鞣酸的溶液中加入氢氧化钠而产生白色沉淀进行鉴定。
Mn2+可以通过加入氢氧化钠和汞齐试剂而鉴定。
试剂与汞齐反应,生成黑色沉淀,同时文中的Mn(OH)2也被沉淀。
Mg2+可以通过向可溶性的Phenolphthalein-indicator(溶于环己酮)溶液中添加MgCl2所生成的红色沉淀进行鉴定。
Al3+可通过加入含有增效剂的Eriochrome Black T试剂检测出来,试剂经络合反应后转变为紫红色,而Al3+呈现出浅紫色。
1. 与HCl反应Ag+ HCl AgCl ↓白色,溶于氨水Hg22+ → Hg2Cl2↓白色,溶于浓HNO3及H2SO4Pb2+ PbCl2 ↓白色,溶于热水,NH4Ac、NaOH2. 与H2SO4反应Ba2+ BaSO4↓白色,难溶于酸Sr2+ H2SO4 SrSO4↓白色,溶于煮沸的酸Ca2+ CaSO4↓白色,溶解度较大,当Ca2+浓度很大时,才析出沉淀Pb2+ PbSO4↓白色,溶于NaOH、NH4Ac、热HCl、浓H2SO4,不溶于稀H2SO4 Ag+ Ag2SO4↓白色,在浓溶液中产生沉淀,溶于热水3. 与NaOH反应Al3+ AlO2-或[Al(OH)4]- 浓NaOHZn2+ 过量NaOH ZnO2-或[Zn(OH)4]2- Cu2+ Cu(OH)42- Pb2+ PbO2-或[Pb(OH)4]2- ΔSb3+ SbO2-或[Sb(OH)4]-Sn2+ SnO22-或[Sn(OH)4]2-4. 与NH3反应Ag+ Ag(NH3)2+Cu2+ 过量NH3 Cu(NH3)42+ 深蓝Cd2+ Cd(NH3)42+Zn2+ Zn(NH3)42+6. 与H2S或(NH4)2S反应Ag+ Ag2S↓黑色Pb2+ PbS↓黑色Cu2+ Cu S↓黑色Cd2+ CdS↓黄色Bi3+ 0.3mol·L-1HCl Bi2S3↓黑色Hg22+ HgS↓+Hg↓黑色溶于王水,Na2SHg2+ H2S HgS↓黑色Sb5+ Sb2S5↓橙色Sb3+ Sb2S3↓橙色溶于浓HCl,NaOH,Na2SSn4+ SnS2↓黄色Sn2+ SnS↓褐色溶于浓HCl,(NH4)2Sx,不溶于NaOH,Zn2+ NH4Cl ZnS↓白色,溶于稀HCl溶液,不溶于HAc溶液Al3+ NH3·H2O,H2S Al(OH)3↓白色,溶于强碱及稀HCl溶液1 实验:常见阳离子的分离与鉴定(一)。