复旦大学有机化学真题——1998
- 格式:doc
- 大小:98.50 KB
- 文档页数:4



简单题目1.用括号内的试剂和方法除去下列各物质的少量杂质,不正确的是A、苯中含有苯酚(浓溴水,过滤)B、乙酸钠中含有碳酸钠(乙酸、蒸发)C、乙酸乙酯中含有乙酸(饱和碳酸钠溶液、分液)D、溴乙烷中含有醇(水、分液)2.下列物质不能使酸性KMnO4溶液褪色的是A、B、C2H2C、CH3D、CH3COOH3.(CH3CH2)2CHCH3的正确命名是A、3-甲基戊烷B、2-甲基戊烷C、2-乙基丁烷D、3-乙基丁烷4.手性分子是指在分子结构中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。
下列分子中指定的碳原子(用*标记)不属于手性碳原子的是A、苹果酸B、丙氨酸C H3CH COOHNH2C、葡萄糖D、甘油醛CH CH2 CHOOHOH5.某烷烃发生氯代反应后,只能生成三种沸点不同的一氯代烃,此烷烃是A、(CH3)2CHCH2CH2CH3B、(CH3CH2)2CHCH3C、(CH3)2CHCH(CH3)2D、(CH3)3CCH2CH36.有—CH3,— OH,—COOH,—C6H5四种基团,两两结合而成的有机化合物中,水溶液具有酸性的有()A、3种B、4种C、5种D、6种7.下列说法错误的是()A、C2H6和C4H10一定是同系物B、C2H4和C4H8一定都能使溴水退色C、C3H6不只表示一种物质D、单烯烃各同系物中碳的质量分数相同8.常见有机反应类型有:①取代反应②加成反应③消去反应④酯化反应⑤加聚反应 ⑥缩聚反应 ⑦氧化反应 ⑧还原反应,其中可能在有机分子中新产生羟基的反应类型是 ( )A 、①②③④B 、⑤⑥⑦⑧C 、①②⑦⑧D 、③④⑤⑥9.乙醛和新制的Cu (OH )2反应的实验中,关键的操作是 ( ) A 、Cu (OH )2要过量 B 、NaOH 溶液要过量 C 、CuSO 4要过量 D 、使溶液pH 值小于710.PHB 塑料是一种可在微生物作用下降解的环保型塑料,其结构简式为:n OCHC 2H 5CO 。

复旦大学2023年博士入学考试化学真题问题1:请根据以下反应式,回答问题1至问题3:3FeS2 + 10HNO3 → 3Fe(NO3)2 + 2NO + 4H2O + 6S1. 在这个反应中,氧化态发生了什么样的变化?在这个反应中,硫的氧化态由-1变为0,氮的氧化态由+5变为+2,铁的氧化态由0变为+2。
2. 在这个反应中,是否发生了还原反应?请简要解释。
是的,这个反应中发生了还原反应。
还原反应是指物质损失氧或得到氢,或两者同时进行的反应。
在这个反应中,硫由-1的氧化态还原到0的氧化态,铁由0的氧化态还原到+2的氧化态。
因此,可以确定这是一个还原反应。
3. 在这个反应中,哪种物质是氧化剂?哪种物质是还原剂?请简要解释。
在这个反应中,硫是氧化剂,而硝酸是还原剂。
氧化剂是指在氧化还原反应中能够氧化其他物质的物质,而还原剂则是指在氧化还原反应中能够还原其他物质的物质。
在这个反应中,硫将铁的氧化态从0氧化到+2,硝酸则将硫的氧化态从-1氧化到0,因此可以确定硫是氧化剂,硝酸是还原剂。
问题2:请根据以下情景,回答问题4至问题5:材料科学研究人员正在开发一种可重复使用的太阳能电池。
该电池的关键部件是由特殊材料制备的光催化剂,它可以将太阳能转化为电能。
研究人员发现,在该太阳能电池中,光催化剂的稳定性是一个关键的问题。
4. 请说明为什么光催化剂的稳定性对太阳能电池的性能至关重要。
光催化剂的稳定性对太阳能电池的性能至关重要,因为太阳能电池的工作原理是将光能转化为电能。
如果光催化剂不稳定,它的效果将会受到影响,无法有效地将太阳能转化为电能。
因此,光催化剂的稳定性直接决定了太阳能电池的性能。
5. 请提出一种可能的方法来提高光催化剂的稳定性。
一种可能的方法来提高光催化剂的稳定性是改进其材料结构。
通过优化材料的组成和结构,可以增加光催化剂的稳定性,使其能够在长时间的工作中保持较高的效率。
此外,可以采用包覆技术将光催化剂包覆在稳定且具有良好导电性的材料上,以增加其耐用性和稳定性。

有机化学答案简介有机化学是研究有机化合物的结构、性质、合成和反应的一个分支学科。
有机化合物是由碳和氢以及其他元素(如氮、氧、硫等)构成的化合物,是生命存在的基础。
有机化学的历史有机化学的起源可以追溯到古代,但真正发展起来的是18世纪末到19世纪初。
由于西班牙医生Alonso de Borjas发现一种具有药用价值的有机化合物——水银硫化物,使得人们开始对有机化合物进行研究。
直到19世纪初,德国化学家Friedrich Wöhler成功地合成了尿素,从而打破了当时的思维定势,即有机物只能通过生命体合成。
随后,有机化学迅速发展,结构理论的提出、合成方法的改进使得有机化学成为化学学科中的一个重要分支。
有机化学的基本原理有机化学的研究对象是有机化合物,它们由碳原子和氢原子以及其他元素构成。
有机化合物具有三个基本特征:1.碳原子的四价性质:碳原子可以与其他原子形成共价键,使得有机化合物具有多样的结构。
2.同系物性质:有机化合物的结构相似,因此同一个有机化合物家族的化合物通常具有类似的性质。
3.功能团性质:有机化合物中的功能团决定了其化学反应的特性。
有机化合物的命名为了方便科学研究和交流,有机化合物需要进行命名。
有机化合物的命名遵循一定的规则,通常包括以下几个方面:1.主链选择:找到碳原子数量最多的连续链作为主链。
2.取代基命名:给主链上的取代基命名,并用数字表示它们在主链上的位置。
3.功能团命名:根据有机化合物中的功能团,标识其类型和位置。
有机化合物的命名规则相对复杂,但它们是整个有机化学的基础,符合规范的命名可以准确描述有机化合物的结构。
有机化合物的常见反应有机化合物具有丰富的反应性,常见的有机化学反应有以下几种:1.取代反应:取代反应是指一个原子或基团被另一个原子或基团代替的反应。
2.加成反应:加成反应是指两个或多个物质结合形成一个新的化合物的反应。
3.消除反应:消除反应是指一个分子中的原子或基团与另一个分子中的原子或基团结合形成两个分子的反应。
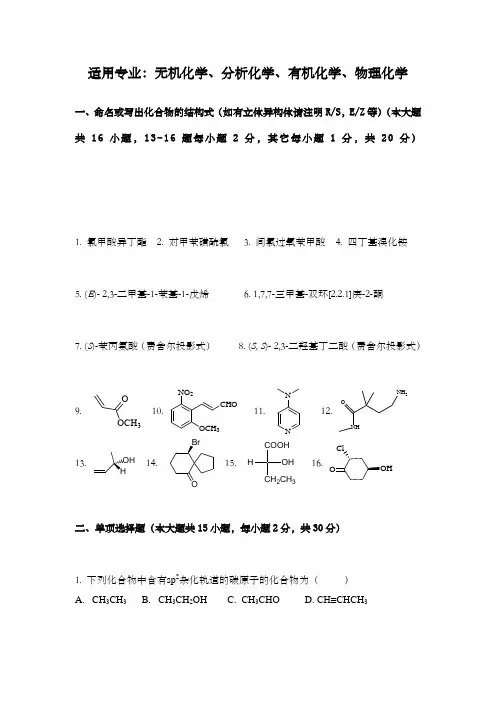
适用专业:无机化学、分析化学、有机化学、物理化学1. 氯甲酸异丁酯2. 对甲苯磺酰氯3. 间氯过氧苯甲酸4. 四丁基溴化铵5. (E )- 2,3-二甲基-1-苯基-1-戊烯6. 1,7,7-三甲基-双环[2.2.1]庚-2-酮7. (S )-苯丙氨酸(费舍尔投影式) 8. (S, S )- 2,3-二羟基丁二酸(费舍尔投影式)9. OCH 3O 10.CHO OCH 3NO 211.N N12.NH 2O13.14.15. H COOHOH CH 2CH 316.1. 下列化合物中含有sp 2杂化轨道的碳原子的化合物为( ) 一、命名或写出化合物的结构式(如有立体异构体请注明R/S ,E/Z 等)(本大题共16小题,13-16题每小题2分,其它每小题1分,共20分)二、单项选择题(本大题共15小题,每小题2分,共30分) A . CH 3CH 3 B . CH 3CH 2OH C . CH 3CHO D .CH≡CH CH 32. 下列化合物中,不能跟乙炔钠反应的是()A. CH3CH2CH2BrB. CH3CH2OCH2CH3C. CH3CH2OHD. CH3COCH33. 二氯丙烷可能的构造异构体数目是多少?()A.2B.4C. 5D. 64. 下列物质中碱性由强到弱的排列顺序是()(1)氢氧化钠(2)乙醇钠(3)苯酚钠(4)叔丁醇钠A. (1)(2)(3)(4)B. (1)(4)(2)(3)C. (1)(2)(4)(3)D. (4)(2)(1)(3)5. 下列试剂中,亲核性最强的是()A. 苯硫酚钠B. 苯酚钠C. 对甲氧基苯硫酚钠D. 对甲氧基苯酚钠6. 2,5-二甲基环戊烷甲酸总共有多少种立体化学异构体?()A. 2B. 4C. 5D. 67. 下列化合物最容易与水反应的是()A. 乙酸酐B. 乙酸乙酯C. 乙酰胺D. 乙酰氯8. 以下化合物碱性最弱的是()A.NHB.NC.NH2D. O2N NH29. 下列化合物,互为对映体的是()A.CH3H OHH BrCH3和BrH CH3H OHCH3 B.COOHH BrH BrH BrCOOH和COOHBr HBr HBr HCOOHC.3和3 D.Br HC2H5HCH3和H BrCH3HC2H510. 对苯二甲酸二乙酯的核磁共振1H谱有几组峰?化学位移由底到高的信号峰的面积比为多少?( )A. 4 组;3:2:1:1B. 4 组;3:1:1:2C. 3 组;3:2:2D. 3 组;2:3:211. 下列化合物构型为R的是()A.CH2OCH3CH2OHHO HB.CH2Cl2 C.H OHCH2OHCH3 D.CH3COOHHNH212. 以下化合物在相同的碱性条件下,水解速度由大到小排列的顺序是()(1)对硝基苯甲酸甲酯(2)苯甲酸甲酯(3)间硝基苯甲酸甲酯(4)对甲基苯甲酸甲酯A. (2)(4)(1)(3)B. (1)(3)(2)(4)C. (3)(1)(2)(4)D. (4)(2)(1)(3)13. 反-2-丁烯与溴加成得到的产物为()A. 内消旋体B. 非对映体C. 外消旋体D. 构造异构体14. 下列有机物进行硝化反应的活性最大的是()A. 氯苯B. 甲苯C. 苯甲醚D. 苯甲醛15. 倍半萜天然产物分子一般含有的碳原子数为( ) A . 5个 B. 10个 C. 15个 D. 20个三、完成下列反应(本大题共14小题,19问,每问2分,共38分)1. CH 3CH CHCH 32?2.?HCl3. HN BrK 2CO 3?4.氢溴酸?5.OZn (Hg ) 浓HCl?6.OCHOCH 2(CO 2Et)+六氢吡啶?7.COOEtCOOEt ??8.OCOCH -??9. CH 3CHO + 4HCHO -? 10.PhCHO +(CH 3CO)2O?11. H +N OH?12.O22+?13. (CH2)2CO2H2332NaH???14.BH3??四、化合物的鉴别或分离(本大题共2小题,共10分,请用流程线表示)1. 鉴别正丁炔、正丁醇、正丁醚、正丁醛、正丁酸及正丁胺。

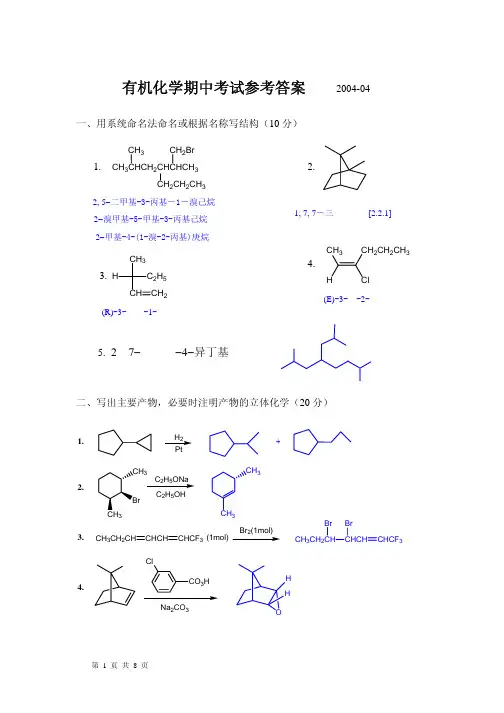

1998年上海高考化学试题第Ⅰ卷一、选择题(本题共20分),每小题2分,只有一个正确选项,答案涂写在答题纸上 1、下列物质中,可用于治疗胃酸过多的是A 碳酸钠B 氢氧化钠C 氧化钠D 碳酸钡2、近年来,加“碘”食盐田较少使用碘化钾,因其口感苦涩且在贮藏和运输中易变化,目前代之加入是 A I 2 B KIO C NaIO D KIO 3 3A B NC -D +4、钛(Ti )金属常被称为未来钢铁。
钛元素的同位素Ti 4622、Ti 4722、Ti 4822、Ti 4922、Ti 5022中,中子数不可能为 A 30 B 28 C 26 D 245、0.05mol 某单质与0.8g 硫在一定条件下完全反应,该单质可能是 A H 2 B O 2 C K D Zn6、 下列反应中,调节反应物用量或浓度不会改变反应产物的是 A 硫化氢在氧气中燃烧 B 铁在硫蒸气中燃烧 C 二氧化硫通入石灰水 D 硫酸中加入锌粉7、二氧化氮存在下列平衡:2NO 2(g)⇔N 2O 4(g)+Q 在测定NO 2的相对分子量时,下列条件中较为适宜的是 A 温度130℃、压强3.03×105Pa B 温度25℃、压强1.01×105Pa C 温度130℃、压强5.05×104Pa D 温度0℃、压强5.05×104Pa8、在100g 浓度为18mol/L 、密度为ρ(g/cm 3)的浓硫酸中加入一定量的水稀释成9mol/L 的硫酸,则加入的水的体积为 A 小于100mL B 等于100mL C 大于100mL D 等于100/ρmL9、在10mL0.01mol/L 的纯碱溶液中,不断搅拌并逐滴加入1.2mL 0.05mol/L 盐酸,完全反应后在标准状况下生成二氧化碳的体积为A 1.34mLB 2.240mLC 0.672mLD 0mL 10、以下现象与电化腐蚀无关的是A 黄铜(铜锌合金)制作的铜锣不易产生铜绿B 生铁比软铁芯(几乎是纯铁)容易生锈C 锈质器件附有铜质配件,在接触处易生铁锈D 银质奖牌久置后表面变暗 二、选择题(本题共30分),每小题3分,只有一个正确选项,答案涂写在答题纸上11、下列反应,其产物的颜色按红、红褐、淡黄、蓝色顺序排列的是 ①金属钠在纯氧中燃烧 ②FeSO 4溶液中滴入NaOH 溶液 ③FeCl 3溶液中滴入KSCN 溶液 ④无水硫酸铜放入医用洒精中 A ②③①④ B ③②①④ C ③①②④ D ①②③④12、设阿佛加德罗常数的符号为N A ,标准状况下某种O 2和N 2的混合气体m 克含有b 个分子,则n 克该混合气体在相同状况下所占的(L )体积应是A 22.4nb/N AB 22.4mb/bN AC 22.4nN A /mbD nbN A /22.4m13、冰箱致冷剂氟氯甲烷在高空中受紫外线辐射产生Cl 原子,并进行下列反应:Cl+O 3→ClO+O 2 ,ClO+O →Cl+O 2下列说法不正确的是A 反应后将O 3转变为O 2B Cl 原子是总反应的催化剂C 氟氯甲烷是总反应的催化剂D Cl 原子反复起分解O 3的作用14、将硫酸钾、硫酸铝、硫酸铝钾三种盐混合溶于硫酸酸化的水中,测得mol/L 15.0C -24SO =、m ol/L 055.0C 3A l =+,溶液的pH=2.0(假设溶液中H 2SO 4完全电离为H +和SO -24),则K +为 A 0.045mol/L B 0.035mol/L C 0.055mol/L D 0.040mol/L15、反应速度V 和反应物浓度的关系是用实验方法测定的。
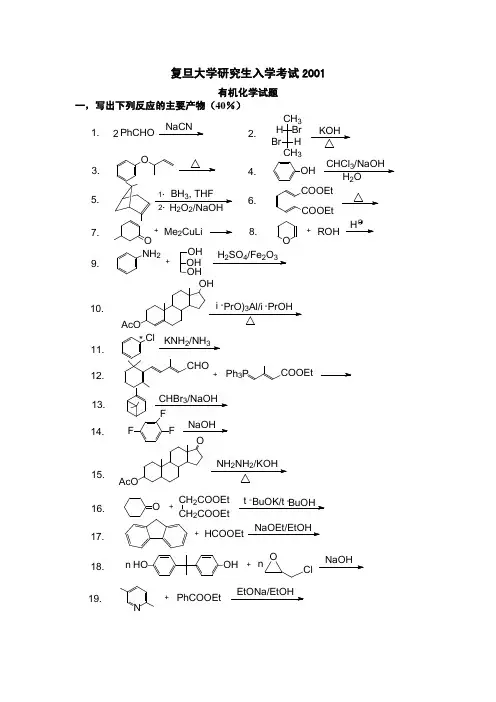

1998年全国高中学生化学竞赛(初赛)试题评析1.某芳香烃A,分子式C9H12。
在光照下用Br2溴化A得到两种一溴衍生物(B1和B2),产率约为1︰1。
在铁催化下用Br2溴化A也得到两种一溴衍生物(C1和C2);C1和C2在铁催化下继续溴化则总共得到4种二溴衍生物(D1、D2、D3、D4)。
(13分)(1)写出A的结构简式。
(5分)(2)写出B1、B2、C1、C2、D1、D2、D3、D4的结构简式。
(8分)【评析】A是“芳香烃”,至少要有一个苯环。
按分子式C9H12,已不可能有比苯环更高级的芳香环,例如萘的分子式是C10H8,已超过9个碳。
因而,C9H12是有烃基侧链的苯的衍生物是无疑的了。
问题是:侧链有几个?侧链的组成?粗想起来,以下所有结构似乎都是可能的:但分析试题提供的信息之一——光照下得到2种一溴衍生物,不必细想,就可以立即排除掉上列的2和7,因为2、7无疑只能得到一种一溴衍生物。
3也可排除,因为当溴取代三个甲基中的一个氢就可得到3种一溴衍生物,超过2种。
如果选手以为7的一溴衍生物不止一种,就说明没有一溴代只发生在侧链的 -碳上的基本知识。
这个基本知识比中学有机化学深,被命题人假设为完全可以通过课外活动达到的最低限度的高一级的有机化学知识。
究竟有多少参赛学生可以达到这个最低限度的高一级的有机化学知识?这需要作统计。
如果统计的结果,超过85% 的学生达不到这个高一级的有机化学知识,说明命题人过高地估计参赛选手的知识水平了,学生解答该题其余部分也就困难了。
1式也可以得到2种一溴代衍生物,但1-溴代甲基-2,3-二甲基苯的产率跟2-溴代甲基-1,3-二甲基苯的产率不会相等,不符合2种一溴衍生物的产率相等的信息。
于是只剩下4、5、6三种可能性。
然后再分析另一个信息——芳香环上的氢被溴取代得到2种一溴衍生物。
这又需要选手有芳香环上的氢被取代的定位知识——烃基是一种邻对位定向基团。
选手有这个超过中学化学知识的高一级的化学知识吗?命题人又一次面临对选手的化学知识的估计的考验。
1998有机化学试题(2×5=10分) 1. 安息香缩合; 2. Wittig 试剂; 3. 黄鸣龙改良法; 4. 重氮盐的偶联反应; 5. Hofmann 降级反应。
二,试比较指定的性质(2×5=10分)1. 酸性:a.CH 3Clb.c.( )>( )>( )2. 水溶液中碱性:N 2H 2N(a)(b)(c)( )>( )>( )3. 芳香族亲核取代反应:NO 2Cl ClNO 2NO 2Cl (a)(b)(c)( )>( )>( )4. 正碳离子的稳定性:CH3CH 3OHCH 3CH 3CH 3CCH 3a. b.c.( )>( )>( )5. 负碳离子稳定性:O O OOH OC 2H 5O Oa. b.c.( )>( )>( )三,在下面反应式括号内填上产物或原料或条件,如产物是手性的则请写出构型式,若无反应也请注明。
(2×10=20分)1.O +( )NaOEtEtOH OCHONa2.O H 3O( ) A3. A OH H 2O( ) 一种香料4.NH 2HO NaNO 2( )5.RLi+CO 2H 3O( )6.O+Br 2( )7.NH 2O 252( )8.OCH 3MgI 干乙醚NH 4Cl 2( )9.O10.3)222( )( )四,试写出下列反应机理(4×5=20分)1.OOHNaHCO 3DMSO 120-140。
1-2hr +A 5%B 80%并说明为什么A 少B 多。
2.CHO NH 2NO+O O NaOEtEtOH 3.CH3O+NH 2OHNO CH3NOCH3+4.3CH 3+五,试合成下列诸化合物(4×5=20分)1. 用CN 和CH3COCH 3合成OO2. 用 CO 2*为标记碳的原料及其它任何原料合成NH 2*3. 试由OHO合成CD 2OH 4. 用≤5C 的任何化合物及Wittig 试剂合成法合成H H(Z)六,试推测结构(10×2=20分)1. 化合物A(C 22H 27NO)不溶于稀酸,稀碱。
目 录
2012年复旦大学有机化学考研真题
2010年复旦大学有机化学考研真题
2009年复旦大学有机化学考研真题及详解
2008年复旦大学有机化学考研真题及详解
2007年复旦大学有机化学考研真题及详解
2006年复旦大学有机化学考研真题及详解
2005年复旦大学有机化学考研真题及详解
2004年复旦大学有机化学考研真题及详解
2003年复旦大学有机化学考研真题及详解
2002年复旦大学有机化学考研真题及详解
2001年复旦大学有机化学考研真题及详解
2000年复旦大学有机化学考研真题及详解
1999年复旦大学有机化学考研真题
1998年复旦大学有机化学考研真题
1997年复旦大学有机化学考研真题(含部分答案)
1996年复旦大学有机化学考研真题及详解
1995年复旦大学有机化学考研真题及详解
1994年复旦大学有机化学考研真题及详解
1993年复旦大学有机化学考研真题及。
有机化学大学真题答案解析一直是许多大学生头疼的科目之一。
近年来,大学考试的难度也越来越大,考生们需要具备深厚的理论知识和实际操作能力。
本文将从几个典型的题目入手,解析其答案,帮助考生更好地备考。
第一题是关于有机化合物的命名。
通常来说,我们需要了解一些命名规则,如丙酮、乙醇等,这些是比较简单的,容易记忆和辨认的有机化合物。
但在实际考试中,往往会涉及一些复杂的有机化合物,需要我们深入理解的原理和规律。
例如,题目给出了一个结构式,让我们给出命名。
这个题目需要考生掌握不同官能团的命名规则,同时要了解有机化合物的结构特点。
通过将有机化合物的官能团和相应的命名规则联系起来,我们可以正确地命名这个复杂的有机化合物。
第二题是有关化学反应机理的问题。
在中,我们经常遇到各种各样的化学反应,如取代反应、加成反应、消除反应等。
对于这些化学反应的机理,我们需要通过实验和理论知识相结合来进行分析。
例如,题目给出了一个反应方程式,让我们推测反应的具体机理。
对于这个题目,考生需要先了解该反应的类型,然后结合已有的实验结果和理论知识,推断出可能的反应机理。
通过分析反应物和产物的结构特点,我们可以推断出反应的可能机理,并进行解析。
第三题是有关有机合成的问题。
有机合成是的重要内容之一,也是考察考生解决实际问题能力的一个重要方面。
在有机合成中,我们需要根据给出的反应方程式和条件,设计合成路线,完成所需有机化合物的合成。
例如,题目给出了一个目标化合物,让我们设计合成路线。
对于这个题目,考生需要先确定首次发生的反应类型,然后考虑需要进行的反应和合成步骤,最后得到所需的有机化合物。
通过思考和分析,我们可以得到最终的合成方案,并进行解析。
作为一门重要的基础科学,除了在大学中学习和应用之外,也在许多行业中发挥着重要的作用。
的知识和技能不仅对于化学专业的学生来说是必备的,对于其他专业的学生也有重要的借鉴意义。
因此,学好,不仅仅是为了应付考试和取得好成绩,更是为了将来工作中的实际应用和发展。
复旦大学研究生入学考试1998
有机化学试题
一,试举例说明下列反应或试剂(不要写机理)(2×5=10分) 1. 安息香缩合; 2. Wittig 试剂; 3. 黄鸣龙改良法; 4. 重氮盐的偶联反应; 5. Hofmann 降级反应。
二,试比较指定的性质(2×5=10分)
1. 酸性:a.
CH 3
Cl
b.
c.
( )>( )>( )
2. 水溶液中碱性:N 2H 2N
(a)(b)
(c)
( )>( )>( )
3. 芳香族亲核取代反应:
NO 2
Cl Cl
NO 22Cl (a)(b)(c)( )>( )>( )
4. 正碳离子的稳定性:
CH
3CH 3OH
CH 3
CH 3
CH 3
C
CH 3a. b.
c.
( )>( )>( )
5. 负碳离子稳定性:O O O
OH OC 2H 5
O O
a. b.
c.
( )>( )>( )
三,在下面反应式括号内填上产物或原料或条件,如产物是手性的则请写出构
型式,若无反应也请注明。
(2×10=20分)
1.O +
( )
NaOEt
EtOH O
CHONa
2.O H 3O
( ) A
3. A OH 2( ) 一种香料
4.2HO NaNO 2( )
5.
RLi
+
CO 2
H 3O
( )
6.O
+
Br 2
( )7.NH 2252
( )8.
O
CH 3MgI 干乙醚
NH 4Cl
2( )
9.
O
10.3)2
22
( )
( )
四,试写出下列反应机理(4×5=20分)
1.
O
OH
NaHCO 3
DMSO 120-140。
1-2hr +
A 5%
B 80%
并说明为什么A 少B 多。
2.CHO NH 2N
O
+
O O NaOEt
EtOH 3.CH
3O
+NH 2
OH N
O CH
3
N
O
CH
3
+
4.
3CH 3+
五,试合成下列诸化合物(4×5=20分)
1. 用
CN 和
CH 3
COCH 3合成
O
O
2. 用 CO 2*为标记碳的原料及其它任何原料合成
NH 2
*3. 试由OH
O
合成CD 2OH 4. 用≤5C 的任何化合物及Wittig 试剂合成法合成
H (Z)
六,试推测结构(10×2=20分)
1. 化合物A(C 22H 27NO)不溶于稀酸,稀碱。
A +HCl/H 2
O 苯甲酸+溶液。
将此溶液碱化生成B, B +苯甲酰氯又生成A 。
B +NaNO 2/HCl 无N 2放出。
B 是非手性的,B +过量CH 3I,再用Ag 2O 处理并加热,生成C(C 9H 19N)和苯乙烯C +过量CH 3I 再用Ag 2O 处理并加热生成一个烯烃D 。
D 和
O
+
Ph 3P=CH 2反应的产物一样。
试写出A,B,C,D 结构。
并简述理由。
2. 长叶薄荷酮和丙酮在EtOH/EtONa 中反应:
O
+
CH 3COCH 3
有几个人分别提出生成产物的结构:O
O
O
O
产物的HNMR IR
0.9,(3H,d) 1640cm 1.1,(6H,s) 1675cm 2.0-2.2,(8H,m) 2.3,(2H,s)6.5,(1H,s)
-1
-1
试判断真正产物是哪一个,并写出波谱数据的归属。
复旦大学研究生入学考试1998
有机化学试题答案
一,试举例说明下列反应或试剂(不要写机理)(2×5=10分)
1. 安息香缩合:ArCHO +KCN
Ar C CH Ar O
Ar= C 6H 5p -CH 3C 6H 5
O
机理:
Ar C H O Ar C
OH
C
O Ar C OH C Ar
H Ar C O
C Ar OH H Ar C CH Ar OH O 2. Wittiy 试剂:Ph 3P =C
R ,
CH 3CHO
+
Ph 3P=C
CH 3322C=C CH 3
COCH 33H
3.
黄鸣龙改良法:RCR O
RCH 2R
,,
C 6H
5COCH 2CH 3
C 6H 5CH 2CH 2CH 3
4. 重氮盐的偶联反应:+
PhR -p
PhN=NPhR -p R=OH , NR 2
PhN 2
X
2+
PhOH -p
PH=8
PhN=NPhOH -p 5. Hofmann 降级反应:RCH 2CH 2N(CH 3)3OH
RCH=CH 2+N(CH 3)
3
CH 3CH 22CH 3
.CH 3I
.AgOH CH 3CH 2CHN(CH 3)3OH
CH 3CH 3CH 2CH =CH 2
二,试比较指定的性质(2×5=10分)。