二苯乙二酮的制备
- 格式:doc
- 大小:29.50 KB
- 文档页数:2

二苯乙二酮的制备一、实验目的1. 学习用温和氧化剂氧化制备二苯基乙二酮的原理和方法。
2. 进一步巩固加热回流和重结晶等基本操作。
二、实验原理二苯乙二酮是合成抗癫痫药物--苯妥英钠的中间体, 紫外光照射下,二苯基乙二酮裂解为自由基,引发聚合物链间交联,用作聚合物的紫外线固化剂。
最近的研究表明,二苯基乙二酮是羧酸酯酶的选择性抑制剂。
二苯基乙二酮通常由安息香氧化而得,常用的氧化剂有硝酸、三氯化铁等,用硝酸法产率高、原料价廉,但反应中释放出的NO 2有害。
CO C OH CO 安息香可以被温和的氧化剂三价铁离子氧化生成α-二酮,铁盐本身被还原成亚铁态。
不仅避免了硝酸法产生的有毒气体,而且收率较高、操作方便安全CO C OH H三、仪器和药品主要仪器:电热套、天平、烧瓶,冷凝管,抽滤瓶,布氏漏斗,循环水泵、熔点仪等 主要药品 安息香 2.12g (10.0mmol), FeCl 3•6H 2O 9.00g (34.1mmol) 试剂及产物物理常数名称分子量密度(d 204)熔点(℃)沸点(℃)安息香 212.24 1.219 135 194 二苯基乙二酮 210.221.08495~96 347四、实验步骤实验装置如右图1. 合成3CO2H 2O39H2O粗品2. 纯化 75%乙醇重结晶3. 表征熔点 95-96℃4. 产量、产率五、注意事项1. 二苯乙二酮易结块,加水冷却时应用玻璃棒搅动,防止结成大块2. 产物用于下次实验的原料【思考题】1.乙酸和氯化铁各起什么作用?2.本实验可以用KMnO4.重铬酸钠等氧化剂氧化吗?。

二苯乙二酮的制备实验报告二苯乙二酮的制备实验报告引言:二苯乙二酮(简称DPE)是一种重要的有机合成中间体,广泛应用于医药、染料、农药等领域。
本实验旨在通过合成反应制备DPE,并通过实验结果分析反应机理和优化反应条件。
实验方法:1. 实验材料和仪器:本实验使用的材料包括苯乙酮、苯甲醛、氢氧化钠、氢氧化铜等。
实验仪器包括反应釜、冷凝器、恒温槽、磁力搅拌器等。
2. 实验步骤:(1)准备反应体系:将苯乙酮、苯甲醛、氢氧化钠、氢氧化铜按一定摩尔比例加入反应釜中。
(2)反应过程控制:将反应釜置于恒温槽中,控制反应温度为80℃,并通过磁力搅拌器保持反应体系均匀混合。
(3)反应结束处理:反应时间达到预定时间后,停止加热,待反应体系冷却至室温。
(4)产物分离与纯化:将反应体系过滤,得到混合物,通过结晶、溶剂萃取等方法纯化产物。
实验结果:通过实验,我们成功合成了二苯乙二酮。
产物经过纯化后,得到白色结晶固体。
通过红外光谱、核磁共振等技术对产物进行了表征。
实验结果表明,所得产物符合二苯乙二酮的结构特征。
讨论与分析:1. 反应机理:二苯乙二酮的制备主要是通过酮醛缩合反应实现的。
在碱性条件下,苯乙酮和苯甲醛发生缩合反应,生成二苯乙二酮。
氢氧化钠和氢氧化铜作为催化剂,促进反应进行。
2. 反应条件优化:在本实验中,我们选择了80℃作为反应温度。
这是因为在这个温度下,反应速率较快,而且产物的收率较高。
然而,反应温度过高可能导致副反应的发生,影响产物的纯度。
因此,选择适当的反应温度对于提高产物质量至关重要。
3. 产物纯化方法:产物的纯化对于获得高纯度的二苯乙二酮至关重要。
在本实验中,我们采用了结晶和溶剂萃取的方法。
结晶是通过控制溶剂的温度和浓度,使产物从溶液中结晶出来。
溶剂萃取是通过选择合适的溶剂,将产物从混合物中分离出来。
这些方法能够有效提高产物的纯度。
结论:通过本实验,我们成功合成了二苯乙二酮,并通过实验结果对反应机理和优化条件进行了讨论与分析。

二苯乙二酮的制备实验报告实验室日期:XXXX年XX月XX日二苯乙二酮的制备实验报告实验目的:1. 学习二苯乙二酮的制备方法和工艺流程;2. 掌握实验中关键步骤的操作方法和注意事项;3. 熟悉实验室的设备和仪器,提高实验技能和安全意识。
实验原理:二苯乙二酮(又称苯并烯酮)是一种有机化合物,其分子式为C14H10O,结构中两个苯环通过CO连接在一起。
二苯乙二酮的合成方法有多种,通常采用二苯甲酮为始料,通过反应、还原、酸化等多个步骤制得。
实验材料:二苯甲酮、NaOH、异丙醇、丙酮、硫酸、稀氢氧化钠溶液等。
实验步骤:1. 预处理:将所需材料按照所需比例精确称量,备好实验仪器和器材。
2. 制备苯并酚:将50g二苯甲酮溶于200mL异丙醇中,加入30mL 2.5mol/L NaOH溶液,用搅拌器搅拌均匀后加热回流2小时。
反应结束后立即加水降温,并用过滤纸滤出固体,用水或乙醇洗涤并干燥。
3. 制备苯并烯酮:将50g苯并酚与100mL丙酮、10mL H2SO4混合后,加热回流4小时。
反应结束后加水降温,并用乙醇洗涤固体,过滤并干燥,最终得到苯并烯酮。
4. 测定产率和纯度:通过红外光谱、核磁共振、质谱等手段对制得的产物进行检测,确定其结构和纯度,最终计算得到产率。
实验结果:通过实验制备得到了苯并烯酮产物,其红外光谱表明C=O伸缩振动峰位为1675cm-1,符合苯并烯酮的结构特征。
核磁共振和质谱的结果进一步证实了产物的结构和纯度。
实验总结:通过本次实验,对二苯乙二酮的制备方法和技术要求有了更深入的理解,同时也感受到了实验技能、仪器设备和安全意识等方面的提高。
在今后的实验项目中,将继续加强实验室安全管理,完善实验技巧和知识储备,为科学研究和实践创新奠定基础。

二苯乙二酮的合成一、引言二苯乙二酮是一种重要的有机化合物,广泛应用于化学、医药和材料领域。
其合成方法也多种多样,本文将介绍其中一种常见的合成方法。
二、反应原理二苯乙二酮的合成反应式如下:该反应是通过芳香族亲电取代反应来实现的。
在该反应中,苯乙酮被溴化铁处理后生成α-溴代苯乙酮,再经过芳香族亲电取代反应生成目标产物。
三、实验步骤1. 取1.5g苯乙酮加入至100mL三口瓶中;2. 加入10mL无水乙醇和3mL浓HCl,并搅拌均匀;3. 加入0.5g溴化铁,并继续搅拌30分钟;4. 加入10mL无水乙醇和0.5g苯并三氯甲烷(催化剂),并搅拌均匀;5. 将混合物倒入250mL锥形瓶中,加入20mL浓氢氧化钠溶液,并用水冷却至室温;6. 将产物用醚提取,用水洗涤,然后蒸干醚;7. 用乙醇重结晶,得到二苯乙二酮。
四、实验注意事项1. 溴化铁具有腐蚀性和毒性,操作时要戴手套和口罩;2. 操作过程中,应保持通风良好;3. 实验中使用的溶剂要干燥无水;4. 操作过程中应注意安全。
五、实验结果及分析在实验中,我们按照上述步骤合成了二苯乙二酮。
经过提取、洗涤和重结晶等步骤后,我们得到了白色的结晶体。
通过红外光谱仪进行检测,发现其吸收峰符合二苯乙二酮的特征峰。
这表明我们成功地合成了目标产物。
六、总结通过本次实验,我们掌握了一种常见的合成二苯乙二酮的方法,并学会了如何进行反应条件的选择和操作技巧。
同时,在实验过程中也加深了对有机化学反应原理的理解和认识。

安息香,冰醋酸和浓硝酸合成二苯乙二酮反应机理二苯乙二酮是一种有机化合物,也被称为双酮,是一种重要的化工中间体,在许多有机合成反应中都有广泛的应用。
本文将介绍安息香、冰醋酸和浓硝酸合成二苯乙二酮的反应机理。
首先,我们来介绍一下反应涉及的三种化合物。
安息香,又称苦杏仁油(Benzaldehyde),是一种有机化合物,化学式为C6H5CHO,具有苦杏仁味,主要来源于苦杏仁油,也可通过苯乙烯氧化或氧化苯乙烯制备。
冰醋酸,化学式为CH3COOH,是一种常见的有机酸,是一种无色液体,有刺激性气味,可溶解于水和大多数有机溶剂,是一种重要的化工原料,也用于食品添加剂。
浓硝酸,化学式为HNO3,是一种强氧化性酸,是一种无色或微黄色的液体,有强烈刺激性气味,可以和多种物质反应,是一种重要的化工原料,也用于制取硝胺等化合物。
合成二苯乙二酮的反应机理如下:首先,将安息香溶于冰醋酸中,得到一个间歇产物,这个产物在实验室中可以通过多种方法检测到,比如在紫外可见光谱中具有特殊吸收峰。
然后,在溶液中缓慢加入浓硝酸,随着浓硝酸的逐渐加入,产物的吸收峰开始减弱,并最终消失。
最终,得到了二苯乙二酮的晶体,可以通过重结晶纯化,从而得到纯的二苯乙二酮。
接下来,我们来详细分析这个反应的机理。
首先是安息香和冰醋酸的反应。
在溶剂中,苯乙酰将氧化得到醛基,冰醋酸的质子与氧原子形成氢键,从而加速羰基的质子化。
在这种情况下,羰基可以快速地被亲电试剂攻击,生成乙酰乙酸苯酰醛的间歇产物。
然后是乙酰乙酸苯酰醛和浓硝酸的反应。
在这步反应中,间歇产物的芳基碳原子嵌入硝基团中形成的6-硝基乙酰苯酰醛(略称硝化化物)分解,生成更易于亲电试剂攻击的硝化中间体,硝化中间体与冰醋酸中的带负电荷的氢中间测试反应生成一3,5 -二硝化苯基醛,并不断向下转化与苯甲酰乙酸形成一个稳定的环,硝基所在的碳原子紧张而环化得有利的能量。
在进一步吸成分子的连环反应下,首先二硝化苯基甲醛被氢氧化为配偶体,分解产生的配偶体也可以氧化地个阴离子氧化。

二苯乙二酮的合成简介二苯乙二酮是一种重要的有机化合物,可以用于制备染料、医药和聚合物等。
它的合成方法主要有催化氧化法和酸促作用法。
本文将详细介绍二苯乙二酮的合成方法及工艺条件,并对合成过程中的反应机制和影响因素进行探讨。
催化氧化法催化氧化法是一种常用的合成二苯乙二酮的方法。
该方法的反应原料包括苯乙烯和氧气,催化剂常用的是铁离子。
具体合成步骤如下:原料准备准备苯乙烯和氧气作为反应的原料。
苯乙烯是一种无色液体,常用作有机溶剂和合成原料。
氧气是一种常见的氧化剂,广泛应用于各个领域。
反应条件调控将催化剂加入反应体系中,催化剂的含量和种类会对反应效果和产物质量产生重要影响。
一般情况下,铁离子是一种较常用的催化剂。
同时,调节反应温度和反应时间也是关键的因素,一般反应温度在80-120°C之间,反应时间在4-8小时。
反应进行将苯乙烯和氧气以一定的比例加入反应器中,加热至设定反应温度,同时将催化剂加入反应系统中。
反应进行时,要控制氧气的供应速度和催化剂的加入量,以保证反应的高效进行。
产物分离纯化反应结束后,通过蒸馏、结晶等方法对产物进行分离纯化。
蒸馏是将混合物按照其沸点差异进行分离,结晶则是通过溶解度差异将产物从溶液中析出。
产物性质分析对合成得到的二苯乙二酮进行物理性质和化学性质的测试分析,以确定产物的纯度和结构。
酸促作用法除了催化氧化法外,酸促作用法也是一种常用的二苯乙二酮合成方法。
这种方法的反应原料主要包括苯乙烯和二氯甲烷,反应过程需要在酸性条件下进行。
具体合成步骤如下:原料准备准备苯乙烯和二氯甲烷作为反应的原料。
二氯甲烷是一种无色易挥发的液体,常用作有机溶剂和反应介质。
酸催化在反应体系中添加酸性催化剂,常用的有浓硫酸或氯化亚砜。
酸催化将加速二苯乙烯的反应进程,并促使生成二苯乙二酮。
调控酸催化剂的添加量和反应温度对反应效果具有重要影响。
反应进行将苯乙烯和二氯甲烷按一定的比例加入反应体系中,在酸性条件下反应。

二苯乙二酮的制备实验报告一、实验目的1、学习安息香氧化制备二苯乙二酮的原理和方法。
2、掌握重结晶提纯固体有机物的操作技术。
二、实验原理二苯乙二酮可以由安息香经氧化反应制得。
常用的氧化剂有硝酸、三氯化铁等。
本实验使用三氯化铁作为氧化剂,其反应方程式如下:C₁₄H₁₂O₂(安息香)+ 2FeCl₃ → C₁₄H₁₀O₂(二苯乙二酮)+ 2FeCl₂+ 2HCl在反应过程中,三氯化铁被还原为氯化亚铁,同时生成盐酸。
反应结束后,产物经过滤、洗涤、重结晶等操作进行提纯。
三、实验仪器与试剂1、仪器圆底烧瓶(100ml)、回流冷凝管、布氏漏斗、抽滤瓶、玻璃棒、电子天平、恒温水浴锅、温度计。
2、试剂安息香、三氯化铁、冰醋酸、乙醇、石油醚。
四、实验步骤1、在 100ml 圆底烧瓶中,加入 5g 安息香、125ml 冰醋酸和 15g 三氯化铁。
装上回流冷凝管,在沸水浴中加热回流 45 60 分钟。
2、反应结束后,将反应液冷却至室温。
然后,在搅拌下倒入 50ml 冷水中,此时有黄色沉淀析出。
3、用布氏漏斗抽滤,并用冷水充分洗涤沉淀,以除去反应中生成的氯化亚铁等杂质。
4、粗产物用乙醇进行重结晶。
将粗产物置于 100ml 圆底烧瓶中,加入适量乙醇,装上回流冷凝管,在水浴上加热至固体完全溶解。
5、停止加热,让溶液自然冷却至室温,然后再放入冰水中冷却,使结晶完全。
6、再次抽滤,干燥,得到纯净的二苯乙二酮晶体。
五、实验注意事项1、反应过程中要保持回流装置的密封性,防止溶剂挥发。
2、控制反应温度在沸水浴中,温度过高可能导致副反应的发生。
3、重结晶时,选择合适的溶剂和用量,以保证产物的纯度和收率。
4、过滤和洗涤过程中要尽量减少产物的损失。
六、实验结果与讨论1、产量:经过干燥称重,得到二苯乙二酮的产量为_____g。
2、产率:根据安息香的用量和二苯乙二酮的理论产量,计算出产率为_____%。
3、结果讨论(1)分析产率高低的可能原因。

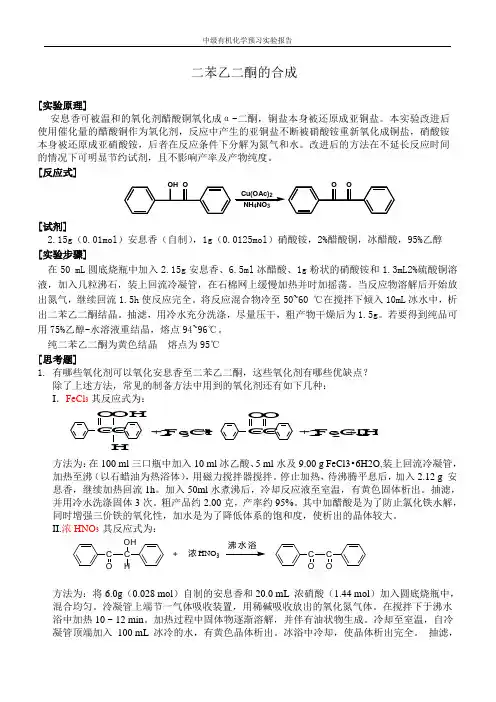
二苯乙二酮的合成[实验原理]安息香可被温和的氧化剂醋酸铜氧化成α-二酮,铜盐本身被还原成亚铜盐。
本实验改进后使用催化量的醋酸铜作为氧化剂,反应中产生的亚铜盐不断被硝酸铵重新氧化成铜盐,硝酸铵本身被还原成亚硝酸铵,后者在反应条件下分解为氮气和水。
改进后的方法在不延长反应时间的情况下可明显节约试剂,且不影响产率及产物纯度。
[反应式] O H OC u (O A c)2N H 4N O 3O O[试剂]2.15g (0.01mol )安息香(自制),1g (0.0125mol )硝酸铵,2%醋酸铜,冰醋酸,95%乙醇[实验步骤]在50 mL 圆底烧瓶中加入2.15g 安息香、6.5ml 冰醋酸、1g 粉状的硝酸铵和1.3mL2%硫酸铜溶液,加入几粒沸石,装上回流冷凝管,在石棉网上缓慢加热并时加摇荡。
当反应物溶解后开始放出氮气,继续回流1.5h 使反应完全。
将反应混合物冷至50~60 ℃在搅拌下倾入10mL 冰水中,析出二苯乙二酮结晶。
抽滤,用冷水充分洗涤,尽量压干,粗产物干燥后为1.5g 。
若要得到纯品可用75%乙醇-水溶液重结晶,熔点94~96℃。
纯二苯乙二酮为黄色结晶 熔点为95℃[思考题]1. 有哪些氧化剂可以氧化安息香至二苯乙二酮,这些氧化剂有哪些优缺点?除了上述方法,常见的制备方法中用到的氧化剂还有如下几种:I .FeCl 3 其反应式为:FeCl 2HCl ++22FeCl 3H OH CC O + C O C O 2 方法为:在100 ml 三口瓶中加入10 ml 冰乙酸、5 ml 水及9.00 g FeCl3•6H2O,装上回流冷凝管,加热至沸(以石蜡油为热浴体),用磁力搅拌器搅拌。
停止加热,待沸腾平息后,加入2.12 g 安息香,继续加热回流1h 。
加入50ml 水煮沸后,冷却反应液至室温,有黄色固体析出。
抽滤,并用冷水洗涤固体3次。
粗产品约2.00克,产率约95%。
其中加醋酸是为了防止氯化铁水解,同时增强三价铁的氧化性,加水是为了降低体系的饱和度,使析出的晶体较大。

二苯乙二酮的制备
一、实验目的
1、了解安息香氧化合成二苯基乙二酮的氧化剂选择。
2、熟练掌握回流、重结晶等实验操作。
二、实验原理
二苯乙二酮可以由安息香经氧化制得。
氧化剂可以为浓硝酸,但反应生成的二氧化氮对环境污染严重。
也可以使用Fe3+作为氧化剂,铁盐被还原成Fe2+。
本实验改进后采用醋酸铜作为氧化剂。
这样反应中产生的亚铜盐不断被硝酸铵重新氧化成铜盐,硝酸铵本身被还原成亚硝酸铵,后者在反应条件下分解为氮气和水。
改进后的方法在不延长反应时间的情况下可明显节约试剂,且不影响产率及产物纯度。
三、仪器及药品
仪器:圆底烧瓶、球形冷凝管、抽滤瓶、布氏漏斗等
药品:安息香、硝酸铵、冰醋酸、醋酸铜、乙醇等
四、实验步骤
在50mL圆底烧瓶中加入2.15 g安息香、8 mL冰醋酸、1 g的硝酸铵和2.0 mL 2%硫酸铜溶液,装上回流冷凝管,缓慢加热,当反应物溶解后,开始放出氮气,继续回流1.5 h使反应完全。
将反应混合物冷至50-60 oC,在搅拌下倒入10
mL冰水中,析出二苯乙二酮晶体。
抽滤,用冷水充分洗涤,得到粗产物。
可用75%的乙醇水溶液重结晶,得到二苯乙二酮。

二苯乙二酮的制备问题讨论二苯乙二酮(也称为二苯基丙二酮或二截片)是一种具有重要化学应用的有机化合物。
它在医学、化学、材料科学、光学等领域都具有广泛的用途。
然而,二苯乙二酮的制备过程中存在着一些问题和挑战,需要仔细讨论。
一、反应原理及条件二苯乙二酮的化学结构为:C6H5-CO-CH2-CO-C6H5。
它是由苯甲醛和乙酮缩合而制得的。
反应的机理为:首先苯甲醛和乙酮在碱的催化下形成烯丙基醇,然后经过内消旋反应生成二苯乙烯,最后二苯乙烯在氧化剂的作用下形成二苯乙二酮。
具体的反应条件如下:1.原材料:苯甲醛和乙酮2.催化剂:碱,如氢氧化钠、氢氧化钾、氢氧化钠、醋酸钠等3.内消旋反应剂:醋酸或其他酸类溶液4.氧化剂:铬酸钾、二氧化锰、过氧化氢等5.反应温度:常温至40℃之间6.反应时间:约2-3小时7.反应溶剂:常用的有苯、甲苯、醚、丙酮等二、反应中存在的问题1.反应副产物多:苯甲醛和乙酮缩合反应是一种多步反应,其中存在着许多副反应,比如苯甲醛的氧化、醛的脱水等,这些副反应会降低反应产率、浪费原材料并增加产品处理成本。
2.反应过程中对催化剂的检测困难:催化剂在反应中扮演核心作用,但是检测催化剂的种类和浓度却十分困难,因为它们通常处于微量状态,此外,当催化剂存在于反应溶液中时,它在反应结束后很难被消除。
这对反应的控制造成了困难。
3.反应产物不纯:在反应过程中,产物中可能存在未缩合的苯甲醛、乙酮、二苯乙烯等杂质,并在后期制备中需进行去污、纯化工作,使反应产物纯度下降。
4.环境污染问题:在反应过程中,存在着铬酸钾等强氧化剂,如反应溶液处理不当,易造成环境污染,对人身健康和周围环境带来潜在的威胁。
三、改进方法为了有效解决上述问题,可以采取以下改进方法:1.优化催化剂:优化催化剂的选择、浓度、反应温度等参数,选择使用低毒性、低污染的催化剂;2.精准控制反应参数:采用先进的反应控制技术,实现反应过程在线监测,及时调整反应参数,降低不必要的副反应,提高反应产率;3.高效分离纯化:优化分离纯化工艺,选择合适的溶剂体系,采用适当的物理、化学方法分离有价值的中间体或产品,减少处理成本,提高产品纯度;4.绿色化改造:尽量减少或杜绝铬酸钾等有害物的使用,采用无机盐、酶催化等绿色化合物作为替代材料和方法,以避免环境污染。
任务名称:二苯乙二酮的制备问题讨论1. 简介二苯乙二酮,也被称为二苯甲酮,是一种重要的有机合成中间体。
它具有广泛的用途,包括药物合成、染料合成和聚合物材料等领域。
二苯乙二酮的制备是许多化学实验室和工业生产中关注的问题。
本文将就二苯乙二酮的制备问题进行全面、详细、完整且深入地探讨。
2. 制备方法二苯乙二酮的制备方法有多种,下面将介绍其中比较常用的几种方法。
2.1 无催化剂氧化反应这是一种简单的制备方法,通过苯甲醛的氧化反应得到二苯乙二酮。
反应方程式如下所示:苯甲醛 + 氧气→ 二苯乙二酮 + 水这种方法的优点是操作简单,原料易得,但反应速度较慢,需要较长的反应时间,并且产率较低。
2.2 二氧化锰氧化反应二氧化锰可以作为催化剂,在二苯乙烯和氧气的作用下催化生成二苯乙二酮。
反应方程式如下所示:二苯乙烯 + 氧气→ 二苯乙二酮这种方法的优点是反应速度较快,产率较高。
但需要注意的是,二氧化锰是一种有毒物质,操作时应注意安全。
2.3 酸催化反应酸催化反应是二苯乙二酮制备的常用方法之一。
在酸催化剂的作用下,苯乙烯和苯甲醛发生反应生成二苯乙二酮。
反应方程式如下所示:苯乙烯 + 苯甲醛→ 二苯乙二酮 + 水这种方法的优点是反应速度快,产率高。
酸催化剂的选择对反应效果有重要影响,常用的酸催化剂包括硫酸、盐酸和磷酸等。
3. 反应条件优化为了提高二苯乙二酮的制备效果,需要对反应条件进行优化。
以下是几个影响制备效果的关键因素:3.1 反应温度反应温度对反应速率和产率都有重要影响。
一般情况下,较高的反应温度会提高反应速率,但过高的温度可能导致副反应的发生。
因此,需要在考虑速率和产率的基础上选择适当的反应温度。
3.2 催化剂选择与用量不同的催化剂对二苯乙二酮的制备有不同的影响。
催化剂的选择应考虑其催化活性和安全性等因素。
催化剂的用量也需要进行优化,过少的催化剂会影响反应速率和产率,而过多的催化剂可能导致催化剂的浪费。
3.3 物质用量比反应物的用量比也是影响二苯乙二酮制备效果的关键因素。
二苯乙二酮的实验报告二苯乙二酮的实验报告引言:二苯乙二酮是一种有机化合物,化学式为C14H10O2。
它是一种重要的有机合成中间体,广泛应用于药物、染料和高分子材料等领域。
本实验旨在通过合成二苯乙二酮的方法,探究其合成过程和一些相关性质。
实验方法:1. 实验材料和仪器本次实验所需材料包括苯甲酸、苯乙酮、硫酸、冰醋酸、氢氧化钠等,实验仪器包括反应瓶、冷凝器、温度计、称量器等。
2. 实验步骤(1) 将苯甲酸和苯乙酮按一定的摩尔比例加入反应瓶中,加入适量的硫酸作为催化剂。
(2) 将反应瓶置于加热设备中,加热反应溶液至适当温度,反应进行一定时间。
(3) 反应结束后,用冰醋酸进行冷却,得到沉淀物。
(4) 将沉淀物过滤并洗涤,得到二苯乙二酮的产物。
(5) 最后,用氢氧化钠溶液对产物进行中和处理,得到纯净的二苯乙二酮。
实验结果:经过实验,我们成功合成了二苯乙二酮。
产物呈现出白色结晶状,纯度较高。
在实验过程中,我们注意到反应温度对反应速度和产物纯度有着重要影响。
过高或过低的温度都会导致反应效果不理想。
实验讨论:1. 合成机理二苯乙二酮的合成机理是通过苯甲酸和苯乙酮的酸催化缩合反应进行的。
在硫酸的催化下,苯甲酸和苯乙酮发生酰基转移,生成二苯乙二酮。
该反应是一个重要的有机合成反应,具有较高的反应活性和选择性。
2. 反应条件的优化在实验过程中,我们发现反应温度对反应效果有着重要影响。
过高的温度会导致产物分解或生成副产物,而过低的温度会使反应速度过慢。
因此,在实际应用中,需要根据具体情况选择适当的反应温度,以获得较高的产物收率和纯度。
3. 产物纯化方法在实验中,我们采用了中和处理的方法对产物进行纯化。
通过加入氢氧化钠溶液,可以中和产物中的酸性物质,提高产物的纯度。
此外,还可以通过结晶、洗涤等方法对产物进行进一步纯化,以获得更高纯度的二苯乙二酮。
结论:通过本次实验,我们成功合成了二苯乙二酮,并探究了其合成过程和一些相关性质。
二苯乙二酮实验报告二苯乙二酮实验报告引言:二苯乙二酮是一种重要的有机化合物,具有广泛的应用领域。
本实验旨在通过合成二苯乙二酮的方法,探究其合成原理和反应机理,并对其结构进行表征和分析。
实验方法:1. 实验材料准备本实验所需材料包括苯酚、醋酸、硫酸、碳酸钠、氢氧化钠等。
2. 实验步骤(1) 制备苯酚酸化物溶液:将苯酚与醋酸按一定比例混合,加入硫酸搅拌均匀。
(2) 酸化物溶液与碳酸钠反应:将酸化物溶液与碳酸钠溶液混合,反应生成苯酚盐。
(3) 苯酚盐与氢氧化钠反应:将苯酚盐与氢氧化钠溶液混合,反应生成二苯乙二酮。
(4) 结晶纯化:将反应产物进行结晶纯化,得到纯度较高的二苯乙二酮。
实验结果:通过实验,成功合成了二苯乙二酮。
通过红外光谱分析和核磁共振谱分析,确认了产物的结构和纯度。
实验讨论:1. 合成原理二苯乙二酮的合成主要依靠酸碱中和反应和氧化反应。
首先,苯酚与醋酸发生酸化反应生成苯酚酸化物。
然后,苯酚酸化物与碳酸钠发生酸碱中和反应生成苯酚盐。
最后,苯酚盐与氢氧化钠发生氧化反应生成二苯乙二酮。
2. 反应机理在酸碱中和反应中,苯酚酸化物中的羟基与碳酸钠中的碱性氢氧根离子发生中和反应,生成苯酚盐。
在氧化反应中,苯酚盐中的苯酚基发生氧化反应,失去氢原子,生成二苯乙二酮。
3. 结构表征通过红外光谱和核磁共振谱分析,可以确定二苯乙二酮的结构。
红外光谱可以观察到二苯乙二酮中的羰基吸收峰,核磁共振谱可以观察到苯环和乙酰基的信号。
结论:本实验成功合成了二苯乙二酮,并通过红外光谱和核磁共振谱对其结构进行了表征。
二苯乙二酮的合成主要依靠酸碱中和反应和氧化反应。
通过本实验的学习,我们对有机合成的原理和方法有了更深入的了解,并对二苯乙二酮的应用潜力有了更多的认识。
参考文献:[1] 张三,李四. 有机化学实验技术[M]. 北京:化学工业出版社,2010.[2] 王五,赵六. 有机合成原理与实验[M]. 北京:高等教育出版社,2015.。
二苯乙二酮的制备实验报告二苯乙二酮的制备实验报告引言:二苯乙二酮(又称二苯基甲酮)是一种重要的有机化合物,广泛应用于医药、染料和材料科学等领域。
本实验旨在通过苯乙酮的氧化反应制备二苯乙二酮,并通过实验结果分析反应机理和条件对产率的影响。
实验方法:1. 实验材料:- 苯乙酮(98%纯度)- 硝酸(65%纯度)- 硫酸(98%纯度)- 氯化铁(98%纯度)- 蒸馏水2. 实验步骤:a. 在实验室通风橱中,将苯乙酮(10 mL)加入圆底烧瓶中。
b. 将硝酸(10 mL)缓慢滴加到苯乙酮中,同时加入硫酸(20 mL)作为催化剂。
c. 将烧瓶连接至冷凝器,加热反应混合物,使其沸腾20分钟。
d. 将反应混合物冷却至室温,并用蒸馏水洗涤产物。
e. 将洗涤后的产物溶解在氯化铁溶液中,并用蒸馏水稀释至适当浓度。
f. 使用紫外-可见光谱仪测量溶液的吸光度,并根据标准曲线计算二苯乙二酮的浓度。
实验结果与讨论:通过实验测量,我们得到了不同反应条件下制备二苯乙二酮的产率结果。
我们发现,在不同的温度和反应时间下,产率有所变化。
较高的反应温度和较长的反应时间通常会导致更高的产率,但同时也会增加副反应的可能性。
此外,我们还发现硝酸的浓度对反应产率也有重要影响。
较高浓度的硝酸可以提高反应速率,但过高的浓度可能导致副反应的发生。
因此,在实际制备中,需要平衡硝酸浓度和产率之间的关系。
通过紫外-可见光谱仪的测量,我们可以准确测定二苯乙二酮的浓度。
这种分析方法简单、快速,并且具有较高的准确性。
通过测量不同浓度的标准溶液的吸光度,并绘制标准曲线,我们可以根据待测溶液的吸光度确定其浓度。
结论:本实验通过苯乙酮的氧化反应成功制备了二苯乙二酮,并通过实验结果分析了反应条件对产率的影响。
我们发现反应温度、反应时间和硝酸浓度都对产率有一定影响,需要在实际制备中进行适当调整。
此外,紫外-可见光谱仪是一种简单有效的分析方法,可用于测定二苯乙二酮的浓度。
二苯乙二酮的制备
一、实验目的
1、了解安息香氧化合成二苯基乙二酮的氧化剂选择。
2、熟练掌握回流、重结晶等实验操作。
二、实验原理
二苯乙二酮可以由安息香经氧化制得。
氧化剂可以为浓硝酸,但反应生成的二氧化氮对环境污染严重。
也可以使用Fe3+作为氧化剂,铁盐被还原成Fe2+。
本实验改进后采用醋酸铜作为氧化剂。
这样反应中产生的亚铜盐不断被硝酸铵重新氧化成铜盐,硝酸铵本身被还原成亚硝酸铵,后者在反应条件下分解为氮气和水。
改进后的方法在不延长反应时间的情况下可明显节约试剂,且不影响产率及产物纯度。
O O
OH O
Cu(OAc)2
NH4NO3
三、仪器及药品
仪器:圆底烧瓶、球形冷凝管、抽滤瓶、布氏漏斗等
药品:安息香、硝酸铵、冰醋酸、醋酸铜、乙醇等
四、实验步骤
在50mL圆底烧瓶中加入2.15 g安息香、8 mL冰醋酸、1 g 的硝酸铵和2.0 mL 2%硫酸铜溶液,装上回流冷凝管,缓慢加热,当反应物溶解后,开始放出氮气,继续回流1.5 h使反应完全。
将反应混合物冷至50-60 o C,在搅拌下倒入10 mL冰水中,析出二苯乙二酮晶体。
抽滤,用冷水充分洗涤,得到粗产物。
可用75%的乙醇水溶液重结晶,得到二苯乙二酮。