化工原理精馏
- 格式:ppt
- 大小:2.15 MB
- 文档页数:8


化工原理实验—精馏1. 概述精馏是一种常用的分离技术,广泛应用于化工工艺中。
它通过将混合液加热至蒸发,然后在冷凝器中冷却并凝结回液体,从而实现混合物中组分的分离。
本实验旨在通过精馏实验,掌握精馏原理、操作步骤和相关设备的使用方法。
2. 实验原理2.1 精馏原理精馏是基于液体混合物中各组分的不同沸点而进行的分离过程。
在加热的作用下,沸点较低的组分会先蒸发,经过冷凝器冷却后变为液体回流,而沸点较高的组分则会滞留在容器中。
通过收集冷凝后的液体,我们可以分离出混合物中的不同组分。
2.2 实验设备在精馏实验中,主要使用以下设备:•加热设备:电热板、油浴等;•冷凝器:通常采用水冷型冷凝器,通过循环冷却水实现液体冷凝;•分馏柱:用于增加接触面积,提高分离效果;•采样装置:用于采集样品,检测组分浓度等。
2.3 操作步骤精馏实验的基本步骤如下:1.准备实验设备:包括加热设备、冷凝器、分馏柱等;2.准备混合液:按照实验要求,将需要分离的混合液制备好;3.装配设备:将冷凝器安装在分馏柱上方,连接好相应的管道和热源;4.开始加热:逐渐加热混合液,将其中的沸点较低组分蒸发出来;5.冷却和回流:通过冷凝器使蒸发的组分冷却并凝结成液体,回流到容器中;6.收集液体:将回流液体收集,并记录途中温度和时间等相关数据;7.结束实验:实验完成后,及时关闭加热设备和冷凝器,整理实验装置。
3. 实验操作及数据记录3.1 实验设备准备首先,确保实验室环境安全,检查仪器设备是否齐全,并找到精馏实验所需的各种设备:•电热板:用来提供加热源;•分馏柱:用来增加接触面积,提高分离效果;•冷凝器:通常为水冷型冷凝器,确保冷却效果良好。
3.2 实验样品准备按照实验要求,取出需要分离的混合液样品。
注意记录样品的成分和浓度等信息。
3.3 装配设备将冷凝器安装在分馏柱上方,并连接好相应的管道和热源。
确保连接紧密,无泄漏。
3.4 开始实验1.打开电热板,设置适当的加热温度;2.将混合液置于分馏烧瓶中,放入加热设备中;3.监测温度变化:通过温度计等工具,记录样品温度的变化。


化工原理精馏实验化工原理精馏实验是化工工程中的一项重要实验内容,它主要用于分离和提纯混合物中的组分。
本文将介绍化工原理精馏实验的基本原理、实验步骤以及实验中需要注意的事项。
1. 实验目的化工原理精馏实验的主要目的是通过温度差异,利用液体蒸汽和凝结的原理,将混合物中的组分分离并得到纯净的产品。
通过这个实验,我们可以了解精馏作为一种分离技术的原理和应用。
2. 实验原理化工原理精馏实验的基本原理是利用混合物中各组分的不同沸点,通过升温使其中具有较低沸点的组分先蒸发,然后通过冷凝使其变为液体,从而实现分离。
在实验过程中,我们需要使用精馏塔,该塔内部设置有填料,用于增加混合物和蒸汽之间的交流面积,并实现更充分的分离。
3. 实验步骤(1) 准备实验所需设备和药品,包括精馏装置、混合物、填料等。
(2) 将混合物加入精馏瓶中,并将瓶塞密封。
(3) 将冷凝管和进料管连接到精馏瓶上,确保连接牢固。
(4) 将精馏瓶放入加热设备中,逐渐升温。
(5) 观察精馏瓶内的液体是否开始蒸发,当温度上升到某一点时,开始收集冷凝液。
(6) 根据实验需要,调整加热温度和收集冷凝液的时间,以实现所需组分的分离和提纯。
4. 实验注意事项(1) 在进行化工原理精馏实验前,需先对所需设备进行检查和清洁,确保实验过程的安全性。
(2) 在实验操作中,热量的传递速度会影响分馏过程的效果,因此需要掌握合适的加热速率。
(3) 为了避免精馏烧坏填料或其他设备,需要控制温度,确保温度在安全范围内。
(4) 实验结束后,应将设备进行清洗和消毒,防止残留物对下次实验的影响。
5. 实验结果分析通过化工原理精馏实验,可以得到分离出的纯净组分,并进行定量分析。
根据实验结果,可以进一步探讨精馏的分离效果、提纯效率等指标,并对所得纯净组分进行性质分析。
总结:化工原理精馏实验是一项重要的实验内容,通过实验可以了解精馏作为一种分离技术的原理和应用。
在实验过程中,需要注意设备的清洁和安全操作,合理控制加热温度和加热速率,以达到较好的分馏效果。






化工原理精馏
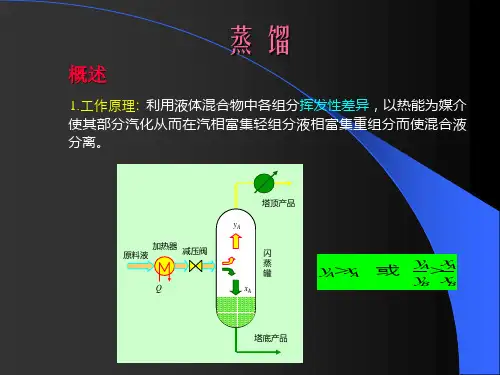
精馏是化工过程中常用的分离方法,用于将混合物中的组分按照其挥发性分离为不同纯度的产品。
精馏过程中,混合物首先加热至沸腾点,然后将生成的蒸气输送到冷凝器中进行冷凝。
冷凝后,液体收集器中会得到不同纯度的产品。
精馏过程基于混合物中不同组分的挥发性差异。
挥发性大的组分在加热后较早转化为蒸气,而挥发性小的组分则在较高温度下才蒸发。
经过冷凝后,收集器中会得到高挥发性组分的纯产品。
余下的低挥发性组分则在塔底收集。
精馏过程中,塔是一个重要的设备。
塔内通常包括填料或板片,用于增大接触面积,促进挥发和冷凝。
高挥发性组分在塔上部可迅速逸出,而低挥发性组分则被慢慢分离。
精馏还可用于提纯液体产品。
通过多级精馏,可以获得更高纯度的产品。
多级精馏是基于挥发性差异的温度差异实现的,每一级都以前一级的塔顶产品作为进料。
总之,精馏是一种重要的化工分离方法,通过控制温度和塔内工艺参数,可以将混合物分离为不同纯度的产品。
化工精馏原理
精馏是一种分离技术,用于将混合物中的组分通过升华和冷凝的方式进行分离。
该过程基于分子之间的不同挥发性和沸点的差异。
精馏的基本原理是利用组分在不同温度下的汽化和冷凝特性。
在精馏塔内,混合物被加热,使得易挥发的组分蒸发成气体,然后通过冷凝器冷却,转变回液体。
随后,这些液体进入分馏塔的不同部位,从而实现对组分的分离。
在精馏塔内,由于塔的高度,温度逐渐降低。
这导致组分的挥发性逐渐降低,使其向下凝结,并最终收集在不同的容器中。
高挥发性的组分在较低温度下首先凝结,低挥发性的组分在较高温度下凝结。
精馏塔内的分馏效果取决于各种因素,包括初始混合物的成分、入口温度、压力、塔的结构和精馏塔体系的设计等。
通过调整这些参数,可以实现较高效率的分离效果。
化工精馏广泛应用于石油、化工、制药等行业。
它可以用于分离原油、制取石油产品,提取溶剂、纯化有机化合物,以及获得高纯度的化学品等。
精馏技术的不断改进和创新也不断提高着分离效率和产品质量。
精馏实验一、实验目的1、了解筛板式精馏塔及其附属设备的基本结构,掌握精馏操作的基本方法;2、掌握精馏过程全回流和部分回流的操作方法;3、掌握测定板式塔全塔效率。
二、实验原理1、全塔效率E T全塔效率又称总板效率,是指达到指定分离效果所需理论板数与实际板数的比值,即-1=T T P N E N (1)式中:T N -完成一定分离任务所需的理论塔板数,包括塔釜;P N -完成一定分离任务所需的实际塔板数。
全塔效率简单地反映了整个塔内塔板的平均效率,表明塔板结构、物性系数、操作状况等因素对塔板分离效果的影响。
对于双组分体系,塔内所需理论塔板数N T ,可通过实验测得塔顶组成x D 、塔釜组成x W 、进料组成x F 及进料热状况q 、回流比R等有关参数,利用相平衡关系和操作线用图解法或逐板计算法求得。
图1塔板气液流向示意图2、单板效率ME 单板效率又称莫弗里板效率,如图1所示,是指气相或液相经过一层实际塔板前后的组成变化值与经过一层理论塔板前后的组成变化值之比。
按气相组成变化表示的单板效率为1*1y =n n MV n n y E y y ++--(2)按液相组成变化表示的单板效率为1*1n n ML n n x x E x x ---=-(3)式中:y n 、1n y +-分别为离开第n 、n+1块塔板的气相组成,摩尔分数;1n x -、n x -分别为离开第n-1、n 块塔板的液相组成,摩尔分数;*ny -与x n 成平衡的气相组成,摩尔分数;*nx -与y n 成平衡的液相组成,摩尔分数。
3、图解法求理论塔板数N T图解法又称麦卡勃-蒂列(McCabe-Thiele)法,简称M-T 法,其原理与逐板计算法完全相同,只是将逐板计算过程在y-x 图上直观地表示出来。
对于恒摩尔流体系,精馏段的操作线方程为:111D n n x R y x R R +=+++(4)式中:1n y +-精馏段第n+1块塔板上升的蒸汽组成,摩尔分数;n x -精馏段第n 块塔板下流的液体组成,摩尔分数;D x -塔顶溜出液的液体组成,摩尔分数;R -回流比。
化工原理第六章精馏第六章精馏一、精馏过程的数学描述在化工生产中,常根据混合液中各组分挥发度的不同,以精馏实现均相混合液的分离,二元连续精馏的基本流程如图6-1所示。
精馏过程的实质是伴有传热的传质过程,传质推动力取决于相互接触汽液两相偏离平衡的程度。
因此精馏过程的严格分析除了要应用相平衡、物料衡算两关系外,还需结合热量衡算及传质速率方程。
为了避开后两关系使分析得以简化,在工程上常引入似下两个概念:(1)理论板,(2)恒摩尔流,前者将影响板上传质速率的全部因素包括在塔板效率中;后者则是对热量衡算的简化。
于是精馏过程的数学描述可归结为全塔物料衡算、逐板组成变化两关系。
以图6-1的流程分离理想溶液;其已知量、未知量之间的关系可用图6-2表示。
图6-2表明,描述二元连续精馏的基本方程为 )(1W F D W D F x x R q N N f x Wx Dx Fx W D F ,,,,,,α=+=+= 由于三式中共涉及11个基本变量)(1R q N N x x x W D F W D F ,,,,,,,,,,α,因此其自由度为8,即须给定其中8个独立变量,才能确定另外3个变量。
二、精馏操作型问题的特点及基本类型精馏操作型问题的特点是:精馏塔已经给定(设塔板效率已知)。
即N 、N 1(或进料位置,通常不一定是最佳进料位置)为巳知量,其主要类型如下。
(1)对现有的精馏塔,在给定精馏条件下,核算其可能达到的分离程度。
如:已知N 、N 1、α、F 、x F 、q 、R 及W ,求D 、x D 、x W 。
(2)对运行中的精馏塔,当某一操作条件改变时,分析分离效果的变化,是否能获得合格的产品及为此需采取的措施;还会产生什么其他的影响。
如:(6-1)①已知N、N1、α、F、x F、q、R不变,若V'减少时,分析D、x D、x W的变化趋势;②已知N、N1、α、F、x F、q、V'不变,若x F下降,能否采取什么措施使x F不降低?通常对类型2,操作条件的变化将引起塔内液,汽流量的改变,并影响塔板效率,若这一影响甚小而能忽略,便可把操作中精馏塔的理论板数视为不变。
化工原理实验—精馏化工原理实验—精馏精馏是一种重要的分离技术,主要用于分离、纯化液体混合物中的各种成分。
在实际生产和科研实验中,精馏已经成为不可或缺的重要技术。
本文将就化工原理实验中的精馏实验进行详细介绍。
一、实验原理精馏的基本原理是根据不同成分在液态和气态之间的平衡关系,在加热条件下将混合物中单一成分蒸发和冷凝来实现分离、提纯目标成分。
实验中要分离的混合物首先被加热到沸腾点以上,因为各种成分的沸点不同,有些成分的沸点比另一些成分高得多,因此在离开混合物比较早的时候,一些液体成分便会压缩成气体形式,通过冷凝的方式回到液体形式,从而分离。
二、实验步骤1.实验前准备:确定实验目的,熟悉仪器使用方法和名词术语,检查实验物品是否准备充分。
2.实验流程:(1)调整设备:将水箱放在上部,并根据实验需要将装有混合物的烧瓶安装在下部。
(2)加热混合物:先在小火下加热,让混合物慢慢升温,确定加热速度以防止挥发速度过快。
随着温度的升高,由混合物挥发出来的单一成分便会通过塞子进入冷凝器,冷凝器中的水为其退回到液体形态,收集并量取所需要的物质。
3.实验结束:(1)关闭所有开关:实验完成后,将电源关闭,并将实验设备切断电源和气源。
(2)清洗设备与仪器:清洗所有已使用的材料和设备,以确保下次的实验能保证卫生和安全。
三、实验注意事项1.将水箱放置在塞子上方,仔细检查所有漏洞的位置和具有修复能力的地方,以避免机械故障与事故到来。
2.在进行实验时,必须小心谨慎地装填液体混合物,尤其是对于易燃物质,必须保持警惕,并根据实验条件和混合物来选择实验设备和材料。
3.在加热过程中,如果需要调整加热器的温度,必须慢慢调整,直到较稳定的加热水平达到。
总之,精馏实验是一项非常重要的化工原理实验,同学们在进行实验时一定要小心谨慎,严格遵守实验规范,才能保证实验的顺利进行。