化工原理精馏培训课件
- 格式:ppt
- 大小:2.45 MB
- 文档页数:26


化工原理蒸馏培训课件(doc 83页)第五章蒸馏化工生产中所处理的原料、中间产物、粗产品等几乎都是由若干组分所组成的混合物,而且其中大部分是均相物系。
生产中常需要将这些混合物分离成为较纯净或几乎纯态的物质(组分)。
对于均相物系,必须要造成一个两相物系,才能将均相混合物分离,并且是根据物系中不同组分间的某种物性的差异,使其中某个组分或某些组分从一相向另一相转移以达到分离的目的。
通常将物质在相间的转移过程称为传质过程或分离操作。
化学工业中常见的传质过程有蒸馏、吸收、萃取及干燥等单元操作。
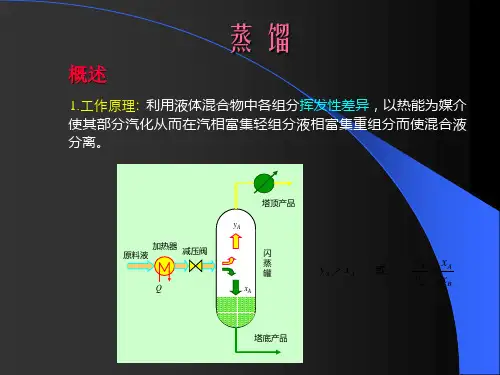
蒸馏就是藉液体混合物中各组分挥发性的差异而进行分离的一种操作。
蒸馏这种操作是将液体混合物部分气化,利用其中各组分挥发度不同的特性来实现分离的目的。
这种分离操作是通过液相和气相间的质量传递来实现的。
通常,将沸点低的组分称为易挥发组分,沸点高的组分称为难挥发组分。
蒸馏过程可以按不同方法分类:按操作流程可分为间歇和连续蒸馏;按蒸馏方式可分为简单蒸馏、平衡蒸馏(闪蒸)、精馏和特殊精馏等;按操作压强可分为常压、加压和减压精馏;按待分离混合物中组分的数目可分为两(双)组分和多组分精馏。
第一节双组分理想溶液的气液平衡蒸馏是气液两相间的传质过程,因此常用组分在两相中的浓度(组成)偏离平衡的程度来衡量传质推动力的大小。
传质过程是以两相达到相平衡为极限的。
由此可见,气液相平衡关系是分析蒸馏原理和进行设备计算的理论基础。
5—1—1 拉乌尔定律和相律一、拉乌尔定律根据溶液中同分子间与异分子间的作用力的差异,可将溶液分为理想溶液和非理想溶液两种。
实验表明,理想溶液的气液平衡关系遵循拉乌尔定律,即:(5—1)(5—1a)式中p ——溶液上方组分的平衡分压,Pa;p0——同温度下纯组分的饱和蒸汽压,Pa,x——溶液中组分的摩尔分率。
(下标A表示易挥发组分、B表示难挥发组分)为简单起见,常略去上式中的下标,习惯上以:x表示液相中易挥发组分的摩尔分率,以(1-x)表示难挥发组分的摩尔分率;y表示气相中易挥发组分的摩尔分率,以(1-y)表示难挥发组分的摩尔分率。




一、问答题1、什么是蒸馏操作?2、蒸馏和精馏有何区别?3、如何选定蒸馏操作压强?4、何谓挥发度与相对挥发度?5、何谓非理想溶液?它们的特点是什么?6、溶液的气液相平衡的条件是什么?7、什么是回流?精馏操作过程中回流有什么作用?8、什么是全回流操作?主要应用?9、从t-x-y图上简述精馏的理论基础?10、何谓理论板?理论塔板数是如何求取的?11、精馏塔为什么要设蒸馏釜或再沸器?12、什么位置为适宜的进料位置?为什么?13、q值的物理意义是什么?不同进料状态下的q值怎样?14、用图解法求理论塔板数时,为什么说一个三角形梯级代表一块理论块?15、恒縻尔流假设的内容?16、为使恒摩尔流假设成立,精馏过程须满足什么条件?17、化工生产中,对精馏塔板有哪些要求?18、何谓液泛、夹带、漏液现象?x下降,而F、q、R、'V19、一正在运行的精馏塔,由于前段工序的原因,使料液组成F仍不变,试分析L、V、'L、D、W及D x、W x将如何变化?20、某分离二元混合物的精馏塔,因操作中的问题,进料并未在设计的最佳位置,而偏x、q、R、'V均同设计值,试分析L、V、'L、D、W、及D x、W x的变下了几块板。
若F、F化趋势?(同原设计值相比)21、设计一精馏塔,其物料性质、进料量及组成、馏出液及釜液组成、回流比、冷却水温度、加热蒸汽压力均不变。
当进料状态由泡点进料改为饱和蒸汽进料时,塔板数是否相同?再沸器所需蒸汽量是否改变?22、有一正在操作的精馏塔分离某混合液。
若下列条件改变,问馏出液及釜液组成有何改变?假设其他条件不变,塔板效率不变。
(1)回流比下降;(1)原料中易挥发组分浓度上升;(2)进料口上移。
23、在精馏塔操作中,若F、V维持不变,而x F由于某种原因降低,问可用哪些措施使x D 维持不变?并比较这些方法的优缺点。
二:计算题1.在101.3 kPa时正庚烷和正辛烷的平衡数据如下:试求:(1)在压力101.3 kPa下,溶液中含正庚烷为0.35(摩尔分数)时的泡点及平衡蒸汽的瞬间组成?(2)在压力101.3 kPa下被加热到117℃时溶液处于什么状态?各相的组成为多少?(3)溶液被加热到什么温度时全部气化为饱和蒸汽?2.根据某理想物系的平衡数据,试计算出相对挥发度并写出相平衡方程式。




化工原理蒸馏培训课件-----------------------作者:-----------------------日期:第五章蒸馏化工生产中所处理的原料、中间产物、粗产品等几乎都是由若干组分所组成的混合物,而且其中大部分是均相物系。
生产中常需要将这些混合物分离成为较纯净或几乎纯态的物质(组分)。
对于均相物系,必须要造成一个两相物系,才能将均相混合物分离,并且是根据物系中不同组分间的某种物性的差异,使其中某个组分或某些组分从一相向另一相转移以达到分离的目的。
通常将物质在相间的转移过程称为传质过程或分离操作。
化学工业中常见的传质过程有蒸馏、吸收、萃取及干燥等单元操作。
蒸馏就是藉液体混合物中各组分挥发性的差异而进行分离的一种操作。
蒸馏这种操作是将液体混合物部分气化,利用其中各组分挥发度不同的特性来实现分离的目的。
这种分离操作是通过液相和气相间的质量传递来实现的。
通常,将沸点低的组分称为易挥发组分,沸点高的组分称为难挥发组分。
蒸馏过程可以按不同方法分类:按操作流程可分为间歇和连续蒸馏;按蒸馏方式可分为简单蒸馏、平衡蒸馏(闪蒸)、精馏和特殊精馏等;按操作压强可分为常压、加压和减压精馏;按待分离混合物中组分的数目可分为两(双)组分和多组分精馏。
第一节双组分理想溶液的气液平衡蒸馏是气液两相间的传质过程,因此常用组分在两相中的浓度(组成)偏离平衡的程度来衡量传质推动力的大小。
传质过程是以两相达到相平衡为极限的。
由此可见,气液相平衡关系是分析蒸馏原理和进行设备计算的理论基础。
5—1—1 拉乌尔定律和相律一、拉乌尔定律根据溶液中同分子间与异分子间的作用力的差异,可将溶液分为理想溶液和非理想溶液两种。
实验表明,理想溶液的气液平衡关系遵循拉乌尔定律,即:(5—1)(5—1a)式中 p ——溶液上方组分的平衡分压,Pa;p0——同温度下纯组分的饱和蒸汽压,Pa,x——溶液中组分的摩尔分率。
(下标A表示易挥发组分、B表示难挥发组分)为简单起见,常略去上式中的下标,习惯上以:x表示液相中易挥发组分的摩尔分率,以(1-x)表示难挥发组分的摩尔分率;y表示气相中易挥发组分的摩尔分率,以(1-y)表示难挥发组分的摩尔分率。