铁氰化钾的循环伏安法
- 格式:ppt
- 大小:1.94 MB
- 文档页数:18


实验五铁氰化钾循环伏安法有关性质的测定一. 实验目的掌握循环伏安法(CV)基本操作;了解可逆电化学过程及条件电极电位的测定;获得峰电流随电位扫描速度的变化曲线,获得峰电流随溶液浓度的变化函数关系;并学会电化学工作站仪器的使用。
二. 循环伏安法原理电化学中随着氧化还原反应的进行,会导致电流和电位的变化。
其中根据公式峰电流与电位扫描速度的1/2次方、溶液浓度成正比。
对于循环伏安法,扫描图像中前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
三. 实验仪器和药品铁氰化钾溶液、氯化钾溶液、铝粉、四个25ml容量瓶、电化学工作站,银电极,铂碳电极,银丝电极四. 实验步骤打开电脑并将仪器预热20分钟,打开电化学工作站操作界面。
将铁氰化钾标准溶液转移至电解池中 插入三支电极连接。
以标准的铁氰化钾溶液测试未磨电极的循环伏安曲线,看电位差的大小;超过100mv则用粗细的铝粉抛光铂碳电极,使得电位差在70--80以下;确定各参量:起始电位在0.5V左右,扫速为10、20、40、80、160mv/s,灵敏度为10-5--10-6,以标准铁氰化钾溶液测定不同扫速下的伏安曲线,测定并保存;配制4组不同浓度的铁氰化钾溶液:0.1、0.2、0.5、1.0ml 的铁氰化钾标准溶液于容量瓶中,在加入5ml氯化钾溶液,定容;控制参量:扫速为80,每个浓度6段三次扫描,依次对四组溶液测定伏安曲线,导出实验数据和曲线。
五.数据处理实验参数设定:打磨后电位差为81mv左右,比较合理。
亚铁氰化钾溶液的条件电极电位:从浓度和电位的表格中,可以根据浓度和电位做出曲线图,根据截距求出初始电位和条件电极电位。
测定峰电流和浓度关系时:Init E (V) = 0 High E (V) = 0.5 Low E (V) = 0 Init P/N = PScan Rate (V/s) = 0.08 Segment = 6 Sample Interval (V) = 0.001Quiet Time (sec) = 2 Sensitivity (A/V) = 1e-5测定峰电流和扫速关系时:Init E (V) = 0 High E (V) = 0.5 Low E (V) = 0 Init P/N = PScan Rate (V/s) = 0.02 Segment = 2 Sample Interval (V) = 0.001Quiet Time (sec) = 2 Sensitivity (A/V) = 1e-5数据表:峰电流和扫速数据表:0.1 0.2 0.5 10.226 0.226 0.231 0.24110mv20mv40mv80mv160mvSegment 1:Segment 1:Segment 1:Segment 1:Segment 1:Ep = 0.227V Ep = 0.226V Ep = 0.231V Ep = 0.239V Ep = 0.248Vip = -3.549e-6A ip = -5.605e-6A ip = -8.951e-6A ip = -1.245e-5A ip = -1.924e-5A Ah = -2.377e-5C Ah = -1.801e-5C Ah = -1.522e-5C Ah = -1.150e-5C Ah = -9.455e-6C Segment 2:Segment 2:Segment 2:Segment 2:Segment 2:Ep = 0.145V Ep = 0.140V Ep = 0.136V Ep = 0.126V Ep = 0.120Vip = 5.963e-6A ip = 8.119e-6A ip = 1.095e-5A ip = 1.437e-5A ip = 1.915e-5A Ah = 3.933e-5C Ah = 2.807e-5C Ah = 1.956e-5C Ah = 1.398e-5C Ah = 9.846e-6C曲线图:浓度和峰电流曲线图:所加体积ml0.10.20.51峰电流均值/10-6 2.6243 4.26310.65321.29峰电流和浓度的表格:0.1ml0.2ml0.5ml 1.0mlSegment 1:Segment 1:Segment 1:Segment 1:Ep = 0.226V Ep = 0.226V Ep = 0.231V Ep = 0.241Vip = -2.606e-6A ip = -3.670e-6A ip = -9.316e-6A ip = -1.788e-5A Ah = -2.189e-6C Ah = -2.997e-6C Ah = -8.084e-6C Ah = -1.722e-5C Segment 2:Segment 2:Segment 2:Segment 2:Ep = 0.144V Ep = 0.140V Ep = 0.132V Ep = 0.121Vip = 2.614e-6A ip = 4.106e-6A ip = 1.047e-5A ip = 2.132e-5A Ah = 2.090e-6C Ah = 3.476e-6C Ah = 9.477e-6C Ah = 2.124e-5C Segment 3:Segment 3:Segment 3:Segment 3:Ep = 0.226V Ep = 0.226V Ep = 0.232V Ep = 0.241Vip = -2.433e-6A ip = -3.807e-6A ip = -9.191e-6A ip = -1.705e-5A Ah = -2.025e-6C Ah = -3.105e-6C Ah = -8.032e-6C Ah = -1.634e-5C Segment 4:Segment 4:Segment 4:Segment 4:Ep = 0.144V Ep = 0.140V Ep = 0.131V Ep = 0.121Vip = 2.623e-6A ip = 4.292e-6A ip = 1.067e-5A ip = 2.133e-5A Ah = 2.092e-6C Ah = 3.622e-6C Ah = 9.763e-6C Ah = 2.123e-5C Segment 5:Segment 5:Segment 5:Segment 5:Ep = 0.226V Ep = 0.226V Ep = 0.232V Ep = 0.241Vip = -2.428e-6A ip = -3.940e-6A ip = -9.339e-6A ip = -1.708e-5A Ah = -2.015e-6C Ah = -3.221e-6C Ah = -8.149e-6C Ah = -1.640e-5C Segment 6:Segment 6:Segment 6:Segment 6:Ep = 0.145V Ep = 0.140V Ep = 0.131V Ep = 0.121Vip = 2.636e-6A ip = 4.391e-6A ip = 1.082e-5A ip = 2.132e-5A Ah = 2.069e-6C Ah = 3.690e-6C Ah = 9.877e-6C Ah = 2.117e-5C。

实验三十四循环伏安法测定铁氰化钾的电极反应过程一、实验目的见《仪器分析实验》p123二、方法原理见《仪器分析实验》p123。
三、仪器和试剂1.JP—303型极谱分析仪2.铁氰化钾标准溶液:5.0×10-2mol/L3.氯化钾溶液:1.0mol/L四、实验步骤1.铁氰化钾试液的配置准确移取1.0mL5.0×10-2mol/L的铁氰化钾标准溶液于10mL的小烧杯中,加入1.0 mol/L 的氯化钾溶液5.0mL,再加蒸溜水4.0mL。
2.测量手续(1)打开303极谱仪的电源。
屏幕显示清晰后,输入当天的日期:××.××.××,按【INT】键。
(2)屏幕显示“运行方式”菜单后,选取“使用当前方法”项,按【YES】键。
屏幕将显示“线性循环伏安法”的方法参数菜单:导数(0~2)0量程(10e nA,e=1~4) 4扫描次数(1~8) 4扫描速率(50~1000mV/s)50起始电位(-4000~4000mV)-100终止电位(-4000~4000mV)600静止时间(0~999s)0如果显示的参数不符合,请按提示修改。
(3)测量铁氰化钾试液在教师指导下,置电极系统于10mL小烧杯的铁氰化钾试液里。
按【运行】键,运行自动完成后,“波高基准”项闪烁,用∧∨键确定“前谷”方法处理图谱,按【YES】键。
请记录波峰电位和波峰电流数据。
按两次【退回】键,再按【方法】键,选取“使用当前方法”项,按【YES】键,显示“线性循环伏安法”的方法参数菜单。
修改扫描速率为100mV,按【ENT】键。
再按【运行】键,照上述的过程一样进行测量。
直至完成扫描速率为50、100、150、200、250mV/s的测量。
上述的循环伏安图打印样本见附图。
五、结果处理见《仪器分析实验》p127五的1、3、5题。
六、问题讨论见《仪器分析实验》p128六的2题。

实验五铁氰化钾循环伏安法有关性质的测定一. 实验目的掌握循环伏安法(CV)基本操作;了解可逆电化学过程及条件电极电位的测定;获得峰电流随电位扫描速度的变化曲线,获得峰电流随溶液浓度的变化函数关系;并学会电化学工作站仪器的使用。
二. 循环伏安法原理电化学中随着氧化还原反应的进行,会导致电流和电位的变化。
其中根据公式峰电流与电位扫描速度的1/2次方、溶液浓度成正比。
对于循环伏安法,扫描图像中前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
三. 实验仪器和药品铁氰化钾溶液、氯化钾溶液、铝粉、四个25ml容量瓶、电化学工作站,银电极,铂碳电极,银丝电极四. 实验步骤打开电脑并将仪器预热20分钟,打开电化学工作站操作界面。
将铁氰化钾标准的循环伏安曲线,看电位差的大小;超过100mv则用粗细的铝粉抛光铂碳电极,使得电位差在70--80以下;确定各参量:起始电位在0.5V左右,扫速为10、20、40、80、160mv/s,灵敏度为10-5--10-6,以标准铁氰化钾溶液测定不同扫速下的伏安曲线,测定并保存;配制4组不同浓度的铁氰化钾溶液:0.1、0.2、0.5、1.0ml 的铁氰化钾标准溶液于容量瓶中,在加入5ml氯化钾溶液,定容;控制参量:扫速为80,每个浓度6段三次扫描,依次对四组溶液测定伏安曲线,导出实验数据和曲线。
五.数据处理实验参数设定:打磨后电位差为81mv左右,比较合理。
亚铁氰化钾溶液的条件电极电位:从浓度和电位的表格中,可以根据浓度和电位做出曲线图,根据截距求出初始电位和条件电极电位。
测定峰电流和浓度关系时:Init E (V) = 0 High E (V) = 0.5 Low E (V) = 0 Init P/N = PScan Rate (V/s) = 0.08 Segment = 6 Sample Interval (V) = 0.001Quiet Time (sec) = 2 Sensitivity (A/V) = 1e-5测定峰电流和扫速关系时:Init E (V) = 0 High E (V) = 0.5 Low E (V) = 0 Init P/N = PScan Rate (V/s) = 0.02 Segment = 2 Sample Interval (V) = 0.001Quiet Time (sec) = 2 Sensitivity (A/V) = 1e-5数据表:峰电流和扫速数据表:0.1 0.2 0.5 10.226 0.226 0.231 0.24110mv20mv40mv80mv160mvSegment 1:Segment 1:Segment 1:Segment 1:Segment 1:Ep = 0.227V Ep = 0.226V Ep = 0.231V Ep = 0.239V Ep = 0.248Vip = -3.549e-6A ip = -5.605e-6A ip = -8.951e-6A ip = -1.245e-5A ip = -1.924e-5A Ah = -2.377e-5C Ah = -1.801e-5C Ah = -1.522e-5C Ah = -1.150e-5C Ah = -9.455e-6C Segment 2:Segment 2:Segment 2:Segment 2:Segment 2:Ep = 0.145V Ep = 0.140V Ep = 0.136V Ep = 0.126V Ep = 0.120Vip = 5.963e-6A ip = 8.119e-6A ip = 1.095e-5A ip = 1.437e-5A ip = 1.915e-5A Ah = 3.933e-5C Ah = 2.807e-5C Ah = 1.956e-5C Ah = 1.398e-5C Ah = 9.846e-6C曲线图:浓度和峰电流曲线图:所加体积ml0.10.20.51峰电流均值/10-6 2.6243 4.26310.65321.29峰电流和浓度的表格:0.1ml0.2ml0.5ml 1.0mlSegment 1:Segment 1:Segment 1:Segment 1:Ep = 0.226V Ep = 0.226V Ep = 0.231V Ep = 0.241Vip = -2.606e-6A ip = -3.670e-6A ip = -9.316e-6A ip = -1.788e-5A Ah = -2.189e-6C Ah = -2.997e-6C Ah = -8.084e-6C Ah = -1.722e-5C Segment 2:Segment 2:Segment 2:Segment 2:Ep = 0.144V Ep = 0.140V Ep = 0.132V Ep = 0.121Vip = 2.614e-6A ip = 4.106e-6A ip = 1.047e-5A ip = 2.132e-5A Ah = 2.090e-6C Ah = 3.476e-6C Ah = 9.477e-6C Ah = 2.124e-5C Segment 3:Segment 3:Segment 3:Segment 3:Ep = 0.226V Ep = 0.226V Ep = 0.232V Ep = 0.241Vip = -2.433e-6A ip = -3.807e-6A ip = -9.191e-6A ip = -1.705e-5A Ah = -2.025e-6C Ah = -3.105e-6C Ah = -8.032e-6C Ah = -1.634e-5C Segment 4:Segment 4:Segment 4:Segment 4:Ep = 0.144V Ep = 0.140V Ep = 0.131V Ep = 0.121Vip = 2.623e-6A ip = 4.292e-6A ip = 1.067e-5A ip = 2.133e-5A Ah = 2.092e-6C Ah = 3.622e-6C Ah = 9.763e-6C Ah = 2.123e-5C Segment 5:Segment 5:Segment 5:Segment 5:Ep = 0.226V Ep = 0.226V Ep = 0.232V Ep = 0.241Vip = -2.428e-6A ip = -3.940e-6A ip = -9.339e-6A ip = -1.708e-5A Ah = -2.015e-6C Ah = -3.221e-6C Ah = -8.149e-6C Ah = -1.640e-5C Segment 6:Segment 6:Segment 6:Segment 6:Ep = 0.145V Ep = 0.140V Ep = 0.131V Ep = 0.121Vip = 2.636e-6A ip = 4.391e-6A ip = 1.082e-5A ip = 2.132e-5A Ah = 2.069e-6C Ah = 3.690e-6C Ah = 9.877e-6C Ah = 2.117e-5C。



实验六铁氰化钾循环伏安法有关性质的测定1.实验目的①掌握循环伏安法(CV)基本操作;掌握受扩散控制电化学过程的判别方法;了解可逆电化学过程及条件电极电位的测定;了解电化学—化学偶联反应过程的循环伏安特点。
并学会电化学工作站仪器的使用。
②测定铁氰化钾相关性质2.实验仪器与试剂电化学工作站、铂碳电极、Ag-AgCl参比电极、饱和甘汞电极、25ml容量瓶铁氰化钾溶液、氯化钾溶液、氧化铝粉、蒸馏水3.实验原理①循环伏安法是在工作电极上施加一个线性变化的循环电压(本实验采用三角波),记录工作电极上得到的电流与施加电压的关系曲线,对溶液中的电活性物质进行分析的方法。
扫描图像中电压上升部分为阴极过程,电压下降部分阳极过程,一次扫描过程中完成一个氧化和还原过程的循环,故称为循环伏安法。
②正向扫描电极上将发生还原反应,反向回扫时,电极上生成的还原态物质将发生氧化反应,形成电流-电压图。
其峰电流与被测物质浓度c、扫描速度v等因素有关。
③从循环伏安图可确定氧化峰峰电流ipa和还原峰电流ipc,氧化峰峰电位值和还原峰峰电位值。
④对于可逆体系,氧化峰峰电流与还原峰峰电流比约等于1。
氧化峰峰电位与还原峰峰电位差严格符合能斯特方程。
由此可判断电极过程的可逆性。
4.实验步骤①依次用粗、细粒径的氧化铝粉末对铂碳电极进行抛光至表面均匀呈镜面。
②验证:亚铁氰化钾溶液中进行循环伏安扫描。
③电极连接,参数设定(起始电位、电位扫描范围、扫描速度等)。
④测定:峰电流随电位扫描速度的变化5.数据处理①计算亚铁氰化钾的条件电极电位;φθ’==0.1893V②作出峰电流~扫速v 1/2图,判断是否是扩散控制过程。
在误差范围内,峰电流与扫速1/2成正比,该过程是扩散控制过程6.实验分析与讨论①本次试验的主要误差在于在于前期电极的打磨,是否做到基本平滑整洁,本实验于电极情况密不可分,这是主要的误差来源。
②实验现象分析:在低扫速的时候有充电电流的干扰,会发生曲线在还原曲线开始的位置和氧化曲线结束的位置发生交叉。


实验六铁氰化钾循环伏安法有关性质的测定1.实验目的①掌握循环伏安法(CV)基本操作;掌握受扩散控制电化学过程的判别方法;了解可逆电化学过程及条件电极电位的测定;了解电化学—化学偶联反应过程的循环伏安特点。
并学会电化学工作站仪器的使用。
②测定铁氰化钾相关性质2.实验仪器与试剂电化学工作站、铂碳电极、Ag-AgCl参比电极、饱和甘汞电极、25ml容量瓶铁氰化钾溶液、氯化钾溶液、氧化铝粉、蒸馏水3.实验原理①循环伏安法是在工作电极上施加一个线性变化的循环电压(本实验采用三角波),记录工作电极上得到的电流与施加电压的关系曲线,对溶液中的电活性物质进行分析的方法。
扫描图像中电压上升部分为阴极过程,电压下降部分阳极过程,一次扫描过程中完成一个氧化和还原过程的循环,故称为循环伏安法。
②正向扫描电极上将发生还原反应,反向回扫时,电极上生成的还原态物质将发生氧化反应,形成电流-电压图。
其峰电流与被测物质浓度c、扫描速度v等因素有关。
③从循环伏安图可确定氧化峰峰电流ipa和还原峰电流ipc,氧化峰峰电位值和还原峰峰电位值。
④对于可逆体系,氧化峰峰电流与还原峰峰电流比约等于1。
氧化峰峰电位与还原峰峰电位差严格符合能斯特方程。
由此可判断电极过程的可逆性。
4.实验步骤①依次用粗、细粒径的氧化铝粉末对铂碳电极进行抛光至表面均匀呈镜面。
②验证:亚铁氰化钾溶液中进行循环伏安扫描。
③电极连接,参数设定(起始电位、电位扫描范围、扫描速度等)。
④测定:峰电流随电位扫描速度的变化5.数据处理①计算亚铁氰化钾的条件电极电位;φθ’==0.1893V②作出峰电流~扫速v 1/2图,判断是否是扩散控制过程。
在误差范围内,峰电流与扫速1/2成正比,该过程是扩散控制过程6.实验分析与讨论①本次试验的主要误差在于在于前期电极的打磨,是否做到基本平滑整洁,本实验于电极情况密不可分,这是主要的误差来源。
②实验现象分析:在低扫速的时候有充电电流的干扰,会发生曲线在还原曲线开始的位置和氧化曲线结束的位置发生交叉。

循环伏安法测定铁氰化钾的电化学行为一、实验目的1、学习循环伏安法测定电极反应参数的基本原理及方法。
2、熟悉CHI660电化学工作站的使用。
3、学会使用伏安极谱仪。
4、学会测量峰电流和峰电位。
二、实验原理循环伏安法(cyclic voltammetry ,CV )是在固定面积的工作电极和参比电极之间加上对称的三角波扫描电压,记录工作电极上得到的电流与施加电位的关系曲线,即循环伏安图。
从伏安图的波形、氧化还原峰电流的数值及其比值、峰电位等可以判断电极反应机理。
可用来检测物质的氧化还原电位, 考察电化学反应的可逆性和反应机理, 判断产物的稳定性,研究活性物质的吸附和脱附现象; 也可用于反应速率的半定量分析等。
循环伏安在工作电极上施加一个线性变化的循环电压,记录工作电极上得到的电流与施加电压的关系曲线,对溶液中的电活性物质进行分析。
由于施加的电压为三角波,这种方法也称为三角波线性扫描极谱法。
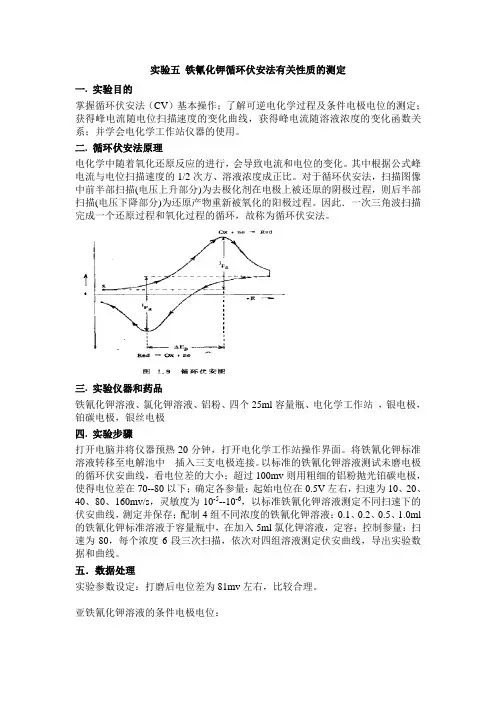
U t + - + + -+ + - +三角波图1 电路的接法一次扫描过程中完成一个氧化和还原过程的循环,称为循环伏安法。
与汞电极相比,物质在固体电极上伏安行为的重现性差,其原因与固体电极的表面状态直接有关,因而了解固体电极表面处理的方法和衡量电极表面被净化的程度,以及测算电极有效表面积的方法,是十分重要的。
一般对这类问题要根据固体电极材料不同而采取适当的方法。
循环伏安法控制电极电位φ随时间t 从φi 线性变化增大(或减小)至某电位φτ后,相同速率线性减小(大)归到最初电位φi 。
其典型的CV 法响应电流对电位曲线(循环伏安图)如图1示。
图2. 循环伏安曲线图假如电位从φi 开始以扫描速度υ向负方向扫描, 置φi 较φ (研究电极的标 准电极电位)正得多, 开始时没有法拉第电流, 当电位移向φ 附近时, 还原电流 出现并逐渐增大, 电位继续负移时, 由于电极反应主要受界面电荷传递动力学控 A g /A g c l 铂盘电极制, 电流进一步增大, 当电位负移到足够负时, 达到扩散控制电位后, 电流则转至受扩散过程限制而衰减, 使i φ曲线上出现电流峰i pc , 对应的峰电位为φpc 。
循环伏安法测定铁氰化钾王燕燕 40507224一、实验目的1、学习固体电极的处理方法2、掌握循环伏安仪的使用技术3、了解扫描速率和浓度对循环伏安图的影响二、实验原理铁氰化钾离子[Fe(CN)6]3-—亚铁氰化钾离子[Fe(CN)6]4-氧化还原电对的标准电极电位为[Fe(CN)6]3- + e-= [Fe(CN)6]4-φθ= 0.36 V(vs.NHE) 电极电位与电极表面活度的Nernst方程式为φ=φθ+ RT/Fln(C Ox/C Red)在一定扫描速率下,从起始电位(-0.2 V)正向扫描到转折电位(+0.8 V)期间,溶液中[Fe(CN)6]4-被氧化生成[Fe(CN)6]3-,产生氧化电流;当负向扫描从转折电位(+0.8 V)变到原起始电位(-0.2 V)期间,在指示电极表面生成的[Fe(CN)6]3-被还原生成[Fe(CN)6]4-,产生还原电流。
为了使液相传质过程只受扩散控制,应在加入电解质和溶液处于静止下进行电解。
在1 M NaCl 溶液中[Fe(CN)6]的扩散系数为0.63×10-5 cm.s-1;电子转移速率大,为可逆体系(1 M NaCl溶液中,25℃时,标准反应速率常数为5.2×10-2 cm·s-1)。
溶液中的溶解氧具有电活性,用通入惰性气体除去。
三、仪器和药品LK98B型循环伏安仪,X-Y记录仪,银电极,铂丝电极,饱和甘汞电极,电解池,移液管等。
0.10 Mol*L-1 K3[Fe(CN)6], 1.00 Mol*L-1 NaCl四、实验步骤(1)指示电极的预处理铂电极用Al2O3粉末(粒径0.05 µm)将电极表面抛光,然后用蒸馏水清洗。
(2)支持电解质的循环伏安图在电解池中放入30 mL 1,0 mol·L-1 NaCl溶液,插入电极,以新处理的铂电极为指示电极,铂丝电极为辅助电极,饱和甘汞电极为参比电极,进行循环伏安仪设定,扫描速率为50 mV/s;起始电位为-0.2 V;终止电位为+0.8 V。
循环伏安法判断铁氰化钾的电极反应过程一、目的要求1.掌握用循环伏安法判断电极反应过程的可逆性2.学会使用电化学工作站3.学会测量峰电流和峰电位,培养学生的动手操作能力及分析问题解决问题能力二、实验用品1.仪器:电化学工作站,三电极系统(两支铂电极,一支甘汞电极),电解杯数只2.试剂:铁氰化钾标准溶液(6.0×10-3 mol/L ,1.00×10-5、1.00×10-4、1.00×10-3、1.00×10-2含KCl 溶液1.0 mol/L ),三、实验原理电化学工作站(Electrochemical workstation )是电化学测量系统的简称,是电化学研究和教学常用的测量设备。
将这种测量系统组成一台整机,内含快速数字信号发生器、高速数据采集系统、电位电流信号滤波器、多级信号增益、IR 降补偿电路以及恒电位仪、恒电流仪。
可直接用于超微电极上的稳态电流测量。
如果与微电流放大器及屏蔽箱连接,可测量1pA 或更低的电流。
如果与大电流放大器连接,电流范围可拓宽为±2A 。
动态范围极为宽广。
可进行循环伏安法、交流阻抗法、交流伏安法等测量。
循环伏安法是用途最广泛的研究电活性物质的电化学分析方法,在电化学、无机化学、有机化学、生物化学等领域得到了广泛的应用。
由于它能在很宽的电位范围内迅速观察研究对象的氧化还原行为,因此电化学研究中常常首先进行的是循环伏安行为研究。
循环伏安是在工作电极上施加一个线性变化的循环电压,记录工作电极上得到的电流与施加电压的关系曲线,对溶液中的电活性物质进行分析。
铁氰化钾离子-亚铁氰化钾离子氧化还原电对的标准电极电位:选择施加在起始点的起始电位,沿负的电位正向扫描,当电位负到能够将O ([Fe(CN)6]3-)还原时,在工作电极上发生还原反应:O+ Ze = R ,阴极电流迅速增加,电流达到最高峰,此后由于电极附近溶液中的O ([Fe(CN)6]3-)转变为R ([Fe(CN)6]4-)而耗尽,电流迅速衰减;电压沿正的方向扫描,当电位正到能够将R ([Fe(CN)6]4-)氧化时,在工作电极表面聚集的R 将发生氧化反应:R= O+Ze ,阳极电流迅速增加,电流达[][]3466Fe(CN)Fe(CN)e ---+=00.36V(.NHE)vs ϕ=到最高峰,此后由于电极附近溶液中的R转变为O([Fe(CN)6]3-)而耗尽,电流迅速衰减;当电压达到的起始电位时便完成了一个循环。
循环伏安法测定铁氰化钾的电极反应过程一、实验原理 1.循环伏安法循环伏安法是将循环变化的电压施加于工作电极和对电极之间,记录工作电极上得到的电流与施加电压的关系曲线。
此方法也称为三角波线性电位扫描方法。
图1-1表明了施加电压的变化方式。
选定电位扫描范围E1~E2 和扫描速率, 从起始电位E1开始扫描到达E2 , 然后连续反向在扫描从E2回到E1。
由图1-2 可见,循环伏安图有两个峰电流和两个峰电位。
i pc 和 i pa 分别表示阴极峰值电流和阳极峰值电流,对应的阴极峰值电位与阳极峰值电位分别为E pc 和E pa 。
图1-1 循环伏安法的典型激发信号 图1-2 K3Fe(CN)6在KCL 溶液中的循环伏安图2.判断电极可逆性根据Nernst 方程,在实验测定温度为298K 时,计算得出 △Ep = Epa- Epc≈59/n mV (1-1) 阳极峰电流ipa 和阴极峰电流ipc 满足以下关系: ipc/ipa ≈1 (1-2)同时满足以上两式,即可认为电极反应是可逆过程。
如果从循环伏安图得出的 △Ep/mv = 55/n ~65/n 范围,也可认为电极反应是可逆的。
3.计算原理铁氰化钾离子-亚铁氰化钾离子氧化还原电对的标准电极电位 [Fe(CN)6]3- + e - = [ Fe(CN)6]4- Φ=0.36v 电极电位与电极表面活度的Nernst 方程:峰电流与电极表面活度的Randles-Savcik 方程: i p = 2.69×105n 3/2ACD 1/2v 1/2 二、实验仪器与试剂0'Ox pa RedC RTIn F C ϕϕ∆=+E / Vt / s阳极 i / μA 阴极ϕ / v仪器: CHI660电化学工作站,电解池铂盘工作电极铂丝辅助电极Ag/AgCl参比电极。
试剂:铁氰化钾溶液:0.1mol/L;硝酸钾溶液:1.0mol/L三、实验步骤1.Pt工作电极预处理不同粒度的α-Al2O3粉,抛光,洗去表面污物,再超声水浴中清洗,每次2-3分钟,重复三次,得到平滑光洁和新鲜的电极表面。
实验六铁氰化钾循环伏安法有关性质的测定一.实验目的掌握循环伏安法(CV)基本操作;掌握受扩散控制电化学过程的判别方法;了解可逆电化学过程及条件电极电位的测定;了解电化学一化学偶联反应过程的循环伏安特点。
并学会电化学工作站仪器的使用。
二.循环伏安法原理扫描电压呈等腰三角形。
如果前半部扫描(电压上升部分)为去极化剂在电极上被还原的阴极过程,则后半部扫描(电压下降部分)为还原产物重新被氧化的阳极过程。
因此.一次三角波扫描完成一个还原过程和氧化过程的循环,故称为循环伏安法。
循环伏安法可用于研究化合物电极过程的机理、双电层、吸附现象和电极反应动力学•成为最有用的电化学方法之一05 T.9 紹坪悅宝网三.实验步骤1.电极表面抛光2.验证:亚铁氰化钾溶液中进行循环伏安扫描(电位差小于70mv)3.电极连接,参数设定(起始电位、电位扫描范围、扫描速度等)4.测定:峰电流随电位扫描速度的变化(处理在一张图上)5.反应模拟器(Simulation):模拟实验(调节:模型、传递系数a标准速率常数k0等)四.数据处理1.计算亚铁氰化钾的条件电极电位;2•作出峰电流~扫速v 1/2图,判断是否是扩散控制过程。
峰电诲与标堆电极此碧的关系为"%十先g 缶由于扩散系数并没有实际测量,这里不做详细计算P^C^-nM 性iw 知” d 亠険"I"屮下 ~—■ Rt 4^up Cartpr^ &i 卢矗IL »:S^i Awr\|E|口蓬jT|回昼・・• r 刮土直 也■年■ | I 宴|Mu. 24.2DW 1* KI T«h - CVFit : IfflM.IDBtf)It E(VJ«O.D£ HflheCVJwgift LcwElVi=gO5Smn 倉血 甘训■■ & bl 导烯rtiE zg 3-^ipi Iftrtrwei tV) * Q001 3«t TIP* |4] ■ g Svrti 眄 |AV| ■ - fl-5iffiM 1O.br —1册胡二0»力 —-1mM aDfrn —-1mM -SD bmimM lOO^riPotential / X扫描速度(V/s)0.01 0.02 0.04 0.08 0.1氧化峰电 流(卩A)-2.734 -3.669 -4.886 -6.500 -7.111FLU!»ia.1,Zb f JOLO/ 2E-0.26-65V•h? •"rb hTrt 勺峰电流--扫速的1/2丄TV5D二=#==】峰电流一扫速的丄/2由上图,峰电流与扫速的1/2在误差允许范围内成正比,所以该过程是扩散控制过程。
实验7 循环伏安法测定铁氰化钾的电极反应过程实验七循环伏安法测定铁氰化钾的电极反应过程一、目的要求1.学习循环伏安法测定电极反应参数的基本原理及方法; 2.学会使用伏安仪;3.掌握用循环伏安法判断电极反应过程的可逆性。
二、试验原理循环伏安法(CV)是最重要的电分析化学研究方法之一。
由于其设备价廉、操作简便、图谱解析直观,能迅速提供电活性物质电极反应过程的可逆性,化学反应历程、电极表面吸附等许多信息。
因而一般是电分析化学的首选方法。
CV方法是将循环变化的电压施加于工作电极和参比电极之间,记录工作电极上得到的电流与施加电压的关系曲线。
这种方法也常称为三角波线性电位扫描方法。
图1中表明了施加电压的变化方式:起扫电位为+0.8V,反向/起扫电位为-0.2V,终点又回扫到+0.8V。
当工作电极被施加的扫描电压激发时,其上将产生响应电流。
以该电流(纵坐标)对电位(横坐标)作图,称为循环伏安图。
典型的循环伏安图如图2所示。
该图是在1.0mol/L的KNO3电解质溶液中,6×10-3mol/L 的K3Fe(CN)6在Pt工作电极上反应得到的结果。
起始电位Ei为+0.8V(a点),然后沿负的电位扫描(如箭头所指方向),当电1位至Fe(CN)63�C可还原时,即析出电位,将产生阴极电流(b点)。
其电极反应为: [Fe(CN)6]3??e?[Fe(CN)6]4?随着电位的变负,阴极电流迅速增加(b-c-d),直至电极表面的Fe(CN)63-浓度趋近零,电流在d点达到最高峰。
然后迅速衰减(d-e-f),这是因为电极表面附近溶液中的Fe(CN)63-几乎全部因电解转变为Fe(CN)64-而耗尽。
当电压开始阳极化扫描时,由于电极电位仍相当的负,扩散至电极表面的Fe(CN)63-仍在不断还原,故仍呈现阴极电流。
当电极电位继续正向变化至Fe(CN)64-的析出电位时,聚集在电极表面附近的还原产物Fe(CN)64-被氧化,其反应为:[Fe(CN)6]4??e?[Fe(CN)6]3?这时产生阳极电流(i-j-k),阳极电流随着扫描电位正移迅速增加,当电极表面的Fe(CN)64-浓度趋于零时,阳极化电流达到峰值(j点)。