1蒸馏分馏及常量法测定沸点(精)
- 格式:ppt
- 大小:82.00 KB
- 文档页数:14
![蒸馏及沸点的测定常量法蒸馏95家当乙醇[最新]](https://uimg.taocdn.com/37ad6d265b8102d276a20029bd64783e09127db1.webp)
青岛大学化学实验教学中心代表性实验教学大纲《无机化学实验》课程实验教学大纲课程编号:课程学时:96/48课程学分:4/1.5适用专业(专业类):化学化工类-化学,应用化学、高分子材料、化学工程与工艺、轻化工程、生物技术、食品科学与工程、药学、医学检验等实验项目18个,学时96。
一、实验的目的与任务1.学习并了解常见无机物制备、分离、和提纯方法。
2.学习并掌握分析天平的使用。
3.学习滴定管、容量瓶、吸量管等容量仪器的校正和使用,确立量的概念。
4.学习几种常数的测定方法,掌握常用测量仪器的使用方法。
5.通过实验培养以下能力:(1)学会查阅相关文献及资料。
(2)正确进行实验操作,取得可靠实验结果。
学会用实验解决相关问题。
(3)通过观察实验现象,学会分析判断、逻辑推理,得出正确结论。
(4)学会实验仪器(一般测量仪器、玻璃仪器等)正确使用方法。
(5)学会正确记录和处理数据、误差表示、并得出可靠结论。
二、实验项目基本情况一览表序号实验项目内容提要学时实验类型必开选开1常用仪器洗涤、干燥;一般溶液配制1.一般仪器及容量仪器洗涤、干燥方法。
2.酸、碱、盐溶液的配制方法。
4验证必开2玻璃工的基本操作1.学习喷灯的使用。
2.学会玻璃弯管、滴管、玻璃棒等的烧拉制作。
4验证必开3分析天平的使用及容量仪器校正1.分析天平的使用。
2.学习滴定管、容量瓶、吸量管等容量仪器的规范操作。
3.掌握量器的校正方法及为什麽校正。
6验证必开4酸碱滴定学习酸式、碱式滴定管的正确使用。
学会盐酸、氢氧化钠溶液的标定方法。
学会正确选择指示剂及终点的判断。
4验证必开5气体常数的测定学会使用分析天平直接称量。
学习测量体积的操作。
4验证必开6弱酸电离常数的测定测定醋酸的电离度、电离常数,学会使用酸度计。
4验证必开7硝酸钾的制备和提纯利用溶解度的不同制备硝酸钾,学习试剂取用、直接加热、减压过滤等基本操作。
并掌握固体溶解、加热、蒸发等基本操作。
4验证必开8磺基水杨酸合铁(Ⅲ)配合物稳定常数的测定了解光度法测定配合物组成和稳定常数的原理和方法。



分馏及常量法测定沸点沸点是物质从液态变为气态所需的温度,是物质性质的重要指标之一。
沸点可用分馏法和常压下常量法来测定。
分馏是根据不同物质的沸点差异来进行分离的过程。
在实验室中,通常采用简单分馏、减压分馏和升华分馏等方法测定沸点。
(一)简单分馏法简单分馏是将液体混合物在气相、液相两相存在情况下进行分离的方法。
实验通常采用酒精灯或热板加热。
具体步骤如下:1.将混合液放入配有分液漏斗的蒸馏瓶中,接上冷凝管。
2.将酒精灯或热板加热器置于蒸馏瓶下方,加热直至混合液开始沸腾。
3.收集温度为固定值时的馏分液(收集时应注意放液速度,以避免气体和液体同时被收集)。
4.根据馏分液的不同物理性质进行分析和鉴定。
简单分馏法测定沸点的主要优点是操作简单,不需要特殊设备,在测定实验室中比较常见。
但它的缺点也十分明显,不适用于沸点相差较小或沸点间隔较窄的成分。
减压分馏法又称为低压分馏法,其基本原理是在减压条件下汽化,使沸点降低。
具体步骤如下:1.将混合液放入装有深度低于液位的圆底烧瓶中。
2.在烧瓶与导管接口处连接入口隔膜渗透泵,使烧瓶内压力降低到所需值。
4.收集温度为固定值时的馏分液。
升华分馏法是利用固体物质高于气体的升华特性进行分离的方法。
适用于高沸点、难分离物质的测定。
1.将混合液加热至沸腾,将蒸发至干燥后的残渣放置在沸石上进行升华分馏。
沸石的物理特性可以隔离不同沸点的组分。
2.根据沸石的特性,分离出馏分液。
升华分馏法的主要优点是适用于多种难分离成分,但操作过程需要极为谨慎,否则容易损坏升华装置。
在一定环境下,同一物质的沸点是不变的,因此可以通过沸点的常量来测定沸点。
(一)水银柱法测定沸点水银柱法测定沸点是通过将沸点物质加热到沸腾,用水银柱记录温度并转换为沸点值的一种方法。
原理为在沸腾时蒸汽压力等于大气压力,此时水银柱的高度与温度有关。
具体操作步骤如下:1.在沸点物质加热器附近安装一个水银柱装置。
2.将沸点物质加热至沸腾状态,水银柱指示值处于稳定状态时记录温度。

蒸馏和沸点的测定
实验蒸馏和沸点的测定
一. 实验目的:
1.了解测定沸点的意义。
2.掌握常量法(蒸馏法)测定沸点的原理和方法。
二. 实验原理:
当液体物质被加热时,该物质的蒸气压达到与外界施于液面的总压力(通常是大气压力)时液体沸腾,这时的温度称为沸点。
常压蒸馏就是将液体加热到沸腾变成蒸气,又将蒸气冷凝得到液体的过程。
每种纯液态的有机物在一定的压力下均有固定的沸点。
利用蒸馏可将二种或两种以上沸点相差较大(>30℃)的液体混合物分开。
纯液体化合物的沸距一般为
0.5~1℃,混合物的沸距则较长。
可以利用蒸馏来测定液体化合物的沸点。
三.实验仪器与药品
蒸馏烧瓶、直形冷凝管、接液管、酒精灯、石棉网、温度计、无水乙醇。
四、实验步骤
在100ml蒸馏瓶中,放置30ml工业酒精和10ml水;放入1~2粒沸石,然后通冷凝水,开始加热并注意观察蒸馏瓶中的现象和温度计读数的变化。
记录第一滴馏出液滴下时的温度,当温度稳定时,换一个已称量过的干燥的锥形瓶作接受器,收集恒定温度+3℃的馏分。
量取所收集馏分的体积,并计算回收率
五、问题讨论
1、沸石(即止暴剂或助沸剂)为什么能止暴?如果加热后才发现没加沸石怎么办?
2、冷凝管通水方向是由下而上,反过来行吗?为什么?
3.在蒸馏装置中,温度计水银球的位置不符合要求会带来什么结果?
相关文档:
更多相关文档请访问:。
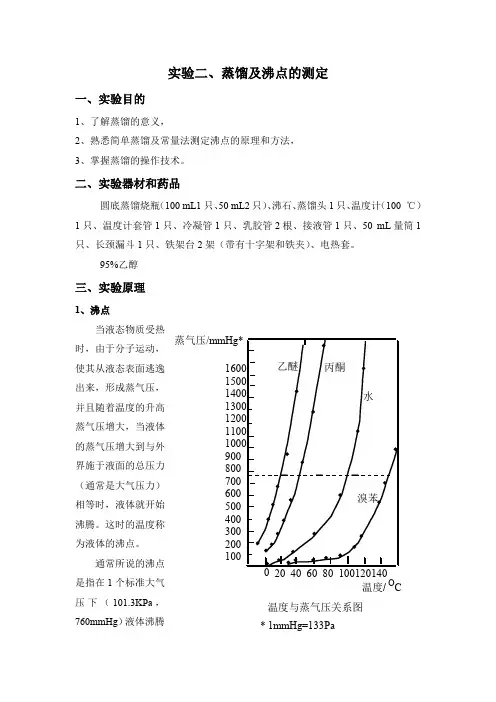
900800700600500400300200100温度/蒸气压/mmHg*O C 温度与蒸气压关系图* 1mmHg=133Pa实验二、蒸馏及沸点的测定一、实验目的1、了解蒸馏的意义,2、熟悉简单蒸馏及常量法测定沸点的原理和方法,3、掌握蒸馏的操作技术。
二、实验器材和药品圆底蒸馏烧瓶(100 mL1只、50 mL2只)、沸石、蒸馏头1只、温度计(100 ℃)1只、温度计套管1只、冷凝管1只、乳胶管2根、接液管1只、50 mL 量筒1只、长颈漏斗1只、铁架台2架(带有十字架和铁夹)、电热套。
95%乙醇三、实验原理1、沸点当液态物质受热时,由于分子运动,使其从液态表面逃逸出来,形成蒸气压,并且随着温度的升高蒸气压增大,当液体的蒸气压增大到与外界施于液面的总压力(通常是大气压力)相等时,液体就开始沸腾。
这时的温度称为液体的沸点。
通常所说的沸点是指在1个标准大气压下(101.3KPa ,760mmHg )液体沸腾时的温度。
2、蒸馏蒸馏是将液体加热到沸腾状态,使液体变为蒸汽,然后将蒸汽冷却又得到液体这两个过程的联合操作。
3、蒸馏的意义(1)测定有机化合物的沸点;初步鉴定不同的有机化合物;检验有机化合物的纯度。
每种纯液体有机化合物,在一定的压力下均具有一定的沸点;不同的有机物具有不同的沸点;纯净有机物在蒸馏过程中的沸点范围(沸程)很小(0.5~1℃),沸程越小,表示该有机物纯度越大,不纯的液体有机物没有恒定的沸点。
注意,具有固定沸点的液体有机物不一定都是纯的有机物。
某些有机化合物能和其他物质形成二元或三元共沸混合物,它们也有固定的沸点,但它们是混合物。
如,水—乙醇共沸物是由4.5%的水和95.5%的乙醇组成的混合物,其沸点为78.1℃(纯乙醇的沸点为78.4℃) (2)液体有机混合物的分离与纯化当蒸馏液态有机混合物时,如果各组分的沸点相差较大(大于30℃),沸点较低的组分先被蒸出,然后是高沸点组分被蒸出,不挥发的组分则留在蒸馏器中,这样可以达到分离与提纯的目的。

蒸馏和沸点的测定一、实验目的1 了解沸点测定的意义2 掌握常量法(蒸馏法)测定沸点的原理和操作技术3 掌握微量法测定沸点的操作技术4 了解蒸馏操作的应用二、实验原理1 沸点的定义:液态物质受热时,蒸汽压增大,当蒸汽压增大到和外界大气压或所给的压力相等时,液体沸腾,此时的温度即为该液体的沸点。
2 纯的液态有机物有固定的沸点,沸程在0.5~1.5℃之间;不纯净的液体没有恒定的沸点,蒸馏过程中温度变化大。
3 蒸馏包括沸腾气化与冷却两个过程4 蒸馏操作的应用:(1)分离液体混合物蒸馏仅对混合物中各成分的沸点相差较大时(≥30℃)才能有效地分离,沸点低者先蒸出。
(2)测定液体化合物的沸点(沸腾时的温度)(3)提纯除去不挥发性杂质(4)回收溶剂或蒸出部分溶剂以浓缩溶液5 为消除过热和爆沸,必须加入止爆剂(助沸剂),引入气化中心。
三、实验仪器和药品1 仪器:圆底烧瓶蒸馏头、温度计套管温度计直形冷凝管尾接管接收瓶(圆底烧瓶或磨口锥形瓶)电热套铁架台(带铁圈、铁夹)2 药品:工业酒精(b.p78.15℃)四、仪器安装仪器安装要求:(1)蒸馏烧瓶内的液体体积占烧瓶容积的1/3~2/3(2)仪器装配原则先下后上,从左至右(3)温度计的水银球的上缘与支管口的下缘持平(4)铁夹不应夹得太紧或太松,应夹在烧瓶的口径壁厚处(5) 130℃以上用空气冷凝管,130℃以下用水冷凝管冷凝(6)各仪器的轴线要求在同一平面上,整套仪器准确端正,无扭曲。
五、蒸馏操作(1)液体经由漏斗加入(2)加入沸石(3)检查是否造成密闭体系(4)先通冷凝水,后加热(5)控制蒸馏速度1~2滴/秒,收集馏分。
(6)烧瓶内残留0.5~1ml时,停止蒸馏或当温度骤降时停止蒸馏,千万不能蒸干,否则易发生事故。
(7)停止蒸馏时,先停止加热,后停止通水(8)拆卸仪器与安装时相反。
七、思考题1.蒸馏过程中应注意的问题?包括仪器的安装和蒸馏操作两部分的注意事项。
2.沸石的作用:沸石是多孔性物质,当加热液体时,孔内的小气泡形成气化中心,使液体平稳地沸腾。

实验项目蒸馏及常量法测沸点液体有机混合物的纯化和分离,溶剂的回收,经常采用蒸馏的方法来完成。
蒸馏包括常压蒸馏(简单蒸馏)、减压蒸馏、水蒸气蒸馏等。
减压蒸馏、水蒸气蒸馏将在后面的学习中介绍。
蒸馏、分馏、减压蒸馏和水蒸气蒸馏都是有机制备中常用的重要操作。
一般用于以下几个方面:(1)分离液体混合物,仅对混合物中各成分的沸点有较大差别时才能达到有效的分离;(2)测定化合物的沸点;(3)提纯,除去不会发的杂质;(4)回收溶剂,或蒸出部分溶剂进行浓缩溶液。
沸点是液体有机化合物的重要物理常数。
根据被测液体的量分为常量法和微量法两种,用蒸馏的方法来测定液体沸点方法叫常量法,此法一般需要样品量不少于10mL,适合对热易分解、易氧化的化合物。
当样品量较少时,需要采用微量法测定沸点。
本次实验利用蒸馏操作进行常量法测液体沸点。
一、实验目的1.了解蒸馏的原理及沸点的意义;2.掌握蒸馏装置仪器选择、连接和拆卸;3.掌握常量法测定沸点、分离提纯乙醇以及简单蒸馏的基本操作。
二、实验原理所谓蒸馏就是将液态物质加热到沸腾变为蒸气,又将蒸气冷凝为液体这两个过程的联合操作。
蒸馏装置是由蒸馏(热源、蒸馏瓶、温度计)、冷凝(冷凝管)、接收(接液管、接收器)三个部分组成(如图7.1)。
7.1当液态物质受热时,由于分子运动使其从液体表面逃逸出来,形成蒸气压,随着温度的升高,蒸气压增大,待蒸气压和大气压相等时,液体沸腾,此时的温度称为该液体的沸点。
每种纯液态有机化合物在一定的压力下均有固定的沸点。
在蒸馏液体混合物时低沸点组分“优先”沸腾,被蒸出来,沸点高的随后蒸出,不挥发的的则留在蒸馏瓶中,由此,可达到分离和提纯的目的。
但在蒸馏沸点比较接近的混合物时,各种物质的蒸气将同时蒸出,只不过低沸点的多一些,故难于达到较好的分离和提纯的目的,因此,蒸馏对于沸点相差较大(如相差30℃)的液态混合物进行分离和提纯,效果较好。
伴随蒸馏的过程中,由此可测得液体混合物不同组分的沸点。

蒸馏及沸点的测定一、实验目的:1、了解沸点测定的意义,掌握常量法测定沸点的原理和操作方法;2、了解蒸馏的应用范围,掌握蒸馏装置的装配和拆卸。
二、实验原理:1、蒸馏的定义和作用:蒸馏的定义:将液态物质加热到沸腾变为蒸气,又将蒸气冷凝为液体并用另一容器去接受,这两个过程的联合操作叫蒸馏。
蒸馏的作用:1)蒸馏可分离液体混合物[仅对混合物中成分的沸点有较大差别(沸点差值大于30℃,利用蒸馏可将液态混合物粗略分开;若要完全分开,沸点差至少在110℃),而又无恒沸点的液态混合物适用];2)测定化合物的沸点;3)提纯除去不挥发的杂质;4)回收溶剂或蒸出部分溶剂以浓缩溶液。
2、沸点的定义和测定沸点的意义和方法:沸点的定义:在大气压下,液态物质的液气两态平衡共存时的温度叫沸点。
[纯液态有机物都有恒定的沸点,在整个沸腾蒸发过程中温度变动很小,只有0.5-1.5℃。
不纯的液态有机物没有恒定的沸点,在整个沸腾蒸发过程中温度变动大,但是恒沸混合物(例:95.57%的乙醇和4.43%的水,其沸点是78.17℃;18.5%的乙醇、74.1%的苯和7.4%的水,其沸点是64.86℃)除外]测定沸点的意义:通过沸点的测定可以初步鉴定有机化合物;鉴别有机化合物;还能定性地检验液体有机化合物的纯度。
测定沸点的方法:常量法(即蒸馏法)和微量法。
三、主要试剂和产物的物理常数:四、实验装置:蒸馏烧瓶为一带支管的圆底烧瓶液体体积一般在其容积的1/3--1/2左1/3-2/3右。
接受器常用接液管和三角烧瓶或圆底烧瓶,应与外界大气相通。
1、蒸馏烧烧瓶:蒸馏烧瓶的选用与被蒸液体量的多少有关,通常装进液体的体积应为蒸馏烧瓶容积1/3-2/3。
液体量过多或过少都不宜。
在蒸馏低沸点液体时,选用长颈蒸馏烧瓶;而蒸馏高沸点液体时,选用短颈蒸馏烧瓶。
2、温度计:应根据被蒸馏液体的沸点来选择温度计,即选择高出被蒸馏液体的沸点10-20℃来适当的温度计。
温度计水银球的位置应使温度计水银球的上缘和蒸馏头支管口的下缘在同一水平面上。

常压蒸馏及沸点的测定实验报告实验二常压蒸馏和沸点的测定实验二、常压蒸馏和沸点的测定一、实验目的了解沸点测定的意义;掌握蒸馏法及微量法测定沸点的原理和方法。
二、基本原理液态物质受热,由于分子运动使其从液体表面逃逸出来,形成蒸气压;随着温度升高,蒸气压加大,当蒸气压和大气压相等时,液体沸腾,此时的温度即为该液体的沸点;每一种纯液态有机化合物在一定压力下均具有固定的沸点。
蒸馏就是将液态物质加热至沸腾变为蒸气,然后将蒸气移到别处,再使蒸气冷凝变为液体的一种操作过程。
蒸馏的原理是利用物质中各组分的沸点差别(相差大于30℃)而将各组分分离。
三、实验步骤演示1、蒸馏装置及安装水银球的上缘位于蒸馏烧瓶支管接口的下缘,使他们在同一水平线上沸点低于130 ℃常用蒸馏装置2、蒸馏操作加料:不纯乙醇30 mL及沸石数颗;加热:先通水再加热;蒸馏速度1-2滴/S;观察沸点及收集馏液:维持原有温度不再有馏出液蒸出而温度又突然下降时,就应停止蒸馏;蒸馏完毕,先停止加热再停止通水,拆卸仪器,其程序与装配时相反。
纯粹液体的沸程一般不超过1-2℃。
液体的沸程常一定程度上代表它的纯度。
本实验用不纯乙醇30 mL,放在60 mL圆底烧瓶中蒸馏,并测定沸点。
四、实验注意事项1、温度计的位置应恰当。
2、不要忘记加沸石。
如果忘记,应使沸腾的液体冷却至沸点以下后才能加入沸石。
3、有机溶剂均应用小口接受器。
4、系统要与大气相通,否则造成封闭体系,引起爆炸事故。
五、应用1、分离液体混合物;2、测定化合物的沸点;3、提纯除去不挥发性杂质;4、回收溶剂或者蒸出部分溶剂以浓缩溶液;篇二:有机化学实验三蒸馏及沸点的测定有机化学实验三蒸馏及沸点的测定实验三蒸馏及沸点的测定一.实验目的:(1)了解测定沸点和蒸馏的意义;(2)掌握蒸馏法测定沸点的原理和操作方法;(3)掌握微量法测定沸点的原理和方法;二.实验重点和难点:(1)蒸馏和沸点的意义;(2)微量法和常量法测定沸点的原理和方法;实验类型:基础性实验学时:4学时三.实验装置和药品:主要实验仪器:温度计沸点管毛细管Thiele管(即b形管)酒精灯液体石蜡温度计蒸馏烧瓶直形冷凝管接液管锥形瓶沸石主要化学试剂:95%乙醇(化学纯,b.p78.5)乙酸(化学级,b.p117.9)酒精(工业级,b.p78.2)四.实验装置图:微量法沸点测定管五.实验原理:1.定义:液体受热时,其蒸气压升高。

蒸馏和沸点的测定实验报告 .报告题目:乙醇的蒸馏及沸点测定专业班级:指导老师:刘明星学生姓名:学号:实验报告生物工程何德维 1108110384xx年3月30日乙醇的蒸馏及沸点测定一.实验目的1、了解用蒸馏法分离和纯化物质及测定化合物沸点的原理与方法。
2、训练蒸馏装置的安装与操作方法,要求整齐、正确。
3、掌握常量法和微量法测定沸点的原理和方法、蒸馏与沸点测定的原理。
二.实验原理蒸馏是分离和提纯液体有机物质的最常用方法之一液体加热时蒸汽压就随着温度升高而加大,当液体的蒸汽压增大到与外压相等时,会有大量气泡从液体内逸出,液体沸腾。
这时的温度称为液体的沸点。
蒸馏是将液体加热到沸腾,使液体变为蒸汽,然后使蒸汽冷却再凝结为液体这两个过程的联合操作。
因为组成液体混合物的各组分的沸点不同,当加热时,低沸点物质就易挥发,变成气态,高沸点物质不易挥发汽化,而留在液体内,这样,我们就能把沸点差别较大(至少30℃以上)的两种以上混合液体分开,以达到纯化的目的。
同时,利用蒸馏法,可以测定液体有机物的纯度,每一种纯的液体有机物质,在平常状况下,都有恒定的沸点(恒沸混合物除外),而且恒定温度间隙小(纯粹液体的沸程一般不超过1-2℃);当有杂质存在,则沸点会有变化(有时升高,有时降低,根据杂质温度高低二变化),而且沸点的范围也会加大。
沸点相近的有机物,蒸汽压也近于相等。
因此,不能用蒸馏法分离,可用分馏法分离;对于沸点高、受热易分解的物质,可用减压蒸馏或水蒸气蒸馏来分离提纯。
三.主要药品及仪器1.工业酒精(滴几滴红汞或其他有色物)20ml(蒸馏用)2.烧瓶(50ml)蒸馏头温度计(100℃)冷凝管接引管三角瓶3.铁夹铁环酒精灯沸石量筒(50ml)铁台四.实验步骤1、清洗所有蒸馏装置,并用量筒量取20ml工业酒精装入烧瓶中,再放入2-3颗沸石。
2、安装蒸馏装置。
首先将所需要的蒸馏装置均准备齐全(如上仪器),先从热源(酒精灯)处开始,然后“由下而上,由左到右”。
2.2 蒸馏及沸点的测定实验目的:了解测定沸点的意义,掌握常量法(即蒸馏法)及微量法测定沸点的原理和方法。
原理:液体在一定的温度下, 具有一定的蒸气压, 一般说来, 液体的蒸气压随着温度的升高而增大。
图1所示典型的蒸气压──温度曲线。
图1蒸气压─温度曲线如果装有液体的容器与大气相通, 液体的沸点将是液体的蒸气压与大气压相等时的温度。
纯液体的蒸气压随温度的升高而稳定地上升直至到达沸点为止, 这时有大量气泡从液体中逸出, 即液体沸腾。
方法:利用液体的这一性质, 将液体加热至沸使其变成蒸气, 再使蒸气通过冷却装置冷凝并将冷凝液体收集到另一容器中。
为了消除在蒸馏过程中的过热现象和保证沸腾的平稳状态, 常加入素烧瓷片或沸石, 或一端封口的毛细管, 因为它们都能防止加热时的暴沸现象, 故把它们叫做止暴剂或叫助沸剂。
在加热蒸馏前就应加入止暴剂。
不能匆忙加入止暴剂。
因为在液体沸腾时投入止暴剂, 将会引起猛烈的暴沸, 液体会冲出瓶口, 若是易燃的液体, 将会引起火灾, 所以应使沸腾的液体冷却至沸点以下后才能加入止暴剂。
如蒸馏中途停止, 后来需要继续蒸馏, 也必须在加热前添加新的止暴剂才安全。
用途:由于低沸点物易挥发, 高沸点物难挥发, 固体物更难挥发, 甚至可粗略地认为大多数固体物不挥发。
因此, 通过蒸馏可把沸点相差较大的两种或两种以上的液体混合物逐一分开, 达到纯化的目的, 也可将易挥发物和难挥发物分开, 达到纯化的目的。
蒸馏时, 首先应将液体加热至沸, 所以只要在液体沸腾后, 测出气液平衡时的温度, 这个温度就是液体的沸程( 沸点的温度范围 ), 纯液体, 在一定的压力下有一定的沸点和沸程1~2℃, 但是只要有杂质存在, 不仅沸点会变化, 而且沸程也会加大, 因此, 测出化合物的沸程便可知其纯度( 恒沸混合物除外)。
故蒸馏也可用于纯度的检验。
步骤:2.2.1 蒸馏(1) 蒸馏装置如图2-4:图2 水冷凝蒸馏装置图3 空气冷凝蒸馏装置图4 滴液蒸馏装置实验室的蒸馏装置主要包括下列三个部分:①蒸馏烧瓶: 为容器,液体在瓶内受热气化,蒸气经支管或蒸馏头的侧管进入冷凝管, 支管与冷凝管间靠单孔塞子相连,支管伸出塞子外2~3厘米。
实验项目蒸馏及常量法测沸点液体有机混合物的纯化和分离,溶剂的回收,经常采用蒸馏的方法来完成。
蒸馏包括常压蒸馏(简单蒸馏)、减压蒸馏、水蒸气蒸馏等。
减压蒸馏、水蒸气蒸馏将在后面的学习中介绍。
蒸馏、分馏、减压蒸馏和水蒸气蒸馏都是有机制备中常用的重要操作。
一般用于以下几个方面:(1)分离液体混合物,仅对混合物中各成分的沸点有较大差别时才能达到有效的分离;(2)测定化合物的沸点;(3)提纯,除去不会发的杂质;(4)回收溶剂,或蒸出部分溶剂进行浓缩溶液。
沸点是液体有机化合物的重要物理常数。
根据被测液体的量分为常量法和微量法两种,用蒸馏的方法来测定液体沸点方法叫常量法,此法一般需要样品量不少于10mL,适合对热易分解、易氧化的化合物。
当样品量较少时,需要采用微量法测定沸点。
本次实验利用蒸馏操作进行常量法测液体沸点。
一、实验目的1.了解蒸馏的原理及沸点的意义;2.掌握蒸馏装置仪器选择、连接和拆卸;3.掌握常量法测定沸点、分离提纯乙醇以及简单蒸馏的基本操作。
二、实验原理所谓蒸馏就是将液态物质加热到沸腾变为蒸气,又将蒸气冷凝为液体这两个过程的联合操作。
蒸馏装置是由蒸馏(热源、蒸馏瓶、温度计)、冷凝(冷凝管)、接收(接液管、接收器)三个部分组成(如图7.1)。
7.1当液态物质受热时,由于分子运动使其从液体表面逃逸出来,形成蒸气压,随着温度的升高,蒸气压增大,待蒸气压和大气压相等时,液体沸腾,此时的温度称为该液体的沸点。
每种纯液态有机化合物在一定的压力下均有固定的沸点。
在蒸馏液体混合物时低沸点组分“优先”沸腾,被蒸出来,沸点高的随后蒸出,不挥发的的则留在蒸馏瓶中,由此,可达到分离和提纯的目的。
但在蒸馏沸点比较接近的混合物时,各种物质的蒸气将同时蒸出,只不过低沸点的多一些,故难于达到较好的分离和提纯的目的,因此,蒸馏对于沸点相差较大(如相差30℃)的液态混合物进行分离和提纯,效果较好。
伴随蒸馏的过程中,由此可测得液体混合物不同组分的沸点。
实验报告姓名:班级:同组人:项目:蒸馏及沸点的测定技术课程:学号:一、实验目的1.了解蒸馏和沸点测定的基本原理和意义。
2.掌握蒸馏和沸点测定的操作技术。
二、实验原理液体分子由于运动有从液面逸出的倾向,这种倾向随着温度的升高而增大,进而在液面上部形成蒸气。
当分子由液体逸出的速率与分子由蒸气中回到液体中的速率相等,液面上的蒸气达到饱和,称为饱和蒸气。
它对液面所施加的压力称为饱和蒸气压。
实验证明,液体的蒸气压只与温度有关,即液体在一定温度下具有一定的蒸气压。
将液体加热,它的蒸气压就随着温度的升高而增大。
当液体的蒸气压增大到与外界施于液面的总压力(通常是大气压力)相等时,液体就开始沸腾。
这时的温度称为液体的沸点。
纯的有机化合物在一定压力下均有恒定的沸点,且沸程很小,一般不超过1~2 ℃。
所以测定沸点是鉴别有机化合物和判断物质纯度的依据之一。
测定沸点常用的方法有常量法(蒸馏法)和微量法两种。
将液体物质加热到沸腾,使其变成蒸气,然后将蒸气冷凝为液体的过程称为蒸馏。
蒸馏是分离和提纯液体化合物最常用的一种方法,通过蒸馏可以把易挥发的物质和不挥发的物质分离,也可将沸点不同的液体混合物分离开来。
但液体混合物中各组分的沸点要相差30 ℃以上,才能取得较好的分离效果。
而要彻底分离,混合物中各组分的沸点要相差110 ℃以上。
蒸馏也是测定液体有机化合物沸点的一种方法。
三、仪器和药品仪器:圆底烧瓶(100 mL、50 mL)、蒸馏头、温度计(100 ℃)、温度计套管、冷凝管、接液管、50 mL量筒、长颈漏斗、铁架台、铁圈、铁夹、橡皮管、石棉网、酒精灯、提勒管、玻璃管(内径为4~5 mm)、毛细管。
沸石、橡皮圈。
药品:95%医用酒精、苯(分析纯)、液体石蜡。
四、内容及步骤(一)蒸馏和常量法测定沸点常量法测定沸点即蒸馏法测定沸点,所用的仪器装置与蒸馏完全一样。
1.实验装置蒸馏装置主要由蒸馏烧瓶、冷凝管和接收器三部分组成,见图。
(1)蒸馏烧瓶待蒸馏液在瓶内受热汽化,蒸气经支管进入冷凝管。
实验蒸馏及沸点的测定一、实验目的1、蒸馏及沸点测定的基本原理;2、用蒸馏法分离工业酒精、测定乙醇沸点的基本操作。
二、实验仪器仪器:水浴锅、蒸馏烧瓶(250ml圆底烧瓶和蒸馏头)、温度计(带橡胶塞)、直形冷凝管、接引管、接受器(三角烧瓶2个)、铁台(2个)、冷凝管夹(2个)、十字夹(2个)、橡胶管(2根)、漏斗、100ml量筒(公用)试剂:工业酒精、沸石三、实验原理1、什么是蒸馏?将液态物质加热到沸腾变成蒸气,再将蒸气冷凝为液体的过程。
2、蒸馏有哪些用途?液体物质的分离与提纯(适用于沸点相差较大的液体化合物);测定化合物的沸点;回收溶剂或浓缩溶液。
3、沸点的定义?液态物质的蒸气压与其所处体系的压力相等时的温度。
物质处于沸点时的特征:液态物质沸腾;液态与气态平衡。
图1 蒸馏装置图图2 温度计的安装位置四、实验操作流程1、接好冷凝水的进出水管(注意检查进出水管——下进上出、冷凝管是否完好)。
2、蒸馏装置的安装:根据装置图按从下往上,从左往右的顺序安装(温度计的水银球上端的位置恰好与蒸馏烧瓶支管的下缘处于同一水平线上)。
3、蒸馏操作:(1)取下温度计,加入少许沸石,通过长颈漏斗或者沿着蒸馏烧瓶支管对面的瓶颈壁小心加入工业酒精样品90ml。
(2)安装温度计。
(3)开通冷凝水。
(4)加热(设置水浴锅温度95℃左右)。
(5)接受馏出液4、沸程记录。
5、结束蒸馏:当温度计读数突然下降,冷凝管中液滴流出缓慢时,说明蒸馏结束。
(1)切断电源,停止加热。
(2)移去接受瓶,并放好。
(3)关闭冷凝水。
(4)冷却后拆卸仪器,并及时清洗玻璃仪器,放回原位。
五、实验结果记录。
有机化学实验指导实验一蒸馏和沸点的测定【实验目的】了解测定沸点的意义和蒸馏的意义,掌握常量法(即蒸馏法)及微量法测定沸点的原理和方法。
【实验原理】1.纯净的液体有机物在一定压力下具有固定的沸点。
沸点是液体有机化合物的物理常数之一,因此通过测定沸点可以鉴别有机化合物并判断其纯度。
2.利用蒸馏可将沸点相差较大(如相差30℃)的液体混合物分开。
液体混合物加热后沸点较低者先蒸出、沸点较高者随后蒸出、不挥发的留在蒸馏瓶内,这样可以达到分离提纯的目的。
【课堂内容】通过提问检查学生预习情况,提问内容如下:1)测沸点有何意义?2)什么是沸点?纯液态有机化合物的沸程是多少?3)什么是蒸馏?蒸馏的意义?4)什么是爆沸?如何防止爆沸?5)沸石为什么能防止爆沸?6)蒸馏的用途?7)何时用常量法测沸点何时用微量法测沸点?8)有机实验室常用的热源?加热的方式有几种?9)热浴的方式有几种?10)安装、拆卸仪器装置的顺序是什么?11)冷凝管的种类有几种?12)蒸馏装置中温度计的位置是怎样的?【实验仪器及设备】1. 30mL圆底烧瓶19#2. 蒸馏头19#×3或19#×2×14#3. 温度计套管19# 或14#4. 温度计100℃5. 直形冷凝管(短的)19#×26. 接尾管19#×27. 30 mL三角瓶1个8. 100 mL烧杯1个9. 30 mL量筒10. 沸点管,温度计100 ℃,胶塞,沸石,乳胶套圈11. 升降架2个12. 250 mL加热套,三角架,s扣,夹子。
【药品】1. 95 % C2H5OH 15 mL/人2. C6H6 (AR纯)【实验内容】常量法测95%乙醇的沸点,蒸馏15 mL 95 % C2H5OH。
【测得结果】 b.p.95 % C2H5OH = 78.0 ℃(理论值78.4 ℃)【注意事项】1. 仪器安装要严密、正确。
2. 注意安装拆卸的顺序。
3. 加热前放沸石,通冷凝水。