盐溶液显酸碱性的原因 课件
- 格式:ppt
- 大小:1.39 MB
- 文档页数:20


盐溶液的酸碱性及原由【教课目的】知识与技术1.掌握盐类水解的观点;以CH3COONa、NH4Cl 为例理解盐类水解的原理。
2.理解盐类水解的特色和规律。
过程和方法1.经过实验研究、分组议论,进一步让学生掌握“提出问题-剖析问题 -理论解说 -解决问题”的科学方法。
2.经过问题研究,培育学生解决本质问题的能力。
感情、态度和价值观1.经过“盐溶液不必定显中性”的教课,让学生知道全面看事物的辩证思想。
2.培育学生脚踏实地、科学研究的精神。
【教课要点】盐类水解的观点、原理和规律【教课难点】理解盐类水解的原理教课过程:【引入】生活中常用的增添剂除了食盐(NaCl)外,还有味精 (C5H8NO4Na),苏打(Na2CO3),小苏打 (NaHCO3)等,这些都属于化学中的盐类。
这节课我们来学习有关盐类的一些知识——盐类的水解。
【知识回首】依据形成盐的酸、碱的强弱来分,盐能够分红哪几类酸 +碱=盐+水(中和反响)【思虑】酸溶液呈酸性,碱溶液呈碱性,那么盐溶液呈什么性呢【过渡】那么盐溶液的酸碱性有什么规律呢【板书】第三节盐类的水解一、研究盐溶液的酸碱性【找寻规律】研究盐溶液的酸碱性盐溶液酸碱性NaCl中性Na2SO4中性NaHCO3碱性Na2CO3碱性CH3COONa碱性NH4Cl酸性(NH4)2SO4酸性从以上的实验中,我们发现有的盐溶液呈中性,有的盐溶液呈酸性,有的盐溶液呈碱性。
【思虑】试用概括法找出盐的构成(分类)与盐溶液酸碱性的关系。
盐的种类与盐溶液酸碱性的关系:盐溶液构成分类酸碱性NaCl强酸强碱盐中性Na2SO4NaHCO3强碱弱酸盐碱性23Na CO3CH COONaNH4Cl强酸弱碱盐酸性(NH4)2SO4【小结】强酸强碱盐呈中性,强酸弱碱盐呈酸性,强碱弱酸盐呈碱性。
【思虑】为何盐溶液会体现不一样的酸碱性这节课我们就来研究这个问题。
【板书】二、盐溶液体现不一样酸碱性的原由【研究原由】盐溶液体现不一样酸碱性的原由纯水中,当分别加入CH3COONa、 NH4Cl、NaCl 形成溶液后,请思虑:、 NH4 Cl、NaCl 是什么种类的电解质2.它们在水中各以什么形式存在3.其水溶液中各存在哪些微粒4.这些微粒能互相反响吗5.若反响,结果怎么样【讲】以 CH3COONa溶液为例剖析强碱弱酸盐溶液呈碱性的原由。





盐的酸碱性强酸弱碱盐溶于水显酸性如Al2(SO4)3溶于水后,Al3+会发生如下水解反应Al3+ +3H2O = Al(OH)3 + 3H+你可以发现水解后得到了H+,说明溶液是酸性的强碱弱酸盐溶于水一般显碱性如Na2S溶于水发生如下水解反应S2- + H2O = HS - + OH-HS- + H2O = H2S + OH-强酸强碱盐一般是中性的,如氯化钠弱酸弱碱盐一般发生双水解Al2S3+6H2O=2Al(OH)3+3H2S1.强碱弱酸盐溶于水呈碱性,例如:碳酸钠,磷酸钠,氟化钠,硫化钠,次氯酸钠,醋酸钠等等弱酸的钾盐,钠盐,钙盐,钡盐等(如果能溶的话)。
2.强酸弱碱盐溶于水呈酸性,例如,硫酸铵,硫酸铁,硫酸铜,硫酸铝等等弱碱的硫酸盐,硝酸盐,氯化物,溴化物,碘化物等(如果能溶的话)3.部分酸式盐溶于水呈碱性,例如,碳酸氢钠,磷酸一氢钠,硫氢化钠。
部分酸式盐溶于水呈酸性,例如,硫酸氢钠,亚硫酸氢钠,磷酸二氢钠。
有些弱酸弱碱盐呈酸性,例如,草酸铵,氟化铵,亚硫酸铵有些弱酸弱碱盐呈碱性,例如,次氯酸铵,碳酸铵,硫化铵。
记住,比醋酸酸性弱的弱酸的铵盐呈碱性,比醋酸酸性强的弱酸的铵盐呈酸性。
常见强酸:硫酸,硝酸,盐酸,氢溴酸,氢碘酸,高氯酸。
常见强碱:氢氧化钠,氢氧化钾,氢氧化钙,氢氧化钡。
常见弱酸:亚硫酸,氢氟酸,磷酸,草酸,醋酸,碳酸,次氯酸,硅酸,氢硫酸。
常见弱碱:氨水,氢氧化铝,氢氧化铁,氢氧化铜,氢氧化亚铁,氢氧化镁。
【知识讲解】一、盐类水解的实质盐类在水溶液中电离出的离子跟水电离出的H+或OH-生成难电离的分子或离子,从而破坏了水的电离平衡,使水的电离度增大。
判断盐类水解能否水解的条件:一看能否溶,不溶不水解;二看有无弱,无弱不水解。
二、盐类水解的类型和规律判断盐类能否发生水解及水解后溶液显酸碱性要看盐电离的离子对应的酸或碱的相对强弱。
1、盐类水解的类型盐的类型是否水解常见能水解的离子溶液PH值一价:CH3COO-、HS-、AlO2-、ClO-、HCO-3 PH> 7强碱弱酸盐水解二价:S2-、CO32-、SiO32 -、HPO42-三价:PO43-、ASO43-一价:NH4+、Ag+ PH< 7强酸弱碱盐水解二价:Fe2+、Cu2+、Sn2+、Zn2+三价:Al3+、Fe3+强酸强碱盐不水解PH= 72、水解规律:有弱才水解,无弱不水解;谁弱谁水解,越弱越水解;三价阳离子都水解,多元弱酸根离子分步水解。


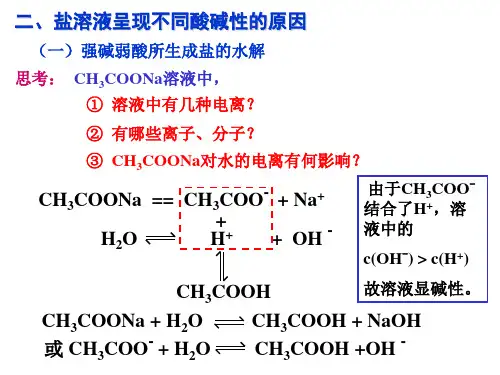
盐溶液呈现不同酸碱性的原因如:CH3COONa溶于水之后,完全电离。
(因为CH3COONa是强电解质。
)CH3COONa ═ CH3COO- + Na+………⑴H2O H+ + OH-………⑵CH3COO- + H+ CH3COOH………⑶把⑴⑵⑶式联立,可得到水解方程式:CH3COONa + H2O CH3COOH + NaOH这说明CH3COONa溶于水后,反应有NaOH生成,所以溶液显碱性。
把上述化学方程式改写成离子方程式。
CH3COO- + H2O CH3COOH + OH-随着CH3COONa的加入,对水的电离有什么影响呢?促进了水的电离,可以看作是使水分解了。
醋酸钠与水反应的实质是:醋酸钠电离出的醋酸根离子和水电离出的氢离子结合生成弱电解质醋酸的过程。
1.弱酸强碱盐,水解显碱性CH3COONa = CH3COO−+ Na++H2O H+ + OH−CH3COOHCH3COONa + H2OCH3COOH + NaOHCH3COO−+ H2OCH3COOH + OH−2.强酸弱碱盐水解显酸性NH4Cl = NH4+ + Cl−+H2O OH− + H+NH3·H2ONH4Cl + H2O NH3·H2O + HClNH4+ + H2O NH3·H2O + H+3.强酸强碱盐:不水解弱酸弱碱盐:双水解,水解程度增大。