二氧化碳和一氧化碳的比较
- 格式:doc
- 大小:34.00 KB
- 文档页数:1

初中化学知识二氧化碳与一氧化碳的比较
普通的,物质的结构决议其性质。
CO2的结构式为O=C=O,分子外形为直线形的,属于非极性分子,表现出在于其它物质起反响时容易失氧,具有氧化性,发作恢复反响,如
CO2+C2CO。
而CO的结构式为O=C,分子外形为直线形的,属于极性分子,表现出在于其它物质起反响时容易得氧,具有恢复性,发作氧化反响,如2CO+O22CO2。
1. 二氧化碳的性质及其用途:不支持熄灭且密度比空气大灭火,干冰制冷剂或人工降雨,与某些物质反响化工产品的原料或植物光协作用,石灰水吸收空气中二氧化碳石灰浆抹墙等。
2. 一氧化碳的性质决议了其用途:(1)一氧化碳的可燃性作燃料,如家庭用煤气(主要成分为一氧化碳)做饭等;(2)一氧化碳的恢复性冶炼金属,如工业冶炼金属铁、铜等;(3)一氧化碳的毒性毒杀一些有害植物,同时留意做好尾气处置,防止对环境污染。
二氧化碳和一氧化碳由于结构不同决议了二者的性质和用
途上的差异。
但二者可以相互转化,如二氧化碳具有氧化性,经过高温的碳层生成一氧化碳。
一氧化碳具有恢复性,可以经过被氧化或冶炼金属失掉二氧化碳。
例3 (2021·桂林市)以下关于一氧化碳和二氧化碳的说法正确的选项是
A.都比空气重
B.都可以用碳和氧气反响失掉
C.都有恢复性
D.都能和廓清石灰水发作反响
提示:二者中只要一氧化碳的密度比空气小,具有恢复性,而且只要二氧化碳能使廓清石灰水变混浊。
碳单质充沛熄灭时生成二氧化碳,不充沛熄灭时生成一氧化碳。
所以选项B 正确。
答案为B。
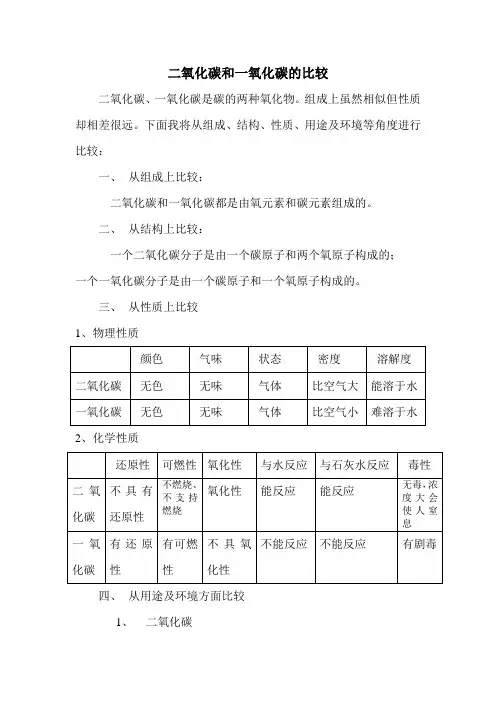
二氧化碳和一氧化碳的比较
二氧化碳、一氧化碳是碳的两种氧化物。
组成上虽然相似但性质却相差很远。
下面我将从组成、结构、性质、用途及环境等角度进行比较:
一、从组成上比较:
二氧化碳和一氧化碳都是由氧元素和碳元素组成的。
二、从结构上比较:
一个二氧化碳分子是由一个碳原子和两个氧原子构成的;
一个一氧化碳分子是由一个碳原子和一个氧原子构成的。
三、从性质上比较
1、物理性质
2、化学性质
四、从用途及环境方面比较
1、二氧化碳
(1)促进植物的光合作用
(2)由于其不燃烧,也不支持燃烧且密度比空气大,可用于灭火(3)生产化肥及作气体肥料
(4)固体二氧化碳叫干冰,升华时会吸收大量的热,可作人工降雨、制冷剂
(5)制作碳酸饮料
(6)对环境的影响——产生温室效应
2、一氧化碳
(1)燃烧能产生大量的热因此可作为能源。
(2)具有还原性,可用于冶炼工业。
以上就是二氧化碳和一氧化碳的比较。

一、二氧化碳的性质及其应用1. 二氧化碳是一种无色、无味、密度大于空气的气体。
它在常温下为固体,常用于灭火器中。
2. 二氧化碳的化学性质稳定,不易与其他物质发生化学反应。
它常被用作一种惰性气体。
3. 二氧化碳广泛应用于制冷、饮料工业等领域。
在制冷系统中,二氧化碳可以起到热交换媒介的作用;在饮料工业中,二氧化碳可以增加饮料的口感和气泡感。
二、一氧化碳的性质及其危害1. 一氧化碳是一种无色、无味、无味、具有毒性的气体。
由于其无色无味特性,一氧化碳很容易被人们忽视,但它对人体的危害却非常严重。
2. 一氧化碳可以与人体血红蛋白结合,影响氧气的输送,从而导致中毒甚至逝去。
一氧化碳也被称为“无声杀手”。
3. 一氧化碳主要来自燃烧不完全的燃料,如煤气、柴油、木炭等。
在家庭生活中,要注意通风,防止一氧化碳中毒。
三、二氧化碳和一氧化碳的区别与通联1. 二氧化碳和一氧化碳在化学结构和性质上都有所不同。
二氧化碳分子由一个碳原子和两个氧原子组成,而一氧化碳分子由一个碳原子和一个氧原子组成。
2. 二氧化碳在自然界中广泛存在,并且对环境和人体健康没有直接危害,可以被充分利用;一氧化碳虽然在自然界中可以被发现,但是它对人体健康有着极大的危害,需要引起高度重视。
3. 二氧化碳和一氧化碳都是一种重要的气体,对人类社会和生产生活都有着重要的影响。
了解二氧化碳和一氧化碳的性质、应用及危害,对人们提高环境意识、健康意识具有重要的意义。
四、如何应对二氧化碳和一氧化碳的相关问题1. 在生产生活中,要加强对燃烧、通风等安全措施的管理,防止一氧化碳危害的发生。
2. 加强对环境保护的宣传和教育,提倡低碳生活,减少二氧化碳的排放。
3. 进一步加强相关法律法规的制定和实施,加大对环境污染和安全隐患的治理力度。
总结:通过本文的介绍,我们可以了解到,二氧化碳和一氧化碳是两种在生产和生活中非常常见的气体。
了解它们的性质、应用和危害,对我们加强环境保护、安全生产具有重要意义。
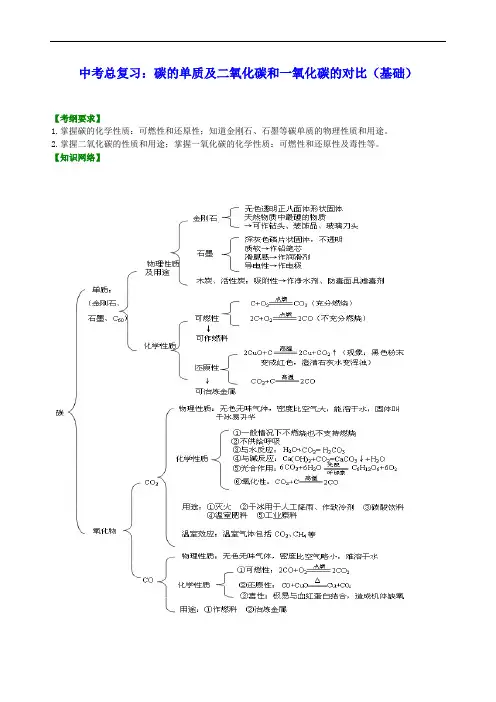
中考总复习:碳的单质及二氧化碳和一氧化碳的对比(基础)【考纲要求】1.掌握碳的化学性质:可燃性和还原性;知道金刚石、石墨等碳单质的物理性质和用途。
2.掌握二氧化碳的性质和用途;掌握一氧化碳的化学性质:可燃性和还原性及毒性等。
【知识网络】【考点梳理】考点一、碳单质(金刚石、石墨)的物理性质和用途比较对比项目 金刚石石墨外 观 无色透明正八面体形状固体深灰色细磷片状固体 光 泽 加工琢磨后有光泽 略有金属光泽硬 度 自然界最硬软 导电性 无 良好 导热性 良好良好用 途钻探机钻头、刻刀、装饰品等电极、铅笔芯、润滑剂等要点诠释:1.由于碳原子排列方式不同,导致金刚石和石墨在物理性质上存在较大差异。
2.炭和碳不同。
碳是指碳元素,是“核电荷数为6的同一类原子的总称”,有广泛、概括的含义,并不具体指某种物质;炭是指具体的物质——由碳元素组成的单质,如木炭、焦炭、活性炭、炭黑等。
碳与炭不能混用。
3.木炭和活性炭具有疏松多孔的结构,因此具有吸附能力,可以吸附一些色素、有异味的物质,吸附过程属于物理变化,并非化学变化。
4.规律总结:物质的组成、结构垐垐?噲垐?决定反映物质的性质垐垐?噲垐?决定反映物质的用途。
考点二:CO 2和CO 性质及用途的比较(高清课堂《二氧化碳和一氧化碳》一)对比项目 CO 2CO物理性质无色无味气体,能溶于水,密度比空气大,干冰易升华 无色无味气体,难溶于水,密度比空气略小化学性质可燃性一般情况下既不能燃烧,也不支持燃烧有可燃性2CO+O 22CO 2还原性没有还原性,有较弱的氧化性C+CO 22CO有还原性 CO+CuOCu+CO 2与水反应 与水反应CO 2+H 2O=H 2CO 3 不能与水反应 与石灰水的反应(碱) 与石灰水反应CO 2+Ca(OH)2=CaCO 3↓+H 2O不能与石灰水反应毒性 无毒有剧毒 主要用途 可制汽水,作制冷剂,灭火,气体肥料气体燃料、高炉炼铁对环境的影响造成温室效应污染空气要点诠释:1.由于CO 和CO 2的分子构成不同,决定了二者性质的不同。

鉴别一氧化碳和二氧化碳的五种方法:一是根据密度不同,分别将它们充入气球;二是根据水溶性不同,分别将它们通入石蕊试液中;三是根据可燃性不同;四是根据还原性不同,分别将它们通入灼热的氧化铜中;五是根据是否与碱溶液反应,分别将它们通入到澄清的石灰水。
【将带火星的木条不能检验二者,因为一氧化碳和二氧化碳都是不支持燃烧的;木炭在氧气中燃烧发出明亮白光是正确的。
】为什么木炭在氧气中燃烧发出明亮白光是正确的?谢谢...回答因为木炭在氧气中燃烧,是在纯氧中发生的剧烈氧化反应CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成HCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2C O3=CaCO3↓ +2KOH 有白色沉淀生成AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成1结晶法定义使物质从液态(溶液或熔融状态)或气态形成晶体的方法即结晶法。

一氧化碳和二氧化碳的相同点一氧化碳和二氧化碳是两种由碳和氧元素组成的化合物,它们在结构、性质和应用方面存在一些相同点。
一氧化碳和二氧化碳都是由碳和氧元素组成的化合物。
一氧化碳由一个碳原子和一个氧原子组成,化学式为CO;而二氧化碳由一个碳原子和两个氧原子组成,化学式为CO2。
它们的分子中都含有碳氧双键,因此都属于含氧化碳的化合物。
一氧化碳和二氧化碳都是无色、无味、无臭的气体。
它们在常温常压下存在,不易溶于水。
由于无色无味,人们很难察觉到它们的存在,这也增加了它们的危险性。
一氧化碳可以通过一些化学反应制备,如不完全燃烧有机物、还原金属氧化物等;而二氧化碳则是通过完全燃烧有机物或碳酸盐的分解等方式生成的。
一氧化碳和二氧化碳都具有一定的毒性。
一氧化碳是一种强大的毒气,它可以与血红蛋白结合,形成一氧化碳血红蛋白,从而影响血液的氧运输功能,导致中毒甚至死亡。
而二氧化碳虽然对人体无直接毒害作用,但在高浓度下会引起窒息,因为它会排挤空气中的氧气。
因此,无论是一氧化碳还是二氧化碳,都需要引起人们的高度重视,避免其在室内或封闭空间中积累过多。
一氧化碳和二氧化碳还具有一些重要的应用。
一氧化碳在工业生产中被广泛用作还原剂、合成气体和燃料。
它可以用于冶金、化工、电子等行业,具有重要的工业价值。
而二氧化碳则被广泛应用于食品和饮料工业,用作酒类、软饮料和啤酒等的气体充装剂。
一氧化碳和二氧化碳在结构、性质和应用方面存在一些相同点。
它们都是由碳和氧元素组成的化合物,无色、无味、无臭,具有一定的毒性,并且在工业生产中具有重要的应用。
然而,尽管它们有一些相同点,但在化学性质、毒性和应用领域上仍存在明显的差异,人们需要正确理解和使用它们,以确保安全。

一氧化碳和二氧化碳的区别在物理性质上的区别:二氧化碳能溶于水,无毒无色,不能燃烧也不支持燃烧。
固体二氧化碳俗称干冰,常用于制冷剂。
一氧化碳难溶于水,有毒,无色无味。
容易和人体内的血红蛋白结合造成缺氧,形成一氧化碳中毒。
一氧化碳(CO)纯品为无色、无臭、无刺激性的气体。
分子量28.01,密度1.250g/l,冰点为-207℃,沸点-190℃。
在水中的溶解度甚低。
空气混合爆炸极限为12.5%~74%。
一氧化碳进入人体之后会和血液中的血红蛋白结合,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。
因此一氧化碳具有毒性。
在化学性质上的区别:一氧化碳化学性质较稳定。
可以燃烧,和氧气结合形成二氧化碳。
二氧化碳和水反应形成碳酸,同时碳酸不稳定,用以分解成水和二氧化碳。
碳酸为一种弱酸。
此外二氧化碳还可以和多种正离子反应形成沉淀。
常用的二氧化碳坚定方法就是将二氧化碳通入石灰水,石灰水变浑浊,加入足量硝酸后,石灰水变澄清,证明该气体为二氧化碳。
二氧化碳是空气中常见的化合物,其分子式为CO?,由两个氧原子与一个碳原子通过共价键连接而成,常温下是一种无色无味气体,密度比空气略大,能溶于水,与水反应生成碳酸。
二氧化碳与一氧化碳的鉴别方法:(1)澄清石灰水:将气体分别通入澄清石灰水中,能使澄清石灰水变浑浊的是二氧化碳,无明显现象的是一氧化碳。
(2)燃着的木条:将气体分别在空气中点燃,能燃烧的是一氧化碳,不能燃烧的是二氧化碳。
(3)紫色石蕊试液:将气体分别通入紫色石蕊试液中,能使石蕊试液变红的是二氧化碳,无明显现象的是一氧化碳。
(4)还原金属氧化物:将气体分别通过灼热的氧化铜,出现黑色粉末变红这一现象的是一氧化碳,没有明显现象的是二氧化碳。
二氧化碳与一氧化碳的除杂方法:1.CO(CO2)(括号内的物质为杂质):通常将气体通人过量的碱溶液(一般用氢氧化钠溶液而不用澄清石灰水)中,二氧化碳与碱溶液反应,从而达到除杂的目的。


二氧化碳和一氧化碳及其比较1.二氧化碳的物理性质在通常状况下,二氧化碳是一种无色气体,能溶于水,在标准状况下,二氧化碳的密度是 1.977 g/L,约是空气的 1.5 倍。
固体二氧化碳又叫做干冰,它可以升华。
2.二氧化碳的化学性质(1)本身不能燃烧,一般也不支持可燃物燃烧,不能供给呼吸。
在一般情况下,CO2既不能燃烧,也不能支持可燃物燃烧。
但在一定条件下,某些物质也可以在CO2中燃烧,如点燃的镁条,伸入盛有CO2的集气瓶中能继续燃烧:(2)跟水反应生成碳酸:CO2+H2O=H2CO3,生成的碳酸可使紫色的石蕊试液变红色。
①CO2能溶解于水,通常1体积的水可以溶解1体积的CO2,增大压强时,还会溶解得更多些。
CO2溶于水的同时还与水发生反应,但水中溶解的CO2只有1%跟水结合成H2CO3,其余仍以分子形式溶解在水中。
②能使紫色石蕊试液变红色的是H2CO3,而不是CO2。
(3)跟石灰水反应产生碳酸钙(白色)沉淀,此反应可用来检验二氧化碳。
CO2+Ca(OH)2=CaCO3↓+H2O3.二氧化碳对生活和环境的影响(1)用途①用于灭火;②用作制冷剂,用来保存食品和用于人工降雨;③作肥料,制纯碱、汽水等。
(2)影响近几十年来,由于人类消耗的能源急剧增加,森林遭到破坏,大气中二氧化碳的含量不断上升,造成“温室效应”。
4.一氧化碳的物理性质通常状况下,一氧化碳是一种无色、无味的气体,它的密度比空气的略小,难溶于水。
5.一氧化碳的化学性质(1)可燃性现象:燃烧时发出蓝色火焰,放出热量。
(2)还原性现象:黑色的氧化铜变红色,同时有使澄清的石灰水变浑浊的气体生成。
(3)毒性正常的血液呈深红色,当通入一氧化碳后,血液由深红色变成鲜红色,原因是一氧化碳能与血液里的血红蛋白结合,使血红蛋白不能很好地跟氧气结合,严重时会危及生命。
6.一氧化碳与二氧化碳的比较从CO和CO2的化学式可看出,CO比CO2少1个氧原子。
由于分子结构不同,就使得 CO和CO2的性质有很大差别。
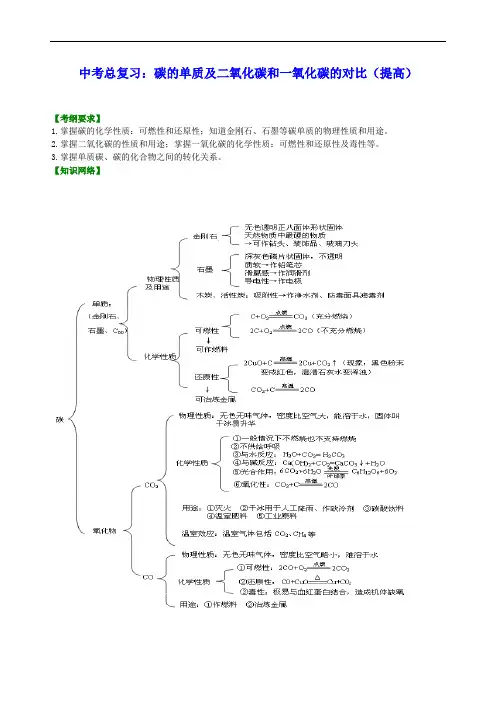
中考总复习:碳的单质及二氧化碳和一氧化碳的对比(提高)【考纲要求】1.掌握碳的化学性质:可燃性和还原性;知道金刚石、石墨等碳单质的物理性质和用途。
2.掌握二氧化碳的性质和用途;掌握一氧化碳的化学性质:可燃性和还原性及毒性等。
3.掌握单质碳、碳的化合物之间的转化关系。
【知识网络】【考点梳理】考点一、碳单质(金刚石、石墨)的物理性质和用途比较对比项目 金刚石石墨外 观 无色透明正八面体形状固体深灰色细磷片状固体 光 泽 加工琢磨后有光泽 略有金属光泽硬 度 自然界最硬软 导电性 无 良好 导热性 良好良好用 途钻探机钻头、刻刀、装饰品等电极、铅笔芯、润滑剂等要点诠释:1.由于碳原子排列方式不同,导致金刚石和石墨在物理性质上存在较大差异。
2.炭和碳不同。
碳是指碳元素,是“核电荷数为6的同一类原子的总称”,有广泛、概括的含义,并不具体指某种物质;炭是指具体的物质——由碳元素组成的单质,如木炭、焦炭、活性炭、炭黑等。
碳与炭不能混用。
3.木炭和活性炭具有疏松多孔的结构,因此具有吸附能力,可以吸附一些色素、有异味的物质,吸附过程属于物理变化,并非化学变化。
4.规律总结:物质的组成、结构垐垐?噲垐?决定反映物质的性质垐垐?噲垐?决定反映物质的用途。
考点二:CO 2和CO 性质及用途的比较(高清课堂《二氧化碳和一氧化碳》一)对比项目CO 2CO物理性质 无色无味气体,能溶于水,密度比空气大,干冰易升华无色无味气体,难溶于水,密度比空气略小化学性质可燃性 一般情况下既不能燃烧,也不支持燃烧有可燃性2CO+O 22CO 2还原性没有还原性,有较弱的氧化性有还原性C+CO22CO CO+CuO Cu+CO2与水反应与水反应CO2+H2O=H2CO3不能与水反应与石灰水的反应(碱)与石灰水反应CO2+Ca(OH)2=CaCO3↓+H2O不能与石灰水反应毒性无毒有剧毒主要用途可制汽水,作制冷剂,灭火,气体肥料气体燃料、高炉炼铁对环境的影响造成温室效应污染空气要点诠释:1.由于CO和CO2的分子构成不同,决定了二者性质的不同。

等质量的一氧化碳和二氧化碳物质的量之比一氧化碳和二氧化碳都是由单个氧原子和一个碳原子组成的,它们都是温室气体,具有增加全球平均温度的能力。
尽管一氧化碳和二氧化碳具有相似的化学结构,但其分子结构不同,也导致其在自然界中和环境中的作用不同。
鉴于这一有趣的事实,我们可能会想知道一氧化碳和二氧化碳物质的量之比是什么。
一氧化碳和二氧化碳在大气中的浓度是相当的。
根据NASA的最新研究,空气中每升大气中,平均含有400毫克CO2和400毫克O2。
根据这一数据,一氧化碳和二氧化碳物质的量之比是1:1。
但在不同的地方,比例可能会有所不同。
比如,地下空气含有较少的一氧化碳,空气在深处的大气含氧量可以比地表空气更高。
这是由于植物利用光能,将大气中的二氧化碳转化为有机物质并释放出氧气。
地下空气因此会有更少的一氧化碳和更多的二氧化碳,所以一氧化碳和二氧化碳物质的量之比可能小于1:1。
另一方面,在湖泊、河流和海洋中,含氧量会低于大气中的含氧量,这也可能会改变一氧化碳和二氧化碳物质的量之比。
湖泊中的CO2会因生物的活动而水解,这会导致CO2的浓度降低,而氧气的浓度升高,因此湖泊中的一氧化碳和二氧化碳物质的量之比可能大于1:1。
总之,一氧化碳和二氧化碳物质的量之比可能会因地点而异。
在大气中,一氧化碳和二氧化碳物质的量之比大致是1:1,而在深海和湖泊中,可能会更高或更低。
因此,为了精准地了解一氧化碳和二氧化碳物质的量之比,我们需要进行现场测量并对结果进行准确的分析。
然而,让我们不要忘记,一氧化碳和二氧化碳的量可能会随着时间的推移而发生变化。
这是因为二氧化碳大部分是由于人类活动而释放到大气中的,而一氧化碳大部分是由于自然因素。
随着气候变暖,人类活动释放的二氧化碳会增加,这将导致一氧化碳和二氧化碳物质的量之比发生变化。
因此,我们研究并观察一氧化碳和二氧化碳物质的量之比,有助于我们更好地了解我们所处的环境,并有效地制定有效的减排措施。
辨别一氧化碳和二氧化碳的五种方式:一是根据密度不同,分别将它们充入气球;二是根据水溶性不同,别离将它们通入石蕊试液中;三是根据可燃性不同;四是根据还原性不同,别离将它们通入灼热的氧化铜中;五是根据是否与碱溶液反应,分别将它们通入到澄清的石灰水。
【将带火星的木条不能检验二者,因为一氧化碳和二氧化碳都是不支持燃烧的;柴炭在氧气中燃烧发出敞亮白光是正确的。
】为何柴炭在氧气中燃烧发出敞亮白光是正确的?谢谢...回答因为柴炭在氧气中燃烧,是在纯氧中发生的猛烈氧化反映CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2查验和石灰浆粉刷墙壁Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成HCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸查验Cl—的原理Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸查验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸查验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反映)应用于查验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反映)应用于查验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成1结晶法概念- #使物质从液态(溶液或熔融状态)或气态形成晶体的方式即结晶法。
化学练习:于二氧化碳与一氧化碳的性质比
较_中考化学
下列关于二氧化碳与一氧化碳的性质比较不正确的是()
A.组成:都是由碳元素和氧元素组成
B.性质:CO2、CO都可以使澄清石灰水变浑浊
C.用途:干冰可用于人工降雨;一氧化碳气体可作燃料
D.危害:二氧化碳会导致;一氧化碳会引起中毒
【答案】B
【解析】
A、根据物质的元素组成分析,一氧化碳和二氧化碳都是由碳元素和氧元素组成的,选项A正确;
B、二氧化碳能使澄清的石灰水变浑浊,一氧化碳不跟澄清石灰水反应,选项B错误;
C、CO2的固体干冰升华吸热,可用于人工降雨;CO 可用作气体燃料、冶炼金属的还原剂等,选项C正确;
D、CO2会造成,CO有毒,极易使人中毒,选项D 正确。
故选B。
助你迎接2020年中考!。